高中化学人教版选修4第四章第二节 化学电源课件(共26张ppt)
文档属性
| 名称 | 高中化学人教版选修4第四章第二节 化学电源课件(共26张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-05 00:00:00 | ||
图片预览






文档简介
(共27张PPT)
第二节
化学电源
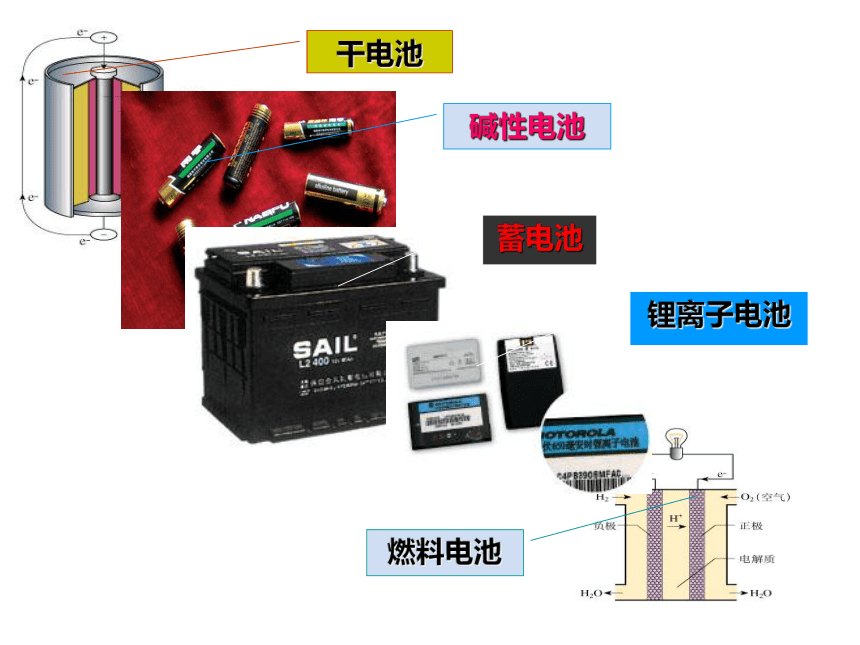
干电池
碱性电池
蓄电池
锂离子电池
燃料电池
化学电源
(1)一次电池(如干电池):用过后不能复原
(2)二次电池(如蓄电池):充电后能继续使用
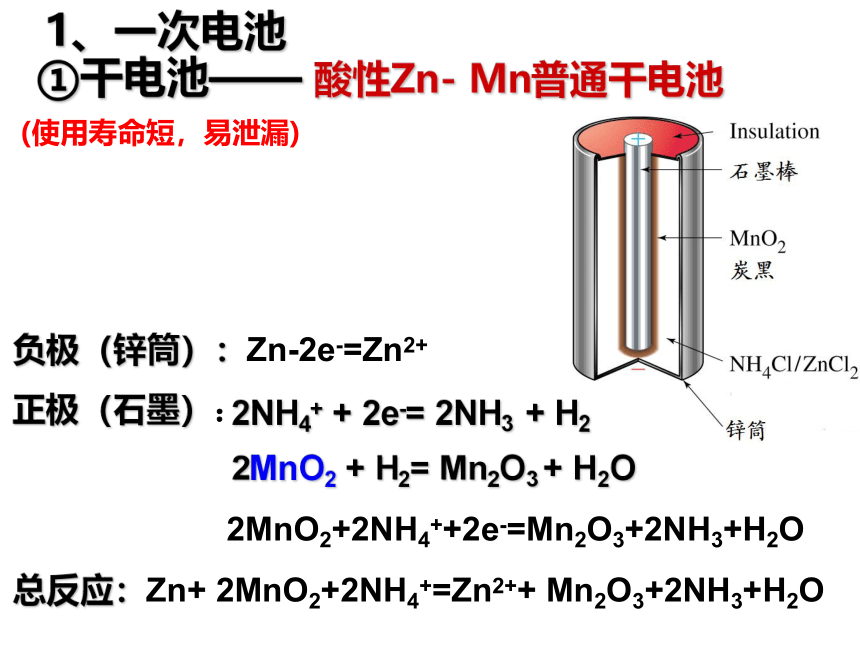
负极(锌筒):Zn-2e-=Zn2+
正极(石墨):
2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O
总反应:Zn+
2MnO2+2NH4+=Zn2++
Mn2O3+2NH3+H2O
①干电池——
酸性Zn-
Mn普通干电池
1、一次电池
2NH4+
+
2e-=
2NH3
+
H2
2MnO2
+
H2=
Mn2O3
+
H2O
(使用寿命短,易泄漏)
锌锰碱性电池是一种新型的干电池。
正极材料为MnO2
,负极材料为Zn,
还原产物为MnOOH,电解质是KOH溶液,
总:
Zn
+
2MnO2
+
2H2O
=
Zn(OH)2
+
2MnO(OH)
请写出电极反应式并分析其工作原理。
负极:Zn
-2e-
+
2OH-
=
Zn(OH)2
正极:2MnO2
+
2H2O
+
2
e-
=
2MnO(OH)
+
2OH-
总反应:Zn
+
2MnO2
+
2H2O
=
Zn(OH)2
+
2MnO(OH)
②碱性Zn-
Mn干电池
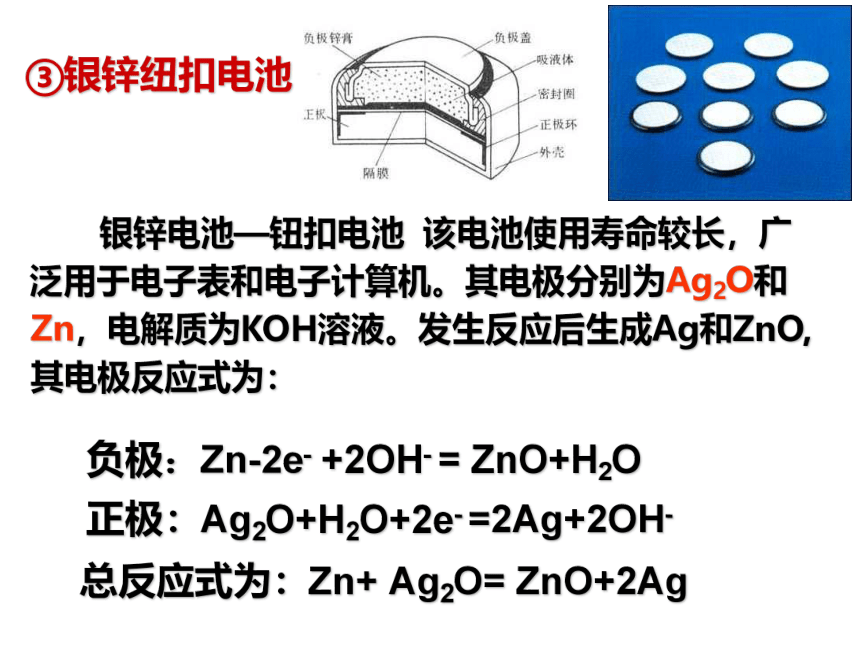
银锌电池—钮扣电池??该电池使用寿命较长,广泛用于电子表和电子计算机。其电极分别为Ag2O和Zn,电解质为KOH溶液。发生反应后生成Ag和ZnO,其电极反应式为:
负极:Zn-2e-?+2OH-
=?ZnO+H2O????????
正极:Ag2O+H2O+2e-
=2Ag+2OH-
③银锌纽扣电池
总反应式为:Zn+?Ag2O=?ZnO+2Ag
①铅蓄电池
(1)电极材料及原料
(2)电解质溶液
(3)电极反应式:
正极:PbO2
负极:Pb
H2SO4溶液
负极(Pb):
Pb-
2e-+
SO4
2
-
=PbSO4
Pb+PbO2+2H2SO4
=2PbSO4
+2H2O
正极(PbO2):
PbO2+4H++SO42
-+
2e-=
PbSO4
+2H2O
总反应:
2、二次电池
阴极(Pb):
PbSO4
+2e-
=
Pb+SO42-
阳极(PbO2):
PbSO4+
2H2O-2e-
=
PbO2+SO42-+4H+
电池总反应:
2PbSO4+2H2O
=
PbO2+Pb+2H2SO4
铅蓄电池的放电过程——原电池
铅蓄电池的充电过程——电解池
放电
充电
2
PbSO4
+
2H2O
PbO2
+
Pb
+
2H2SO4
铅蓄电池的充放电过程
②镍镉充电电池:
它是一种体积少,具有残留性记忆的充电电池,可重复使用500次以上。它以Cd为负极,NiO(OH)为正极,KOH为电解液。广泛用于收录机、无线对讲机、电子闪光灯、电动剃须刀等,但有毒,废旧电池要回收处理,防止污染环境。
2NiO(OH)+Cd+2H2O
2Ni(OH)2+
Cd(OH)2
充电
放电
写出原电池的电极反应式
负极(Cd)
正极(
NiO(OH)
)
Cd
-
2e-
+
2OH-
=
Cd(OH)2
2NiO(OH)+2e-+2H2O=2Ni(OH)2+2OH-
③锂离子电池
负极材料:Li
放电时:Li+向正极移动
负极反应:Li-e-
=Li+
练习:蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下面是爱迪生蓄电池分别在充电和放电时发生的反应:
下列有关爱迪生蓄电池的推断错误的是(
)
A.放电时,Fe是负极,NiO2是正极
B.蓄电池的电极可以浸入某种酸性电解质溶液中C.蓄电池的电极可以浸入KOH溶液中
D.放电时,电解质溶液中的阴离子向负极方向移动
B
①原理:
③两极材料:惰性材料,只具导电性,可相同。
②反应物不储存在电池内部,外加提供燃料和氧化剂。
④两极判断:
⑤导电介质:
⑥高效、环境友好。
将燃料和氧化剂(如:O2)反应所放出的化学能转化为电能。
负极:通入可燃物的一极(或作还原剂的一极)
正极:通入O2或空气的一极
可以是电解质溶液,也可以是新型的导离子介质。
3、新型燃料电池
氢氧燃料电池
电极:Pt制作的惰性电极
O2
燃料电池电极反应式的书写
(1)电极:惰性电极。
(2)燃料包含:H2、CO、烃(如CH4、C2H6)、醇(如C2H5OH)等。
(3)电解质包含:
①酸性电解质溶液,如H2SO4溶液;
②碱性电解质溶液,如NaOH溶液;
③熔融氧化物,如Y2O3;
④熔融碳酸盐,如K2CO3等。
第一步:写出电池总反应式
燃料电池的总反应与燃料的燃烧反应方程式一致,若产物能和电解质反应则总反应为加和后的总反应。
如氢氧燃料电池的总反应式为
2H2+O2=
2H2O;
甲烷燃料电池(电解质溶液为NaOH溶液)的反应式为
CH4+2O2=
CO2+2H2O ①
CO2+2NaOH=Na2CO3+H2O ②
①式+②式得燃料电池总反应式为
CH4+2O2+2NaOH=Na2CO3+3H2O
第二步:写出电池的正极反应式
负极反应式=总反应式-正极反应式
注意:在将两个反应式相减时,要消去正极的反应物O2。
第三步:根据电池总反应式和正极反应式写出电池的负极反应式
CH4、O2、NaOH组成的燃料电池
1.燃烧总化学反应:
CH4+2O2=CO2+2H2O
2.燃料电池总反应:
3.正极:
4.负极:
CH4+2OH-
+2O2
=
CO3
2
-
+3H2O
2O2+4H2O+8e-
=
8OH-
CH4+10OH-
-
8e-
=
CO32-
+7H2O
甲醇燃料电池是由甲醇和氧气及强碱电解质溶液构成的新型手机电池,电量可达现用镍氢或锂电池的十倍,可连续使用一个月才充一次电。据此回答:
(1)甲醇是
极,
电极反应式是:
;
(2)电池反应的离子方程式:
2CH3OH+16OH-
-12e-=2CO32-
+12H2O
2CH3OH+3O2+4OH-
=2CO32-
+6H2O.
负
(10安徽)某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2
=
2H2O,下列有关说法正确的是(
)
A.
电子通过外电路从b极流向a极
B.
b极上的电极反应式为:O2+2H2O+4e-
=
4OH-
C.
每转移0.1
mol电子,消耗1.12
L的H2
D.
H+由a极通过固体酸电解质传递到b极
D
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见下图。下列说法正确的是( )
A.a为CH4,b为CO2
B.CO32—
向正极移动
C.此电池在常温时也能工作
D.正极电极反应式为O2+2CO2+4e-=
2CO32—
D
(4)海水电池
1991年,我国首创以铝-空气-海水为能源的新型电
池,用作航海标志灯。该电池以取之不的海水为电
解质,靠空气中的氧气使铝不断氧化而产生电流。
这种海水电池的能量比“干电池”高20~50倍。电极
反应式为:
负极:
正极:
电池总反应:
4Al
-
12e-=
4Al
3+
3O2+
6H2O
+12e-=
12
OH
-
4Al+3O2+
6H2O
=
4Al
(OH)3↓
第二节
化学能与电能
1、银锌电池广泛用作各种电子仪器的电源,其充电和放电过程可以表示为:
2Ag+Zn(OH)2
Ag2O+Zn+H2O
,则
此电池放电时,负极上发生反应的物质是(
)
(A)Ag
(B)Zn
(OH)2
(C)Ag2O
(D)Zn
D
练习
第二节
化学能与电能
2.某金属能和盐酸反应生成氢气,该金属与锌组成原电池时,锌为负极,则该金属可能为(
)
A.铝
B.铜
C.锡
D.硅
3.已知空气-锌电池的电极反应为:
锌片:Zn+20H--2e-
=ZnO+H20
石墨:02+2H20+4e-
=40H-
根据此判断,锌片是(
)
A.负极,并被氧化
B.负极,并被还原
C.正极,并被氧化
D.正极,并被还原
A
C
第二节
化学能与电能
6.据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染,其电池反应为:2Zn
+
O2
=
2ZnO,原料为锌粒、电解液和空气,则下列叙述正确的是(
)
A.锌为正极,空气进入负极反应
B.负极反应为Zn
–
2e-
=
Zn2+
C.正极发生氧化反应
D.电解液肯定是强酸
B
第二节
化学能与电能
7.下列叙述中正确的是(
)
A.构成原电池正极和负极的材料必须是两种金属
B.由Cu、Zn做电极与CuSO4溶液组成的原电池中Cu是负极
C.马口铁(镀锡铁)破损时与电解质液接触锡先被腐蚀
D.铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过
D
第二节
化学能与电能
8、一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2— 。下列对该燃料电池说法正确的是(
)
A.电池的总反应是:
2C4H10+13O2=8CO2+10H2O
B.在熔融电解质中,O2—由负极移向正极
C.通入空气的一极是正极,电极反应为:
O2+4e—
=2
O2—
D.通入丁烷的—极是正极,电极反应为:
C4H10+26e—+13O2—=4CO2+5H2O
AC
第二节
化学电源
干电池
碱性电池
蓄电池
锂离子电池
燃料电池
化学电源
(1)一次电池(如干电池):用过后不能复原
(2)二次电池(如蓄电池):充电后能继续使用
负极(锌筒):Zn-2e-=Zn2+
正极(石墨):
2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O
总反应:Zn+
2MnO2+2NH4+=Zn2++
Mn2O3+2NH3+H2O
①干电池——
酸性Zn-
Mn普通干电池
1、一次电池
2NH4+
+
2e-=
2NH3
+
H2
2MnO2
+
H2=
Mn2O3
+
H2O
(使用寿命短,易泄漏)
锌锰碱性电池是一种新型的干电池。
正极材料为MnO2
,负极材料为Zn,
还原产物为MnOOH,电解质是KOH溶液,
总:
Zn
+
2MnO2
+
2H2O
=
Zn(OH)2
+
2MnO(OH)
请写出电极反应式并分析其工作原理。
负极:Zn
-2e-
+
2OH-
=
Zn(OH)2
正极:2MnO2
+
2H2O
+
2
e-
=
2MnO(OH)
+
2OH-
总反应:Zn
+
2MnO2
+
2H2O
=
Zn(OH)2
+
2MnO(OH)
②碱性Zn-
Mn干电池
银锌电池—钮扣电池??该电池使用寿命较长,广泛用于电子表和电子计算机。其电极分别为Ag2O和Zn,电解质为KOH溶液。发生反应后生成Ag和ZnO,其电极反应式为:
负极:Zn-2e-?+2OH-
=?ZnO+H2O????????
正极:Ag2O+H2O+2e-
=2Ag+2OH-
③银锌纽扣电池
总反应式为:Zn+?Ag2O=?ZnO+2Ag
①铅蓄电池
(1)电极材料及原料
(2)电解质溶液
(3)电极反应式:
正极:PbO2
负极:Pb
H2SO4溶液
负极(Pb):
Pb-
2e-+
SO4
2
-
=PbSO4
Pb+PbO2+2H2SO4
=2PbSO4
+2H2O
正极(PbO2):
PbO2+4H++SO42
-+
2e-=
PbSO4
+2H2O
总反应:
2、二次电池
阴极(Pb):
PbSO4
+2e-
=
Pb+SO42-
阳极(PbO2):
PbSO4+
2H2O-2e-
=
PbO2+SO42-+4H+
电池总反应:
2PbSO4+2H2O
=
PbO2+Pb+2H2SO4
铅蓄电池的放电过程——原电池
铅蓄电池的充电过程——电解池
放电
充电
2
PbSO4
+
2H2O
PbO2
+
Pb
+
2H2SO4
铅蓄电池的充放电过程
②镍镉充电电池:
它是一种体积少,具有残留性记忆的充电电池,可重复使用500次以上。它以Cd为负极,NiO(OH)为正极,KOH为电解液。广泛用于收录机、无线对讲机、电子闪光灯、电动剃须刀等,但有毒,废旧电池要回收处理,防止污染环境。
2NiO(OH)+Cd+2H2O
2Ni(OH)2+
Cd(OH)2
充电
放电
写出原电池的电极反应式
负极(Cd)
正极(
NiO(OH)
)
Cd
-
2e-
+
2OH-
=
Cd(OH)2
2NiO(OH)+2e-+2H2O=2Ni(OH)2+2OH-
③锂离子电池
负极材料:Li
放电时:Li+向正极移动
负极反应:Li-e-
=Li+
练习:蓄电池在放电时起原电池的作用,在充电时起电解池的作用。下面是爱迪生蓄电池分别在充电和放电时发生的反应:
下列有关爱迪生蓄电池的推断错误的是(
)
A.放电时,Fe是负极,NiO2是正极
B.蓄电池的电极可以浸入某种酸性电解质溶液中C.蓄电池的电极可以浸入KOH溶液中
D.放电时,电解质溶液中的阴离子向负极方向移动
B
①原理:
③两极材料:惰性材料,只具导电性,可相同。
②反应物不储存在电池内部,外加提供燃料和氧化剂。
④两极判断:
⑤导电介质:
⑥高效、环境友好。
将燃料和氧化剂(如:O2)反应所放出的化学能转化为电能。
负极:通入可燃物的一极(或作还原剂的一极)
正极:通入O2或空气的一极
可以是电解质溶液,也可以是新型的导离子介质。
3、新型燃料电池
氢氧燃料电池
电极:Pt制作的惰性电极
O2
燃料电池电极反应式的书写
(1)电极:惰性电极。
(2)燃料包含:H2、CO、烃(如CH4、C2H6)、醇(如C2H5OH)等。
(3)电解质包含:
①酸性电解质溶液,如H2SO4溶液;
②碱性电解质溶液,如NaOH溶液;
③熔融氧化物,如Y2O3;
④熔融碳酸盐,如K2CO3等。
第一步:写出电池总反应式
燃料电池的总反应与燃料的燃烧反应方程式一致,若产物能和电解质反应则总反应为加和后的总反应。
如氢氧燃料电池的总反应式为
2H2+O2=
2H2O;
甲烷燃料电池(电解质溶液为NaOH溶液)的反应式为
CH4+2O2=
CO2+2H2O ①
CO2+2NaOH=Na2CO3+H2O ②
①式+②式得燃料电池总反应式为
CH4+2O2+2NaOH=Na2CO3+3H2O
第二步:写出电池的正极反应式
负极反应式=总反应式-正极反应式
注意:在将两个反应式相减时,要消去正极的反应物O2。
第三步:根据电池总反应式和正极反应式写出电池的负极反应式
CH4、O2、NaOH组成的燃料电池
1.燃烧总化学反应:
CH4+2O2=CO2+2H2O
2.燃料电池总反应:
3.正极:
4.负极:
CH4+2OH-
+2O2
=
CO3
2
-
+3H2O
2O2+4H2O+8e-
=
8OH-
CH4+10OH-
-
8e-
=
CO32-
+7H2O
甲醇燃料电池是由甲醇和氧气及强碱电解质溶液构成的新型手机电池,电量可达现用镍氢或锂电池的十倍,可连续使用一个月才充一次电。据此回答:
(1)甲醇是
极,
电极反应式是:
;
(2)电池反应的离子方程式:
2CH3OH+16OH-
-12e-=2CO32-
+12H2O
2CH3OH+3O2+4OH-
=2CO32-
+6H2O.
负
(10安徽)某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2
=
2H2O,下列有关说法正确的是(
)
A.
电子通过外电路从b极流向a极
B.
b极上的电极反应式为:O2+2H2O+4e-
=
4OH-
C.
每转移0.1
mol电子,消耗1.12
L的H2
D.
H+由a极通过固体酸电解质传递到b极
D
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见下图。下列说法正确的是( )
A.a为CH4,b为CO2
B.CO32—
向正极移动
C.此电池在常温时也能工作
D.正极电极反应式为O2+2CO2+4e-=
2CO32—
D
(4)海水电池
1991年,我国首创以铝-空气-海水为能源的新型电
池,用作航海标志灯。该电池以取之不的海水为电
解质,靠空气中的氧气使铝不断氧化而产生电流。
这种海水电池的能量比“干电池”高20~50倍。电极
反应式为:
负极:
正极:
电池总反应:
4Al
-
12e-=
4Al
3+
3O2+
6H2O
+12e-=
12
OH
-
4Al+3O2+
6H2O
=
4Al
(OH)3↓
第二节
化学能与电能
1、银锌电池广泛用作各种电子仪器的电源,其充电和放电过程可以表示为:
2Ag+Zn(OH)2
Ag2O+Zn+H2O
,则
此电池放电时,负极上发生反应的物质是(
)
(A)Ag
(B)Zn
(OH)2
(C)Ag2O
(D)Zn
D
练习
第二节
化学能与电能
2.某金属能和盐酸反应生成氢气,该金属与锌组成原电池时,锌为负极,则该金属可能为(
)
A.铝
B.铜
C.锡
D.硅
3.已知空气-锌电池的电极反应为:
锌片:Zn+20H--2e-
=ZnO+H20
石墨:02+2H20+4e-
=40H-
根据此判断,锌片是(
)
A.负极,并被氧化
B.负极,并被还原
C.正极,并被氧化
D.正极,并被还原
A
C
第二节
化学能与电能
6.据报道,锌电池可能取代目前广泛使用的铅蓄电池,因为锌电池容量更大,而且没有铅污染,其电池反应为:2Zn
+
O2
=
2ZnO,原料为锌粒、电解液和空气,则下列叙述正确的是(
)
A.锌为正极,空气进入负极反应
B.负极反应为Zn
–
2e-
=
Zn2+
C.正极发生氧化反应
D.电解液肯定是强酸
B
第二节
化学能与电能
7.下列叙述中正确的是(
)
A.构成原电池正极和负极的材料必须是两种金属
B.由Cu、Zn做电极与CuSO4溶液组成的原电池中Cu是负极
C.马口铁(镀锡铁)破损时与电解质液接触锡先被腐蚀
D.铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过
D
第二节
化学能与电能
8、一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2— 。下列对该燃料电池说法正确的是(
)
A.电池的总反应是:
2C4H10+13O2=8CO2+10H2O
B.在熔融电解质中,O2—由负极移向正极
C.通入空气的一极是正极,电极反应为:
O2+4e—
=2
O2—
D.通入丁烷的—极是正极,电极反应为:
C4H10+26e—+13O2—=4CO2+5H2O
AC
