高中化学人教版必修一第四章第三节硫和氮的氧化物---二氧化硫 课件(共21张ppt)
文档属性
| 名称 | 高中化学人教版必修一第四章第三节硫和氮的氧化物---二氧化硫 课件(共21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-07 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
二氧化硫
二
氧
化
硫
人教版必修一第四章第三节
问题1
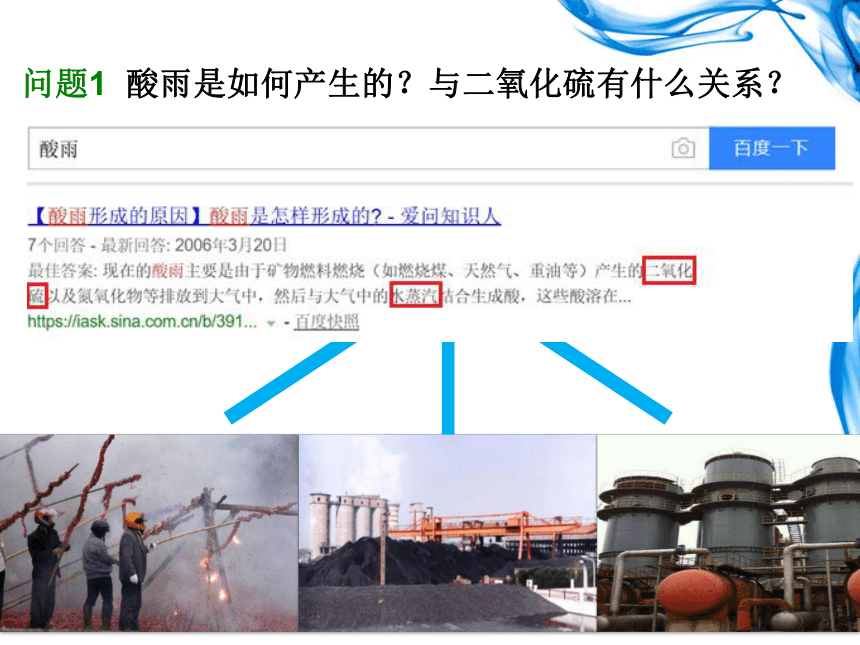
酸雨是如何产生的?与二氧化硫有什么关系?
问题2
葡萄酒中为什么要加入二氧化硫呢?
问题3
用硫磺熏蒸的银耳为什么会变白?
问题汇总
问题4
旧报纸为什么会泛黄呢?
问题1
酸雨是如何产生的?与二氧化硫有什么关系?
SO2
+雨水
酸雨
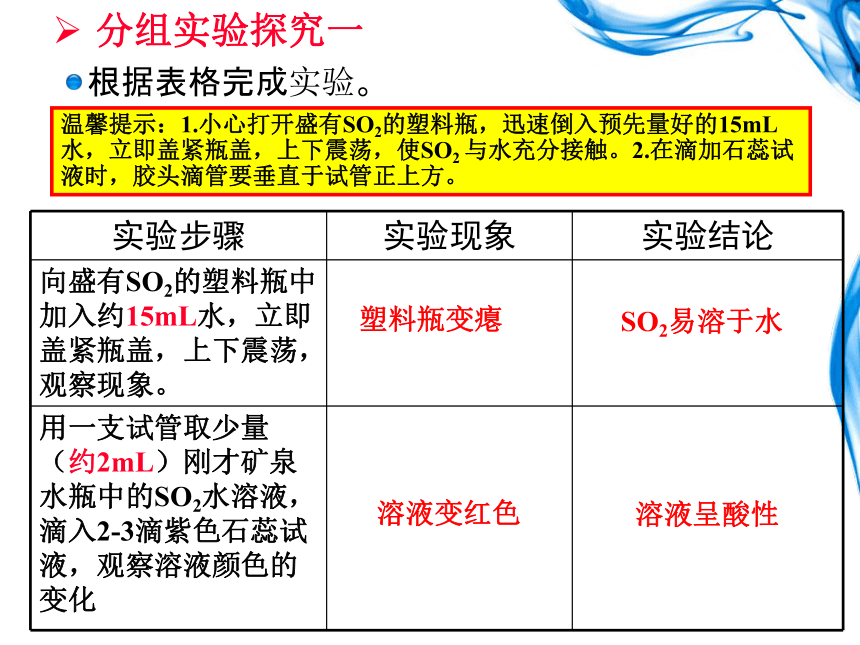
分组实验探究一
根据表格完成实验。
实验步骤
实验现象
实验结论
向盛有SO2的塑料瓶中加入约15mL水,立即盖紧瓶盖,上下震荡,观察现象。
用一支试管取少量(约2mL)刚才矿泉水瓶中的SO2水溶液,滴入2-3滴紫色石蕊试液,观察溶液颜色的变化
温馨提示:1.小心打开盛有SO2的塑料瓶,迅速倒入预先量好的15mL水,立即盖紧瓶盖,上下震荡,使SO2
与水充分接触。2.在滴加石蕊试液时,胶头滴管要垂直于试管正上方。
塑料瓶变瘪
SO2易溶于水
溶液变红色
溶液呈酸性
颜
色
气
味
状
态
密
度
溶解性
毒
性
沸
点
注:在常温常压下,1体积水大约能溶解40体积的SO2
二氧化硫的物理性质
小结
酸雨与二氧化硫
SO2
+
H2O
H2SO3(亚硫酸)
(可逆号)
可逆反应
酸性氧化物
思考:类比二氧化碳的性质,预测SO2
能与哪些物质发生反应?
与碱反应
NaOH
Ca(OH)2
与碱性氧化物反应
CaO
Na2O
……
二氧化硫的化学性质——酸性氧化物的通性
小结
酸雨中的酸性物质就是H2SO3吗?
pH传感器
pH
数据说明了溶液酸性增强
从上述图表你有哪些猜测?
酸雨形成过程
体现了SO2的还原性
有H2SO4生成
SO2
+4
+6
被氧化
SO3
H2SO3
+4
H2SO4
+6
问题1
酸雨是如何产生的?与二氧化硫有什么关系?
该过程体现了二氧化硫的什么化学性质?
深度思考
分组实验探究二
设计实验来验证SO2的氧化性、还原性
备选试剂:
酸性KMnO4溶液
石蕊溶液
氢氧化钠溶液
溴水等
实验探究二
探究二氧化硫的氧化性、还原性
KMnO4溶液紫色褪去
SO2具有还原性
实验步骤
实验现象
实验结论
在
KMnO4溶液中滴加SO2的水溶液,振荡,观察现象
在溴水中滴加SO2的水溶液,充分振荡,观察现象
溴水橙色褪去
我可以抗氧化哦
问题2
葡萄酒中为什么要加入二氧化硫呢?
SO2具有氧化性吗?什么物质能够还原SO2?
2H2S+SO2=3S↓+2H2O
阅读P91《资料卡片》“预防硫化氢中毒”,了解硫化氢的性质
深度思考
S
S
S(SO2)
S
-2
0
+4
+6
二氧化硫的化学性质——氧化性和还原性
小结
KMnO4酸性溶液
溴水
O2
Cl2、Fe3+、I2等
H2S
还原性为主
氧化性为次
问题3
用硫磺熏蒸的银耳为什么会变白?
问题4
旧报纸为什么会泛黄呢?
实验步骤
现象
结论
往装有SO2溶液的试管内滴入2-3滴品红溶液,然后震荡试管
把试管内液体用酒精灯加热至沸腾
品红溶液褪色
SO2有漂白作用
溶液变回红色
被SO2漂白不稳定,容易变回原来的颜色
分组实验探究三
SO2
有
机
色
素
无色物质
1、SO2的漂白是暂时性漂白。
2、SO2漂白具有选择性,如某些指示剂不能被漂白。
失去SO2
有
机
色
素
加热
不稳定的
二氧化硫的化学特性——漂白性
小结
特性:漂白性
物理性质:色、态、味、密度、溶解性等
化学性质
物质的
性质
酸、碱性的角度:
酸性氧化物的性质
氧化还原角度:
主要体现还原性
课堂小结
SO2对人类是有“功”还是有“过”呢?
小组辩论
我们的收获
二氧化硫
二氧化硫与水反应
(物质分类的角度)
还原性
(氧化还原的角度)
漂白性
(特性的角度)
酸雨与
二氧化硫
环保化学
从生活到化学
二氧化硫的
物理性质
绿色化学
从化学到生活
二氧化硫
在生活中的应用
二氧化硫
二
氧
化
硫
人教版必修一第四章第三节
问题1
酸雨是如何产生的?与二氧化硫有什么关系?
问题2
葡萄酒中为什么要加入二氧化硫呢?
问题3
用硫磺熏蒸的银耳为什么会变白?
问题汇总
问题4
旧报纸为什么会泛黄呢?
问题1
酸雨是如何产生的?与二氧化硫有什么关系?
SO2
+雨水
酸雨
分组实验探究一
根据表格完成实验。
实验步骤
实验现象
实验结论
向盛有SO2的塑料瓶中加入约15mL水,立即盖紧瓶盖,上下震荡,观察现象。
用一支试管取少量(约2mL)刚才矿泉水瓶中的SO2水溶液,滴入2-3滴紫色石蕊试液,观察溶液颜色的变化
温馨提示:1.小心打开盛有SO2的塑料瓶,迅速倒入预先量好的15mL水,立即盖紧瓶盖,上下震荡,使SO2
与水充分接触。2.在滴加石蕊试液时,胶头滴管要垂直于试管正上方。
塑料瓶变瘪
SO2易溶于水
溶液变红色
溶液呈酸性
颜
色
气
味
状
态
密
度
溶解性
毒
性
沸
点
注:在常温常压下,1体积水大约能溶解40体积的SO2
二氧化硫的物理性质
小结
酸雨与二氧化硫
SO2
+
H2O
H2SO3(亚硫酸)
(可逆号)
可逆反应
酸性氧化物
思考:类比二氧化碳的性质,预测SO2
能与哪些物质发生反应?
与碱反应
NaOH
Ca(OH)2
与碱性氧化物反应
CaO
Na2O
……
二氧化硫的化学性质——酸性氧化物的通性
小结
酸雨中的酸性物质就是H2SO3吗?
pH传感器
pH
数据说明了溶液酸性增强
从上述图表你有哪些猜测?
酸雨形成过程
体现了SO2的还原性
有H2SO4生成
SO2
+4
+6
被氧化
SO3
H2SO3
+4
H2SO4
+6
问题1
酸雨是如何产生的?与二氧化硫有什么关系?
该过程体现了二氧化硫的什么化学性质?
深度思考
分组实验探究二
设计实验来验证SO2的氧化性、还原性
备选试剂:
酸性KMnO4溶液
石蕊溶液
氢氧化钠溶液
溴水等
实验探究二
探究二氧化硫的氧化性、还原性
KMnO4溶液紫色褪去
SO2具有还原性
实验步骤
实验现象
实验结论
在
KMnO4溶液中滴加SO2的水溶液,振荡,观察现象
在溴水中滴加SO2的水溶液,充分振荡,观察现象
溴水橙色褪去
我可以抗氧化哦
问题2
葡萄酒中为什么要加入二氧化硫呢?
SO2具有氧化性吗?什么物质能够还原SO2?
2H2S+SO2=3S↓+2H2O
阅读P91《资料卡片》“预防硫化氢中毒”,了解硫化氢的性质
深度思考
S
S
S(SO2)
S
-2
0
+4
+6
二氧化硫的化学性质——氧化性和还原性
小结
KMnO4酸性溶液
溴水
O2
Cl2、Fe3+、I2等
H2S
还原性为主
氧化性为次
问题3
用硫磺熏蒸的银耳为什么会变白?
问题4
旧报纸为什么会泛黄呢?
实验步骤
现象
结论
往装有SO2溶液的试管内滴入2-3滴品红溶液,然后震荡试管
把试管内液体用酒精灯加热至沸腾
品红溶液褪色
SO2有漂白作用
溶液变回红色
被SO2漂白不稳定,容易变回原来的颜色
分组实验探究三
SO2
有
机
色
素
无色物质
1、SO2的漂白是暂时性漂白。
2、SO2漂白具有选择性,如某些指示剂不能被漂白。
失去SO2
有
机
色
素
加热
不稳定的
二氧化硫的化学特性——漂白性
小结
特性:漂白性
物理性质:色、态、味、密度、溶解性等
化学性质
物质的
性质
酸、碱性的角度:
酸性氧化物的性质
氧化还原角度:
主要体现还原性
课堂小结
SO2对人类是有“功”还是有“过”呢?
小组辩论
我们的收获
二氧化硫
二氧化硫与水反应
(物质分类的角度)
还原性
(氧化还原的角度)
漂白性
(特性的角度)
酸雨与
二氧化硫
环保化学
从生活到化学
二氧化硫的
物理性质
绿色化学
从化学到生活
二氧化硫
在生活中的应用
