人教版初中化学九年级上册3.3 元素 课件(24张PPT)
文档属性
| 名称 | 人教版初中化学九年级上册3.3 元素 课件(24张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-08 00:00:00 | ||
图片预览







文档简介
课题3 元素
元素名称
化学元素的拉丁文名称都具有一定含义,如为了纪念发现地点、发现者的祖国,或是为了纪念某科学家,或是为了表示这一元素的某一特性。
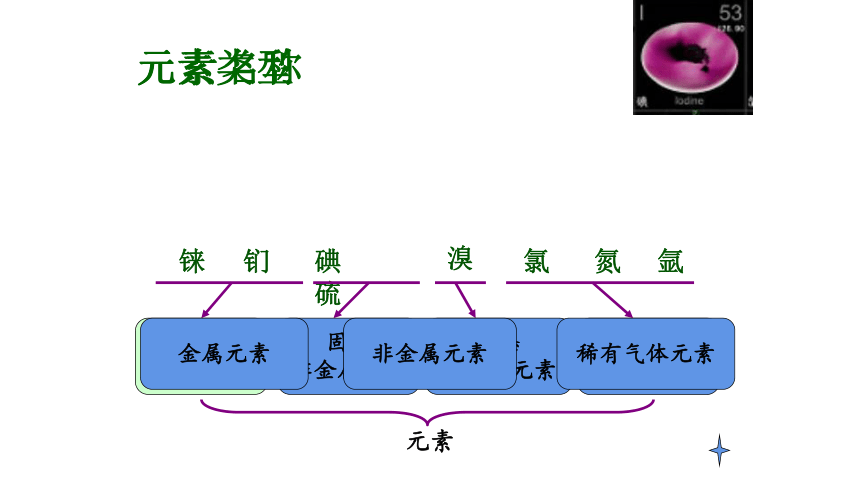
碘 硫
金属元素
固态
非金属元素
液态
非金属元素
气态
非金属元素
元素
铼 钔
氯 氮
溴
氩
金属元素
非金属元素
稀有气体元素
元素类型
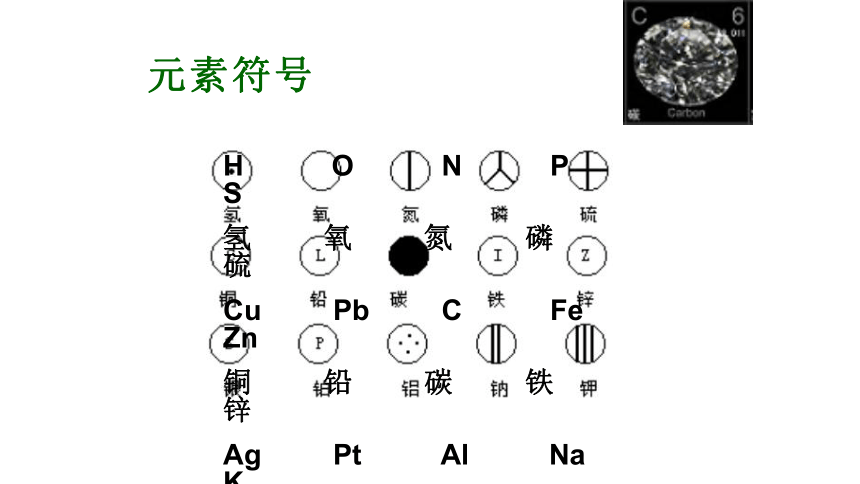
元素符号
H O N P S
氢 氧 氮 磷 硫
Cu Pb C Fe Zn
铜 铅 碳 铁 锌
Ag Pt Al Na K
银 铂 铝 钠 钾
(1)由一个字母表示的元素符号要大写,如:O、N、P、S
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如:Al、Na、He、Cu、Ca、Hg
1、元素符号的写法
元素符号
将下列写错的元素符号加以改正
铜CU, 锌 ZN, 银AG, 氯cl, 钙cA
铜Cu, 锌 Zn, 银Ag, 氯Cl, 钙Ca
2、元素符号的意义
宏观上:表示氧元素
微观上:表示一个氧原子
宏观上:表示一种元素
微观上:表示这种元素的一个原子
O
2O
表示两个氧原子
元素符号前面一旦有了数字,
就失去了宏观意义,
只表示微观意义。
请说出下列元素符号的意义
H 2S
Cl 2C
练一练
H
C
Na
O
Fe
S
K
Ca
S
元
素
周
期
表
如何将这些元素有序的编排起来?
事情的发展或运动遵循连续重复的规律
1829年,德国耶那大学的化学教授德贝莱纳(D Obereiner)根据元素性质的相似性,提出了“三素组”学说。
但是,在当时已发现的54种元素中却只能把15种元素归入“三素组”。
1865年,英国人纽兰兹(Newlands)把当时已知的元素按原子量由小到大的顺序排列,发现每7种元素之后,会重复出现相似的性质。他把他的发现称为“八音律”,就象音乐里的八度音阶一样。
性质相似元素周期性出现
Li
Be
B
C
N
O
F
Ne
Na
Mg
Al
Si
P
S
Cl
Ar
He
H
C
B
O
F
Li
He
Be
N
H
H
He
Li
Be
B
C
N
O
F
Ne
Na
Mg
Al
Si
P
S
Cl
Ar
H
He
Li
Be
B
C
N
O
F
Ne
Na
Mg
Al
Si
P
S
Cl
Ar
观整体:元素周期表有几横行?几纵行?
7横行——7个周期
18个纵行——16个族
13 Al
铝
26.98
原子序数
相对原子质量
元素符号
元素名称
看个别:元素周期表能给我们提供哪些信息?
原子序数=质子数=核电荷数
请从元素周期表中找到下列元素,并查询这些元素的相关信息(位置、原子序数、元素符号、相对原子质量等)
氧 碳 氮 钙
练一练
元素周期表前18号元素
找规律:同一周期中,关注元素的种类,
你能看出什么规律?
Na
11钠
H
1氢
Li
3锂
Be
4铍
B
5硼
C
6碳
N
7氮
O
8氧
F
9氟
Ne
10氖
Mg
12镁
Al
13铝
Si
14硅
P
15磷
S
16硫
Cl
17氯
Ar
18氩
He
2氦
Li
3锂
Be
4铍
Mg
12镁
Al
13铝
Na
11钠
Ne
10氖
Ar
18氩
He
2氦
金属 非金属 稀有气体
元素的类型、性质均呈现周期性变化规律
元素周期表前18号元素
(2)同一族从上到下:(电子层数/最外层电子数)
(1)同周期从左到右:(质子数/电子层数/最外层电子数)
从原子结构上能看出哪些规律?
②电子层数相同
1.同周期元素的原子(从左到右):
2.同一族元素的原子(从上到下):
①质子数依次递增
③最外层电子数从1递增到8,呈周期性变化
②最外层电子数相同
①电子层数依次增加
元素的原子结构呈现周期性变化
元素的化学性质呈现周期性变化
同族元素最外层电子数相同
同族元素具有相似的化学性质
练习:1、下表为元素周期表的部分元素的相关信息,利用下表回答相关问题:
练习:2、下表为元素周期表的部分元素的相关信息,利用下表回答相关问题
通过这堂课的学习,你有哪些收获?
1、元素符号的写法
三、元素符号
2、元素符号的意义
(1)表示元素 (宏观)
(2)表示该元素的一个原子(微观)
四、元素周期表简介
原子序数=质子数=核电荷数
一、元素名称
总 结
二、元素类型
元素名称
化学元素的拉丁文名称都具有一定含义,如为了纪念发现地点、发现者的祖国,或是为了纪念某科学家,或是为了表示这一元素的某一特性。
碘 硫
金属元素
固态
非金属元素
液态
非金属元素
气态
非金属元素
元素
铼 钔
氯 氮
溴
氩
金属元素
非金属元素
稀有气体元素
元素类型
元素符号
H O N P S
氢 氧 氮 磷 硫
Cu Pb C Fe Zn
铜 铅 碳 铁 锌
Ag Pt Al Na K
银 铂 铝 钠 钾
(1)由一个字母表示的元素符号要大写,如:O、N、P、S
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如:Al、Na、He、Cu、Ca、Hg
1、元素符号的写法
元素符号
将下列写错的元素符号加以改正
铜CU, 锌 ZN, 银AG, 氯cl, 钙cA
铜Cu, 锌 Zn, 银Ag, 氯Cl, 钙Ca
2、元素符号的意义
宏观上:表示氧元素
微观上:表示一个氧原子
宏观上:表示一种元素
微观上:表示这种元素的一个原子
O
2O
表示两个氧原子
元素符号前面一旦有了数字,
就失去了宏观意义,
只表示微观意义。
请说出下列元素符号的意义
H 2S
Cl 2C
练一练
H
C
Na
O
Fe
S
K
Ca
S
元
素
周
期
表
如何将这些元素有序的编排起来?
事情的发展或运动遵循连续重复的规律
1829年,德国耶那大学的化学教授德贝莱纳(D Obereiner)根据元素性质的相似性,提出了“三素组”学说。
但是,在当时已发现的54种元素中却只能把15种元素归入“三素组”。
1865年,英国人纽兰兹(Newlands)把当时已知的元素按原子量由小到大的顺序排列,发现每7种元素之后,会重复出现相似的性质。他把他的发现称为“八音律”,就象音乐里的八度音阶一样。
性质相似元素周期性出现
Li
Be
B
C
N
O
F
Ne
Na
Mg
Al
Si
P
S
Cl
Ar
He
H
C
B
O
F
Li
He
Be
N
H
H
He
Li
Be
B
C
N
O
F
Ne
Na
Mg
Al
Si
P
S
Cl
Ar
H
He
Li
Be
B
C
N
O
F
Ne
Na
Mg
Al
Si
P
S
Cl
Ar
观整体:元素周期表有几横行?几纵行?
7横行——7个周期
18个纵行——16个族
13 Al
铝
26.98
原子序数
相对原子质量
元素符号
元素名称
看个别:元素周期表能给我们提供哪些信息?
原子序数=质子数=核电荷数
请从元素周期表中找到下列元素,并查询这些元素的相关信息(位置、原子序数、元素符号、相对原子质量等)
氧 碳 氮 钙
练一练
元素周期表前18号元素
找规律:同一周期中,关注元素的种类,
你能看出什么规律?
Na
11钠
H
1氢
Li
3锂
Be
4铍
B
5硼
C
6碳
N
7氮
O
8氧
F
9氟
Ne
10氖
Mg
12镁
Al
13铝
Si
14硅
P
15磷
S
16硫
Cl
17氯
Ar
18氩
He
2氦
Li
3锂
Be
4铍
Mg
12镁
Al
13铝
Na
11钠
Ne
10氖
Ar
18氩
He
2氦
金属 非金属 稀有气体
元素的类型、性质均呈现周期性变化规律
元素周期表前18号元素
(2)同一族从上到下:(电子层数/最外层电子数)
(1)同周期从左到右:(质子数/电子层数/最外层电子数)
从原子结构上能看出哪些规律?
②电子层数相同
1.同周期元素的原子(从左到右):
2.同一族元素的原子(从上到下):
①质子数依次递增
③最外层电子数从1递增到8,呈周期性变化
②最外层电子数相同
①电子层数依次增加
元素的原子结构呈现周期性变化
元素的化学性质呈现周期性变化
同族元素最外层电子数相同
同族元素具有相似的化学性质
练习:1、下表为元素周期表的部分元素的相关信息,利用下表回答相关问题:
练习:2、下表为元素周期表的部分元素的相关信息,利用下表回答相关问题
通过这堂课的学习,你有哪些收获?
1、元素符号的写法
三、元素符号
2、元素符号的意义
(1)表示元素 (宏观)
(2)表示该元素的一个原子(微观)
四、元素周期表简介
原子序数=质子数=核电荷数
一、元素名称
总 结
二、元素类型
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
