鲁教版九年级化学第二单元第四节元素课后练习(含解析)
文档属性
| 名称 | 鲁教版九年级化学第二单元第四节元素课后练习(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 117.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-09 00:00:00 | ||
图片预览




文档简介
第二单元第四节元素课后练习
学校:___________姓名:___________班级:___________考号:___________
一、单选题
市场上有“加碘食盐”、“富硒酱油”、“高钙牛奶”等商品,这里的“碘、硒、钙”指的是
A.
元素
B.
分子
C.
离子
D.
原子
氢元素与氧元素的本质区别在于原子的
A.
质子数不同
B.
电子数不同
C.
电子层数不同
D.
最外层电子数不同
下列物质组合中,前者属于化合物,后者属于混合物的是
A.
氧气、空气
B.
四氧化三铁、氧化汞
C.
红磷、五氧化二磷
D.
蒸馏水、矿泉水
下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是
A.
Ne
B.
O
C.
D.
CO
逻辑推理是化学学习中常用的思维方法,以下推理完全正确的是
A.
离子化合物是由阴阳离子构成的,所以阴阳离子构成的化合物是离子化合物。
B.
同种元素的粒子具有相同的质子数,所以质子数相同的粒子属于同种元素。
C.
化学性质相似的原子最外层电子数相同,所以最外层电子数相同的原子化学性质相似。
D.
单质都是由同种元素组成的,所以同种元素组成的物质是单质。
硒在元素周期表中的某些信息如图,下列说法不正确的是
A.
硒属于非金属元素
B.
硒原子的中子数是34
C.
硒原子的质子数是34
D.
硒的相对原子质量是
下列因果关系错误的是
A.
因为分子构成不同,所以水和过氧化氢的化学性质不同
B.
因为质子数不同,所以碳原子和氮原子所属的元素种类不同
C.
因为所含元素种类不同,所以纯净物可分为单质和化合物
D.
因为原子的最外层电子数相同,所以氦元素和镁元素的化学性质相似
“归纳推理”是化学学习过程中常用的思维方法,以下类推结果正确的是
A.
、的最外层电子数均为8,则最外层电子数为8的粒子都是离子
B.
单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质
C.
元素是指具有相同质子数的一类原子的总称,具有相同质子数的粒子一定是同种元素
D.
化学变化中分子种类发生改变,则分子种类发生改变的变化一定是化学变化
分类是研究物质的常用方法。下列分类中正确的是
A.
纯净物:氧气、二氧化碳、洁净的空气
B.
混合物:水泥砂浆、人呼出的气体、冰水共存物
C.
单质:氦气、汞、液氮
D.
化合物:硬水、二氧化锰、氯化钾
元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,下列有关说法正确的是
A.
铁的相对原子质量为
B.
锰元素为非金属元素
C.
铬原子的原子核内有52个质子
D.
等质量的铬、锰、铁中,含原子个数最多的是铬
二、填空题
在宏观、微观和符号之间律立联系是化学学科的特点。
如图中甲是______。
在汞氮气氯化钠水二氧化碳五种物质中,由原子构成的是______,由离子构成的是______填序号。
有下列物质,水
氧气
二氧化碳
铁粉
空气
自来水
五氧化二磷
高锰酸钾
澄清石灰水.用序号填空:
属于纯净物的有______,属于混合物的有______;属于单质的有______,属于化合物的有______.
写出元素符号Ar的含义:________________________;
________________________;
________________________;
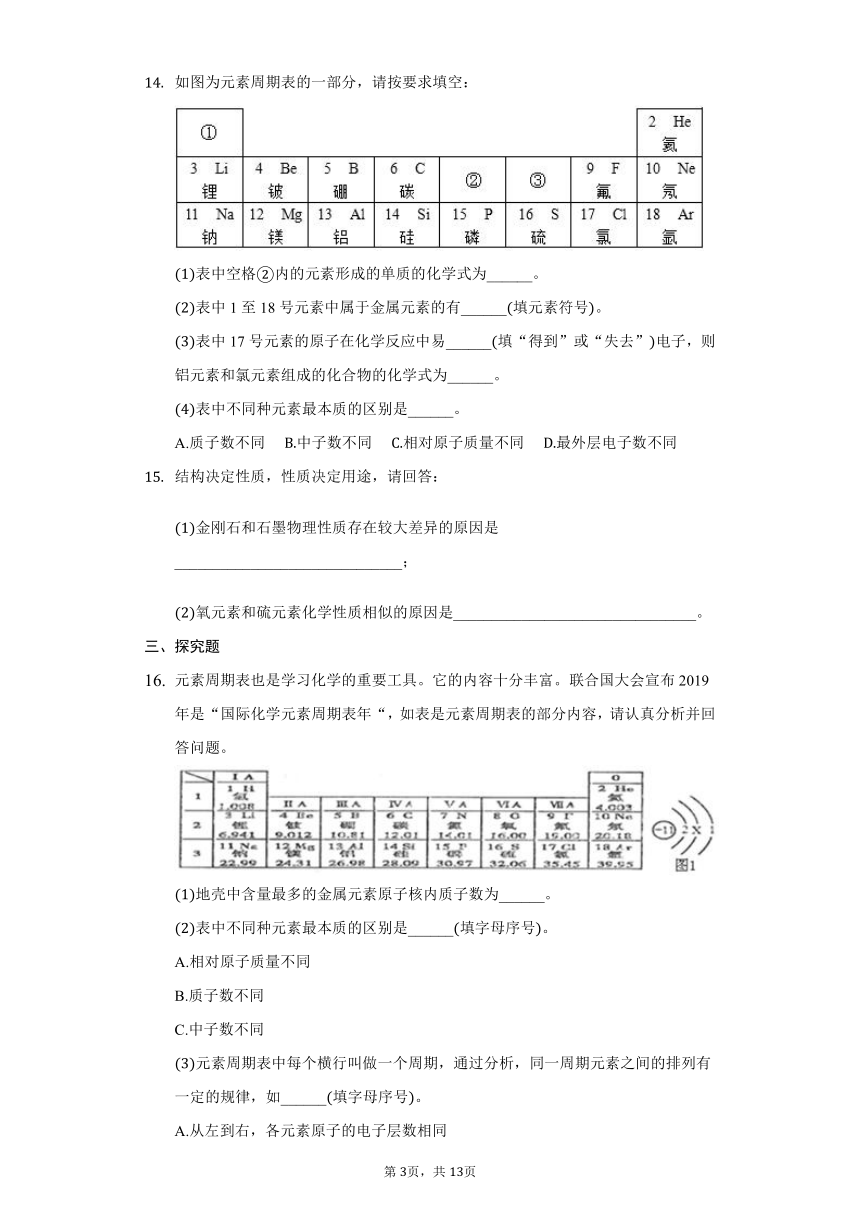
如图为元素周期表的一部分,请按要求填空:
表中空格内的元素形成的单质的化学式为______。
表中1至18号元素中属于金属元素的有______填元素符号。
表中17号元素的原子在化学反应中易______填“得到”或“失去”电子,则铝元素和氯元素组成的化合物的化学式为______。
表中不同种元素最本质的区别是______。
A.质子数不同???
中子数不同???
相对原子质量不同???
最外层电子数不同
结构决定性质,性质决定用途,请回答:
金刚石和石墨物理性质存在较大差异的原因是______________________________;
氧元素和硫元素化学性质相似的原因是________________________________。
三、探究题
元素周期表也是学习化学的重要工具。它的内容十分丰富。联合国大会宣布2019年是“国际化学元素周期表年“,如表是元素周期表的部分内容,请认真分析并回答问题。
地壳中含量最多的金属元素原子核内质子数为______。
表中不同种元素最本质的区别是______填字母序号。
A.相对原子质量不同
B.质子数不同
C.中子数不同
元素周期表中每个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如______填字母序号。
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
模型是联系宏观与微观的桥梁,如图1是钠原子结构示意图,其中:
的数值为______;
“1”指的是______。
钠原子在化学反应中易______填“得到”或“失去”电子,形成______填离子符号。
我国纪念军成立70周年海上阅兵活动在青岛进行。建造航母、核潜艇等战舰时,常用稀有气体做焊接金属保护气。在元素周期表中,稀有气体元素氖与氩位于同一族,性质有许多相似之处,这也说明元素的化学性质与原子的______关系密切。
图中的、分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。试回答下列问题:
画出钠原子的原子结构示意图________________;
所表示的元素位于元素周期表的第________周期,C表示的粒子符号是________;
、B、C中属于同种元素的粒子是________;
和B两种粒子具有相似的化学性质,是因为它们的________相同,在化学反应中都容易________填“得到”或“失去”电子;
钠原子和氯原子反应所形成的化合物是由________填“分子”、“原子”或“离子”构成的。
答案和解析
1.【答案】A
【解析】
【分析】
本题考查物质的组成,知识物质由元素组成即可解答。
【解答】
物质是由元素组成的,加碘食盐”、“富硒酱油”、“高钙牛奶”等商品,这里的“碘、硒、钙”指的是元素。
故选A。
2.【答案】A
【解析】
【分析】
本题很简单,考查学生对元素的概念的理解和不同种元素之间的本质区别是质子数不同进行解题的能力。
【解答】
元素是具有相同核电荷数即核内质子数的一类原子的总称,不同种元素最本质的区别是核电荷数即核内质子数不同,所以氢元素与氧元素的本质区别在于原子的核电荷数即核内质子数不同。
故选A。
3.【答案】D
【解析】解:A、氧气是由氧元素组成的纯净物,属于单质,空气中含有氮气、氧气等物质,属于混合物;
B、四氧化三铁是由不同种元素组成的纯净物,属于化合物,氧化汞是由不同种元素组成的纯净物,属于化合物;
C、红磷是由磷元素组成的纯净物,属于单质,五氧化二磷是由不同种元素组成的纯净物,属于化合物;
D、蒸馏水是由不同种元素组成的纯净物,属于化合物,矿泉水中含有水和溶于水的矿物质,属于混合物。
故选:D。
纯净物由一种物质组成,混合物由两种或两种以上的物质组成;????????????????????????????????
??????????????????????????
单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物。
判断纯净物和混合物时,就是判断物质的物质组成;判断是否是单质、化合物时,既要判断元素组成,又要判断物质组成。
4.【答案】A
【解析】解:元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符号又是化学式时,就同时具备了上述三层意义。
A、Ne属于稀有气体元素,可表示氖元素,表示一个氖原子,还能表示氖气这一纯净物,故选项正确。
B、O属于气态非金属元素,可表示氧元素,表示一个氧原子,但不能表示一种物质,故选项错误。
C、该符号是氮气的化学式,不是元素符号,故选项错误。
D、该符号是一氧化氮的化学式,不是元素符号,故选项错误。
故选:A。
根据化学式与元素符号的含义进行分析解答,金属、大多数固体非金属等都是由原子直接构成的,故它们的元素符号,既能表示一个原子,又能表示一种元素,还能表示一种物质。
本题难度不大,掌握由原子构成的物质的化学式一般有三层含义宏观:表示一种元素、一种单质,微观:表示一个原子是正确解答此类题的关键。
5.【答案】A
【解析】
【分析】
本题考查了有关的概念,完成此题,可以依据已有的知识进行。要求同学们熟练理解有关的基本概念,以便灵活应用。
【解答】
A.离子化合物是由阴阳离子构成的,所以阴阳离子构成的化合物是离子化合物,故A正确;
B.质子数相同的一类原子是同种元素,但质子数相同的粒子,不一定是同种元素,如水分子和氖原子质子数都是10,但不属于同种元素,故B错误;
C.原子的最外层电子数相同其化学性质不一定相似,比如氦原子和镁原子,故C错误;
D.单质是由同种元素组成的纯净物,但是由同种元素组成的物质不一定是单质,例如氧气和臭氧组成的物质只含有一种元素,但不是单质,是混合物,故D错误。
故选A。
6.【答案】B
【解析】
【分析】
本题难度不大,考查学生灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量进行分析解题的能力。
【解答】
A.中间的汉字表示元素名称,该元素的名称是硒,属于非金属元素,故选项A说法正确;
B.左上角的数字为34,该元素的原子序数为34,则该元素的核内质子数为34,其中子数相对原子质量质子数,故选项B说法不正确;
C.左上角的数字为34,表示原子序数为34;根据原子中,原子序数核电荷数质子数核外电子数,则硒原子中的质子数为34,故选项C说法正确;
D.汉字下面的数字表示相对原子质量,该元素的相对原子质量为,故选项D说法正确。
故选B。
7.【答案】D
【解析】解:A、结构决定性质,因为分子构成不同,所以水和过氧化氢的化学性质不同,故A因果关系正确;
B、质子数决定元素的种类,因为质子数不同,所以碳原子和氮原子所属的元素种类不同,故B因果关系正确;
C、根据纯净物中所含元素种类的多少,将纯净物可分为单质含一种元素和化合物含两种或两种以上元素,故C因果关系正确;
D、决定元素化学性质的是原子结构中的最外层电子数,但氦原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;镁原子的最外层电子数为2,在化学反应中易失去2个电子而形成阳离子,尽管最外层电子数相同,但它们化学性质不相似,故D因果关系错误。
故选:D。
A、根据分子的结构决定物质的性质分析;
B、根据元素的定义分析;
C、根据纯净物的分类依据分析;
D、根据原子的结构与原子性质之间的关系的特殊性分析。
本题主要考查物质的结构、性质分类方面的知识,解答时要理解物质的结构决定物质的性质,还应注意特殊性。
8.【答案】D
【解析】解:A、最外层电子数为8的粒子可能是稀有气体元素的原子,故选项错误;
B、单质是由同种元素组成的物质,由同种元素组成的物质一定是单质错误,如氧气和臭氧的混合物;故选项错误;
C、只有具有相同质子数的原子而不是粒子才一定是同种元素,如水分子和氖原子都含有10个质子,但属于不同元素,故选项错误;
D、化学变化是指有新物质即新分子生成的变化,所以分子种类发生改变的变化一定是化学变化,故选项正确。
故选:D。
A、最外层电子数为8的粒子可能是稀有气体元素的原子;
B、由同种元素组成的纯净物叫单质;
C、元素的种类是由核内质子数或核电荷数决定的;
D、根据化学变化的特点考虑。
本考点考查了元素的概念、物质的分类、构成物质的粒子,要加强记忆有关的知识点,并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空题中。
9.【答案】C
【解析】
【分析】
本题考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物等基本概念,并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空题中。
【解答】
A.纯净物是由一种物质组成,氧气、二氧化碳属于纯净物,洁净的空气中含有氮气,氧气等,属于混合物;故选项错误;
B.混合物是由两种或两种以上的物质组成,水泥砂浆、人呼出的气体属于混合物,冰水共存物中只有水分子,属于纯净物;故选项错误;
C.由同种元素组成的纯净物叫单质,氦气、汞、液氮都属于单质;故选项正确;
D.化合物是指由两种或两种以上元素组成的纯净物,二氧化锰、氯化钾属于化合物,硬水中含有多种物质,属于混合物;故选项错误。
故选C。
10.【答案】D
【解析】
【分析】
本题难度不大,考查学生灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量进行分析解题的能力。根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
【解答】
A.根据铁元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为,相对原子质量单位是“1”,不是“克”,故选项说法错误;
B.锰带“钅”字旁,属于金属元素,故选项说法错误;
C.根据铬元素周期表中的一格可知,左上角的数字为24,表示原子序数为24;根据原子中原子序数核电荷数质子数,则铬原子的原子核内有24个质子,故选项说法错误;
D.原子的相对原子质量与其实际质量是成正比,由于相对原子质量的大小关系是铁锰铬,真实质量也是这一关系,故等质量的三种原子中,所含原子个数由多到少的顺序是:铬锰铁,故所含原子个数最多的是铬原子,故选项说法正确。
故选D。
11.【答案】分子?
?
【解析】解:物质是由原子、分子、离子构成的,原子可以构成分子,则图中甲是分子。
汞属于金属单质,是由汞原子直接构成的。
氮气属于气态非金属单质,是由氮分子构成的。
氯化钠是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的。
水是由非金属元素组成的化合物,是由水分子构成的。
二氧化碳是由非金属元素组成的化合物,是由二氧化碳分子构成的。
故答案为:
分子;
;。
根据构成物质的粒子,进行分析解答。
根据金属、大多数固态非金属单质、稀有气体等由原子构成;有些物质是由分子构成的,气态的非金属单质和一般由非金属元素组成的化合物,如氢气、水等;有些物质是由离子构成的,一般是含有金属元素和非金属元素的化合物,如氯化钠,进行分析解答。
本题难度不大,主要考查了构成物质的微观粒子方面的知识,对物质进行分类与对号入座、掌握常见物质的粒子构成是正确解答本题的关键.
12.【答案】?
?
?
【解析】解:混合物是由两种或两种以上的物质组成,空气、自来水、澄清石灰水都属于混合物;纯净物是由一种物质组成,水、氧气、二氧化碳、铁粉、五氧化二磷、高锰酸钾都属于纯净物.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质,氧气、铁粉都属于单质;由两种或两种以上的元素组成的纯净物叫化合物,水、二氧化碳、五氧化二磷、高锰酸钾都属于化合物;故答案为:;;;;
物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成,空气、自来水、澄清石灰水都属于混合物;纯净物是由一种物质组成,水、氧气、二氧化碳、铁粉、五氧化二磷、高锰酸钾都属于纯净物.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质,氧气、铁粉都属于单质;由两种或两种以上的元素组成的纯净物叫化合物,水、二氧化碳、五氧化二磷、高锰酸钾都属于化合物.
本考点考查了物质的分类,物质的分类是历届中考的重点,学生在进行辨别时,往往误以元素种类的多少进行混合物与纯净物的判断,或者忽略了单质、化合物必须是纯净物这一大前提,本考点的基础性比较强,主要出现在选择题和填空题中.
13.【答案】表示氩气这种物质??
表示氩元素
表示一个氩原子
【解析】
【分析】
本题主要考查了元素符号的意义,题目较易。
【解答】元素符号可表示一种元素或这种元素的一个原子,由原子构成的物质其元素符号还表示这种物质,氩气是由原子构成的物质,故还可表示氩气这种物质,
故答案是:
表示氩气这种物质??
表示氩元素
表示一个氩原子
14.【答案】
?
Li、Be、Na、Mg、Al
?
得到
?
?
A
【解析】解:表中空格内的元素是氮元素,氮元素形成的单质是氮气,每个氮分子由2个氮原子构成,因此氮气的化学式为。
故填:。
表中1至18号元素中属于金属元素的有Li、Be、Na、Mg、Al。
故填:Li、Be、Na、Mg、Al。
表中17号元素氯元素的原子最外层电子数是7,在化学反应中易得到1个电子形成带1个单位负电荷的氯离子,在化合物中化合价是,铝原子最外层电子数是3,反应中容易失去3个电子形成带3个单位正电荷的铝离子,在化合物中化合价是,根据化合物中元素化合价代数和为零可知,铝元素和氯元素组成的化合物是氯化铝,可以表示为。
故填:。
表中不同种元素最本质的区别是质子数不同。
故填:A。
原子中,核电荷数核内质子数核外电子数原子序数;
元素是具有相同质子数的一类原子的总称;
元素核外电子层数是几,所处周期就是几;
一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,等于4的,既不容易得到电子,也不容易失去电子,最外层电子数是8的是一种稳定结构,第一层也是最外层时,达到2个电子也是一种稳定结构。
元素周期表反映了元素之间的内在联系,要注意理解和应用。
15.【答案】碳原子排列方式不同
最外层电子数相同
【解析】
【分析】
本题考查物质的性质以及元素的化学性质,物质的性质有多种,要分清物质的用途是由那种性质决定的。
【解答】
因为金刚石、石墨的内部碳原子的排列方式不同,导致两种物质物理性质差异很大;故填:碳原子排列方式不同;
氧元素和硫元素的最外层电子数相同,所以它们有相似的化学性质;故填:最外层电子数相同。
16.【答案】13?
B?
AB?
8?
最外层电子数?
失去?
?
最外层电子数
【解析】解:地壳中含量最多的金属元素是铝元素,其原子核内质子数为13。
表中不同种元素最本质的区别是质子数不同。
从左到右,各元素原子的电子层数相同,正确;
B.从左到右,各元素原子的原子序数依次增加,正确;
C.从左到右,各元素原子的最外层电子数依次增加,错误;
模型是联系宏观与微观的桥梁,如图1是钠原子结构示意图,其中:
据图可以看出,X的数值为;
“1”指的是最外层电子数。
钠原子在化学反应中易失去电子,形成带一个单位的正电荷的。
在元素周期表中,稀有气体元素氖与氩位于同一族,性质有许多相似之处,这也说明元素的化学性质与原子的最外层电子数关系密切。
故答案为:;
;
;
;
最外层电子数;
失去;;
最外层电子数。
根据元素周期表的意义以及原子结构的知识进行分析解答即可。
本题考查的是元素周期表的知识,完成此题,可以依据已有的知识进行。
17.【答案】
?
二;
?
?
最外层电子数;得到
?
离子
【解析】
【分析】
本题考查学生对在原子中,原子序数,质子数,核外电子数,核电荷数之间的关系及元素的最外层电子数决定元素的化学性质的理解与掌握。
【解答】
根据原子序数核电荷数质子数,则钠元素的原子核内质子数为11;钠原子核内有11个质子,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有1个电子,其原子结构示意图为;故填:;
原子核外有2个电子层,故位于第二周期;C表示的粒子表示氯离子,其符号为,故填:二;;
根据决定元素种类的是核电荷数即核内质子数,因为BC的核内质子数相同,所以BC属于同种元素的粒子;故填:BC;
由图示可知A、B两者的最外层电子数相同,都是7,所以它们具有相似的化学性质,在化学反应中都容易得到电子;故填:最外层电子数;得到;
钠原子和氯原子反应所形成的化合物中含有钠离子和氯离子,所以氯化钠是由离子构成;故填:离子。
第6页,共13页
第5页,共13页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
市场上有“加碘食盐”、“富硒酱油”、“高钙牛奶”等商品,这里的“碘、硒、钙”指的是
A.
元素
B.
分子
C.
离子
D.
原子
氢元素与氧元素的本质区别在于原子的
A.
质子数不同
B.
电子数不同
C.
电子层数不同
D.
最外层电子数不同
下列物质组合中,前者属于化合物,后者属于混合物的是
A.
氧气、空气
B.
四氧化三铁、氧化汞
C.
红磷、五氧化二磷
D.
蒸馏水、矿泉水
下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是
A.
Ne
B.
O
C.
D.
CO
逻辑推理是化学学习中常用的思维方法,以下推理完全正确的是
A.
离子化合物是由阴阳离子构成的,所以阴阳离子构成的化合物是离子化合物。
B.
同种元素的粒子具有相同的质子数,所以质子数相同的粒子属于同种元素。
C.
化学性质相似的原子最外层电子数相同,所以最外层电子数相同的原子化学性质相似。
D.
单质都是由同种元素组成的,所以同种元素组成的物质是单质。
硒在元素周期表中的某些信息如图,下列说法不正确的是
A.
硒属于非金属元素
B.
硒原子的中子数是34
C.
硒原子的质子数是34
D.
硒的相对原子质量是
下列因果关系错误的是
A.
因为分子构成不同,所以水和过氧化氢的化学性质不同
B.
因为质子数不同,所以碳原子和氮原子所属的元素种类不同
C.
因为所含元素种类不同,所以纯净物可分为单质和化合物
D.
因为原子的最外层电子数相同,所以氦元素和镁元素的化学性质相似
“归纳推理”是化学学习过程中常用的思维方法,以下类推结果正确的是
A.
、的最外层电子数均为8,则最外层电子数为8的粒子都是离子
B.
单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质
C.
元素是指具有相同质子数的一类原子的总称,具有相同质子数的粒子一定是同种元素
D.
化学变化中分子种类发生改变,则分子种类发生改变的变化一定是化学变化
分类是研究物质的常用方法。下列分类中正确的是
A.
纯净物:氧气、二氧化碳、洁净的空气
B.
混合物:水泥砂浆、人呼出的气体、冰水共存物
C.
单质:氦气、汞、液氮
D.
化合物:硬水、二氧化锰、氯化钾
元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,下列有关说法正确的是
A.
铁的相对原子质量为
B.
锰元素为非金属元素
C.
铬原子的原子核内有52个质子
D.
等质量的铬、锰、铁中,含原子个数最多的是铬
二、填空题
在宏观、微观和符号之间律立联系是化学学科的特点。
如图中甲是______。
在汞氮气氯化钠水二氧化碳五种物质中,由原子构成的是______,由离子构成的是______填序号。
有下列物质,水
氧气
二氧化碳
铁粉
空气
自来水
五氧化二磷
高锰酸钾
澄清石灰水.用序号填空:
属于纯净物的有______,属于混合物的有______;属于单质的有______,属于化合物的有______.
写出元素符号Ar的含义:________________________;
________________________;
________________________;
如图为元素周期表的一部分,请按要求填空:
表中空格内的元素形成的单质的化学式为______。
表中1至18号元素中属于金属元素的有______填元素符号。
表中17号元素的原子在化学反应中易______填“得到”或“失去”电子,则铝元素和氯元素组成的化合物的化学式为______。
表中不同种元素最本质的区别是______。
A.质子数不同???
中子数不同???
相对原子质量不同???
最外层电子数不同
结构决定性质,性质决定用途,请回答:
金刚石和石墨物理性质存在较大差异的原因是______________________________;
氧元素和硫元素化学性质相似的原因是________________________________。
三、探究题
元素周期表也是学习化学的重要工具。它的内容十分丰富。联合国大会宣布2019年是“国际化学元素周期表年“,如表是元素周期表的部分内容,请认真分析并回答问题。
地壳中含量最多的金属元素原子核内质子数为______。
表中不同种元素最本质的区别是______填字母序号。
A.相对原子质量不同
B.质子数不同
C.中子数不同
元素周期表中每个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如______填字母序号。
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
模型是联系宏观与微观的桥梁,如图1是钠原子结构示意图,其中:
的数值为______;
“1”指的是______。
钠原子在化学反应中易______填“得到”或“失去”电子,形成______填离子符号。
我国纪念军成立70周年海上阅兵活动在青岛进行。建造航母、核潜艇等战舰时,常用稀有气体做焊接金属保护气。在元素周期表中,稀有气体元素氖与氩位于同一族,性质有许多相似之处,这也说明元素的化学性质与原子的______关系密切。
图中的、分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。试回答下列问题:
画出钠原子的原子结构示意图________________;
所表示的元素位于元素周期表的第________周期,C表示的粒子符号是________;
、B、C中属于同种元素的粒子是________;
和B两种粒子具有相似的化学性质,是因为它们的________相同,在化学反应中都容易________填“得到”或“失去”电子;
钠原子和氯原子反应所形成的化合物是由________填“分子”、“原子”或“离子”构成的。
答案和解析
1.【答案】A
【解析】
【分析】
本题考查物质的组成,知识物质由元素组成即可解答。
【解答】
物质是由元素组成的,加碘食盐”、“富硒酱油”、“高钙牛奶”等商品,这里的“碘、硒、钙”指的是元素。
故选A。
2.【答案】A
【解析】
【分析】
本题很简单,考查学生对元素的概念的理解和不同种元素之间的本质区别是质子数不同进行解题的能力。
【解答】
元素是具有相同核电荷数即核内质子数的一类原子的总称,不同种元素最本质的区别是核电荷数即核内质子数不同,所以氢元素与氧元素的本质区别在于原子的核电荷数即核内质子数不同。
故选A。
3.【答案】D
【解析】解:A、氧气是由氧元素组成的纯净物,属于单质,空气中含有氮气、氧气等物质,属于混合物;
B、四氧化三铁是由不同种元素组成的纯净物,属于化合物,氧化汞是由不同种元素组成的纯净物,属于化合物;
C、红磷是由磷元素组成的纯净物,属于单质,五氧化二磷是由不同种元素组成的纯净物,属于化合物;
D、蒸馏水是由不同种元素组成的纯净物,属于化合物,矿泉水中含有水和溶于水的矿物质,属于混合物。
故选:D。
纯净物由一种物质组成,混合物由两种或两种以上的物质组成;????????????????????????????????
??????????????????????????
单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物。
判断纯净物和混合物时,就是判断物质的物质组成;判断是否是单质、化合物时,既要判断元素组成,又要判断物质组成。
4.【答案】A
【解析】解:元素符号能表示一种元素,还能表示该元素的一个原子;化学式能表示一种物质,当元素符号又是化学式时,就同时具备了上述三层意义。
A、Ne属于稀有气体元素,可表示氖元素,表示一个氖原子,还能表示氖气这一纯净物,故选项正确。
B、O属于气态非金属元素,可表示氧元素,表示一个氧原子,但不能表示一种物质,故选项错误。
C、该符号是氮气的化学式,不是元素符号,故选项错误。
D、该符号是一氧化氮的化学式,不是元素符号,故选项错误。
故选:A。
根据化学式与元素符号的含义进行分析解答,金属、大多数固体非金属等都是由原子直接构成的,故它们的元素符号,既能表示一个原子,又能表示一种元素,还能表示一种物质。
本题难度不大,掌握由原子构成的物质的化学式一般有三层含义宏观:表示一种元素、一种单质,微观:表示一个原子是正确解答此类题的关键。
5.【答案】A
【解析】
【分析】
本题考查了有关的概念,完成此题,可以依据已有的知识进行。要求同学们熟练理解有关的基本概念,以便灵活应用。
【解答】
A.离子化合物是由阴阳离子构成的,所以阴阳离子构成的化合物是离子化合物,故A正确;
B.质子数相同的一类原子是同种元素,但质子数相同的粒子,不一定是同种元素,如水分子和氖原子质子数都是10,但不属于同种元素,故B错误;
C.原子的最外层电子数相同其化学性质不一定相似,比如氦原子和镁原子,故C错误;
D.单质是由同种元素组成的纯净物,但是由同种元素组成的物质不一定是单质,例如氧气和臭氧组成的物质只含有一种元素,但不是单质,是混合物,故D错误。
故选A。
6.【答案】B
【解析】
【分析】
本题难度不大,考查学生灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量进行分析解题的能力。
【解答】
A.中间的汉字表示元素名称,该元素的名称是硒,属于非金属元素,故选项A说法正确;
B.左上角的数字为34,该元素的原子序数为34,则该元素的核内质子数为34,其中子数相对原子质量质子数,故选项B说法不正确;
C.左上角的数字为34,表示原子序数为34;根据原子中,原子序数核电荷数质子数核外电子数,则硒原子中的质子数为34,故选项C说法正确;
D.汉字下面的数字表示相对原子质量,该元素的相对原子质量为,故选项D说法正确。
故选B。
7.【答案】D
【解析】解:A、结构决定性质,因为分子构成不同,所以水和过氧化氢的化学性质不同,故A因果关系正确;
B、质子数决定元素的种类,因为质子数不同,所以碳原子和氮原子所属的元素种类不同,故B因果关系正确;
C、根据纯净物中所含元素种类的多少,将纯净物可分为单质含一种元素和化合物含两种或两种以上元素,故C因果关系正确;
D、决定元素化学性质的是原子结构中的最外层电子数,但氦原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;镁原子的最外层电子数为2,在化学反应中易失去2个电子而形成阳离子,尽管最外层电子数相同,但它们化学性质不相似,故D因果关系错误。
故选:D。
A、根据分子的结构决定物质的性质分析;
B、根据元素的定义分析;
C、根据纯净物的分类依据分析;
D、根据原子的结构与原子性质之间的关系的特殊性分析。
本题主要考查物质的结构、性质分类方面的知识,解答时要理解物质的结构决定物质的性质,还应注意特殊性。
8.【答案】D
【解析】解:A、最外层电子数为8的粒子可能是稀有气体元素的原子,故选项错误;
B、单质是由同种元素组成的物质,由同种元素组成的物质一定是单质错误,如氧气和臭氧的混合物;故选项错误;
C、只有具有相同质子数的原子而不是粒子才一定是同种元素,如水分子和氖原子都含有10个质子,但属于不同元素,故选项错误;
D、化学变化是指有新物质即新分子生成的变化,所以分子种类发生改变的变化一定是化学变化,故选项正确。
故选:D。
A、最外层电子数为8的粒子可能是稀有气体元素的原子;
B、由同种元素组成的纯净物叫单质;
C、元素的种类是由核内质子数或核电荷数决定的;
D、根据化学变化的特点考虑。
本考点考查了元素的概念、物质的分类、构成物质的粒子,要加强记忆有关的知识点,并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空题中。
9.【答案】C
【解析】
【分析】
本题考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物等基本概念,并能够区分应用。本考点的基础性比较强,主要出现在选择题和填空题中。
【解答】
A.纯净物是由一种物质组成,氧气、二氧化碳属于纯净物,洁净的空气中含有氮气,氧气等,属于混合物;故选项错误;
B.混合物是由两种或两种以上的物质组成,水泥砂浆、人呼出的气体属于混合物,冰水共存物中只有水分子,属于纯净物;故选项错误;
C.由同种元素组成的纯净物叫单质,氦气、汞、液氮都属于单质;故选项正确;
D.化合物是指由两种或两种以上元素组成的纯净物,二氧化锰、氯化钾属于化合物,硬水中含有多种物质,属于混合物;故选项错误。
故选C。
10.【答案】D
【解析】
【分析】
本题难度不大,考查学生灵活运用元素周期表中元素的信息原子序数、元素符号、元素名称、相对原子质量进行分析解题的能力。根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
【解答】
A.根据铁元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为,相对原子质量单位是“1”,不是“克”,故选项说法错误;
B.锰带“钅”字旁,属于金属元素,故选项说法错误;
C.根据铬元素周期表中的一格可知,左上角的数字为24,表示原子序数为24;根据原子中原子序数核电荷数质子数,则铬原子的原子核内有24个质子,故选项说法错误;
D.原子的相对原子质量与其实际质量是成正比,由于相对原子质量的大小关系是铁锰铬,真实质量也是这一关系,故等质量的三种原子中,所含原子个数由多到少的顺序是:铬锰铁,故所含原子个数最多的是铬原子,故选项说法正确。
故选D。
11.【答案】分子?
?
【解析】解:物质是由原子、分子、离子构成的,原子可以构成分子,则图中甲是分子。
汞属于金属单质,是由汞原子直接构成的。
氮气属于气态非金属单质,是由氮分子构成的。
氯化钠是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的。
水是由非金属元素组成的化合物,是由水分子构成的。
二氧化碳是由非金属元素组成的化合物,是由二氧化碳分子构成的。
故答案为:
分子;
;。
根据构成物质的粒子,进行分析解答。
根据金属、大多数固态非金属单质、稀有气体等由原子构成;有些物质是由分子构成的,气态的非金属单质和一般由非金属元素组成的化合物,如氢气、水等;有些物质是由离子构成的,一般是含有金属元素和非金属元素的化合物,如氯化钠,进行分析解答。
本题难度不大,主要考查了构成物质的微观粒子方面的知识,对物质进行分类与对号入座、掌握常见物质的粒子构成是正确解答本题的关键.
12.【答案】?
?
?
【解析】解:混合物是由两种或两种以上的物质组成,空气、自来水、澄清石灰水都属于混合物;纯净物是由一种物质组成,水、氧气、二氧化碳、铁粉、五氧化二磷、高锰酸钾都属于纯净物.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质,氧气、铁粉都属于单质;由两种或两种以上的元素组成的纯净物叫化合物,水、二氧化碳、五氧化二磷、高锰酸钾都属于化合物;故答案为:;;;;
物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成,空气、自来水、澄清石灰水都属于混合物;纯净物是由一种物质组成,水、氧气、二氧化碳、铁粉、五氧化二磷、高锰酸钾都属于纯净物.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质,氧气、铁粉都属于单质;由两种或两种以上的元素组成的纯净物叫化合物,水、二氧化碳、五氧化二磷、高锰酸钾都属于化合物.
本考点考查了物质的分类,物质的分类是历届中考的重点,学生在进行辨别时,往往误以元素种类的多少进行混合物与纯净物的判断,或者忽略了单质、化合物必须是纯净物这一大前提,本考点的基础性比较强,主要出现在选择题和填空题中.
13.【答案】表示氩气这种物质??
表示氩元素
表示一个氩原子
【解析】
【分析】
本题主要考查了元素符号的意义,题目较易。
【解答】元素符号可表示一种元素或这种元素的一个原子,由原子构成的物质其元素符号还表示这种物质,氩气是由原子构成的物质,故还可表示氩气这种物质,
故答案是:
表示氩气这种物质??
表示氩元素
表示一个氩原子
14.【答案】
?
Li、Be、Na、Mg、Al
?
得到
?
?
A
【解析】解:表中空格内的元素是氮元素,氮元素形成的单质是氮气,每个氮分子由2个氮原子构成,因此氮气的化学式为。
故填:。
表中1至18号元素中属于金属元素的有Li、Be、Na、Mg、Al。
故填:Li、Be、Na、Mg、Al。
表中17号元素氯元素的原子最外层电子数是7,在化学反应中易得到1个电子形成带1个单位负电荷的氯离子,在化合物中化合价是,铝原子最外层电子数是3,反应中容易失去3个电子形成带3个单位正电荷的铝离子,在化合物中化合价是,根据化合物中元素化合价代数和为零可知,铝元素和氯元素组成的化合物是氯化铝,可以表示为。
故填:。
表中不同种元素最本质的区别是质子数不同。
故填:A。
原子中,核电荷数核内质子数核外电子数原子序数;
元素是具有相同质子数的一类原子的总称;
元素核外电子层数是几,所处周期就是几;
一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,等于4的,既不容易得到电子,也不容易失去电子,最外层电子数是8的是一种稳定结构,第一层也是最外层时,达到2个电子也是一种稳定结构。
元素周期表反映了元素之间的内在联系,要注意理解和应用。
15.【答案】碳原子排列方式不同
最外层电子数相同
【解析】
【分析】
本题考查物质的性质以及元素的化学性质,物质的性质有多种,要分清物质的用途是由那种性质决定的。
【解答】
因为金刚石、石墨的内部碳原子的排列方式不同,导致两种物质物理性质差异很大;故填:碳原子排列方式不同;
氧元素和硫元素的最外层电子数相同,所以它们有相似的化学性质;故填:最外层电子数相同。
16.【答案】13?
B?
AB?
8?
最外层电子数?
失去?
?
最外层电子数
【解析】解:地壳中含量最多的金属元素是铝元素,其原子核内质子数为13。
表中不同种元素最本质的区别是质子数不同。
从左到右,各元素原子的电子层数相同,正确;
B.从左到右,各元素原子的原子序数依次增加,正确;
C.从左到右,各元素原子的最外层电子数依次增加,错误;
模型是联系宏观与微观的桥梁,如图1是钠原子结构示意图,其中:
据图可以看出,X的数值为;
“1”指的是最外层电子数。
钠原子在化学反应中易失去电子,形成带一个单位的正电荷的。
在元素周期表中,稀有气体元素氖与氩位于同一族,性质有许多相似之处,这也说明元素的化学性质与原子的最外层电子数关系密切。
故答案为:;
;
;
;
最外层电子数;
失去;;
最外层电子数。
根据元素周期表的意义以及原子结构的知识进行分析解答即可。
本题考查的是元素周期表的知识,完成此题,可以依据已有的知识进行。
17.【答案】
?
二;
?
?
最外层电子数;得到
?
离子
【解析】
【分析】
本题考查学生对在原子中,原子序数,质子数,核外电子数,核电荷数之间的关系及元素的最外层电子数决定元素的化学性质的理解与掌握。
【解答】
根据原子序数核电荷数质子数,则钠元素的原子核内质子数为11;钠原子核内有11个质子,核外有3个电子层,第一层上有2个电子、第二层上有8个电子,最外层上有1个电子,其原子结构示意图为;故填:;
原子核外有2个电子层,故位于第二周期;C表示的粒子表示氯离子,其符号为,故填:二;;
根据决定元素种类的是核电荷数即核内质子数,因为BC的核内质子数相同,所以BC属于同种元素的粒子;故填:BC;
由图示可知A、B两者的最外层电子数相同,都是7,所以它们具有相似的化学性质,在化学反应中都容易得到电子;故填:最外层电子数;得到;
钠原子和氯原子反应所形成的化合物中含有钠离子和氯离子,所以氯化钠是由离子构成;故填:离子。
第6页,共13页
第5页,共13页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
