2020年人教版九年级化学上学期第七单元 燃料及其利用压轴同步卷带答案
文档属性
| 名称 | 2020年人教版九年级化学上学期第七单元 燃料及其利用压轴同步卷带答案 |  | |
| 格式 | zip | ||
| 文件大小 | 192.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-10 20:36:59 | ||
图片预览




文档简介
2020年人教版九年级化学上学期第7单元《燃料及其利用》压轴同步卷
带答案
一.选择题(共10小题、每小题3分、共30分)
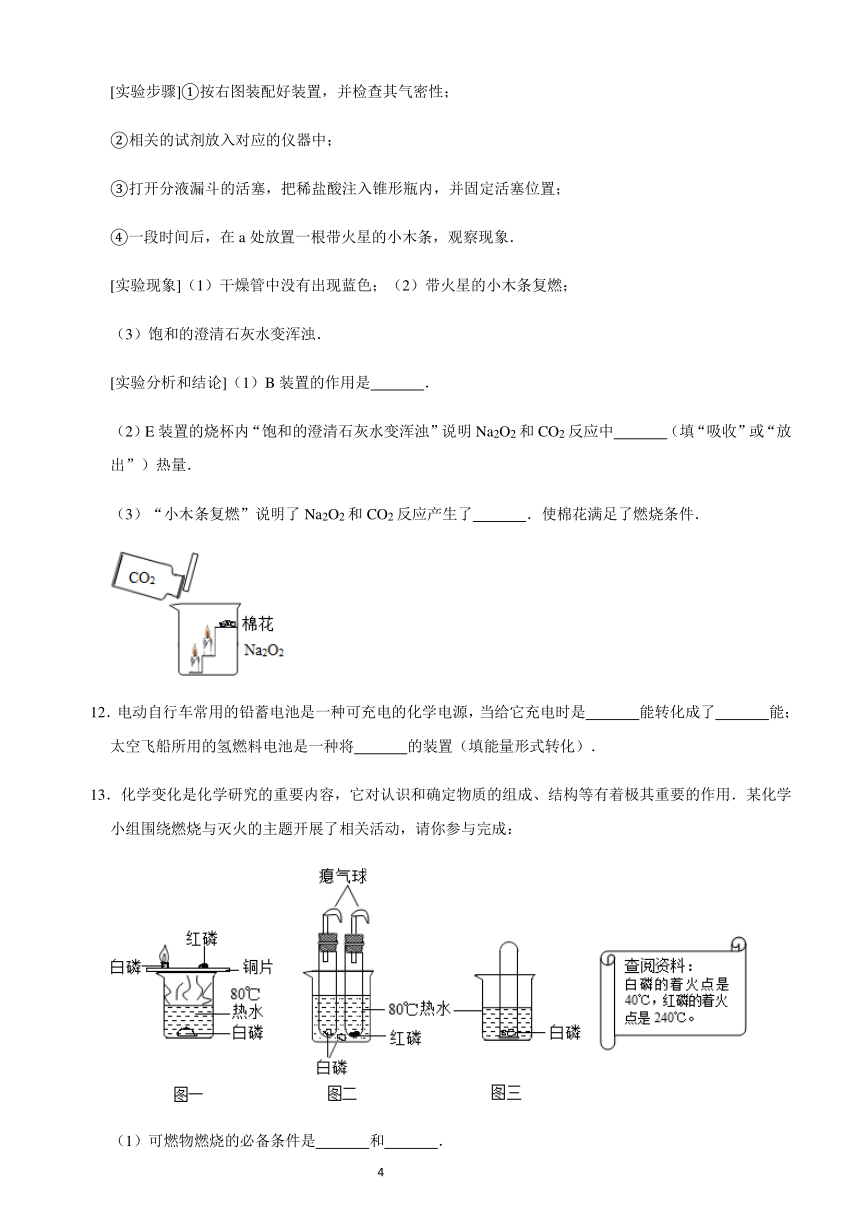
1.图甲和图乙所示实验方法均可用来探究可燃物燃烧的条件.
小颖同学用图乙所示装置进行实验,得到以下实验事实:
①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;
③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧.
该实验中,能证明可燃物通常需要接触空气才能燃烧的实验事实是( )
A.①②
B.③④
C.②④
D.①④
2.下列化学反应过程中,需要吸收热量的是( )
A.绿色植物光合作用
B.镁条与稀盐酸反应
C.蜡烛燃烧
D.农家肥的腐熟
3.吴宇森主导的电影《赤壁》中有这样的一个场面:吴蜀联军在船上装满枯枝浇足油,借着东南风向曹军驶去,接近曹军时点燃船上枯枝弃船而走.火借风势,火船宛如火龙一样冲向连在一起的
曹军木船.一眨眼,曹军水寨已经烧成一片火海.下列关于火海形成的叙述中,不正确的是( )
A.东南风降低了木船的着火点
B.枯枝和油为燃烧提供了充足的可燃物
C.东南风为木船燃烧提供了充足的氧气
D.相连的曹军木船没有及时隔离
4.野外烧火时,通常把木柴架空一些才能燃烧更旺,其原因是( )
A.可以降低木柴的着火点
B.使散热的速度加快
C.使木柴与空气的接触面积变大
D.便于提高温度
5.能源的开发和利用关系到社会的进步和发展,有关能源的认识错误的是( )
A.使煤等燃料充分燃烧能够节约化石燃料
B.使用天然气不会对环境造成任何污染
C.乙醇汽油的使用可以节省石油资源,减少汽车尾气的污染
D.开发新能源可解决能源短缺问题
6.下列灭火措施中不恰当的是( )
①炒菜时,锅里的油起火应采取的最佳灭火措施是端下油锅;
②秸秆、柴草着火,用水泼灭;
③熄灭酒精灯最好用嘴吹灭;
④电器着火,最先应当切断电源,再用干粉灭火器灭火;
⑤汽油着火,应该立即用水浇灭;
⑥洒在实验桌上的酒精着火,应用湿抹布盖灭。
A.①③⑤
B.②④⑥
C.①③⑥
D.②③⑤
7.当危险发生时,以下应急措施正确的是( )
A.地震发生时,在底楼的同学快速跑到空旷的地方
B.火灾发生时,打开所有门窗通风
C.煤气泄漏时,打开电灯检查漏气管道
D.发现有人触电时,立即用手把触电者拉开
8.将下列气体和空气混合后点燃,可能发生爆炸的是( )
A.二氧化碳
B.甲烷
C.氧气
D.氮气
9.下列措施不利于化石燃料资源保护的是( )
A.开发新能源
B.研制节能产品
C.提高燃料利用率
D.提倡煤做家庭燃料
10.下列能源中,不会对环境造成污染且取之不尽的是( )
A.太阳能
B.煤
C.石油
D.天然气
二.填空题(共5小题、每空2分、共32分)
11.过氧化钠(Na2O2)是一种浅黄色固体.某次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入烧杯中(见右图),缓慢倒入CO2后发现下面的蜡烛先熄灭,上面的后熄灭,同时也惊奇的发现棉花燃烧起来了.
Ⅰ.实验过程中“下面的蜡烛先熄灭,上面的后熄灭”的现象说明二氧化碳具有
的性质.
Ⅱ.棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了满足“棉花是可燃物”这一条件外,还需满足另外两个条件是
、
.
[提出问题]在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:在常温下Na2O2和CO2、Na2O2和H2O均能发生化学反应.无水硫酸铜遇水由白色变成蓝色.
设计实验:经过讨论后,小组同学设计了如图的实验进行探究.
[实验步骤]①按右图装配好装置,并检查其气密性;
②相关的试剂放入对应的仪器中;
③打开分液漏斗的活塞,把稀盐酸注入锥形瓶内,并固定活塞位置;
④一段时间后,在a处放置一根带火星的小木条,观察现象.
[实验现象](1)干燥管中没有出现蓝色;(2)带火星的小木条复燃;
(3)饱和的澄清石灰水变浑浊.
[实验分析和结论](1)B装置的作用是
.
(2)E装置的烧杯内“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应中
(填“吸收”或“放出”)热量.
(3)“小木条复燃”说明了Na2O2和CO2反应产生了
.使棉花满足了燃烧条件.
12.电动自行车常用的铅蓄电池是一种可充电的化学电源,当给它充电时是
能转化成了
能;太空飞船所用的氢燃料电池是一种将
的装置(填能量形式转化).
13.化学变化是化学研究的重要内容,它对认识和确定物质的组成、结构等有着极其重要的作用.某化学小组围绕燃烧与灭火的主题开展了相关活动,请你参与完成:
(1)可燃物燃烧的必备条件是
和
.
(2)改进后的装置(如图二)与图一相比,其优点是
.欲使图二中的红磷着火,可将试管从水中取出并
后才能对试管加热.
(3)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是
.
(4)“水火不相容”是指水能灭,其实水有时也可以“生火”,比如钠遇水会立刻着火,因为钠遇水生成H2和一种碱,该反应是
(填“吸热”或“放热”)反应.
14.天然气是当今世界上重要而又洁净的气体化石燃料,我市乌审旗内发现一个世界级的大型天然气田﹣苏里格气田,他已经成为“西气东输”工程的气源之一。
(1)家庭用煤经过了从“煤球”到“蜂窝煤”的变化,这种变化的优点是
(2)天然气燃烧的化学方程式
(3)空气质量日报中计入污染指数的项目暂定为①二氧化氮②二氧化硫③一氧化碳④臭氧⑤可吸入颗粒物。用天然气代替煤后,上述污染物含量明显降低的是
(填序号)。
(4)化石燃料等不可再生能源将日趋枯竭,我们在使用时必须节约,并开发、利用新能源。下图表示我国节能标志的是
(填序号)。
15.焚烧秸秆既浪费资源又污染环境,把秸秆、杂草、人畜粪便等废弃物放在密闭的沼气池中发酵,就能产生甲烷,用作燃料.写出甲烷完全燃烧的化学方程式:
;若甲烷不完全燃烧,则还会生成一氧化碳,在煤矿洞中就可能产生瓦斯爆炸.请写出甲烷不完全燃烧的化学方程式:
.
三.解答题(共5小题、每空2分、共38分)
16.某化学兴趣小组的同学在教师指导下进行了“可燃物燃烧条件”的实验探究.
【提出问题】可燃物燃烧通常需要什么条件?
【猜想与假设】可燃物燃烧需要氧气和一定的温度.
【查阅资料】白磷的着火点为40℃,红磷的着火点为240℃.
【实验探究】同学们用图一所示装置进行了实验探究.
【现象与结论】铜片上的白磷燃烧,产生大量白烟;铜片上的红磷和水中的白磷不燃烧.
(1)白磷燃烧的化学方程式为
.
(2)分析实验现象,得出结论:可燃物燃烧的条件是
、
.
【反思与评价】同学们发现,产生的白烟会刺激人的呼吸道.讨论后认为图一所示装置存在不足,于是对其进行了如图二所示的改进,改进后的装置与图一相比,其优点是
.
【拓展实验】待发生燃烧反应的试管冷却后,小组同学将试管倒立在水中,小心取下气球,观察到试管中的现象是
;同学们做此“拓展实验”的目的是
.
17.燃烧是一种发光、放热的剧烈的化学反应。认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。
[查阅资料]物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,发生燃烧的另外两个条件分别是
;
。
[实验目的]验证木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧(两个条件须分别验证)。
[实验设计与操作]下面是验证燃烧条件的实验装置图(可通过开启、关闭活塞控制液体)。
在完成气密性检查后加入药品,并已设法在整个装置中充满了氮气。若要求实验过程中不得拆、装仪器,请设计后续的实验步骤,并按要求填表。
步骤
操作
预计现象及得出的结论
①
在活塞关闭的状态下,点燃酒精灯加热
②
盖灭酒精灯,待仪器恢复到常温
﹣﹣﹣
③
④
[反思评价]实验过程中,装置B的作用可能是
。
18.为了使煤炉燃烧得更旺,小明的爸爸向炉子里填加了一锹煤块,小明却提醒爸爸说,应该填煤粉,理由是煤粉与氧气的接触面积大,可事实上爸爸的做法是正确的.你能解释其中的原因吗?
19.化学在防治大气污染和水污染等方面发挥了重要作用,使更多地化学生产工艺和产品向着环境友好的方向发展.
(1)为从源头消除污染,生产、生活中要选择对环境影响小的燃料,已知充分燃烧1kg天然气和煤所产生的CO2和SO2气体的质量如图所示,则
燃烧产生的气体更易导致酸雨.
(2)某火力发电厂为了防止环境污染,需将废气中的二氧化硫进行处理,其发生的主要反应为2CaCO3+2SO2+O2=2CaSO4+2CO2,若100g废气中含有1.6g二氧化硫,则处理1000g这种废气需含碳酸钙80%的石灰石
g.
(3)某工厂以流量10L/s(升/秒)排出含硫酸9.8%的工业废水,现向该废水中排入含氢氧化钠2%的工业废水,与硫酸反应后再排出,要使处理后的废水呈中性,则含氢氧化钠2%的工业废水的流量应为
L/s(上述含酸废水和含碱废水的密度均近似为1g/cm3).
20.阅读材料,回答问题.
材料一:2010年2月13日,某市一酒吧发生特大火灾.起因是几个年轻人在酒吧内燃放烟花,引燃聚氨酯泡沫塑料天花板,燃烧时产生大量有毒烟气,造成人员中毒死亡.
材料二:氢氧化镁是一种新型的阻燃剂.当温度达到380℃时,开始分解出水蒸气,同时生成耐高温的氧化镁固体.利用其这一性质,将其添加在塑料等易燃材料中能起阻燃作用.
(1)聚氨酯泡沫塑料的一点化学性质是
;
(2)氢氧化镁受热分解的化学方程式
;
(3)据灭火原理分析氢氧化镁能作阻燃剂的原因是:
.
参考答案
一.选择题(共10小题)
1-10BAACBAABDA
二.填空题(共5小题)
11.(1)除去HCl;
(2)放出;
(3)氧气.
12.电;化学;化学能直接转化为电能.
13.(1)与氧气接触,温度达到可燃物的着火点;
(2)减少污染,擦干;
(3)氧气;
(4)放热.
14.(1)增大了煤与氧气的接触面积,能够使煤充分燃烧,提高燃烧效率;
(2)CH4+2O2CO2+2H2O;
(3)①②⑤;
(4)③。
15.4CH4+7O22CO2+2CO+8H2O.
三.解答题(共5小题)
16.(1)4P+5O22P2O5;(2)温度达到该物质的着火点;与氧气接触;[反思与评价]:防止有毒
物质逸入空气,防止空气污染;
[拓展实验]:试管内水面上升至约距试管口处;测定空气中氧气的含量.
17.(1)与氧气充分接触;温度达到着火点
(2)
步骤
操作
预计现象及得出的结论
①
木炭不燃烧,说明可燃物不与氧气接触不能燃烧
②
③
打开分液漏斗活塞,通入氧气一段时间(驱除装置中的N2)
木炭不燃烧,说明可燃物的温度未达到着火点不能燃烧
④
继续通入氧气,点燃酒精灯加热,
木炭燃烧,C中澄清的石灰水变浑浊,说明可燃物燃烧必须同时满足:与氧气接触、温度达到着火点两个条件
(3)防止澄清石灰水直接倒吸入平行玻璃管,使之炸裂。
18.尽管煤粉的表面积大,但煤粉的透气性不好,如果炉内的煤粉填得过多,炉内的通风变差,炉子可能
就会被压灭,而煤块之间的空隙大,使炉内的通风性很好,所以,煤炉会越烧越旺的.
19.(1)煤.(2)31.25.(3)40.
20.(1)聚氨酯有可燃性;
(2)Mg(OH)2MgO+H2O;
(3)氢氧化镁分解需要吸热,且生成的氧化镁耐高温
1
带答案
一.选择题(共10小题、每小题3分、共30分)
1.图甲和图乙所示实验方法均可用来探究可燃物燃烧的条件.
小颖同学用图乙所示装置进行实验,得到以下实验事实:
①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;
③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧.
该实验中,能证明可燃物通常需要接触空气才能燃烧的实验事实是( )
A.①②
B.③④
C.②④
D.①④
2.下列化学反应过程中,需要吸收热量的是( )
A.绿色植物光合作用
B.镁条与稀盐酸反应
C.蜡烛燃烧
D.农家肥的腐熟
3.吴宇森主导的电影《赤壁》中有这样的一个场面:吴蜀联军在船上装满枯枝浇足油,借着东南风向曹军驶去,接近曹军时点燃船上枯枝弃船而走.火借风势,火船宛如火龙一样冲向连在一起的
曹军木船.一眨眼,曹军水寨已经烧成一片火海.下列关于火海形成的叙述中,不正确的是( )
A.东南风降低了木船的着火点
B.枯枝和油为燃烧提供了充足的可燃物
C.东南风为木船燃烧提供了充足的氧气
D.相连的曹军木船没有及时隔离
4.野外烧火时,通常把木柴架空一些才能燃烧更旺,其原因是( )
A.可以降低木柴的着火点
B.使散热的速度加快
C.使木柴与空气的接触面积变大
D.便于提高温度
5.能源的开发和利用关系到社会的进步和发展,有关能源的认识错误的是( )
A.使煤等燃料充分燃烧能够节约化石燃料
B.使用天然气不会对环境造成任何污染
C.乙醇汽油的使用可以节省石油资源,减少汽车尾气的污染
D.开发新能源可解决能源短缺问题
6.下列灭火措施中不恰当的是( )
①炒菜时,锅里的油起火应采取的最佳灭火措施是端下油锅;
②秸秆、柴草着火,用水泼灭;
③熄灭酒精灯最好用嘴吹灭;
④电器着火,最先应当切断电源,再用干粉灭火器灭火;
⑤汽油着火,应该立即用水浇灭;
⑥洒在实验桌上的酒精着火,应用湿抹布盖灭。
A.①③⑤
B.②④⑥
C.①③⑥
D.②③⑤
7.当危险发生时,以下应急措施正确的是( )
A.地震发生时,在底楼的同学快速跑到空旷的地方
B.火灾发生时,打开所有门窗通风
C.煤气泄漏时,打开电灯检查漏气管道
D.发现有人触电时,立即用手把触电者拉开
8.将下列气体和空气混合后点燃,可能发生爆炸的是( )
A.二氧化碳
B.甲烷
C.氧气
D.氮气
9.下列措施不利于化石燃料资源保护的是( )
A.开发新能源
B.研制节能产品
C.提高燃料利用率
D.提倡煤做家庭燃料
10.下列能源中,不会对环境造成污染且取之不尽的是( )
A.太阳能
B.煤
C.石油
D.天然气
二.填空题(共5小题、每空2分、共32分)
11.过氧化钠(Na2O2)是一种浅黄色固体.某次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入烧杯中(见右图),缓慢倒入CO2后发现下面的蜡烛先熄灭,上面的后熄灭,同时也惊奇的发现棉花燃烧起来了.
Ⅰ.实验过程中“下面的蜡烛先熄灭,上面的后熄灭”的现象说明二氧化碳具有
的性质.
Ⅱ.棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知识,推理出棉花要燃烧,除了满足“棉花是可燃物”这一条件外,还需满足另外两个条件是
、
.
[提出问题]在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:在常温下Na2O2和CO2、Na2O2和H2O均能发生化学反应.无水硫酸铜遇水由白色变成蓝色.
设计实验:经过讨论后,小组同学设计了如图的实验进行探究.
[实验步骤]①按右图装配好装置,并检查其气密性;
②相关的试剂放入对应的仪器中;
③打开分液漏斗的活塞,把稀盐酸注入锥形瓶内,并固定活塞位置;
④一段时间后,在a处放置一根带火星的小木条,观察现象.
[实验现象](1)干燥管中没有出现蓝色;(2)带火星的小木条复燃;
(3)饱和的澄清石灰水变浑浊.
[实验分析和结论](1)B装置的作用是
.
(2)E装置的烧杯内“饱和的澄清石灰水变浑浊”说明Na2O2和CO2反应中
(填“吸收”或“放出”)热量.
(3)“小木条复燃”说明了Na2O2和CO2反应产生了
.使棉花满足了燃烧条件.
12.电动自行车常用的铅蓄电池是一种可充电的化学电源,当给它充电时是
能转化成了
能;太空飞船所用的氢燃料电池是一种将
的装置(填能量形式转化).
13.化学变化是化学研究的重要内容,它对认识和确定物质的组成、结构等有着极其重要的作用.某化学小组围绕燃烧与灭火的主题开展了相关活动,请你参与完成:
(1)可燃物燃烧的必备条件是
和
.
(2)改进后的装置(如图二)与图一相比,其优点是
.欲使图二中的红磷着火,可将试管从水中取出并
后才能对试管加热.
(3)将装有某气体的大试管口朝下垂直插入水中,使试管罩住白磷(如图三所示),结果观察到了“水火相容”的奇观,则大试管所装气体可能是
.
(4)“水火不相容”是指水能灭,其实水有时也可以“生火”,比如钠遇水会立刻着火,因为钠遇水生成H2和一种碱,该反应是
(填“吸热”或“放热”)反应.
14.天然气是当今世界上重要而又洁净的气体化石燃料,我市乌审旗内发现一个世界级的大型天然气田﹣苏里格气田,他已经成为“西气东输”工程的气源之一。
(1)家庭用煤经过了从“煤球”到“蜂窝煤”的变化,这种变化的优点是
(2)天然气燃烧的化学方程式
(3)空气质量日报中计入污染指数的项目暂定为①二氧化氮②二氧化硫③一氧化碳④臭氧⑤可吸入颗粒物。用天然气代替煤后,上述污染物含量明显降低的是
(填序号)。
(4)化石燃料等不可再生能源将日趋枯竭,我们在使用时必须节约,并开发、利用新能源。下图表示我国节能标志的是
(填序号)。
15.焚烧秸秆既浪费资源又污染环境,把秸秆、杂草、人畜粪便等废弃物放在密闭的沼气池中发酵,就能产生甲烷,用作燃料.写出甲烷完全燃烧的化学方程式:
;若甲烷不完全燃烧,则还会生成一氧化碳,在煤矿洞中就可能产生瓦斯爆炸.请写出甲烷不完全燃烧的化学方程式:
.
三.解答题(共5小题、每空2分、共38分)
16.某化学兴趣小组的同学在教师指导下进行了“可燃物燃烧条件”的实验探究.
【提出问题】可燃物燃烧通常需要什么条件?
【猜想与假设】可燃物燃烧需要氧气和一定的温度.
【查阅资料】白磷的着火点为40℃,红磷的着火点为240℃.
【实验探究】同学们用图一所示装置进行了实验探究.
【现象与结论】铜片上的白磷燃烧,产生大量白烟;铜片上的红磷和水中的白磷不燃烧.
(1)白磷燃烧的化学方程式为
.
(2)分析实验现象,得出结论:可燃物燃烧的条件是
、
.
【反思与评价】同学们发现,产生的白烟会刺激人的呼吸道.讨论后认为图一所示装置存在不足,于是对其进行了如图二所示的改进,改进后的装置与图一相比,其优点是
.
【拓展实验】待发生燃烧反应的试管冷却后,小组同学将试管倒立在水中,小心取下气球,观察到试管中的现象是
;同学们做此“拓展实验”的目的是
.
17.燃烧是一种发光、放热的剧烈的化学反应。认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。
[查阅资料]物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,发生燃烧的另外两个条件分别是
;
。
[实验目的]验证木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧(两个条件须分别验证)。
[实验设计与操作]下面是验证燃烧条件的实验装置图(可通过开启、关闭活塞控制液体)。
在完成气密性检查后加入药品,并已设法在整个装置中充满了氮气。若要求实验过程中不得拆、装仪器,请设计后续的实验步骤,并按要求填表。
步骤
操作
预计现象及得出的结论
①
在活塞关闭的状态下,点燃酒精灯加热
②
盖灭酒精灯,待仪器恢复到常温
﹣﹣﹣
③
④
[反思评价]实验过程中,装置B的作用可能是
。
18.为了使煤炉燃烧得更旺,小明的爸爸向炉子里填加了一锹煤块,小明却提醒爸爸说,应该填煤粉,理由是煤粉与氧气的接触面积大,可事实上爸爸的做法是正确的.你能解释其中的原因吗?
19.化学在防治大气污染和水污染等方面发挥了重要作用,使更多地化学生产工艺和产品向着环境友好的方向发展.
(1)为从源头消除污染,生产、生活中要选择对环境影响小的燃料,已知充分燃烧1kg天然气和煤所产生的CO2和SO2气体的质量如图所示,则
燃烧产生的气体更易导致酸雨.
(2)某火力发电厂为了防止环境污染,需将废气中的二氧化硫进行处理,其发生的主要反应为2CaCO3+2SO2+O2=2CaSO4+2CO2,若100g废气中含有1.6g二氧化硫,则处理1000g这种废气需含碳酸钙80%的石灰石
g.
(3)某工厂以流量10L/s(升/秒)排出含硫酸9.8%的工业废水,现向该废水中排入含氢氧化钠2%的工业废水,与硫酸反应后再排出,要使处理后的废水呈中性,则含氢氧化钠2%的工业废水的流量应为
L/s(上述含酸废水和含碱废水的密度均近似为1g/cm3).
20.阅读材料,回答问题.
材料一:2010年2月13日,某市一酒吧发生特大火灾.起因是几个年轻人在酒吧内燃放烟花,引燃聚氨酯泡沫塑料天花板,燃烧时产生大量有毒烟气,造成人员中毒死亡.
材料二:氢氧化镁是一种新型的阻燃剂.当温度达到380℃时,开始分解出水蒸气,同时生成耐高温的氧化镁固体.利用其这一性质,将其添加在塑料等易燃材料中能起阻燃作用.
(1)聚氨酯泡沫塑料的一点化学性质是
;
(2)氢氧化镁受热分解的化学方程式
;
(3)据灭火原理分析氢氧化镁能作阻燃剂的原因是:
.
参考答案
一.选择题(共10小题)
1-10BAACBAABDA
二.填空题(共5小题)
11.(1)除去HCl;
(2)放出;
(3)氧气.
12.电;化学;化学能直接转化为电能.
13.(1)与氧气接触,温度达到可燃物的着火点;
(2)减少污染,擦干;
(3)氧气;
(4)放热.
14.(1)增大了煤与氧气的接触面积,能够使煤充分燃烧,提高燃烧效率;
(2)CH4+2O2CO2+2H2O;
(3)①②⑤;
(4)③。
15.4CH4+7O22CO2+2CO+8H2O.
三.解答题(共5小题)
16.(1)4P+5O22P2O5;(2)温度达到该物质的着火点;与氧气接触;[反思与评价]:防止有毒
物质逸入空气,防止空气污染;
[拓展实验]:试管内水面上升至约距试管口处;测定空气中氧气的含量.
17.(1)与氧气充分接触;温度达到着火点
(2)
步骤
操作
预计现象及得出的结论
①
木炭不燃烧,说明可燃物不与氧气接触不能燃烧
②
③
打开分液漏斗活塞,通入氧气一段时间(驱除装置中的N2)
木炭不燃烧,说明可燃物的温度未达到着火点不能燃烧
④
继续通入氧气,点燃酒精灯加热,
木炭燃烧,C中澄清的石灰水变浑浊,说明可燃物燃烧必须同时满足:与氧气接触、温度达到着火点两个条件
(3)防止澄清石灰水直接倒吸入平行玻璃管,使之炸裂。
18.尽管煤粉的表面积大,但煤粉的透气性不好,如果炉内的煤粉填得过多,炉内的通风变差,炉子可能
就会被压灭,而煤块之间的空隙大,使炉内的通风性很好,所以,煤炉会越烧越旺的.
19.(1)煤.(2)31.25.(3)40.
20.(1)聚氨酯有可燃性;
(2)Mg(OH)2MgO+H2O;
(3)氢氧化镁分解需要吸热,且生成的氧化镁耐高温
1
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
