鲁科版(2019)高中物理 选择性必修第三册 第4章 第4节 玻尔原子模型课件32 张PPT
文档属性
| 名称 | 鲁科版(2019)高中物理 选择性必修第三册 第4章 第4节 玻尔原子模型课件32 张PPT |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2020-12-10 00:00:00 | ||
图片预览










文档简介
第4节 玻尔原子模型
核心素养
物理观念
科学思维
科学态度与责任
1.知道玻尔原子理论的基本假设的主要内容。
2.了解能级、跃迁、能量量子化以及基态、激发态等概念。
3.会计算原子跃迁时吸收或辐射光子的能量。
用玻尔原子理论简单解释氢原子光谱的实验规律。
了解玻尔原子结构理论的意义并知道其不足。
知识点一 玻尔原子模型
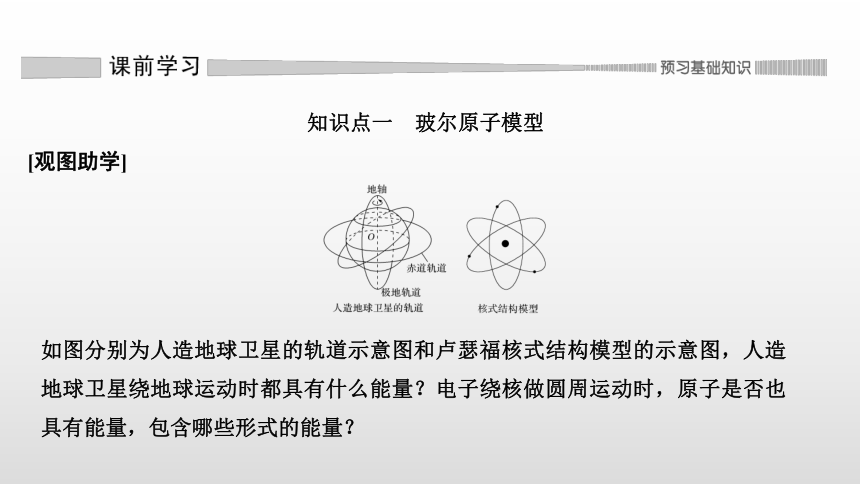
[观图助学]
如图分别为人造地球卫星的轨道示意图和卢瑟福核式结构模型的示意图,人造地球卫星绕地球运动时都具有什么能量?电子绕核做圆周运动时,原子是否也具有能量,包含哪些形式的能量?
1.卢瑟福原子核式结构模型遇到的困难
稳定性
卢瑟福的原子核式结构模型不能解释原子的 和原子光谱的 。
2.玻尔原子模型
(1)轨道定态
原子核外的电子只能在一些分立的特定轨道上绕核运动;电子在这些轨道上运动时,原子具有一定能量,其数值也是分立的,电子的轨道和原子的能量都是__________。电子虽然做圆周运动,但不向外辐射能量,处于 状态,电子处于分立轨道的这些状态称为定态。
不连续性
量子化的
稳定的
(2)频率条件
当电子从能量较高的定态轨道跃迁到能量较低的定态轨道时,原子会 光子。反之,当 光子时,电子会从能量较低的定态轨道跃迁到能量较高的定态轨道。辐射(或吸收)的光子的能量hν由两个定态的能量差决定,即该光子的能量应满足频率条件: (m> n)。
辐射
吸收
hν=Em-En
[思考判断]
(1)玻尔认为电子运行轨道半径是任意的,就像人造地球卫星,能量大一些,轨道半径就会大点。( )
(2)玻尔认为原子的能量是量子化的,不能连续取值。( )
(3)当电子从能量较高的定态轨道跃迁到能量较低的定态轨道时,原子会辐射光子。( )
×
√
√
知识点二 氢原子的能级结构、解释氢原子光谱
1.氢原子的能级结构
(1) 能级:在玻尔的原子模型中,原子只能处于一系列 的能量状态。在每个状态中,原子的能量值都是 ,各个确定的能量值称为能级。
(3)基态和激发态:在正常状态下,原子处于最低能级,电子受核的作用力最大而处于离核 的轨道,这时原子的状态称为基态。电子 能量后,原子从低能级跃迁到高能级,这时原子的状态称为激发态。
不连续
确定的
n2r1
最近
吸收
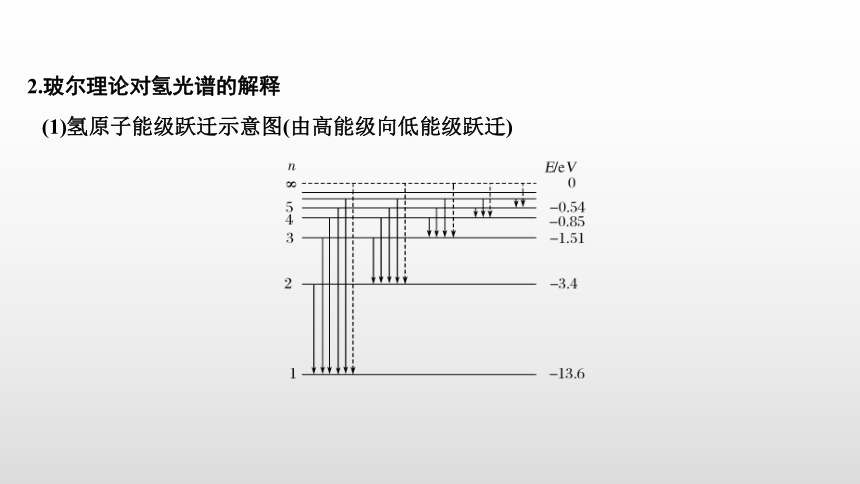
2.玻尔理论对氢光谱的解释
(1)氢原子能级跃迁示意图(由高能级向低能级跃迁)
[思考判断]
(1)处于基态的原子是不稳定的,会自发地向其他能级跃迁,放出光子。( )
(2) 第m个定态和第n个定态的轨道半径rm和rn之比为rm∶rn=m2∶n2。( )
(3)玻尔的原子理论模型可以很好地解释氢原子的光谱现象。( )
×
√
√
知识点三 玻尔理论的局限
1.成功之处
玻尔理论冲破了经典物理中能量连续变化的束缚,解释了原子结构和氢原子光谱的关系。引入了普朗克的 概念,认为电子轨道和能量都是 的。
量子化
量子化
2.局限性
没有跳出经典力学的范围,认为电子是经典粒子,运动有 轨道。因此,玻尔理论是一种半经典的量子论,是向描述微观粒子规律的量子力学过渡阶段中的一个理论。
3.电子云
电子是微观粒子,其运动与宏观物体运动不同,没有确定的方向和 。它们在原子核周围各处出现的概率是不同的。人们将这些概率用点的方式表现出来,若某一空间范围内电子出现的概率大,则这里的点就 ;若某一空间范围内电子出现的概率小,则这里的点就 。这种用点的疏密表示电子出现的概率分布的图形,称为电子云。
确定的
轨迹
密集
稀疏
[思考判断]
(1)玻尔的原子理论将量子观念引入到了原子领域。( )
(2)玻尔的原子理论把电子的运动仍然看作经典力学描述下的轨道运动。( )
(3)电子云图形中点密集的地方电子的数目比稀疏的地方多。( )
√
√
×
[问题探究]
按照经典理论,核外电子在库仑引力作用下绕原子核做圆周运动。我们知道,库仑引力和万有引力形式上有相似之处,电子绕原子核的运动与卫星绕地球的运动也一定有某些相似之处,那么若将卫星—地球模型缩小是否就可以变为电子—原子核模型呢?
答案 不可以。在玻尔理论中,电子的轨道半径只可能是某些分立的数值,而卫星的轨道半径可按需要任意取值。
核心要点
对玻尔理论的理解
[探究归纳]
1.轨道量子化
(1)轨道半径只能够是一些不连续的、某些分立的数值。
(2)氢原子的电子最小轨道半径为r1=0.053 nm=0.53×10-10 m,其余轨道半径满足rn=n2r1,式中n称为量子数,对应不同的轨道,只能取正整数。
2.能量量子化
(1)不同轨道对应不同的状态,在这些状态中,尽管电子做变速运动,却不辐射能量,因此这些状态是稳定的,原子在不同状态有不同的能量,所以原子的能量也是量子化的。
(2)基态:原子最低的能量状态称为基态,对应的电子在离核最近的轨道上运动,氢原子基态能量E1=-13.6 eV。
(3)激发态:除基态之外的其他能量状态称为激发态,对应的电子在离核较远的轨道上运动。
3.跃迁
[经典示例]
[例1] (多选)按照玻尔原子理论,下列表述正确的是( )
A.核外电子运动轨道半径可取任意值
B.氢原子中的电子离原子核越远,氢原子的能量越大
C.电子跃迁时,辐射或吸收光子的能量由能级的能量差决定,即hν=|Em-En|
D.氢原子从激发态向基态跃迁的过程,可能辐射能量,也可能吸收能量
解析 根据玻尔理论,核外电子运动的轨道半径是确定的值,而不是任意值,A错误;氢原子中的电子离原子核越远,能级越高,能量越大,B正确;由跃迁规律可知C正确;氢原子从激发态向基态跃迁的过程中,应辐射能量,D错误。
答案 BC
[例2] 氢原子的核外电子从距核较近的轨道跃迁到距核较远的轨道的过程中( )
A.原子要吸收光子,电子的动能增大,原子的电势能增大
B.原子要放出光子,电子的动能减小,原子的电势能减小
C.原子要吸收光子,电子的动能增大,原子的电势能减小
D.原子要吸收光子,电子的动能减小,原子的电势能增大
答案 D
(3)当电子的轨道半径增大时,库仑引力做负功,原子的电势能增大,反之,电势能减小。
(4)电子的轨道半径增大时,说明原子吸收了光子,从能量较低的轨道跃迁到了能量较高的轨道上。即电子轨道半径越大,原子的能量越大。
[针对训练1] (多选)对原子发射和吸收光子的过程,下列说法正确的是( )
A.原子从基态跃迁到激发态要放出光子,放出光子的能量等于原子在始、末两个能级的能量差
B.原子不能从低能级向高能级跃迁
C.原子吸收光子后从低能级跃迁到高能级,放出光子后从较高能级跃迁到较低能级
D.原子无论是吸收光子还是放出光子,吸收的光子或放出的光子的能量恒等于始、末两个能级的能量差值
解析 由玻尔理论的跃迁假设知,原子处于激发态不稳定,可自发地向低能级发生跃迁,以光子的形式放出能量,光子的吸收是光子发射的逆过程,原子在吸收光子后,会从较低能级向较高能级跃迁,但不管是吸收光子还是发射光子,光子的能量总等于两能级之差,即hν=Em-En(m>n),故选项C、D正确。
答案 CD
[问题探究]
根据如图所示的氢原子的能级图,说明:
(1)氢原子从高能级向低能级跃迁时,放出的光子的能量如何计算?
(2)一群处于n=4的激发态的氢原子向低能级跃迁时能辐射出多少种频率不同的光子?
核心要点
玻尔理论对氢原子光谱的解释
答案 (1)氢原子辐射光子的能量取决于两个能级的能量差hν=Em-En(n(2)氢原子能级跃迁图如图所示。从图中可以看出能辐射出6种频率不同的光子,它们分别是n=4→n=3,n=4→n=2,n=4→n=1,n=3→n=2,n=3→n=1,n=2→n=1。
[探究归纳]
1.能级图中n称为量子数,E1代表氢原子的基态能量,即量子数n=1时对应的能量,其值为-13.6 eV。En代表电子在第n个轨道上运动时的能量。 n=1是原子的基态,n→∞是原子电离时对应的状态。
2.原子从低能级向高能级跃迁:只能吸收一定能量的光子,即当一个光子的能量满足hν=E末-E初时,才可能被某一个原子吸收,而当光子能量hν大于或小于E末-E初时都不能被原子吸收;原子从高能级向低能级跃迁,以光子的形式向外辐射能量,所辐射的光子能量恰等于发生跃迁时的两能级间的能量差。
[经典示例]
[例3] (多选)氢原子能级图如图所示,当氢原子从n=3跃迁到n=2的能级时,辐射光的波长为656 nm。以下判断正确的是( )
A.氢原子从n=2跃迁到n=1的能级时,辐射光的波长大于656 nm
B.用波长为325 nm的光照射,可使氢原子从n=1跃迁到n=2的能级
C.一群处于n=3能级上的氢原子向低能级跃迁时最多产生3种谱线
D.用波长为633 nm的光照射,不能使氢原子从n=2跃迁到n=3的能级
答案 CD
[针对训练2] 如图所示,1、2、3、4为玻尔理论中氢原子最低的四个能级。处在n=4能级的一群氢原子向低能级跃迁时,能发出若干种频率不同的光子,在这些光子中,波长最长的是( )
A.n=4跃迁到n=1时辐射的光子
B.n=4跃迁到n=3时辐射的光子
C.n=2跃迁到n=1时辐射的光子
D.n=3跃迁到n=2时辐射的光子
答案 B
核心素养
物理观念
科学思维
科学态度与责任
1.知道玻尔原子理论的基本假设的主要内容。
2.了解能级、跃迁、能量量子化以及基态、激发态等概念。
3.会计算原子跃迁时吸收或辐射光子的能量。
用玻尔原子理论简单解释氢原子光谱的实验规律。
了解玻尔原子结构理论的意义并知道其不足。
知识点一 玻尔原子模型
[观图助学]
如图分别为人造地球卫星的轨道示意图和卢瑟福核式结构模型的示意图,人造地球卫星绕地球运动时都具有什么能量?电子绕核做圆周运动时,原子是否也具有能量,包含哪些形式的能量?
1.卢瑟福原子核式结构模型遇到的困难
稳定性
卢瑟福的原子核式结构模型不能解释原子的 和原子光谱的 。
2.玻尔原子模型
(1)轨道定态
原子核外的电子只能在一些分立的特定轨道上绕核运动;电子在这些轨道上运动时,原子具有一定能量,其数值也是分立的,电子的轨道和原子的能量都是__________。电子虽然做圆周运动,但不向外辐射能量,处于 状态,电子处于分立轨道的这些状态称为定态。
不连续性
量子化的
稳定的
(2)频率条件
当电子从能量较高的定态轨道跃迁到能量较低的定态轨道时,原子会 光子。反之,当 光子时,电子会从能量较低的定态轨道跃迁到能量较高的定态轨道。辐射(或吸收)的光子的能量hν由两个定态的能量差决定,即该光子的能量应满足频率条件: (m> n)。
辐射
吸收
hν=Em-En
[思考判断]
(1)玻尔认为电子运行轨道半径是任意的,就像人造地球卫星,能量大一些,轨道半径就会大点。( )
(2)玻尔认为原子的能量是量子化的,不能连续取值。( )
(3)当电子从能量较高的定态轨道跃迁到能量较低的定态轨道时,原子会辐射光子。( )
×
√
√
知识点二 氢原子的能级结构、解释氢原子光谱
1.氢原子的能级结构
(1) 能级:在玻尔的原子模型中,原子只能处于一系列 的能量状态。在每个状态中,原子的能量值都是 ,各个确定的能量值称为能级。
(3)基态和激发态:在正常状态下,原子处于最低能级,电子受核的作用力最大而处于离核 的轨道,这时原子的状态称为基态。电子 能量后,原子从低能级跃迁到高能级,这时原子的状态称为激发态。
不连续
确定的
n2r1
最近
吸收
2.玻尔理论对氢光谱的解释
(1)氢原子能级跃迁示意图(由高能级向低能级跃迁)
[思考判断]
(1)处于基态的原子是不稳定的,会自发地向其他能级跃迁,放出光子。( )
(2) 第m个定态和第n个定态的轨道半径rm和rn之比为rm∶rn=m2∶n2。( )
(3)玻尔的原子理论模型可以很好地解释氢原子的光谱现象。( )
×
√
√
知识点三 玻尔理论的局限
1.成功之处
玻尔理论冲破了经典物理中能量连续变化的束缚,解释了原子结构和氢原子光谱的关系。引入了普朗克的 概念,认为电子轨道和能量都是 的。
量子化
量子化
2.局限性
没有跳出经典力学的范围,认为电子是经典粒子,运动有 轨道。因此,玻尔理论是一种半经典的量子论,是向描述微观粒子规律的量子力学过渡阶段中的一个理论。
3.电子云
电子是微观粒子,其运动与宏观物体运动不同,没有确定的方向和 。它们在原子核周围各处出现的概率是不同的。人们将这些概率用点的方式表现出来,若某一空间范围内电子出现的概率大,则这里的点就 ;若某一空间范围内电子出现的概率小,则这里的点就 。这种用点的疏密表示电子出现的概率分布的图形,称为电子云。
确定的
轨迹
密集
稀疏
[思考判断]
(1)玻尔的原子理论将量子观念引入到了原子领域。( )
(2)玻尔的原子理论把电子的运动仍然看作经典力学描述下的轨道运动。( )
(3)电子云图形中点密集的地方电子的数目比稀疏的地方多。( )
√
√
×
[问题探究]
按照经典理论,核外电子在库仑引力作用下绕原子核做圆周运动。我们知道,库仑引力和万有引力形式上有相似之处,电子绕原子核的运动与卫星绕地球的运动也一定有某些相似之处,那么若将卫星—地球模型缩小是否就可以变为电子—原子核模型呢?
答案 不可以。在玻尔理论中,电子的轨道半径只可能是某些分立的数值,而卫星的轨道半径可按需要任意取值。
核心要点
对玻尔理论的理解
[探究归纳]
1.轨道量子化
(1)轨道半径只能够是一些不连续的、某些分立的数值。
(2)氢原子的电子最小轨道半径为r1=0.053 nm=0.53×10-10 m,其余轨道半径满足rn=n2r1,式中n称为量子数,对应不同的轨道,只能取正整数。
2.能量量子化
(1)不同轨道对应不同的状态,在这些状态中,尽管电子做变速运动,却不辐射能量,因此这些状态是稳定的,原子在不同状态有不同的能量,所以原子的能量也是量子化的。
(2)基态:原子最低的能量状态称为基态,对应的电子在离核最近的轨道上运动,氢原子基态能量E1=-13.6 eV。
(3)激发态:除基态之外的其他能量状态称为激发态,对应的电子在离核较远的轨道上运动。
3.跃迁
[经典示例]
[例1] (多选)按照玻尔原子理论,下列表述正确的是( )
A.核外电子运动轨道半径可取任意值
B.氢原子中的电子离原子核越远,氢原子的能量越大
C.电子跃迁时,辐射或吸收光子的能量由能级的能量差决定,即hν=|Em-En|
D.氢原子从激发态向基态跃迁的过程,可能辐射能量,也可能吸收能量
解析 根据玻尔理论,核外电子运动的轨道半径是确定的值,而不是任意值,A错误;氢原子中的电子离原子核越远,能级越高,能量越大,B正确;由跃迁规律可知C正确;氢原子从激发态向基态跃迁的过程中,应辐射能量,D错误。
答案 BC
[例2] 氢原子的核外电子从距核较近的轨道跃迁到距核较远的轨道的过程中( )
A.原子要吸收光子,电子的动能增大,原子的电势能增大
B.原子要放出光子,电子的动能减小,原子的电势能减小
C.原子要吸收光子,电子的动能增大,原子的电势能减小
D.原子要吸收光子,电子的动能减小,原子的电势能增大
答案 D
(3)当电子的轨道半径增大时,库仑引力做负功,原子的电势能增大,反之,电势能减小。
(4)电子的轨道半径增大时,说明原子吸收了光子,从能量较低的轨道跃迁到了能量较高的轨道上。即电子轨道半径越大,原子的能量越大。
[针对训练1] (多选)对原子发射和吸收光子的过程,下列说法正确的是( )
A.原子从基态跃迁到激发态要放出光子,放出光子的能量等于原子在始、末两个能级的能量差
B.原子不能从低能级向高能级跃迁
C.原子吸收光子后从低能级跃迁到高能级,放出光子后从较高能级跃迁到较低能级
D.原子无论是吸收光子还是放出光子,吸收的光子或放出的光子的能量恒等于始、末两个能级的能量差值
解析 由玻尔理论的跃迁假设知,原子处于激发态不稳定,可自发地向低能级发生跃迁,以光子的形式放出能量,光子的吸收是光子发射的逆过程,原子在吸收光子后,会从较低能级向较高能级跃迁,但不管是吸收光子还是发射光子,光子的能量总等于两能级之差,即hν=Em-En(m>n),故选项C、D正确。
答案 CD
[问题探究]
根据如图所示的氢原子的能级图,说明:
(1)氢原子从高能级向低能级跃迁时,放出的光子的能量如何计算?
(2)一群处于n=4的激发态的氢原子向低能级跃迁时能辐射出多少种频率不同的光子?
核心要点
玻尔理论对氢原子光谱的解释
答案 (1)氢原子辐射光子的能量取决于两个能级的能量差hν=Em-En(n
[探究归纳]
1.能级图中n称为量子数,E1代表氢原子的基态能量,即量子数n=1时对应的能量,其值为-13.6 eV。En代表电子在第n个轨道上运动时的能量。 n=1是原子的基态,n→∞是原子电离时对应的状态。
2.原子从低能级向高能级跃迁:只能吸收一定能量的光子,即当一个光子的能量满足hν=E末-E初时,才可能被某一个原子吸收,而当光子能量hν大于或小于E末-E初时都不能被原子吸收;原子从高能级向低能级跃迁,以光子的形式向外辐射能量,所辐射的光子能量恰等于发生跃迁时的两能级间的能量差。
[经典示例]
[例3] (多选)氢原子能级图如图所示,当氢原子从n=3跃迁到n=2的能级时,辐射光的波长为656 nm。以下判断正确的是( )
A.氢原子从n=2跃迁到n=1的能级时,辐射光的波长大于656 nm
B.用波长为325 nm的光照射,可使氢原子从n=1跃迁到n=2的能级
C.一群处于n=3能级上的氢原子向低能级跃迁时最多产生3种谱线
D.用波长为633 nm的光照射,不能使氢原子从n=2跃迁到n=3的能级
答案 CD
[针对训练2] 如图所示,1、2、3、4为玻尔理论中氢原子最低的四个能级。处在n=4能级的一群氢原子向低能级跃迁时,能发出若干种频率不同的光子,在这些光子中,波长最长的是( )
A.n=4跃迁到n=1时辐射的光子
B.n=4跃迁到n=3时辐射的光子
C.n=2跃迁到n=1时辐射的光子
D.n=3跃迁到n=2时辐射的光子
答案 B
同课章节目录
- 第1章 分子动理论与气体实验定律
- 第1节 分子动理论的基本观点
- 第2节 科学测量:用油膜法估测油酸分子的大小
- 第3节 气体分子速率分布的统计规律
- 第4节 科学探究:气体压强与体积的关系
- 第5节 气体实验定律
- 第2章 固体与液体
- 第1节 固体类型及微观结构
- 第2节 表面张力和毛细现象
- 第3节 材料及其应用
- 第3章 热力学定律
- 第1节 热力学第一定律
- 第2节 能量的转化与守恒
- 第3节 热力学第二定律
- 第4节 熵——系统无序程度的量度
- 第4章 原子结构
- 第1节 电子的发现与汤姆孙原子模型
- 第2节 原子的核式结构模型
- 第3节 光谱与氢原子光谱
- 第4节 玻尔原子模型
- 第5章 原子核与核能
- 第1节 认识原子核
- 第2节 原子核衰变及半衰期
- 第3节 核力与核能
- 第4节 核裂变和核聚变
- 第5节 核能的利用与环境保护
- 第6章 波粒二象性
- 第1节 光电效应及其解释
- 第2节 实物粒子的波粒二象性
