湖北省汉川市官备塘中学2020年九年级化学下册第8单元课题 2 金属的化学性质—《金属的化学性质》基础选择题综合训练(无答案)
文档属性
| 名称 | 湖北省汉川市官备塘中学2020年九年级化学下册第8单元课题 2 金属的化学性质—《金属的化学性质》基础选择题综合训练(无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 560.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-15 00:00:00 | ||
图片预览




文档简介
《金属的化学性质》基础选择题综合训练
1.下列金属放入Cu(NO3)2溶液中,能生成红色固体,溶液由蓝色变成浅绿色的是 ( )
A.Ag
B.Zn
C.Cu
D.Fe
2.黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。常言说:“真金不怕火炼”主要是指 ( )
A.熔点高
B.延展性好
C.有金属光泽
D.化学性质稳定
3.下列各物质恰好完全反应,所得溶液的颜色是无色的是 ( )
A.铁和硫酸铜溶液
B.铁和稀硫酸
C.锌和稀硫酸
D.铁和稀盐酸
4.将一根洁净的铁钉放入稀硫酸中,下列预测可能不正确的是
( )
A.铁钉表面将产生气泡
B.铁钉表面将很快出现铁锈
C.溶液由无色变为浅绿色
D.溶液质量将增加
5.市面上有不法商贩使用颜色和外形与黄金十分相似的假黄金(铜锌合金)来蒙骗消费者。请你利用所学知识判断,下列方案不能区分真假黄金的是 ( )
A.放在稀硫酸中
B.在空气中灼烧
C.测密度
D.认真观察颜色
6.根据金属活动性顺序进行分析,下列描述或判断错误的是
( )
A.常温下,金属镁在空气中要比铁容易氧化
B.常温下,铝能和稀盐酸反应,而银不能
C.在氧气中灼烧时,铁丝要比铜丝反应剧烈
D.将铜丝插入硝酸银溶液中,不能反应得到银
7.金属M与AgNO3溶液反应的化学方程式为M
+
2AgNO3
M(NO3)2+2Ag。下列说法不正确的是 ( )
A.该反应属于置换反应
B.金属M可能是铝
C.M的金属活动性比Ag强
D.反应前后M的化合价改变
8.“真金不怕火炼”的原因是( )
A.金的硬度大
B.金的熔点高
C.金的密度大
D.金的化学性质稳定
9.下列有关金属性质的说法错误的是( )
A.铜、银等金属具有良好的导电性,可制造导线
B.铁在纯氧气中能燃烧,生成四氧化三铁
C.铝制品能形成致密的保护膜,则不可磨损铝的表面
D.铁与稀盐酸反应可生成氯化铁
10.将少量的生铁放入足量的盐酸中充分反应,有黑色的残渣剩余,该残渣主要是( )
A.单质碳
B.氯化铁
C.氯化亚铁
D.单质铁
11.下列各组实验,不能说明铁和铜的金属活动性强弱的是( )
A.铁丝和铜丝分别插入稀硫酸中
B.铁丝和铜丝分别插入硝酸银溶液中
C.铜丝插入硫酸亚铁溶液中
D.铁丝插入硫酸铜溶液中
12.下列物质可由金属与酸直接反应制得的是( )
A.AgCl
B.CuSO4
C.Fe2(SO4)3
D.AlCl3
13.铜、镁的金属活动性时,下列现象、分析或结论正确的是( )
A.盐酸的浓度可以不同
B.铜片表面有气泡
C.镁片的试管表面发烫
D.活动性Zn>Mg>Cu
14.为了验证Zn、Fe、Cu三种金属的活动顺序为:Zn>Fe>Cu这一结论,下面实验设计合理的是( )
A.将Zn、Cu两金属片分别放入稀硫酸中
B.将Fe、Cu两金属片分别放入稀盐酸中
C.将Zn、Fe两金属片分别放入CuSO4溶液中
D.将Zn、Cu两金属片分别放入FeSO4溶液中
15.“愚人金”实为铜锌合金,外观与黄金极为相似,常被不法商贩冒充黄金牟取暴利。下列关于鉴别“愚人金”与黄金的实验方案,合理的是( )
A.测质量,质量小的是“愚人金”
B.灼烧,表面变紫红色的是“愚人金”
C.浸没在稀硫酸中,表面有气泡产生的是“愚人金”
D.浸没在硫酸锌溶液中,表面附着白色物质的是“愚人金”
16.下列有关铁的化学方程式中正确的是(
)
A.4Fe+3O22Fe2O3
B.Fe+H2SO4
====
FeSO4+H2↑
C.2Fe+6HCl
====
2FeCl3+3H2↑
D.2Fe+3CuSO4
====
3Cu+Fe2(SO4)3
17.能与无色硝酸银溶液反应,使溶液变为蓝色的金属是(
)
A.铝
B.铁
C.铜
D.银
18.把金属X放入Cu(NO3)2溶液中,X表面有红色固体析出;若放入Mg(NO3)2溶液中,无明显现象。则X、Cu、Mg三种金属活动性由强到弱的顺序正确的是(
)
A.Mg、X、Cu
B.X、Mg、Cu
C.Mg、Cu、X
D.Cu、X、Mg
19.将一枚洁净的铁钉浸入稀硫酸中,下列叙述中正确的是(
)
①铁钉表面产生气泡;②液体由无色逐渐变为浅绿色;③铁钉的质量减轻;
④液体的质量减轻。
A.②③
B.①②④
C.①②③
D.①②③④
20.下列事实不能说明Zn比Ag活泼的是(
)
A.Zn能与AgNO3溶液反应,置换出Ag
B.Zn能与稀硫酸反应,Ag则不能
C.自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D.Zn的熔点为420
℃,Ag的熔点为962
℃
21.下列有关金属的说法正确的是(
)
A.铝具有很好的抗腐蚀性能
B.铜能置换出酸中的氢
C.钢是纯净物
D.银能把铁从氯化亚铁溶液中置换出来
22.把铁粉放入硝酸银、硝酸铜和硝酸锌的混合溶液中,充分反应后过滤,所得到的固体中一定没有的是(
)
A.锌
B.铁
C.铜
D.银
23.常见金属活动性顺序表如下:
下列各组物质不能发生化学反应的是(
)
A.汞与硝酸银溶液
B.铜与硝酸镁溶液
C.锌与硫酸亚铁溶液
D.铝与稀盐酸
24.甲、乙、丙、丁四种金属。甲即使在高温时也不与氧气反应。乙、丙、丁在一定条件下都能与氧气反应。丁盐的水溶液可用丙制的容器盛放,但不能用乙制的容器盛放。这四种金属的活动性由强到弱的顺序是(
)
A.甲>乙>丁>丙
B.丙>丁>乙>甲
C.丙>乙>丁>甲
D.乙>丁>丙>甲
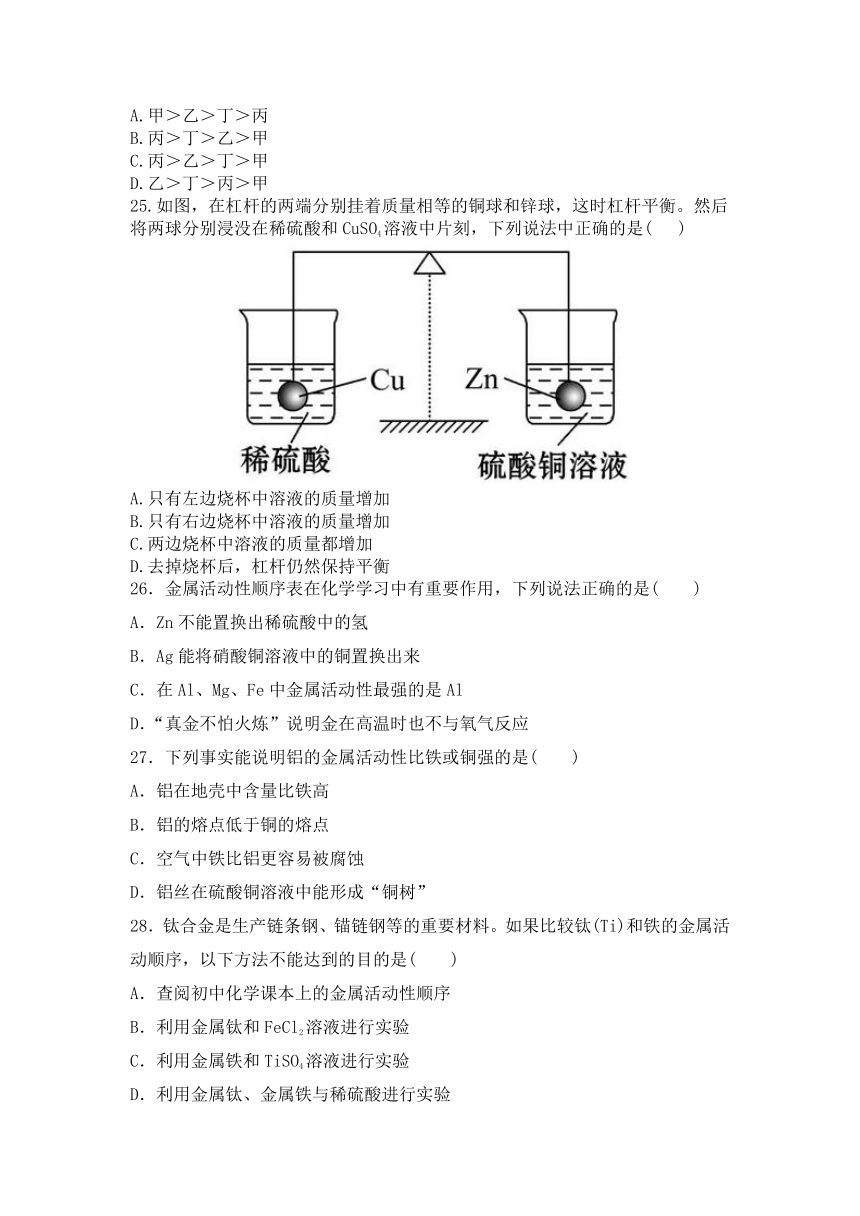
25.如图,在杠杆的两端分别挂着质量相等的铜球和锌球,这时杠杆平衡。然后将两球分别浸没在稀硫酸和CuSO4溶液中片刻,下列说法中正确的是(
)
A.只有左边烧杯中溶液的质量增加
B.只有右边烧杯中溶液的质量增加
C.两边烧杯中溶液的质量都增加
D.去掉烧杯后,杠杆仍然保持平衡
26.金属活动性顺序表在化学学习中有重要作用,下列说法正确的是( )
A.Zn不能置换出稀硫酸中的氢
B.Ag能将硝酸铜溶液中的铜置换出来
C.在Al、Mg、Fe中金属活动性最强的是Al
D.“真金不怕火炼”说明金在高温时也不与氧气反应
27.下列事实能说明铝的金属活动性比铁或铜强的是( )
A.铝在地壳中含量比铁高
B.铝的熔点低于铜的熔点
C.空气中铁比铝更容易被腐蚀
D.铝丝在硫酸铜溶液中能形成“铜树”
28.钛合金是生产链条钢、锚链钢等的重要材料。如果比较钛(Ti)和铁的金属活动顺序,以下方法不能达到的目的是( )
A.查阅初中化学课本上的金属活动性顺序
B.利用金属钛和FeCl2溶液进行实验
C.利用金属铁和TiSO4溶液进行实验
D.利用金属钛、金属铁与稀硫酸进行实验
29.常见金属X与硝酸银溶液反应的化学方程式为X+3AgNO3===3Ag+X(NO3)3,有关该反应说法错误的是( )
A.该反应是置换反应
B.X可能是铁
C.金属活动性X>Ag
D.X表面有固体析出
30.下列事实不能用金属的活动性顺序加以解释的是( )
A.不能用铜与稀硫酸反应制取氢气
B.铁能置换出硫酸铜溶液中的铜
C.在化合物中,铁显+2、+3价,铜显+1、+2价
D.相同条件下,锌和铁与稀硫酸反应的剧烈程度
31.现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质,再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从大到小的顺序是( )
A.甲>乙>丙
B.乙>甲>丙
C.甲>丙>乙
D.无法判断
32.X、Y、Z为三种金属,已知①X+H2SO4===XSO4+H2↑;②Y+2ZNO3===Y(NO3)2+2Z;③Y与稀硫酸不反应,则下列符合要求的X、Y、Z分别是( )
A.Fe Cu Ag
B.Cu Hg Ag
C.Mg Zn Fe
D.Fe Ag Cu
33.验证Zn、Fe、Cu金属的活动性强弱,下列的实际组合实验方案不能达到实验目的的是( )
A.FeSO4溶液、Zn、Cu
B.ZnSO4溶液、稀盐酸溶液、Fe、Cu
C.ZnSO4溶液、FeSO4溶液、Cu
D.ZnCl2溶液、CuCl2溶液、Fe
34.国产大飞机C919机壳采用了先进的铝锂合金材料。已知金属锂(Li)的活动性比铝强,下列有关说法错误的是( )
A.铝锂合金硬度大、密度小
B.铝在空气中表面会形成致密的氧化膜
C.锂能与盐酸反应,放出热量、生成氢气
D.锂能与氧气反应,生成的Li2O中Li显+2价
35.在试管中放入一根镁条(已去除氧化膜),往其中加入硝酸银溶液至浸没镁条,观察到如下现象:①镁条表面迅速覆盖一层疏松的固体物质,经检验发现生成的固体物质中有单质银;②镁条表面有明显的气泡产生,经检验发现气泡中有氢气。
对于上述实验现象的分析错误的是( )
A.镁能从硝酸银溶液中置换出银
B.镁跟硝酸银溶液反应会生成氢气
C.镁投入硝酸银溶液中只发生2AgNO3+Mg===Mg(NO3)2+2Ag
D.根据该实验可判断镁比银化学活动性强
36.化学小组为探究铝、铜、银三种金属的活动性顺序,设计了下图所示实验方案,下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.由实验甲、乙、丙可知金属活动性:Al>Cu>Ag
D.实验甲中的CuSO4改为CuCl2不能完成本实验探究
37.在Cu(NO3)2、AgNO3混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中滴加稀硫酸时无气泡产生,下列说法正确的是( )
A.滤渣中一定有Ag和Cu
B.滤渣中一定有Ag
C.滤液中一定有Cu(NO3)2
D.滤液中一定没有AgNO3
38.现有等质量的甲、乙、丙三种金属,分别放入三份浓度相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中不正确的是( )
A.生成氢气的质量:甲>乙>丙
B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:甲>乙>丙
39.下列关于金属的说法正确的是( )
A.各种金属在常温下都不能与氧气反应
B.各种金属在高温下都能与氧气反应
C.根据金属与氧气反应的难易程度可以初步比较金属的活动性
D.各种金属都能与盐酸发生置换反应
40.下列金属单质不能与稀盐酸反应放出氢气的是( )
A.Cu
B.Zn
C.Mg
D.Fe
41.下列描述中,属于金属化学性质的是( )
A.铜是紫红色固体
B.汞在常温下呈液态
C.铝能与酸反应
D.钠的质地较软
42.下列金属在一定条件下能与氧气反应,且生成物为黑色固体的一组是( )
①Mg ②Al ③Fe ④Au ⑤Cu
A.①③
B.只有③
C.③④⑤
D.③⑤
43.黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。常言道:“真金不怕火炼”主要是指( )
A.熔点高
B.延展性好
C.有金属光泽
D.化学性质稳定
44.下列属于置换反应的是( )
A.H2+CuOCu+H2O
B.2KMnO4K2MnO4+MnO2+O2↑
C.NaOH+HCl===NaCl+H2O
D.2Mg+O22MgO
45.如图,将等质量的锌和铁分别放入左、右试管中,加入等质量、等浓度的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好),下列说法正确的是( )
A.右试管中溶液为浅绿色
B.充分反应后两试管中消耗的金属的质量相等
C.U型管中液面左升右降
D.右试管比左试管产生气泡的速率快
46.金属与盐酸的反应的示意图如图所示,下列说法正确的是( )
A.实验室可用铜和稀盐酸制氢气
B.四种金属中活动性最强的是镁
C.四种金属中活动性最弱的是铁
D.铁与稀盐酸反应的化学方程式为:2Fe+6HCl===2FeCl3+3H2↑
47.以下是四个化学反应的微观示意图,图中不同的圆圈代表不同的原子,其中能表示置换反应的是( )
A B
C D
48.有A,B两种金属分别放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B
B.生成氢气的质量A>B
C.反应的硫酸质量A<B
D.反应的金属质量A<B
49.要除去铜粉中的少量铁粉,可加入下列试剂中的(
)
A.水??????B.稀盐酸????C.硫酸亚铁???
D.硝酸银溶液
50.下列反应中,溶液质量减少的是(
)
A.铁与稀硫酸
B.锌与氯化亚铁
C.铁与硫酸铜
D.镁与盐酸
51.把铁片放入下列溶液中充分反应,反应后固体的质量比反应前增加的是(
)
A.稀硫酸
B.硫酸锌溶液
C.硫酸亚铁溶液
D.硝酸银溶液
52.向氯化铜和氯化镁的混合液中,加入过量的锌粉,充分反应后过滤,滤纸上得到的固体物质是(
)
A.锌和铜
B.铜
C.镁和铜和锌
D.锌
53.将一定量的Zn、Fe混合粉末加入一定量CuSO4溶液中,充分反应后过滤,则下列对滤渣和滤液的判断中正确的是(
)
A.滤渣中加入稀硫酸一定产生气体
B.滤液不可能为无色
C.滤液中一定含Zn2+
D.滤渣不可能为三种金属
54.向AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,再向滤出的固体中加入稀硫酸,有气体产生,则滤出的固体中一定有(
)
A.Ag、Zn
B.Cu、Ag
C.Ag、Fe
D.Ag、Cu、Fe
55.向溶解有硝酸银和硝酸铜的溶液中加入一定量的铁粉,充分反应后溶液中仍有金属固体。过滤后往滤渣中加入盐酸,没有气体放出。根据上述现象,下列说法正确的是(
)
A.滤渣中一定没有Fe和Cu??
B.滤渣中一定有Ag和Cu?
C.滤液中一定有Fe(NO3)2????D.滤液中一定没有AgNO3,一定有Cu(NO3)2
56.等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系
如图所示,下列叙述正确的是(
)
A.M、N两种金属中较活泼的是N
B.生成H2的质量M<N
C.相对原子质量较大的是M
D.
产生H2的速率M>N
1.下列金属放入Cu(NO3)2溶液中,能生成红色固体,溶液由蓝色变成浅绿色的是 ( )
A.Ag
B.Zn
C.Cu
D.Fe
2.黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。常言说:“真金不怕火炼”主要是指 ( )
A.熔点高
B.延展性好
C.有金属光泽
D.化学性质稳定
3.下列各物质恰好完全反应,所得溶液的颜色是无色的是 ( )
A.铁和硫酸铜溶液
B.铁和稀硫酸
C.锌和稀硫酸
D.铁和稀盐酸
4.将一根洁净的铁钉放入稀硫酸中,下列预测可能不正确的是
( )
A.铁钉表面将产生气泡
B.铁钉表面将很快出现铁锈
C.溶液由无色变为浅绿色
D.溶液质量将增加
5.市面上有不法商贩使用颜色和外形与黄金十分相似的假黄金(铜锌合金)来蒙骗消费者。请你利用所学知识判断,下列方案不能区分真假黄金的是 ( )
A.放在稀硫酸中
B.在空气中灼烧
C.测密度
D.认真观察颜色
6.根据金属活动性顺序进行分析,下列描述或判断错误的是
( )
A.常温下,金属镁在空气中要比铁容易氧化
B.常温下,铝能和稀盐酸反应,而银不能
C.在氧气中灼烧时,铁丝要比铜丝反应剧烈
D.将铜丝插入硝酸银溶液中,不能反应得到银
7.金属M与AgNO3溶液反应的化学方程式为M
+
2AgNO3
M(NO3)2+2Ag。下列说法不正确的是 ( )
A.该反应属于置换反应
B.金属M可能是铝
C.M的金属活动性比Ag强
D.反应前后M的化合价改变
8.“真金不怕火炼”的原因是( )
A.金的硬度大
B.金的熔点高
C.金的密度大
D.金的化学性质稳定
9.下列有关金属性质的说法错误的是( )
A.铜、银等金属具有良好的导电性,可制造导线
B.铁在纯氧气中能燃烧,生成四氧化三铁
C.铝制品能形成致密的保护膜,则不可磨损铝的表面
D.铁与稀盐酸反应可生成氯化铁
10.将少量的生铁放入足量的盐酸中充分反应,有黑色的残渣剩余,该残渣主要是( )
A.单质碳
B.氯化铁
C.氯化亚铁
D.单质铁
11.下列各组实验,不能说明铁和铜的金属活动性强弱的是( )
A.铁丝和铜丝分别插入稀硫酸中
B.铁丝和铜丝分别插入硝酸银溶液中
C.铜丝插入硫酸亚铁溶液中
D.铁丝插入硫酸铜溶液中
12.下列物质可由金属与酸直接反应制得的是( )
A.AgCl
B.CuSO4
C.Fe2(SO4)3
D.AlCl3
13.铜、镁的金属活动性时,下列现象、分析或结论正确的是( )
A.盐酸的浓度可以不同
B.铜片表面有气泡
C.镁片的试管表面发烫
D.活动性Zn>Mg>Cu
14.为了验证Zn、Fe、Cu三种金属的活动顺序为:Zn>Fe>Cu这一结论,下面实验设计合理的是( )
A.将Zn、Cu两金属片分别放入稀硫酸中
B.将Fe、Cu两金属片分别放入稀盐酸中
C.将Zn、Fe两金属片分别放入CuSO4溶液中
D.将Zn、Cu两金属片分别放入FeSO4溶液中
15.“愚人金”实为铜锌合金,外观与黄金极为相似,常被不法商贩冒充黄金牟取暴利。下列关于鉴别“愚人金”与黄金的实验方案,合理的是( )
A.测质量,质量小的是“愚人金”
B.灼烧,表面变紫红色的是“愚人金”
C.浸没在稀硫酸中,表面有气泡产生的是“愚人金”
D.浸没在硫酸锌溶液中,表面附着白色物质的是“愚人金”
16.下列有关铁的化学方程式中正确的是(
)
A.4Fe+3O22Fe2O3
B.Fe+H2SO4
====
FeSO4+H2↑
C.2Fe+6HCl
====
2FeCl3+3H2↑
D.2Fe+3CuSO4
====
3Cu+Fe2(SO4)3
17.能与无色硝酸银溶液反应,使溶液变为蓝色的金属是(
)
A.铝
B.铁
C.铜
D.银
18.把金属X放入Cu(NO3)2溶液中,X表面有红色固体析出;若放入Mg(NO3)2溶液中,无明显现象。则X、Cu、Mg三种金属活动性由强到弱的顺序正确的是(
)
A.Mg、X、Cu
B.X、Mg、Cu
C.Mg、Cu、X
D.Cu、X、Mg
19.将一枚洁净的铁钉浸入稀硫酸中,下列叙述中正确的是(
)
①铁钉表面产生气泡;②液体由无色逐渐变为浅绿色;③铁钉的质量减轻;
④液体的质量减轻。
A.②③
B.①②④
C.①②③
D.①②③④
20.下列事实不能说明Zn比Ag活泼的是(
)
A.Zn能与AgNO3溶液反应,置换出Ag
B.Zn能与稀硫酸反应,Ag则不能
C.自然界没有以单质形式存在的Zn,而有以单质形式存在的Ag
D.Zn的熔点为420
℃,Ag的熔点为962
℃
21.下列有关金属的说法正确的是(
)
A.铝具有很好的抗腐蚀性能
B.铜能置换出酸中的氢
C.钢是纯净物
D.银能把铁从氯化亚铁溶液中置换出来
22.把铁粉放入硝酸银、硝酸铜和硝酸锌的混合溶液中,充分反应后过滤,所得到的固体中一定没有的是(
)
A.锌
B.铁
C.铜
D.银
23.常见金属活动性顺序表如下:
下列各组物质不能发生化学反应的是(
)
A.汞与硝酸银溶液
B.铜与硝酸镁溶液
C.锌与硫酸亚铁溶液
D.铝与稀盐酸
24.甲、乙、丙、丁四种金属。甲即使在高温时也不与氧气反应。乙、丙、丁在一定条件下都能与氧气反应。丁盐的水溶液可用丙制的容器盛放,但不能用乙制的容器盛放。这四种金属的活动性由强到弱的顺序是(
)
A.甲>乙>丁>丙
B.丙>丁>乙>甲
C.丙>乙>丁>甲
D.乙>丁>丙>甲
25.如图,在杠杆的两端分别挂着质量相等的铜球和锌球,这时杠杆平衡。然后将两球分别浸没在稀硫酸和CuSO4溶液中片刻,下列说法中正确的是(
)
A.只有左边烧杯中溶液的质量增加
B.只有右边烧杯中溶液的质量增加
C.两边烧杯中溶液的质量都增加
D.去掉烧杯后,杠杆仍然保持平衡
26.金属活动性顺序表在化学学习中有重要作用,下列说法正确的是( )
A.Zn不能置换出稀硫酸中的氢
B.Ag能将硝酸铜溶液中的铜置换出来
C.在Al、Mg、Fe中金属活动性最强的是Al
D.“真金不怕火炼”说明金在高温时也不与氧气反应
27.下列事实能说明铝的金属活动性比铁或铜强的是( )
A.铝在地壳中含量比铁高
B.铝的熔点低于铜的熔点
C.空气中铁比铝更容易被腐蚀
D.铝丝在硫酸铜溶液中能形成“铜树”
28.钛合金是生产链条钢、锚链钢等的重要材料。如果比较钛(Ti)和铁的金属活动顺序,以下方法不能达到的目的是( )
A.查阅初中化学课本上的金属活动性顺序
B.利用金属钛和FeCl2溶液进行实验
C.利用金属铁和TiSO4溶液进行实验
D.利用金属钛、金属铁与稀硫酸进行实验
29.常见金属X与硝酸银溶液反应的化学方程式为X+3AgNO3===3Ag+X(NO3)3,有关该反应说法错误的是( )
A.该反应是置换反应
B.X可能是铁
C.金属活动性X>Ag
D.X表面有固体析出
30.下列事实不能用金属的活动性顺序加以解释的是( )
A.不能用铜与稀硫酸反应制取氢气
B.铁能置换出硫酸铜溶液中的铜
C.在化合物中,铁显+2、+3价,铜显+1、+2价
D.相同条件下,锌和铁与稀硫酸反应的剧烈程度
31.现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质,再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从大到小的顺序是( )
A.甲>乙>丙
B.乙>甲>丙
C.甲>丙>乙
D.无法判断
32.X、Y、Z为三种金属,已知①X+H2SO4===XSO4+H2↑;②Y+2ZNO3===Y(NO3)2+2Z;③Y与稀硫酸不反应,则下列符合要求的X、Y、Z分别是( )
A.Fe Cu Ag
B.Cu Hg Ag
C.Mg Zn Fe
D.Fe Ag Cu
33.验证Zn、Fe、Cu金属的活动性强弱,下列的实际组合实验方案不能达到实验目的的是( )
A.FeSO4溶液、Zn、Cu
B.ZnSO4溶液、稀盐酸溶液、Fe、Cu
C.ZnSO4溶液、FeSO4溶液、Cu
D.ZnCl2溶液、CuCl2溶液、Fe
34.国产大飞机C919机壳采用了先进的铝锂合金材料。已知金属锂(Li)的活动性比铝强,下列有关说法错误的是( )
A.铝锂合金硬度大、密度小
B.铝在空气中表面会形成致密的氧化膜
C.锂能与盐酸反应,放出热量、生成氢气
D.锂能与氧气反应,生成的Li2O中Li显+2价
35.在试管中放入一根镁条(已去除氧化膜),往其中加入硝酸银溶液至浸没镁条,观察到如下现象:①镁条表面迅速覆盖一层疏松的固体物质,经检验发现生成的固体物质中有单质银;②镁条表面有明显的气泡产生,经检验发现气泡中有氢气。
对于上述实验现象的分析错误的是( )
A.镁能从硝酸银溶液中置换出银
B.镁跟硝酸银溶液反应会生成氢气
C.镁投入硝酸银溶液中只发生2AgNO3+Mg===Mg(NO3)2+2Ag
D.根据该实验可判断镁比银化学活动性强
36.化学小组为探究铝、铜、银三种金属的活动性顺序,设计了下图所示实验方案,下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.由实验甲、乙、丙可知金属活动性:Al>Cu>Ag
D.实验甲中的CuSO4改为CuCl2不能完成本实验探究
37.在Cu(NO3)2、AgNO3混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中滴加稀硫酸时无气泡产生,下列说法正确的是( )
A.滤渣中一定有Ag和Cu
B.滤渣中一定有Ag
C.滤液中一定有Cu(NO3)2
D.滤液中一定没有AgNO3
38.现有等质量的甲、乙、丙三种金属,分别放入三份浓度相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。则下列说法中不正确的是( )
A.生成氢气的质量:甲>乙>丙
B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:甲>乙>丙
39.下列关于金属的说法正确的是( )
A.各种金属在常温下都不能与氧气反应
B.各种金属在高温下都能与氧气反应
C.根据金属与氧气反应的难易程度可以初步比较金属的活动性
D.各种金属都能与盐酸发生置换反应
40.下列金属单质不能与稀盐酸反应放出氢气的是( )
A.Cu
B.Zn
C.Mg
D.Fe
41.下列描述中,属于金属化学性质的是( )
A.铜是紫红色固体
B.汞在常温下呈液态
C.铝能与酸反应
D.钠的质地较软
42.下列金属在一定条件下能与氧气反应,且生成物为黑色固体的一组是( )
①Mg ②Al ③Fe ④Au ⑤Cu
A.①③
B.只有③
C.③④⑤
D.③⑤
43.黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。常言道:“真金不怕火炼”主要是指( )
A.熔点高
B.延展性好
C.有金属光泽
D.化学性质稳定
44.下列属于置换反应的是( )
A.H2+CuOCu+H2O
B.2KMnO4K2MnO4+MnO2+O2↑
C.NaOH+HCl===NaCl+H2O
D.2Mg+O22MgO
45.如图,将等质量的锌和铁分别放入左、右试管中,加入等质量、等浓度的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好),下列说法正确的是( )
A.右试管中溶液为浅绿色
B.充分反应后两试管中消耗的金属的质量相等
C.U型管中液面左升右降
D.右试管比左试管产生气泡的速率快
46.金属与盐酸的反应的示意图如图所示,下列说法正确的是( )
A.实验室可用铜和稀盐酸制氢气
B.四种金属中活动性最强的是镁
C.四种金属中活动性最弱的是铁
D.铁与稀盐酸反应的化学方程式为:2Fe+6HCl===2FeCl3+3H2↑
47.以下是四个化学反应的微观示意图,图中不同的圆圈代表不同的原子,其中能表示置换反应的是( )
A B
C D
48.有A,B两种金属分别放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
A.金属活动性A>B
B.生成氢气的质量A>B
C.反应的硫酸质量A<B
D.反应的金属质量A<B
49.要除去铜粉中的少量铁粉,可加入下列试剂中的(
)
A.水??????B.稀盐酸????C.硫酸亚铁???
D.硝酸银溶液
50.下列反应中,溶液质量减少的是(
)
A.铁与稀硫酸
B.锌与氯化亚铁
C.铁与硫酸铜
D.镁与盐酸
51.把铁片放入下列溶液中充分反应,反应后固体的质量比反应前增加的是(
)
A.稀硫酸
B.硫酸锌溶液
C.硫酸亚铁溶液
D.硝酸银溶液
52.向氯化铜和氯化镁的混合液中,加入过量的锌粉,充分反应后过滤,滤纸上得到的固体物质是(
)
A.锌和铜
B.铜
C.镁和铜和锌
D.锌
53.将一定量的Zn、Fe混合粉末加入一定量CuSO4溶液中,充分反应后过滤,则下列对滤渣和滤液的判断中正确的是(
)
A.滤渣中加入稀硫酸一定产生气体
B.滤液不可能为无色
C.滤液中一定含Zn2+
D.滤渣不可能为三种金属
54.向AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,再向滤出的固体中加入稀硫酸,有气体产生,则滤出的固体中一定有(
)
A.Ag、Zn
B.Cu、Ag
C.Ag、Fe
D.Ag、Cu、Fe
55.向溶解有硝酸银和硝酸铜的溶液中加入一定量的铁粉,充分反应后溶液中仍有金属固体。过滤后往滤渣中加入盐酸,没有气体放出。根据上述现象,下列说法正确的是(
)
A.滤渣中一定没有Fe和Cu??
B.滤渣中一定有Ag和Cu?
C.滤液中一定有Fe(NO3)2????D.滤液中一定没有AgNO3,一定有Cu(NO3)2
56.等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系
如图所示,下列叙述正确的是(
)
A.M、N两种金属中较活泼的是N
B.生成H2的质量M<N
C.相对原子质量较大的是M
D.
产生H2的速率M>N
同课章节目录
