2020年人教版九年级化学下学期第8单元 课题 3 金属资源的利用和保护:铁的冶炼精选练习题27道(无答案)
文档属性
| 名称 | 2020年人教版九年级化学下学期第8单元 课题 3 金属资源的利用和保护:铁的冶炼精选练习题27道(无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 382.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-15 00:00:00 | ||
图片预览



文档简介
2020年人教版九年级化学下学期第8单元:铁的冶炼精选练习题27道无答案
一.选择题(共5小题)
1.下列关于铁的说法中正确的是( )
A.纯铁比生铁硬
B.铁矿石、焦炭、石灰石是高炉炼铁的原料
C.可用铁制容器配制波尔多液
D.钢的含碳量比生铁高
2.下列说法正确的是( )
A.原子通过得失电子形成离子,离子也可以通过得失电子变成原子
B.化学反应中原子数目不变,则分子数目也不变
C.高炉炼铁中焦炭的作用只是提高炉温
D.甲烷燃烧生成CO2和H2O,则甲烷中一定含有C、H、O元素
3.下列有关金属及其合金的叙述,正确的是( )
A.生铁的熔点比纯铁高
B.高炉冶铁最终得到的是纯铁
C.铝比铁的抗腐蚀性好,是因为其表面易形成致密的氧化物保护膜
D.铜与盐酸反应生成氢气
4.下列与铁有关的说法正确的是( )
A.生铁和钢都是铁的合金
B.炼铁是把单质铁变成氧化铁的过程
C.铁制污水管道可常用废酸液冲洗
D.被腐蚀的铁制品属于不可回收垃圾
5.下列叙述正确的是( )
A.英国化学家拉瓦锡用定量的方法研究了空气的成分,弄清了燃烧的本质
B.工业炼铁的原理是在高温的条件下,利用一氧化碳将铁矿石中的铁置换出来
C.含有同种元素且由一种物质组成,则该物质一定是单质
D.将煤砸成小块可以使煤充分的燃烧,减少一氧化碳和二氧化硫的产生
二.多选题(共1小题)
6.下列属于冶铁过程中发生的是还原反应的是( )
A.C+O2CO2
B.CO2+C2CO
C.2CO+O22CO2
D.Fe3O4+4CO3Fe+4CO2
三.填空题(共13小题)
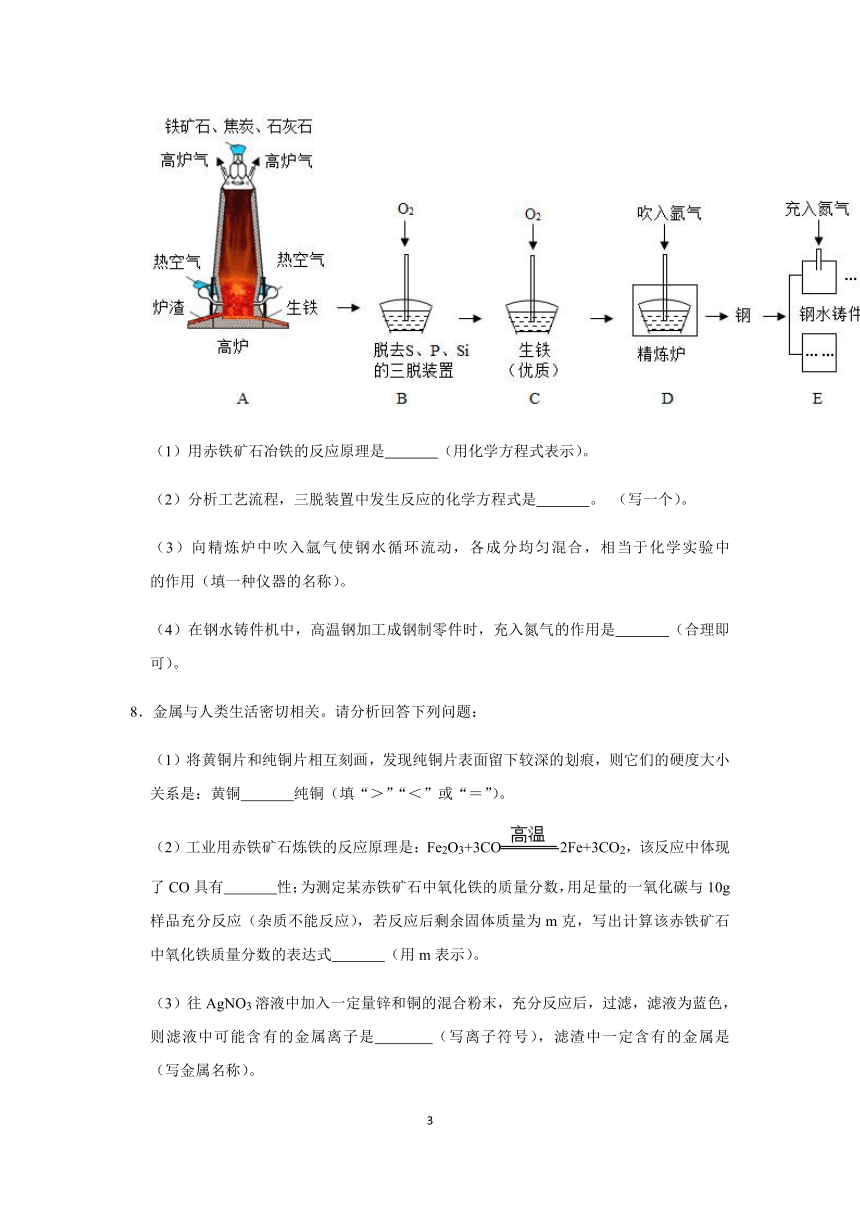
7.科学精神与社会责任,是化学学科素养更高层面的价值追求。在一次实践活动中,小红和同学们一起参观了某钢铁公司,大家对矿石选取、冶铁和炼钢的工艺流程(如图)、生铁和钢的区别等,有了全新的认识。
(1)用赤铁矿石冶铁的反应原理是
(用化学方程式表示)。
(2)分析工艺流程,三脱装置中发生反应的化学方程式是
。
(写一个)。
(3)向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,相当于化学实验中
的作用(填一种仪器的名称)。
(4)在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是
(合理即可)。
8.金属与人类生活密切相关。请分析回答下列问题:
(1)将黄铜片和纯铜片相互刻画,发现纯铜片表面留下较深的划痕,则它们的硬度大小关系是:黄铜
纯铜(填“>”“<”或“=”)。
(2)工业用赤铁矿石炼铁的反应原理是:Fe2O3+3CO2Fe+3CO2,该反应中体现了CO具有
性;为测定某赤铁矿石中氧化铁的质量分数,用足量的一氧化碳与10g样品充分反应(杂质不能反应),若反应后剩余固体质量为m克,写出计算该赤铁矿石中氧化铁质量分数的表达式
(用m表示)。
(3)往AgNO3溶液中加入一定量锌和铜的混合粉末,充分反应后,过滤,滤液为蓝色,则滤液中可能含有的金属离子是
(写离子符号),滤渣中一定含有的金属是
(写金属名称)。
(4)稀土元素铕是激光和原子能应用的重要材料。已知三氯化铕的化学式为EuCl3,则氧化铕的化学式为
。
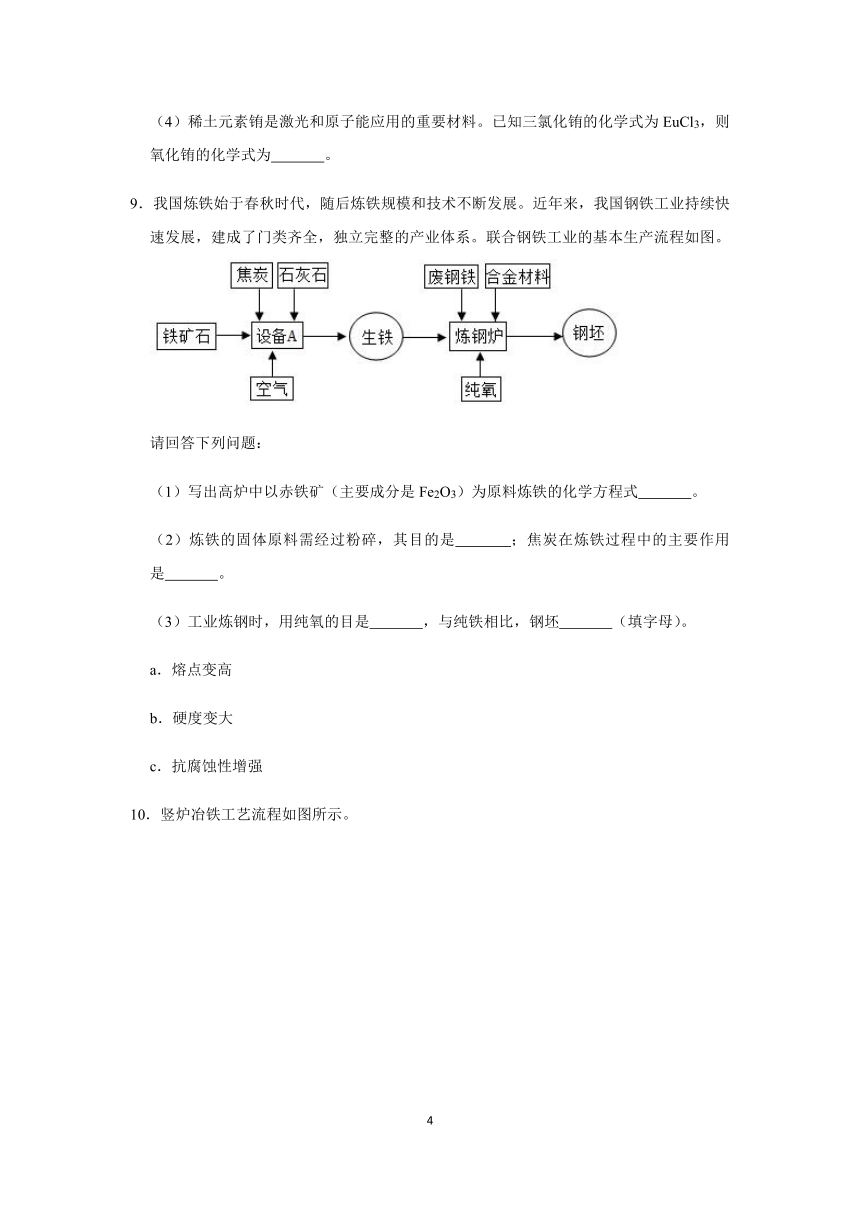
9.我国炼铁始于春秋时代,随后炼铁规模和技术不断发展。近年来,我国钢铁工业持续快速发展,建成了门类齐全,独立完整的产业体系。联合钢铁工业的基本生产流程如图。
请回答下列问题:
(1)写出高炉中以赤铁矿(主要成分是Fe2O3)为原料炼铁的化学方程式
。
(2)炼铁的固体原料需经过粉碎,其目的是
;焦炭在炼铁过程中的主要作用是
。
(3)工业炼钢时,用纯氧的目是
,与纯铁相比,钢坯
(填字母)。
a.熔点变高
b.硬度变大
c.抗腐蚀性增强
10.竖炉冶铁工艺流程如图所示。
回答下列问题:
(1)该工艺流程中,甲烷的作用是
,冶炼出的铁水属于
(填“纯净物”或“混合物”)。
(2)用化学方程式表示还原反应室内炼铁的原理
。(写一个)
(3)该工艺流程中,可循环利用的物质是
。
11.某钢厂高炉炼铁的主要原料是焦炭、赤铁矿(主要成分是Fe2O3)、空气等,主要反应过程如下所示:
焦炭[A][B]生铁
(1)请写出A、B的化学式:A
B
(2)写出②、③两步反应的化学方程式.
②
,
③
.
(3)从高炉上排出的废气叫高炉废气,请推测高炉废气的主要成份为
.
12.炼铁选用的铁矿不仅要选含铁量高的,还要选“有害元素”少的.常见的铁矿有:磁铁矿(主要成分是Fe3O4)、赤铁矿(主要成分是Fe2O3)、褐铁矿(主要成分是2Fe2O3?3H2O)、菱铁矿(主要成分是FeCO3)、黄铁矿(主要成分是FeS2).你认为最适宜炼铁的矿石是
,理由是
.
13.能源与污染是当今两大难题:
(1)煤作为燃料时常会伴随产生二氧化硫而引起酸雨,请写出煤燃烧过程中由于硫单质燃烧产生二氧化硫的化学方程式
。
(2)汽车尾气中含有CO、NO,会污染空气,一种新型催化剂能使二者发生反应,反应的化学方程式为2CO+2NOX+2CO2,X的化学式为
。
(3)为了使空气更清新,为了环境更美好,下列做法正确的是
(填序号)。
A、出行尽量使用公共交通工具,少开私家车
B、工业废气处理合格后再排放
C、大力发展火力发电,增强电力
D、多植树造林,增强绿化
(4
)请写出工业上用赤铁矿炼铁的化学反应方程式
。
14.工业上用赤铁矿(主要成分为Fe2O3)和CO炼铁,该反应的化学方程式为:
。
15.工业上经常用赤铁矿(主要成分是Fe2O3)和一氧化碳在高温条件下来炼铁,同时产生二氧化碳气体,试写出该反应的化学方程式
;工人师傅经常用金刚石做成的玻璃刀来划玻璃,这是利用金刚石的
的物理性质.
16.铁和铁的合金是目前使用非常广泛的一种金属材料,如图是铁原子结构示意图,仔细分析并回答:
(1)人体缺铁容易患贫血病,这里的“铁”是指
(填“分子、原子、离子、元素”);
(2)铁原子结构示意图中,有
个电子层,x的值为
;
(3)工业上用赤铁矿(主要成分是Fe2O3)来炼铁,化学反应原理是:
。
17.我国金属冶炼的技术在不断发展。
(1)春秋时期由于炉温较低,铁矿石未完全反应,得到的“块炼铁”中含有较多杂质。“块炼铁”属于
(填“混合物”或“纯净物”)。
(2)宋代《天工开物》中记载,为提高冶炼温度,使用了一种固体化石燃料来代替木炭,这种固体化石燃料是
;同时,还用风箱鼓入空气,其中利用氧气的性质是
。
18.活性炭可用于净水,其净水原理是
使新型自来水消毒剂ClO2可由如下的反应制取:Cl2+2X=2NaCl+2ClO2,则x的化学式为
工业上高炉炼铁的原理(以磁铁矿为例,用化学方程式表示)
。
19.如图是炼铁高炉的结构示意图,请回答下列与此有关的问题。
(1)炼铁的反应原理是用CO还原氧化铁
(写出化学方程式)。
(2)在炼铁原料中使用焦炭的目的是
(答一点)。
(3)铁及铁合金在空气中存放时易生锈,铁生锈与空气中的
有关。用硝酸盐
(填化学式)溶液可以一次性验证Fe、Cu、Ag三种金属的活动性顺序。
四.解答题(共8小题)
20.我国是钢铁大国,粗钢产量占世界的一半。工业炼钢的主要流程如图所示。
(1)高炉中用CO还原Fe2O3的化学方程式为
。
(2)除铁矿石外,高炉中主要还有下列物质发生了反应:
①CaCO3CaO+CO2↑
②CO2+C2CO
③C+O2CO2
其中属于化合反应的是
(填数字序号);这三个反应中,碳元素的化合价共有
种。
(3)根据信息推测,转炉中产生的气体X可能是
(写出一种即可)。
21.金属在日常生活、工农业生产和科学研究方面应用广泛。
(1)铜可用来制作导线,是因为其具有良好的延展性和
。
(2)天津的解放桥是一座全钢结构可开启的桥梁,它是天津的标志性建筑物之一。
①钢属于
(填“单质”、“纯净物”或“混合物”)。
②工业上用一氧化碳和赤铁矿炼铁的原理是
(写化学方程式)。
③建造这座桥大约用了112t铁,理论需要含氧化铁80%的赤铁矿
t。
(3)为探究铁、铜、银的金属活动性顺序,同学们设计了如图所示的两步实验。
①第1步实验的目的是
。
②第2步实验中,为了达到实验目的,溶液甲可以是
(填序号)。
A.稀盐酸
B.FeSO4溶液
C.CuSO4溶液
D.ZnSO4溶液
22.如图是冶炼生铁及相关流程。请认真读图回答问题:
(1)赤铁矿需要经过粉碎处理,其目的是
。
(2)该工艺流程中,“燃烧室”发生的反应化学方程式是
,冶炼出的铁水属于
(填“纯净物”或“混合物”)。
(3)该工艺流程中,可循环利用的物质是
。
(4)生铁比钢的含碳量
(填“高”或“低”),写出生铁炼钢的主要反应原理
(用化学方程式表示)。
23.2018年10月23日,举世瞩目的港珠澳大桥正式开通,其总用钢量接近100万吨!请根据所学金属的有关知识回答:
(1)以赤铁矿为例,写出工业炼铁的反应原理。
(2)向m克AgNO3、Cu(NO3)2
和Fe(NO3)2的混合溶液中加入Zn,充分反应后过滤,所得滤液质量仍为m克,则滤渣中一定有什么物质?并写出可能发生的反应的化学方程式。
24.竖炉炼铁是一种重要的炼铁方法,其工艺流程如图所示。
(1)赤铁矿属于
(填“纯净物”或“混合物”)。
(2)用化学方程式表示竖炉内进行的反应:
a.还原反应室内
(任意选择一个)。
b.燃烧室内
。
(3)下列说法正确的是
(填序号)。
A.加入的铁矿石要进行粉碎,目的是加快反应速率和提高原料利用率
B.该工艺流程中,可循环利用的物质有高温尾气(CO2和H2O)和CH4
C.燃烧室内进行的反应为炼铁提供了大量热量
D.竖炉炼铁得到的产品为纯铁
25.下面连环画(图1)记录了雯雯参观中国地质博物馆的一天。
请据图回答问题
(1)她吃早餐。陶瓷餐盘的主要成分之一是硅酸钙(CaSiO3),其中硅元素的化合价是
。
(2)她出发了。如图③所示,乘坐地铁禁止携带的物品中,属于易燃易爆品的是
。
(3)她来到博物馆门口。同学们在地质学家李四光的大理石雕像前,了解他的生平事迹。大理石的主要成分是
。
(4)她和同学们进入博物馆。
她看到了许多矿石标本,其中的4
种矿石及其主要成分如图2:
①上述矿石标本的主要成分中,所含元素种类最多的是
(填字母序号)。
②她根据辉铜矿的主要成分,推测以辉铜矿为原料,可制得含铜元素或含硫元素的产品,她的依据是化学反应前后不变。
③她依据化学式计算出Cu2(OH)2CO3的相对分子质量为222,计算式为
。
(5)参观结束时,老师进行了小结,并就金属冶炼和金属回收再利用提出了一些问题,请同学们作答。
①工业上用一氧化碳和赤铁矿炼铁的原理是
(用化学方程式表示)。
②我国是世界上最早采用湿法冶金提取铜的国家,写出铁与硫酸铜溶液反应制取铜的化学方程式
,该反应的现象是
。
③在含有氯化锌、氯化铜和氯化亚铁的废液中加入一定量的铁粉可以充分回收利用金属资源,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生,可以判断滤液的可能成分是
。
26.铁是我们日常生活中一种常见的金属,但你是否真正了解它呢,快来参加“铁知识竞赛吧。
(1)铁它是由
(选填“原子”、“分子”或“离子”)构成的物质。日常生活中我们所用的钢铁是一种
(选填“纯金属“或“合金”)。
(2)工业中常用一氧化碳还原赤铁矿来炼铁,其中赤铁矿的主要成分是
,写出工业炼铁时,高炉内发生一氧化碳还原赤铁矿反应的化学方程式:
。
(3)若要验证的Fe、Cu和Al的金属活动性顺序,只需一种试剂直接与上述三种金属反应就能达到目的,该试剂是
(填序号)。
A.硫酸铝溶液
B.硫酸亚铁溶液
C.硫酸铜溶液
27.运用广泛的金属材料是钢铁,如图是冶炼生铁相关流程。请认真读图回答问题:
(1)高炉冶炼生铁的原料有铁矿石、焦炭和
。
冶炼时将原料粉碎后再使用的原因是
。
(2)焦炭在冶炼中的作用为①提供高温,②
。赤铁矿(主要成分Fe2O3)炼铁的反应原理是
。
(3)炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是
。
(4)钢铁的锈蚀造成极大的损失和浪费。但如果将“铁生锈”原理应用得当,同样可以造福人类,请举例
(写一条)。
一.选择题(共5小题)
1.下列关于铁的说法中正确的是( )
A.纯铁比生铁硬
B.铁矿石、焦炭、石灰石是高炉炼铁的原料
C.可用铁制容器配制波尔多液
D.钢的含碳量比生铁高
2.下列说法正确的是( )
A.原子通过得失电子形成离子,离子也可以通过得失电子变成原子
B.化学反应中原子数目不变,则分子数目也不变
C.高炉炼铁中焦炭的作用只是提高炉温
D.甲烷燃烧生成CO2和H2O,则甲烷中一定含有C、H、O元素
3.下列有关金属及其合金的叙述,正确的是( )
A.生铁的熔点比纯铁高
B.高炉冶铁最终得到的是纯铁
C.铝比铁的抗腐蚀性好,是因为其表面易形成致密的氧化物保护膜
D.铜与盐酸反应生成氢气
4.下列与铁有关的说法正确的是( )
A.生铁和钢都是铁的合金
B.炼铁是把单质铁变成氧化铁的过程
C.铁制污水管道可常用废酸液冲洗
D.被腐蚀的铁制品属于不可回收垃圾
5.下列叙述正确的是( )
A.英国化学家拉瓦锡用定量的方法研究了空气的成分,弄清了燃烧的本质
B.工业炼铁的原理是在高温的条件下,利用一氧化碳将铁矿石中的铁置换出来
C.含有同种元素且由一种物质组成,则该物质一定是单质
D.将煤砸成小块可以使煤充分的燃烧,减少一氧化碳和二氧化硫的产生
二.多选题(共1小题)
6.下列属于冶铁过程中发生的是还原反应的是( )
A.C+O2CO2
B.CO2+C2CO
C.2CO+O22CO2
D.Fe3O4+4CO3Fe+4CO2
三.填空题(共13小题)
7.科学精神与社会责任,是化学学科素养更高层面的价值追求。在一次实践活动中,小红和同学们一起参观了某钢铁公司,大家对矿石选取、冶铁和炼钢的工艺流程(如图)、生铁和钢的区别等,有了全新的认识。
(1)用赤铁矿石冶铁的反应原理是
(用化学方程式表示)。
(2)分析工艺流程,三脱装置中发生反应的化学方程式是
。
(写一个)。
(3)向精炼炉中吹入氩气使钢水循环流动,各成分均匀混合,相当于化学实验中
的作用(填一种仪器的名称)。
(4)在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是
(合理即可)。
8.金属与人类生活密切相关。请分析回答下列问题:
(1)将黄铜片和纯铜片相互刻画,发现纯铜片表面留下较深的划痕,则它们的硬度大小关系是:黄铜
纯铜(填“>”“<”或“=”)。
(2)工业用赤铁矿石炼铁的反应原理是:Fe2O3+3CO2Fe+3CO2,该反应中体现了CO具有
性;为测定某赤铁矿石中氧化铁的质量分数,用足量的一氧化碳与10g样品充分反应(杂质不能反应),若反应后剩余固体质量为m克,写出计算该赤铁矿石中氧化铁质量分数的表达式
(用m表示)。
(3)往AgNO3溶液中加入一定量锌和铜的混合粉末,充分反应后,过滤,滤液为蓝色,则滤液中可能含有的金属离子是
(写离子符号),滤渣中一定含有的金属是
(写金属名称)。
(4)稀土元素铕是激光和原子能应用的重要材料。已知三氯化铕的化学式为EuCl3,则氧化铕的化学式为
。
9.我国炼铁始于春秋时代,随后炼铁规模和技术不断发展。近年来,我国钢铁工业持续快速发展,建成了门类齐全,独立完整的产业体系。联合钢铁工业的基本生产流程如图。
请回答下列问题:
(1)写出高炉中以赤铁矿(主要成分是Fe2O3)为原料炼铁的化学方程式
。
(2)炼铁的固体原料需经过粉碎,其目的是
;焦炭在炼铁过程中的主要作用是
。
(3)工业炼钢时,用纯氧的目是
,与纯铁相比,钢坯
(填字母)。
a.熔点变高
b.硬度变大
c.抗腐蚀性增强
10.竖炉冶铁工艺流程如图所示。
回答下列问题:
(1)该工艺流程中,甲烷的作用是
,冶炼出的铁水属于
(填“纯净物”或“混合物”)。
(2)用化学方程式表示还原反应室内炼铁的原理
。(写一个)
(3)该工艺流程中,可循环利用的物质是
。
11.某钢厂高炉炼铁的主要原料是焦炭、赤铁矿(主要成分是Fe2O3)、空气等,主要反应过程如下所示:
焦炭[A][B]生铁
(1)请写出A、B的化学式:A
B
(2)写出②、③两步反应的化学方程式.
②
,
③
.
(3)从高炉上排出的废气叫高炉废气,请推测高炉废气的主要成份为
.
12.炼铁选用的铁矿不仅要选含铁量高的,还要选“有害元素”少的.常见的铁矿有:磁铁矿(主要成分是Fe3O4)、赤铁矿(主要成分是Fe2O3)、褐铁矿(主要成分是2Fe2O3?3H2O)、菱铁矿(主要成分是FeCO3)、黄铁矿(主要成分是FeS2).你认为最适宜炼铁的矿石是
,理由是
.
13.能源与污染是当今两大难题:
(1)煤作为燃料时常会伴随产生二氧化硫而引起酸雨,请写出煤燃烧过程中由于硫单质燃烧产生二氧化硫的化学方程式
。
(2)汽车尾气中含有CO、NO,会污染空气,一种新型催化剂能使二者发生反应,反应的化学方程式为2CO+2NOX+2CO2,X的化学式为
。
(3)为了使空气更清新,为了环境更美好,下列做法正确的是
(填序号)。
A、出行尽量使用公共交通工具,少开私家车
B、工业废气处理合格后再排放
C、大力发展火力发电,增强电力
D、多植树造林,增强绿化
(4
)请写出工业上用赤铁矿炼铁的化学反应方程式
。
14.工业上用赤铁矿(主要成分为Fe2O3)和CO炼铁,该反应的化学方程式为:
。
15.工业上经常用赤铁矿(主要成分是Fe2O3)和一氧化碳在高温条件下来炼铁,同时产生二氧化碳气体,试写出该反应的化学方程式
;工人师傅经常用金刚石做成的玻璃刀来划玻璃,这是利用金刚石的
的物理性质.
16.铁和铁的合金是目前使用非常广泛的一种金属材料,如图是铁原子结构示意图,仔细分析并回答:
(1)人体缺铁容易患贫血病,这里的“铁”是指
(填“分子、原子、离子、元素”);
(2)铁原子结构示意图中,有
个电子层,x的值为
;
(3)工业上用赤铁矿(主要成分是Fe2O3)来炼铁,化学反应原理是:
。
17.我国金属冶炼的技术在不断发展。
(1)春秋时期由于炉温较低,铁矿石未完全反应,得到的“块炼铁”中含有较多杂质。“块炼铁”属于
(填“混合物”或“纯净物”)。
(2)宋代《天工开物》中记载,为提高冶炼温度,使用了一种固体化石燃料来代替木炭,这种固体化石燃料是
;同时,还用风箱鼓入空气,其中利用氧气的性质是
。
18.活性炭可用于净水,其净水原理是
使新型自来水消毒剂ClO2可由如下的反应制取:Cl2+2X=2NaCl+2ClO2,则x的化学式为
工业上高炉炼铁的原理(以磁铁矿为例,用化学方程式表示)
。
19.如图是炼铁高炉的结构示意图,请回答下列与此有关的问题。
(1)炼铁的反应原理是用CO还原氧化铁
(写出化学方程式)。
(2)在炼铁原料中使用焦炭的目的是
(答一点)。
(3)铁及铁合金在空气中存放时易生锈,铁生锈与空气中的
有关。用硝酸盐
(填化学式)溶液可以一次性验证Fe、Cu、Ag三种金属的活动性顺序。
四.解答题(共8小题)
20.我国是钢铁大国,粗钢产量占世界的一半。工业炼钢的主要流程如图所示。
(1)高炉中用CO还原Fe2O3的化学方程式为
。
(2)除铁矿石外,高炉中主要还有下列物质发生了反应:
①CaCO3CaO+CO2↑
②CO2+C2CO
③C+O2CO2
其中属于化合反应的是
(填数字序号);这三个反应中,碳元素的化合价共有
种。
(3)根据信息推测,转炉中产生的气体X可能是
(写出一种即可)。
21.金属在日常生活、工农业生产和科学研究方面应用广泛。
(1)铜可用来制作导线,是因为其具有良好的延展性和
。
(2)天津的解放桥是一座全钢结构可开启的桥梁,它是天津的标志性建筑物之一。
①钢属于
(填“单质”、“纯净物”或“混合物”)。
②工业上用一氧化碳和赤铁矿炼铁的原理是
(写化学方程式)。
③建造这座桥大约用了112t铁,理论需要含氧化铁80%的赤铁矿
t。
(3)为探究铁、铜、银的金属活动性顺序,同学们设计了如图所示的两步实验。
①第1步实验的目的是
。
②第2步实验中,为了达到实验目的,溶液甲可以是
(填序号)。
A.稀盐酸
B.FeSO4溶液
C.CuSO4溶液
D.ZnSO4溶液
22.如图是冶炼生铁及相关流程。请认真读图回答问题:
(1)赤铁矿需要经过粉碎处理,其目的是
。
(2)该工艺流程中,“燃烧室”发生的反应化学方程式是
,冶炼出的铁水属于
(填“纯净物”或“混合物”)。
(3)该工艺流程中,可循环利用的物质是
。
(4)生铁比钢的含碳量
(填“高”或“低”),写出生铁炼钢的主要反应原理
(用化学方程式表示)。
23.2018年10月23日,举世瞩目的港珠澳大桥正式开通,其总用钢量接近100万吨!请根据所学金属的有关知识回答:
(1)以赤铁矿为例,写出工业炼铁的反应原理。
(2)向m克AgNO3、Cu(NO3)2
和Fe(NO3)2的混合溶液中加入Zn,充分反应后过滤,所得滤液质量仍为m克,则滤渣中一定有什么物质?并写出可能发生的反应的化学方程式。
24.竖炉炼铁是一种重要的炼铁方法,其工艺流程如图所示。
(1)赤铁矿属于
(填“纯净物”或“混合物”)。
(2)用化学方程式表示竖炉内进行的反应:
a.还原反应室内
(任意选择一个)。
b.燃烧室内
。
(3)下列说法正确的是
(填序号)。
A.加入的铁矿石要进行粉碎,目的是加快反应速率和提高原料利用率
B.该工艺流程中,可循环利用的物质有高温尾气(CO2和H2O)和CH4
C.燃烧室内进行的反应为炼铁提供了大量热量
D.竖炉炼铁得到的产品为纯铁
25.下面连环画(图1)记录了雯雯参观中国地质博物馆的一天。
请据图回答问题
(1)她吃早餐。陶瓷餐盘的主要成分之一是硅酸钙(CaSiO3),其中硅元素的化合价是
。
(2)她出发了。如图③所示,乘坐地铁禁止携带的物品中,属于易燃易爆品的是
。
(3)她来到博物馆门口。同学们在地质学家李四光的大理石雕像前,了解他的生平事迹。大理石的主要成分是
。
(4)她和同学们进入博物馆。
她看到了许多矿石标本,其中的4
种矿石及其主要成分如图2:
①上述矿石标本的主要成分中,所含元素种类最多的是
(填字母序号)。
②她根据辉铜矿的主要成分,推测以辉铜矿为原料,可制得含铜元素或含硫元素的产品,她的依据是化学反应前后不变。
③她依据化学式计算出Cu2(OH)2CO3的相对分子质量为222,计算式为
。
(5)参观结束时,老师进行了小结,并就金属冶炼和金属回收再利用提出了一些问题,请同学们作答。
①工业上用一氧化碳和赤铁矿炼铁的原理是
(用化学方程式表示)。
②我国是世界上最早采用湿法冶金提取铜的国家,写出铁与硫酸铜溶液反应制取铜的化学方程式
,该反应的现象是
。
③在含有氯化锌、氯化铜和氯化亚铁的废液中加入一定量的铁粉可以充分回收利用金属资源,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生,可以判断滤液的可能成分是
。
26.铁是我们日常生活中一种常见的金属,但你是否真正了解它呢,快来参加“铁知识竞赛吧。
(1)铁它是由
(选填“原子”、“分子”或“离子”)构成的物质。日常生活中我们所用的钢铁是一种
(选填“纯金属“或“合金”)。
(2)工业中常用一氧化碳还原赤铁矿来炼铁,其中赤铁矿的主要成分是
,写出工业炼铁时,高炉内发生一氧化碳还原赤铁矿反应的化学方程式:
。
(3)若要验证的Fe、Cu和Al的金属活动性顺序,只需一种试剂直接与上述三种金属反应就能达到目的,该试剂是
(填序号)。
A.硫酸铝溶液
B.硫酸亚铁溶液
C.硫酸铜溶液
27.运用广泛的金属材料是钢铁,如图是冶炼生铁相关流程。请认真读图回答问题:
(1)高炉冶炼生铁的原料有铁矿石、焦炭和
。
冶炼时将原料粉碎后再使用的原因是
。
(2)焦炭在冶炼中的作用为①提供高温,②
。赤铁矿(主要成分Fe2O3)炼铁的反应原理是
。
(3)炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是
。
(4)钢铁的锈蚀造成极大的损失和浪费。但如果将“铁生锈”原理应用得当,同样可以造福人类,请举例
(写一条)。
同课章节目录
