2020年人教版九年级化学下学期第9单元 课题2 溶解度:固体溶解度曲线及其作用精选练习题44道带答案
文档属性
| 名称 | 2020年人教版九年级化学下学期第9单元 课题2 溶解度:固体溶解度曲线及其作用精选练习题44道带答案 |
|
|
| 格式 | zip | ||
| 文件大小 | 273.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-16 00:00:00 | ||
图片预览



文档简介
2020年人教版九年级化学下学期第九单元:固体溶解度曲线及其作用精选练习题44道带答案
一.选择题(共17小题)
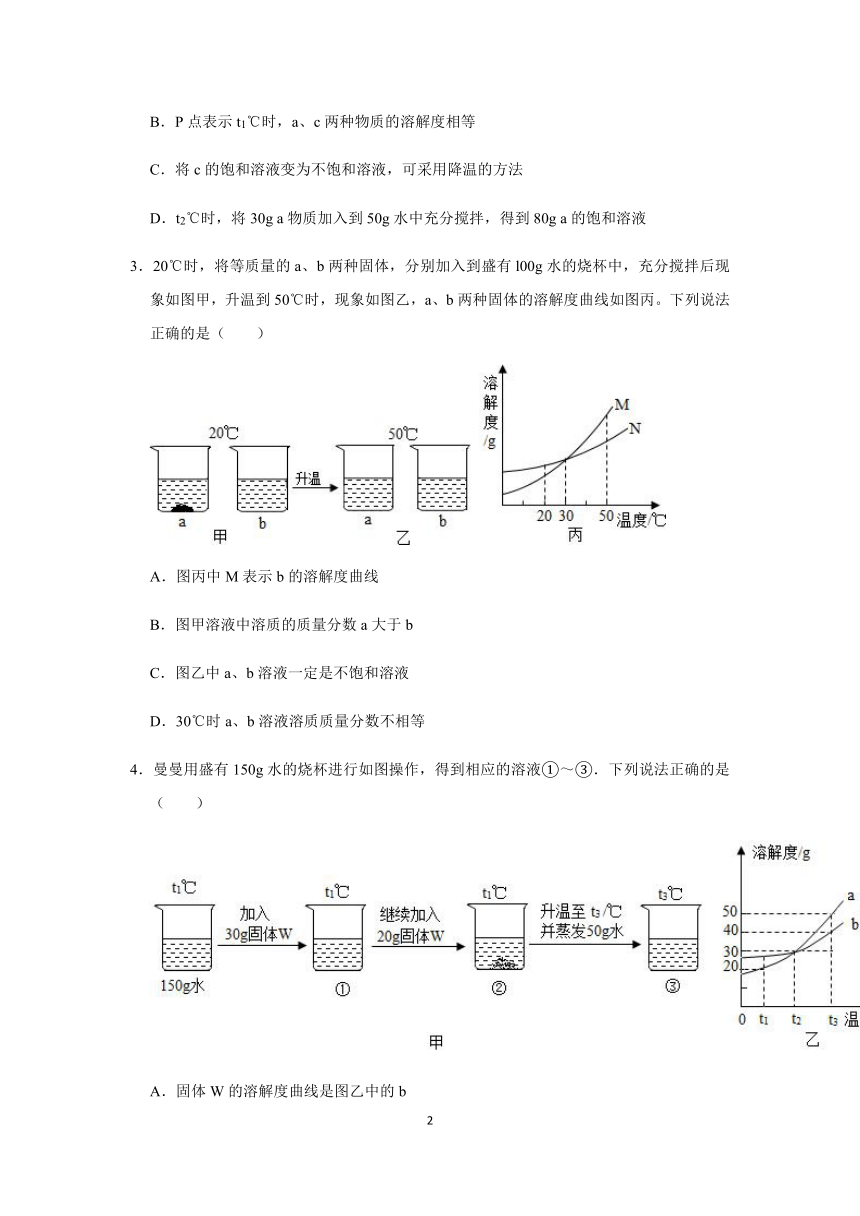
1.如图是a,b,c三种固体物质的溶解度曲线,下列叙述正确的是( )
A.将a、b、c三种物质t1℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数大小关系是a>b>c
B.t2℃时30g物质a加入到50g水中不断搅拌,形成80g溶液
C.t1℃时a,b,c三种物质的饱和溶液中含有溶质质量按由小到大的顺序排列是b>a=c
D.若a中混有少量c,可以采用冷却热饱和溶液的方法提纯a
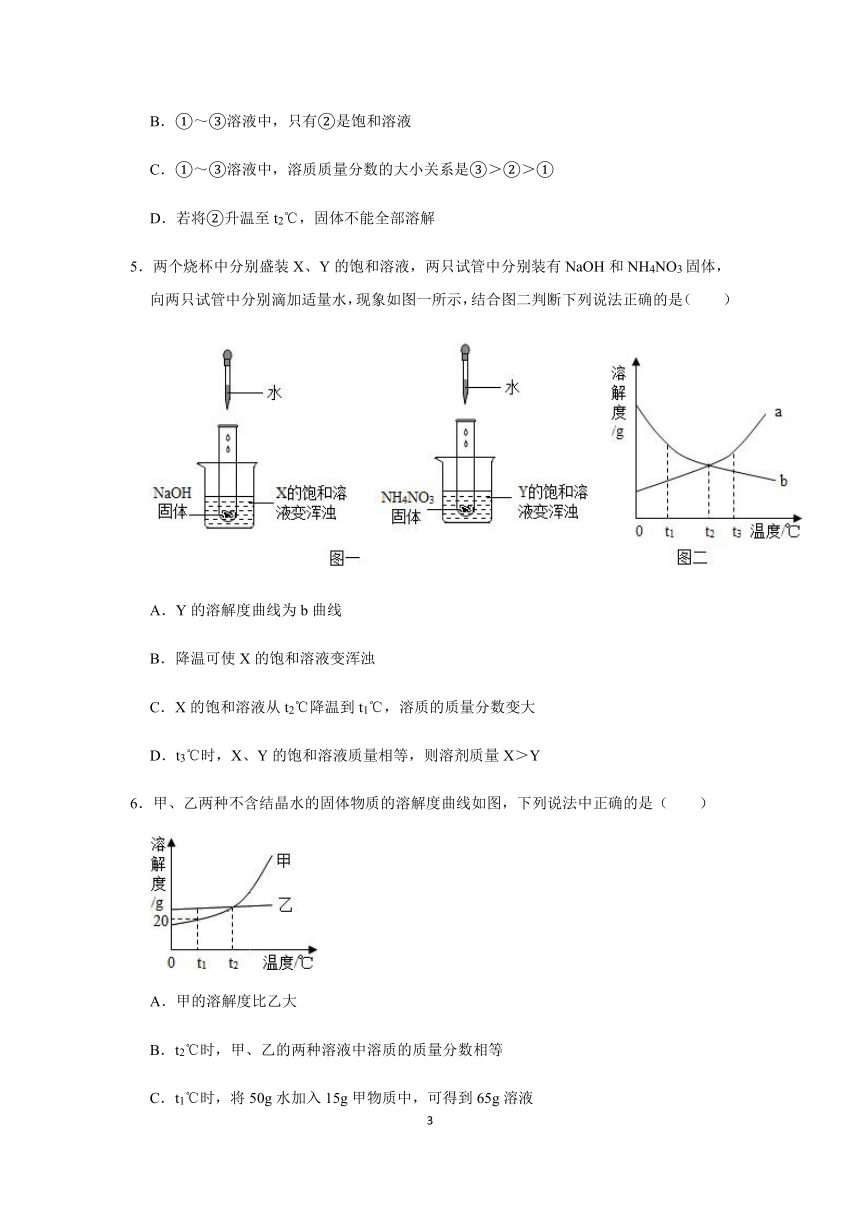
2.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
A.t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B.P点表示t1℃时,a、c两种物质的溶解度相等
C.将c的饱和溶液变为不饱和溶液,可采用降温的方法
D.t2℃时,将30g
a物质加入到50g水中充分搅拌,得到80g
a的饱和溶液
3.20℃时,将等质量的a、b两种固体,分别加入到盛有l00g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是( )
A.图丙中M表示b的溶解度曲线
B.图甲溶液中溶质的质量分数a大于b
C.图乙中a、b溶液一定是不饱和溶液
D.30℃时a、b溶液溶质质量分数不相等
4.曼曼用盛有150g水的烧杯进行如图操作,得到相应的溶液①~③.下列说法正确的是( )
A.固体W的溶解度曲线是图乙中的b
B.①~③溶液中,只有②是饱和溶液
C.①~③溶液中,溶质质量分数的大小关系是③>②>①
D.若将②升温至t2℃,固体不能全部溶解
5.两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( )
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2℃降温到t1℃,溶质的质量分数变大
D.t3℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
6.甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
A.甲的溶解度比乙大
B.t2℃时,甲、乙的两种溶液中溶质的质量分数相等
C.t1℃时,将50g水加入15g甲物质中,可得到65g溶液
D.要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法
7.如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是( )
A.t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4
B.P点表示甲、丙两种物质的饱和溶液质量相等
C.t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液
D.将三种物质的溶液从t2℃降至t1℃,析出晶体最多的是甲物质
8.甲、乙两种物质(不含结晶水)的溶解度曲线如图所示,下列叙述正确的是( )
A.甲和乙的溶解度相等且均为30g
B.甲物质的溶解度随温度的升高而减小
C.a1℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7
D.将a2℃150g甲的饱和溶液降温到a1℃,有20g固体析出
9.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
A.t1℃时,甲、乙两物质的溶解度大小关系:甲>乙
B.t2℃时,等质量的甲、乙溶液中,溶剂的质量一定相等
C.t3℃时,若将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D.将t1℃时甲、乙的饱和溶液升温至t3℃,所得甲、乙的溶液仍都是饱和溶液
10.a,b两种物质的溶解度曲线如图所示。下列说法不正确的是( )
A.将t1℃时b的饱和溶液加水可变为不饱和溶液
B.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变
C.t2℃时,两种物质的饱和溶液中溶质质量分数a>b
D.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等
11.A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是( )
A.t1℃时,A、C两种物质的饱和溶液中溶质的质量相等
B.t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3
C.将t2℃时A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是B>C=A
D.将C的饱和溶液变为不饱和溶液,可采用升温的方法
12.如图是甲、乙两种固体的溶解度曲线。下列说法中不正确的是( )
A.t1℃时,甲和乙的溶解度相等
B.t1℃时,30g乙加到100g水中形成饱和溶液
C.t2℃时,各100g饱和溶液降温至t1℃析出固体甲多于乙
D.t2℃时,75g甲的饱和溶液中加100g水得到20%的溶液
13.如图是甲、乙两种固体物质的溶解度曲线。下列说法错误的是( )
A.T℃时,甲、乙两物质的溶解度相等
B.乙的饱和溶液降温时,溶质质量分数保持不变
C.甲中混有少量乙,可采用降温结晶的方法提纯甲
D.T℃时,甲的饱和溶液溶质质量分数为20%
14.甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如图所示,下列说法正确的是( )
A.甲的溶解度是102.5g
B.甲的溶解度随温度的升高而增大
C.20℃时,100
g甲的饱和溶液中溶质质量为28.6g
D.将70℃甲的饱和溶液升高温度或降低温度,都有晶体析出
15.PbO能溶解在不同浓度的NaOH溶液中,其溶解度曲线如图所示。下列叙述错误的是( )
A.100℃时,PbO在35%NaOH溶液中的溶解度为100g?L﹣1
B.60℃时,PbO在35%NaOH溶液中的溶解度大于在10%NaOH溶液中的溶解度
C.20℃时,PbO在10%NaOH溶液中所溶解的质量,一定小于在35%NaOH溶液中所溶解的质量
D.80℃时,将PbO溶解在10%NaOH溶液中达到饱和,然后降温至40℃,该过程中一定析出固体
16.甲、乙两种固体物质的溶解度曲线如图所示,据图判断下列说法正确的是( )
A.甲物质的溶解度大于乙
B.20℃时,等质量的甲、乙饱和溶液中甲的溶剂质量比乙小
C.60℃时,甲的饱和溶液的溶质质量分数为25%
D.将60℃时甲、乙的饱和溶液降温至t℃,溶液的溶质质量分数甲>乙
17.如图为甲乙两物质的溶解度曲线,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15%
C.要使接近饱和的乙溶液转化为饱和溶液,可以采用蒸发溶剂的方法
D.t2℃时,将50克甲物质放入100克水中,得到溶液的质量为150克
二.多选题(共2小题)
18.如图为A物质的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
A.从N→M:先向N中加入适量固体A再降温到t2
B.从N→M:先将N降温到t1再加入适量固体A
C.从M→N:先将M降温到t1再将其升温
D.从M→N:先将M升温到t3再加入适量的水
19.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时甲、乙两物质形成的饱和溶液中溶质质量分数相等
C.当甲中含有少量的乙时,可以采用降温结晶的方法提纯甲
D.将M点的甲溶液变为饱和溶液可采取升高温度的方法
三.填空题(共17小题)
20.t2℃时,将甲、乙各80g分别放在盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一,甲和乙的溶解度曲线如图二。请结合图示回答下列问题:
(1)固体甲对应的溶解度曲线是
(填“a”或“b”)。
(2)M点的含义
。
(3)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分甲析出,你认为“全部溶解”的原因是
。
(4)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法正确的是
(填字母)。
a.甲溶液仍为饱和溶液
b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙
d.两溶液溶质质量分数甲>乙。
21.如图甲是A、B、C三种固体物质的溶解度曲线图.
(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是
.P点所表示的含义为
.
(2)t2℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法是
.
(3)t2℃时,当A中混有少量的C时,可用
方法提纯A.
(4)若物质A在t2℃时的溶解度为60克,t1℃时的溶解度为20克,把100克质量分数为10%的A溶液从t2℃降温到t1℃,此时A溶液的质量分数为
.
(5)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?
.原因是
.
22.如图是a、b、c三种物质的溶解度曲线.根据图回答:
(1)
℃时,a和c的溶解度相等.
(2)t3℃时,把20克
a、b、c三种物质分别加入到盛有50克水的烧杯中不断搅拌,所得溶液的溶质质量分数大小关系
(填字母,下同);若将温度降低到t1℃时,溶液质量的大小关系为
.
A.c>a=b
B.b>a=c
C.a>b>c
D.b>a>c
(3)在t2℃下,将c物质的不饱和溶液变为饱和溶液,下列有关说法不正确的是
(填字母).
A.溶剂的质量可能变小B.溶液的质量可能变大
C.溶质的质量分数一定变大
D.溶质的质量一定不变.
23.硝酸钾和氯化钾的溶解度曲线如图所示
(1)t1℃时,硝酸钾的溶解度为
g。
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为
。
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是
。
(4)将t3℃时硝酸钾和氯化钾的饱和溶液各100g,降温至t2℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是
。
A.都是饱和溶液
B.溶液质量a<b
C.溶质质量a=b
D.溶剂质量a<b
E.溶质的质量分数a>b
24.如图为甲、乙、丙三种物质的溶解度曲线。回答下列问题:
(1)P点的意义是
。
(2)t2℃时,向30g甲物质中加入50g水,充分溶解后,所得溶液质量为
,将其升高到t3℃时,所得溶液中溶质和溶液质量比为
。
(3)t4℃时,把等质量的甲、乙、丙三种物质分别配制成饱和溶液,所得溶液质量由大到小的顺序为
。
(4)将t4℃时甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序为
。
25.溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是
。
A.只有固体
B.只有液体
C.只有气体
D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为
,水的体积为
mL
(水的密度近似看作1g/cm3)。
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t1℃时,甲物质的溶解度是
。t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是
(填“甲”或“乙”)物质的饱和溶液。
(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是
。
选项
x
y
A
水
氧化钙
B
水
硝酸铵
C
浓硫酸
水
D
稀盐酸
镁
26.如图是X、Y、Z三种固体物质的溶解度曲线,请回答下列问题:
(1)t1℃时三种物质溶解度由大到小的顺序是
;
(2)要配制溶质质量分数相同的Y、Z饱和溶液,需要把温度控制在
℃;
(3)t2℃时,25g
X的饱和溶液中含有5gX,则此时X的溶解度是
g;
(4)固体X中含有少量的Y,要得到较纯净的X,可以采用的方法是
;
(5)t3℃的X、Y、Z的饱和溶液降温至t2℃时,溶质质量分数由大到小的顺序是
;
(6)t3℃接近饱和的X溶液逐渐冷却至t1℃,图2中有关量随时间变化的趋势正确的是
.
27.认识溶液的变化。
根据如图甲、乙、丙三种固体的溶解度曲线回答:
①M点表示的含义是
。
②50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为
。
③20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数
(填“变大”、“变小”或“不变”)。
④分别将50℃的三种物质的饱和溶液100g降温到20℃时,甲、乙、丙溶液质量大小关系为
。
28.请根据如图a、b、c三种固体物质的溶解度曲线,回答下列问题:
(1)在
℃时,a、c两种物质的溶解度相等;
(2)在t2℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为
g。
(3)若a物质中混有少量b物质,最好采用
(填“降温结晶”或“蒸发结晶”)的方法提纯a;
(4)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是
。
29.硝酸钾和氯化钾的溶解度曲线如图所示:
(1)t1℃时,硝酸钾的溶解度为
。
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为
。
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是
。
(4)将t3℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t2℃过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是
A.都是饱和溶液
B.溶液质量a<b
C.溶质质量a=b
D.溶剂质量a<b
E.溶质的质量分数a=b
30.如图是A、B、C三种物质的溶解度曲线,请认真分析并回答:
(1)t3℃时,A、B、C三种物质的溶解度由小到大的顺序为
。
(2)t2℃时,A、B、C三种物质的饱和溶液降温到t1℃时变为不饱和溶液的是
。
(3)当A中含有少量的B,可采用
(填“降温”或“蒸发”)结晶的方法提纯A物质。
(4)t3℃时,若用A、B两物质各50g配成饱和溶液,则所需加水的质量A
B(填“>”,“<”,“=”号)
31.硝酸钾、硝酸钠、氯化钾、氯化钠四种物质的溶解度曲线如图。
(1)由图可知:10℃时,溶解度最小的是
。
(2)若75g硝酸钠固体溶解在50g水中恰好得到饱和溶液,此时溶液温度为
(选填下列编号)。
A.60℃B.70℃C.80℃D.90℃
(3)60℃时,若分别溶解相同质量的硝酸钾、硝酸钠、氯化钾、氯化钠恰好形成饱和溶液。则加入水最多的是
。
(4)固体M是由硝酸钾和氯化钾中的一种成二种组成。现取40gM加入50g50℃的热水(水温保持不变),固体完全溶解。对M的成分判断正确的是
(选填下列编号)
A.可能只有硝酸钾
B.可能只有氯化钾
C.可能是硝酸钾和氯化钾的混合物
D.一定是硝酸钾和氯化钾的混合物
32.甲、乙两种物质的溶解度曲线如图所示,请回答下列问题:
(1)P点表示的含义是
;
(2)30℃时,甲物质的溶解度
乙物质的溶解度(填“大于”、小于”、“等于”);
(3)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有
(写一种).
33.如图是X、Y两种固体物质的溶解度曲线图.请据图回答:
①t3℃时,将澄清的饱和溶液X、Y降温到t2℃,有固体析出的是
溶液.
②Y溶液的溶质可能是
(填序号).
A.NaCl
B.KNO3
C.Ca(OH)2
③t3℃时,保持温度不变,将X、Y饱和溶液蒸发一定量的水,则蒸发水后两溶液的溶质质量分数X
Y(填“>”、“<”或“=”).
34.请根据如图a、b、c三种固体物质的溶解度曲线,回答下列问题:
(1)在
℃时,a、c两种物质的溶解度相等。
(2)在t2℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为
g。
(3)若a物质中混有少量b物质,最好采用
的方法提纯。(填“降温结晶”或“蒸发结晶”)。
(4)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是
。
(5)下列说法正确的是
。
A.将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
B.将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量一定减小
C.配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高
35.将80gM物质加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示,按要求填空。
(1)A点时,该溶液的溶质质量分数为
。
(2)A、B、C三点所对应的溶液,属于不饱和溶液的是
(填字母)。
(3)在40℃时,M物质的溶解度为
g,若保持溶剂的质量不变,从C点对应的溶液获得M的晶体,可以采用的方法是
。
36.如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题。
(1)P点的含义是
。
(2)在t1℃时,将20gA物质加入到50g水中,充分溶解,得到溶液的质量为
。
(3)将t3℃时A、B、C三种物质的饱和溶液降温到t2℃,此时三种溶液中溶质的质量分数大小关系是
。
(4)若A中混有少量B时,最好采用
方法提纯A。
四.计算题(共1小题)
37.M是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组用物质M进行了如图2所示的实验。
(1)t1℃时,氯化铵的溶解度为
g;
(2)烧杯①中溶质质量分数的计算式为
;
(3)物质M是
。
五.解答题(共7小题)
38.如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题。
(1)0℃时,三种物质溶解度最小的是
;
(2)t2℃时,甲物质的溶解度是
g;
(3)将t1℃时甲、乙、丙三种物质的饱和溶液分别升高到t2℃,有固体析出的是
;
(4)t2℃时,将一定质量甲物质加到100g
水中完全溶解,再降温到t1℃,析出甲物质15g,则t2℃时,加入甲物质的质量为
g。
39.如图为a、b、c三种固体物质的溶解度曲线,请回答:
(1)t2℃时b物质的溶解度是
g。
(2)a中混有少量b,要提纯a可采用采用的结晶方法是
。
(3)t3℃时各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是
。此时,将温度降至t1℃,所得溶液中溶质的质量分数不变的是
。
40.结合如图中KNO3和NaCl的溶解度曲线,回答下列问题。
(1)10℃时,溶解度较大的物质是
;
(2)20℃时,将20gNaCl加入到100g水中,充分溶解后,得到
(填“饱和”或“不饱和”)溶液;
(3)将50℃的KNO3饱和溶液降温至10℃,下列分析正确的是
。
A.溶液中溶质质量不变
B.降温后的溶液仍是饱和溶液
C.溶液中溶质的质量分数变大
41.如图
1
是
A、B、C
三种固体物质的溶解度曲线,请回答下列问题:
(1)t1℃时,A、B、C
三种物质的溶解度大小关系是
。
(2)t2℃时,把
30gA
放入50g
水中,充分搅拌,形成溶液的溶质与溶液质量
之比为
。
(3)向图2装有氧化钙的试管中滴入2mL水后,若
X
中有固体析出,则
X为
(选填“A、B、C”)。
(4)若饱和
C溶液中混有少量
B,可采用
结晶提纯
C。
42.甲、乙、丙三种固体物质的溶解度曲线如图1所示。请回答:
(1)0℃时,三种物质中溶解度最大的是
。
(2)t2℃时,在盛有50g水的烧杯中加入35g甲物质,充分搅拌后所得溶液的质量是
g。
(3)将t3℃的甲、乙、丙三种物质的饱和溶液降温到t1℃时,所得溶液中溶质的质量分数关系为
(用“=”“<”或“>”符号连接)。
(4)将甲溶液由A点转变为B点,可采用的方法是
(填一种即可)。
(5)如图2,将放有固体X的试管放入烧杯中,然后向试管内加入液体Y,一段时间后丙溶液中有固体析出,则对应的X和Y物质是
(填序号)。
A.氯化钠和水
B.镁条和稀盐酸
C.硝酸铵和水
D.氢氧化钠和水
43.甲、乙、丙三种物质的溶解度曲线如图所示。据图回答:
(1)30℃时,丙物质的溶解度是
。
(2)12℃时,甲和丙的溶解度曲线相交于a点,a点的意义是
。
(3)要使接近饱和的丙物质溶液变为饱和溶液,可采取的一种措施是
(写出一种方法即可)。
(4)30℃时,三种物质的溶解度由大到小的顺序为
。
(5)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,析出晶体最多的是
,所得溶液中溶质质量分数最小的是
。
(6)甲中含少量乙,要提纯甲,应该用
方法。
44.根据如图的溶解度曲线图回答
(1)在40℃时,在l00g水中加入30gKCl固体,所形成的溶液是
溶液(“饱和”或“不饱和”);将上述溶液蒸发掉50g水后恢复到40℃,析出固体质量是
g。
(2)在40℃时,饱和KCl溶液的溶质质量分数是
。(只列计算式)
(3)在温度为
时,Na2SO4的溶解度大于KCl的溶解度。
(4)KCl的溶解度与温度变化的关系是
。
参考答案
一.选择题(共17小题)
1-17DDCDDDADCBBDDDCDC
二.多选题(共2小题)
18.BC。
19.BC。
三.填空题(共17小题)
20.(1)a;(2)t1℃时,甲、乙物质的溶解度相等;
(3)甲物质溶于水放热,温度升高,溶解度增大;(4)abd。
21.(1)A;t1℃时,B和C的溶解度相等;
(2)增加溶质(合理答案均可);
(3)冷却热饱和溶液;
(4)10%;
(5)C;C的溶解度随温度的升高而减小,镁条和稀盐酸反应放热,温度升高,C的溶解度变小,溶解的物质减少,多余的溶质析出.
22.(1)t1;(2)C;B;(3)D.
23.(1)25g;(2)20%;(3)蒸发溶剂;(4)ABD。
24.(1)t2℃时,甲丙两种物质溶解度相等都是50g(只答二者溶解度相等不得分);
(2)75g;3:8;
(3)丙>乙>甲(或丙
乙
甲);
(4)乙>丙>甲(或乙
丙
甲)。
25.(1)D;(2)16g;84;(3)40g;乙;(4)AD;
26.(1)Z>Y>X;
(2)t2;(3)25;(4)降温结晶;(5)Y>Z>X;(6)C.
27.①在50℃时,甲、乙物质的溶解度相等;②2:5;③不变;④丙>乙>甲。
28.(1)t1;(2)75;(3)降温结晶;(4)c>b>a。
29.(1)25g;(2)20%;(3)蒸发结晶;(4)ABDE。
30.(1)C<B<A;(2)C;(3)降温;(4)<。
31.(1)硝酸钾;(2)C;(3)氯化钠;(4)AC。
32.(1)在t1℃时,甲乙两物质的溶解度相等;(2)大于;
(3)降低温度或加溶质或蒸发溶剂;
33.①X.②C;③>.
34.(1)t1;(2)75;(3)降温结晶;(4)c>b>a或cba;(5)BC
35.(1)50%;(2)C;(3)降温结晶;
36.(1)t2℃时,A、C物质的溶解度相等;(2)60g;(3)B>A>C;(4)降温结晶。
四.计算题(共1小题)
37.(1)由溶解度曲线可知:t1℃时,氯化铵的溶解度为40g;故答案为:40;
(2)烧杯①中溶质质量分数的计算式为:;故答案为:;
(3)物质M是硝酸钾,因为在t1℃时,60gM全部溶于100g水中;故答案为:硝酸钾;
五.解答题(共7小题)
38.(1)甲;(2)80;(3)丙;(4)75。
39.(1)50;(2)降温结晶;(3)c,b。
40.(1)NaCl;(2)不饱和;(3)B;
41.(1)B>C>A;(2)15:65(或
3:13);(3)C;(4)升温。
42.(1)丙;(2)80;(3)丙>甲=乙;(4)增加溶质;(5)BD。
43.(1)10g。(2)12℃时,甲和丙的溶解度相等。(3)加入丙物质。
(4)乙、甲、丙。(5)甲;丙。(6)降温结晶。
44.(1)不饱和,10;(2);
(3)25℃~63℃;(4)溶解度随温度的升高而增大
一.选择题(共17小题)
1.如图是a,b,c三种固体物质的溶解度曲线,下列叙述正确的是( )
A.将a、b、c三种物质t1℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数大小关系是a>b>c
B.t2℃时30g物质a加入到50g水中不断搅拌,形成80g溶液
C.t1℃时a,b,c三种物质的饱和溶液中含有溶质质量按由小到大的顺序排列是b>a=c
D.若a中混有少量c,可以采用冷却热饱和溶液的方法提纯a
2.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
A.t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B.P点表示t1℃时,a、c两种物质的溶解度相等
C.将c的饱和溶液变为不饱和溶液,可采用降温的方法
D.t2℃时,将30g
a物质加入到50g水中充分搅拌,得到80g
a的饱和溶液
3.20℃时,将等质量的a、b两种固体,分别加入到盛有l00g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是( )
A.图丙中M表示b的溶解度曲线
B.图甲溶液中溶质的质量分数a大于b
C.图乙中a、b溶液一定是不饱和溶液
D.30℃时a、b溶液溶质质量分数不相等
4.曼曼用盛有150g水的烧杯进行如图操作,得到相应的溶液①~③.下列说法正确的是( )
A.固体W的溶解度曲线是图乙中的b
B.①~③溶液中,只有②是饱和溶液
C.①~③溶液中,溶质质量分数的大小关系是③>②>①
D.若将②升温至t2℃,固体不能全部溶解
5.两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是( )
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X的饱和溶液从t2℃降温到t1℃,溶质的质量分数变大
D.t3℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
6.甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
A.甲的溶解度比乙大
B.t2℃时,甲、乙的两种溶液中溶质的质量分数相等
C.t1℃时,将50g水加入15g甲物质中,可得到65g溶液
D.要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法
7.如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是( )
A.t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4
B.P点表示甲、丙两种物质的饱和溶液质量相等
C.t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液
D.将三种物质的溶液从t2℃降至t1℃,析出晶体最多的是甲物质
8.甲、乙两种物质(不含结晶水)的溶解度曲线如图所示,下列叙述正确的是( )
A.甲和乙的溶解度相等且均为30g
B.甲物质的溶解度随温度的升高而减小
C.a1℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7
D.将a2℃150g甲的饱和溶液降温到a1℃,有20g固体析出
9.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
A.t1℃时,甲、乙两物质的溶解度大小关系:甲>乙
B.t2℃时,等质量的甲、乙溶液中,溶剂的质量一定相等
C.t3℃时,若将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D.将t1℃时甲、乙的饱和溶液升温至t3℃,所得甲、乙的溶液仍都是饱和溶液
10.a,b两种物质的溶解度曲线如图所示。下列说法不正确的是( )
A.将t1℃时b的饱和溶液加水可变为不饱和溶液
B.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变
C.t2℃时,两种物质的饱和溶液中溶质质量分数a>b
D.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等
11.A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是( )
A.t1℃时,A、C两种物质的饱和溶液中溶质的质量相等
B.t2℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3
C.将t2℃时A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是B>C=A
D.将C的饱和溶液变为不饱和溶液,可采用升温的方法
12.如图是甲、乙两种固体的溶解度曲线。下列说法中不正确的是( )
A.t1℃时,甲和乙的溶解度相等
B.t1℃时,30g乙加到100g水中形成饱和溶液
C.t2℃时,各100g饱和溶液降温至t1℃析出固体甲多于乙
D.t2℃时,75g甲的饱和溶液中加100g水得到20%的溶液
13.如图是甲、乙两种固体物质的溶解度曲线。下列说法错误的是( )
A.T℃时,甲、乙两物质的溶解度相等
B.乙的饱和溶液降温时,溶质质量分数保持不变
C.甲中混有少量乙,可采用降温结晶的方法提纯甲
D.T℃时,甲的饱和溶液溶质质量分数为20%
14.甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如图所示,下列说法正确的是( )
A.甲的溶解度是102.5g
B.甲的溶解度随温度的升高而增大
C.20℃时,100
g甲的饱和溶液中溶质质量为28.6g
D.将70℃甲的饱和溶液升高温度或降低温度,都有晶体析出
15.PbO能溶解在不同浓度的NaOH溶液中,其溶解度曲线如图所示。下列叙述错误的是( )
A.100℃时,PbO在35%NaOH溶液中的溶解度为100g?L﹣1
B.60℃时,PbO在35%NaOH溶液中的溶解度大于在10%NaOH溶液中的溶解度
C.20℃时,PbO在10%NaOH溶液中所溶解的质量,一定小于在35%NaOH溶液中所溶解的质量
D.80℃时,将PbO溶解在10%NaOH溶液中达到饱和,然后降温至40℃,该过程中一定析出固体
16.甲、乙两种固体物质的溶解度曲线如图所示,据图判断下列说法正确的是( )
A.甲物质的溶解度大于乙
B.20℃时,等质量的甲、乙饱和溶液中甲的溶剂质量比乙小
C.60℃时,甲的饱和溶液的溶质质量分数为25%
D.将60℃时甲、乙的饱和溶液降温至t℃,溶液的溶质质量分数甲>乙
17.如图为甲乙两物质的溶解度曲线,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15%
C.要使接近饱和的乙溶液转化为饱和溶液,可以采用蒸发溶剂的方法
D.t2℃时,将50克甲物质放入100克水中,得到溶液的质量为150克
二.多选题(共2小题)
18.如图为A物质的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
A.从N→M:先向N中加入适量固体A再降温到t2
B.从N→M:先将N降温到t1再加入适量固体A
C.从M→N:先将M降温到t1再将其升温
D.从M→N:先将M升温到t3再加入适量的水
19.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时甲、乙两物质形成的饱和溶液中溶质质量分数相等
C.当甲中含有少量的乙时,可以采用降温结晶的方法提纯甲
D.将M点的甲溶液变为饱和溶液可采取升高温度的方法
三.填空题(共17小题)
20.t2℃时,将甲、乙各80g分别放在盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一,甲和乙的溶解度曲线如图二。请结合图示回答下列问题:
(1)固体甲对应的溶解度曲线是
(填“a”或“b”)。
(2)M点的含义
。
(3)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分甲析出,你认为“全部溶解”的原因是
。
(4)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法正确的是
(填字母)。
a.甲溶液仍为饱和溶液
b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙
d.两溶液溶质质量分数甲>乙。
21.如图甲是A、B、C三种固体物质的溶解度曲线图.
(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是
.P点所表示的含义为
.
(2)t2℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法是
.
(3)t2℃时,当A中混有少量的C时,可用
方法提纯A.
(4)若物质A在t2℃时的溶解度为60克,t1℃时的溶解度为20克,把100克质量分数为10%的A溶液从t2℃降温到t1℃,此时A溶液的质量分数为
.
(5)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?
.原因是
.
22.如图是a、b、c三种物质的溶解度曲线.根据图回答:
(1)
℃时,a和c的溶解度相等.
(2)t3℃时,把20克
a、b、c三种物质分别加入到盛有50克水的烧杯中不断搅拌,所得溶液的溶质质量分数大小关系
(填字母,下同);若将温度降低到t1℃时,溶液质量的大小关系为
.
A.c>a=b
B.b>a=c
C.a>b>c
D.b>a>c
(3)在t2℃下,将c物质的不饱和溶液变为饱和溶液,下列有关说法不正确的是
(填字母).
A.溶剂的质量可能变小B.溶液的质量可能变大
C.溶质的质量分数一定变大
D.溶质的质量一定不变.
23.硝酸钾和氯化钾的溶解度曲线如图所示
(1)t1℃时,硝酸钾的溶解度为
g。
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为
。
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是
。
(4)将t3℃时硝酸钾和氯化钾的饱和溶液各100g,降温至t2℃,过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是
。
A.都是饱和溶液
B.溶液质量a<b
C.溶质质量a=b
D.溶剂质量a<b
E.溶质的质量分数a>b
24.如图为甲、乙、丙三种物质的溶解度曲线。回答下列问题:
(1)P点的意义是
。
(2)t2℃时,向30g甲物质中加入50g水,充分溶解后,所得溶液质量为
,将其升高到t3℃时,所得溶液中溶质和溶液质量比为
。
(3)t4℃时,把等质量的甲、乙、丙三种物质分别配制成饱和溶液,所得溶液质量由大到小的顺序为
。
(4)将t4℃时甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序为
。
25.溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是
。
A.只有固体
B.只有液体
C.只有气体
D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为
,水的体积为
mL
(水的密度近似看作1g/cm3)。
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t1℃时,甲物质的溶解度是
。t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是
(填“甲”或“乙”)物质的饱和溶液。
(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是
。
选项
x
y
A
水
氧化钙
B
水
硝酸铵
C
浓硫酸
水
D
稀盐酸
镁
26.如图是X、Y、Z三种固体物质的溶解度曲线,请回答下列问题:
(1)t1℃时三种物质溶解度由大到小的顺序是
;
(2)要配制溶质质量分数相同的Y、Z饱和溶液,需要把温度控制在
℃;
(3)t2℃时,25g
X的饱和溶液中含有5gX,则此时X的溶解度是
g;
(4)固体X中含有少量的Y,要得到较纯净的X,可以采用的方法是
;
(5)t3℃的X、Y、Z的饱和溶液降温至t2℃时,溶质质量分数由大到小的顺序是
;
(6)t3℃接近饱和的X溶液逐渐冷却至t1℃,图2中有关量随时间变化的趋势正确的是
.
27.认识溶液的变化。
根据如图甲、乙、丙三种固体的溶解度曲线回答:
①M点表示的含义是
。
②50℃时,将40g甲物质投入到50g水中,形成的溶液中溶质与溶剂的质量比为
。
③20℃时,处于a点状态甲溶液,升温至50℃,溶质质量分数
(填“变大”、“变小”或“不变”)。
④分别将50℃的三种物质的饱和溶液100g降温到20℃时,甲、乙、丙溶液质量大小关系为
。
28.请根据如图a、b、c三种固体物质的溶解度曲线,回答下列问题:
(1)在
℃时,a、c两种物质的溶解度相等;
(2)在t2℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为
g。
(3)若a物质中混有少量b物质,最好采用
(填“降温结晶”或“蒸发结晶”)的方法提纯a;
(4)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是
。
29.硝酸钾和氯化钾的溶解度曲线如图所示:
(1)t1℃时,硝酸钾的溶解度为
。
(2)t1℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为
。
(3)t2℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是
。
(4)将t3℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t2℃过滤,得到溶液a和溶液b。对于溶液a和溶液b,下列说法正确的是
A.都是饱和溶液
B.溶液质量a<b
C.溶质质量a=b
D.溶剂质量a<b
E.溶质的质量分数a=b
30.如图是A、B、C三种物质的溶解度曲线,请认真分析并回答:
(1)t3℃时,A、B、C三种物质的溶解度由小到大的顺序为
。
(2)t2℃时,A、B、C三种物质的饱和溶液降温到t1℃时变为不饱和溶液的是
。
(3)当A中含有少量的B,可采用
(填“降温”或“蒸发”)结晶的方法提纯A物质。
(4)t3℃时,若用A、B两物质各50g配成饱和溶液,则所需加水的质量A
B(填“>”,“<”,“=”号)
31.硝酸钾、硝酸钠、氯化钾、氯化钠四种物质的溶解度曲线如图。
(1)由图可知:10℃时,溶解度最小的是
。
(2)若75g硝酸钠固体溶解在50g水中恰好得到饱和溶液,此时溶液温度为
(选填下列编号)。
A.60℃B.70℃C.80℃D.90℃
(3)60℃时,若分别溶解相同质量的硝酸钾、硝酸钠、氯化钾、氯化钠恰好形成饱和溶液。则加入水最多的是
。
(4)固体M是由硝酸钾和氯化钾中的一种成二种组成。现取40gM加入50g50℃的热水(水温保持不变),固体完全溶解。对M的成分判断正确的是
(选填下列编号)
A.可能只有硝酸钾
B.可能只有氯化钾
C.可能是硝酸钾和氯化钾的混合物
D.一定是硝酸钾和氯化钾的混合物
32.甲、乙两种物质的溶解度曲线如图所示,请回答下列问题:
(1)P点表示的含义是
;
(2)30℃时,甲物质的溶解度
乙物质的溶解度(填“大于”、小于”、“等于”);
(3)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有
(写一种).
33.如图是X、Y两种固体物质的溶解度曲线图.请据图回答:
①t3℃时,将澄清的饱和溶液X、Y降温到t2℃,有固体析出的是
溶液.
②Y溶液的溶质可能是
(填序号).
A.NaCl
B.KNO3
C.Ca(OH)2
③t3℃时,保持温度不变,将X、Y饱和溶液蒸发一定量的水,则蒸发水后两溶液的溶质质量分数X
Y(填“>”、“<”或“=”).
34.请根据如图a、b、c三种固体物质的溶解度曲线,回答下列问题:
(1)在
℃时,a、c两种物质的溶解度相等。
(2)在t2℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为
g。
(3)若a物质中混有少量b物质,最好采用
的方法提纯。(填“降温结晶”或“蒸发结晶”)。
(4)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是
。
(5)下列说法正确的是
。
A.将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
B.将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量一定减小
C.配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高
35.将80gM物质加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示,按要求填空。
(1)A点时,该溶液的溶质质量分数为
。
(2)A、B、C三点所对应的溶液,属于不饱和溶液的是
(填字母)。
(3)在40℃时,M物质的溶解度为
g,若保持溶剂的质量不变,从C点对应的溶液获得M的晶体,可以采用的方法是
。
36.如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题。
(1)P点的含义是
。
(2)在t1℃时,将20gA物质加入到50g水中,充分溶解,得到溶液的质量为
。
(3)将t3℃时A、B、C三种物质的饱和溶液降温到t2℃,此时三种溶液中溶质的质量分数大小关系是
。
(4)若A中混有少量B时,最好采用
方法提纯A。
四.计算题(共1小题)
37.M是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组用物质M进行了如图2所示的实验。
(1)t1℃时,氯化铵的溶解度为
g;
(2)烧杯①中溶质质量分数的计算式为
;
(3)物质M是
。
五.解答题(共7小题)
38.如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题。
(1)0℃时,三种物质溶解度最小的是
;
(2)t2℃时,甲物质的溶解度是
g;
(3)将t1℃时甲、乙、丙三种物质的饱和溶液分别升高到t2℃,有固体析出的是
;
(4)t2℃时,将一定质量甲物质加到100g
水中完全溶解,再降温到t1℃,析出甲物质15g,则t2℃时,加入甲物质的质量为
g。
39.如图为a、b、c三种固体物质的溶解度曲线,请回答:
(1)t2℃时b物质的溶解度是
g。
(2)a中混有少量b,要提纯a可采用采用的结晶方法是
。
(3)t3℃时各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是
。此时,将温度降至t1℃,所得溶液中溶质的质量分数不变的是
。
40.结合如图中KNO3和NaCl的溶解度曲线,回答下列问题。
(1)10℃时,溶解度较大的物质是
;
(2)20℃时,将20gNaCl加入到100g水中,充分溶解后,得到
(填“饱和”或“不饱和”)溶液;
(3)将50℃的KNO3饱和溶液降温至10℃,下列分析正确的是
。
A.溶液中溶质质量不变
B.降温后的溶液仍是饱和溶液
C.溶液中溶质的质量分数变大
41.如图
1
是
A、B、C
三种固体物质的溶解度曲线,请回答下列问题:
(1)t1℃时,A、B、C
三种物质的溶解度大小关系是
。
(2)t2℃时,把
30gA
放入50g
水中,充分搅拌,形成溶液的溶质与溶液质量
之比为
。
(3)向图2装有氧化钙的试管中滴入2mL水后,若
X
中有固体析出,则
X为
(选填“A、B、C”)。
(4)若饱和
C溶液中混有少量
B,可采用
结晶提纯
C。
42.甲、乙、丙三种固体物质的溶解度曲线如图1所示。请回答:
(1)0℃时,三种物质中溶解度最大的是
。
(2)t2℃时,在盛有50g水的烧杯中加入35g甲物质,充分搅拌后所得溶液的质量是
g。
(3)将t3℃的甲、乙、丙三种物质的饱和溶液降温到t1℃时,所得溶液中溶质的质量分数关系为
(用“=”“<”或“>”符号连接)。
(4)将甲溶液由A点转变为B点,可采用的方法是
(填一种即可)。
(5)如图2,将放有固体X的试管放入烧杯中,然后向试管内加入液体Y,一段时间后丙溶液中有固体析出,则对应的X和Y物质是
(填序号)。
A.氯化钠和水
B.镁条和稀盐酸
C.硝酸铵和水
D.氢氧化钠和水
43.甲、乙、丙三种物质的溶解度曲线如图所示。据图回答:
(1)30℃时,丙物质的溶解度是
。
(2)12℃时,甲和丙的溶解度曲线相交于a点,a点的意义是
。
(3)要使接近饱和的丙物质溶液变为饱和溶液,可采取的一种措施是
(写出一种方法即可)。
(4)30℃时,三种物质的溶解度由大到小的顺序为
。
(5)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,析出晶体最多的是
,所得溶液中溶质质量分数最小的是
。
(6)甲中含少量乙,要提纯甲,应该用
方法。
44.根据如图的溶解度曲线图回答
(1)在40℃时,在l00g水中加入30gKCl固体,所形成的溶液是
溶液(“饱和”或“不饱和”);将上述溶液蒸发掉50g水后恢复到40℃,析出固体质量是
g。
(2)在40℃时,饱和KCl溶液的溶质质量分数是
。(只列计算式)
(3)在温度为
时,Na2SO4的溶解度大于KCl的溶解度。
(4)KCl的溶解度与温度变化的关系是
。
参考答案
一.选择题(共17小题)
1-17DDCDDDADCBBDDDCDC
二.多选题(共2小题)
18.BC。
19.BC。
三.填空题(共17小题)
20.(1)a;(2)t1℃时,甲、乙物质的溶解度相等;
(3)甲物质溶于水放热,温度升高,溶解度增大;(4)abd。
21.(1)A;t1℃时,B和C的溶解度相等;
(2)增加溶质(合理答案均可);
(3)冷却热饱和溶液;
(4)10%;
(5)C;C的溶解度随温度的升高而减小,镁条和稀盐酸反应放热,温度升高,C的溶解度变小,溶解的物质减少,多余的溶质析出.
22.(1)t1;(2)C;B;(3)D.
23.(1)25g;(2)20%;(3)蒸发溶剂;(4)ABD。
24.(1)t2℃时,甲丙两种物质溶解度相等都是50g(只答二者溶解度相等不得分);
(2)75g;3:8;
(3)丙>乙>甲(或丙
乙
甲);
(4)乙>丙>甲(或乙
丙
甲)。
25.(1)D;(2)16g;84;(3)40g;乙;(4)AD;
26.(1)Z>Y>X;
(2)t2;(3)25;(4)降温结晶;(5)Y>Z>X;(6)C.
27.①在50℃时,甲、乙物质的溶解度相等;②2:5;③不变;④丙>乙>甲。
28.(1)t1;(2)75;(3)降温结晶;(4)c>b>a。
29.(1)25g;(2)20%;(3)蒸发结晶;(4)ABDE。
30.(1)C<B<A;(2)C;(3)降温;(4)<。
31.(1)硝酸钾;(2)C;(3)氯化钠;(4)AC。
32.(1)在t1℃时,甲乙两物质的溶解度相等;(2)大于;
(3)降低温度或加溶质或蒸发溶剂;
33.①X.②C;③>.
34.(1)t1;(2)75;(3)降温结晶;(4)c>b>a或cba;(5)BC
35.(1)50%;(2)C;(3)降温结晶;
36.(1)t2℃时,A、C物质的溶解度相等;(2)60g;(3)B>A>C;(4)降温结晶。
四.计算题(共1小题)
37.(1)由溶解度曲线可知:t1℃时,氯化铵的溶解度为40g;故答案为:40;
(2)烧杯①中溶质质量分数的计算式为:;故答案为:;
(3)物质M是硝酸钾,因为在t1℃时,60gM全部溶于100g水中;故答案为:硝酸钾;
五.解答题(共7小题)
38.(1)甲;(2)80;(3)丙;(4)75。
39.(1)50;(2)降温结晶;(3)c,b。
40.(1)NaCl;(2)不饱和;(3)B;
41.(1)B>C>A;(2)15:65(或
3:13);(3)C;(4)升温。
42.(1)丙;(2)80;(3)丙>甲=乙;(4)增加溶质;(5)BD。
43.(1)10g。(2)12℃时,甲和丙的溶解度相等。(3)加入丙物质。
(4)乙、甲、丙。(5)甲;丙。(6)降温结晶。
44.(1)不饱和,10;(2);
(3)25℃~63℃;(4)溶解度随温度的升高而增大
同课章节目录
