等效平衡2
图片预览






文档简介
(共18张PPT)
Br2+H2 2HBr
N2+3H2 2NH3
N2+3H2 2NH3
CO+H2O CO2+H2
Br2+H2 2HBr
等效平衡在化学平衡中的应用
等效平衡
达到平衡时反应混合物中各组成成分的含量决定于什么条件?
相同物质的起始浓度、压强、温度
等效平衡的条件是什么?
保持同一物质相同的起始浓度、压强、温度
V
2molSO2 1molO2
4molSO2 2molO2
在一定温度下,带有自由滑动活塞的密闭容器中进行如下反应:
催化剂
2SO2(g)+O2(g) 2SO3(g)
达平衡后两个容器中各组分的_____、_________分别相等,但__________不相等。
模型
浓度
百分含量
物质的量
2V
4mol SO2
2mol O2
2mol SO2
1mol O2
2mol SO2
1mol O2
2mol SO2 1mol O2
开始
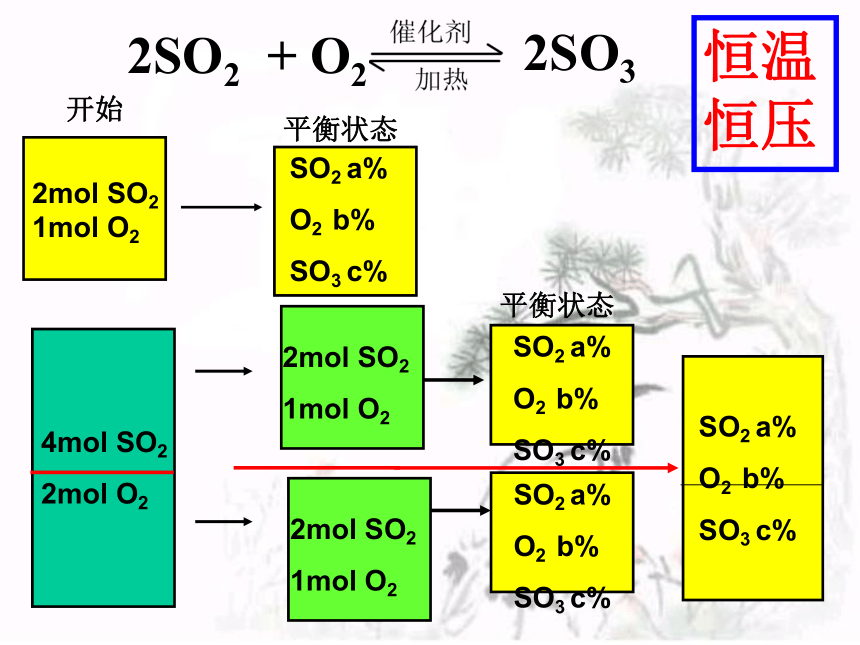
恒温恒压
SO2 a%
O2 b%
SO3 c%
平衡状态
SO2 a%
O2 b%
SO3 c%
平衡状态
SO2 a%
O2 b%
SO3 c%
2SO2 + O2
2SO3
SO2 a%
O2 b%
SO3 c%
探究二
等温等压条件下等效平衡的条件
相同物质的起始物质的量之比相等
等温等压条件下等效平衡的条件
把不同的起始状态,通过化学方程式中的计量数,换算成同一边物质(反应物一边或生成物一边),如果各反应物或生成物的_____________相同,则是等效平衡。
判断方法
物质的量之比
2.恒温、恒压下的等效平衡问题
判断方法:
使用极限转化法将各种情况变换成同一反应物或生成物,然后观察有关物质的物质的量比是否相等。
练习6、在一个1L的密闭容器中,加2molA 1molB ,发生下述反应:
达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的压强和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L(或C的体积分数仍是a%)的是
A、3mol C+1mol D
B、1mol A+0.5mol B+1.5mol C+0.5mol D
C、1mol A+0.5mol B+1.5mol C
D、4mol A+2mol B
ABD
练习7、在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:
3A(气)+2B(气) xC(气)+yD(气)
达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA 、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则X,Y的值分别为( )
A x=3 y=1 B x=4 y=1
C x=5 y =1 D x=10 y=2
C D
﹏
练习9恒温、恒压下,在一个可变容积的容器中发生如下发应:A(气)+B(气) C(气)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时A的物质的量为
(2)若开始时放入3molA和3molB,到达平衡后,生成C物质的量为 mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3a mol,则x= mol,y= mol。
3a
(1-a)mol
2
3-3a
练习10、某温度下,向某密闭容器中加入1molN2和3molH2,使之反应合成NH3,平衡后测得NH3的体积分数为m。若T不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为m,若N2、H2、NH3的加入量用X、Y、Z表示应满足:
(2)恒定T、P:
[1]若X=0、Y=0,则Z 。
[2]若X=0.75,则Y ,Z 。
[3]X、Y、Z应满足的一般条件是 。
>0
=2.25mol
≥0
Y=3X,
Z≥0
探究三
1molBr2
2molH2
A
500℃ 1L
请总结反应前后气体计量数之和相等反应的等效平衡条件。
B
1molH2 2molHBr
500℃
1molH2 2molHBr
1L
1L
C
500℃ 1L
H2
Br2
HBr
1molH2 2molHBr
1molH2 2molHBr
反应前后气体计量数之和相等
反应的等效平衡条件
探究三
反应前后气体计量数之和相等的反应等效平衡的条件
相同物质的起始物质的量之比相等
反应前后气体计量数之和相等
反应的等效平衡条件
把不同的起始状态,通过化学方程式中的计量数,换算成同一边物质(反应物一边或生成物一边),如果各反应物或生成物的_______________相同,则是等效平衡。
判断方法
物质的量之比
总结
等效平衡的条件[xA(g)+yB(g) pC(g)+qD(g)]
等温等容:相同起始物质的物质的量相等
等温等压:相同起始物质的物质的量之比相等
A、x+y≠ p+q
B、x+y = p+q
相同起始物质的物质的量之比相等
应用二
恒温、恒压下,在一个可变容积的容器中发生如下反应: ?A(g)+B(g) C(g) ①若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为______mol。 ②若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为______mol。 ③若开始时放入xmolA、2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3amol,则x=__mol,y=___ __ mol。平衡时,B的物质的量______(选填一个编号)。 (A)大于2mol (B)等于2mol (C)小于2mol (D) 以上都有可能 做出此判断的理由是__________________________________ ④若在③的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是__________。
1-a
3a
2
3(1-a)
D
达到平衡的过程中反应的方向不能确定。
a/(2-a)
等效平衡小结
条件 等效条件 结果
恒温恒容
(气体总体积改变) 投料换算成相同物质表示时量相同 两次平衡时各组分百分量、n、c均相同
恒温恒容
(气体总体积不变) 投料换算成相同物质表示时等比例 两次平衡时各组分百分量相同,n、c同比例变化
恒温恒压 投料换算成相同物质表示时等比例 两次平衡时各组分百分量、c相同,n同比例变化
等效平衡问题
条件 等效条件 结果
恒温恒容
(△n(g)≠0)
恒温恒容
(△n(g)=0)
恒温恒压
等效平衡小结
投料换算成相同物质表示时量相同
两次平衡时各组分百分量、n、c均相同
投料换算成相同物质表示时等比例
两次平衡时各组分百分量相同,n、c同比例变化
投料换算成相同物质表示时等比例
两次平衡时各组分百分量、c相同,n同比例变化
2.在下列平衡体系中,保持温度一定时,改变某物质的浓度,混合气体的颜色会改变;改变压强时,颜色也会改变,但平衡并不移动,这个反应是
A.2NO+O2 2NO2 B.N2O4 2NO2
C.Br2(g)+H2 2HBr
D.6NO+4NH3 5N2+3H2O
3.(04广东)在恒温时,一固定容积的容器内发生如下反应:2NO2(g) N2O4(g),达平衡是,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数
A、不变 B、增大
C、减小 D、无法判断
若改成恒压,又是那个答案 .
C
C
C
例A、B两容器,A容器容积固定,B容器容积可变。一定温度下,在A中加入2molN2和3molH2,当 N2 (g)+3H2 (g) 2NH3 (g)反应达平衡时,生成的NH3的物质的量为m。相同温度下,保持B的容积为A的一半,并加入1molNH3,当B中反应达平衡时要使B中各物质的质量分数与上述A容器中达到平衡时相同,则起始时应加入 molN2 和 molH2
A
B
0.5
0
Br2+H2 2HBr
N2+3H2 2NH3
N2+3H2 2NH3
CO+H2O CO2+H2
Br2+H2 2HBr
等效平衡在化学平衡中的应用
等效平衡
达到平衡时反应混合物中各组成成分的含量决定于什么条件?
相同物质的起始浓度、压强、温度
等效平衡的条件是什么?
保持同一物质相同的起始浓度、压强、温度
V
2molSO2 1molO2
4molSO2 2molO2
在一定温度下,带有自由滑动活塞的密闭容器中进行如下反应:
催化剂
2SO2(g)+O2(g) 2SO3(g)
达平衡后两个容器中各组分的_____、_________分别相等,但__________不相等。
模型
浓度
百分含量
物质的量
2V
4mol SO2
2mol O2
2mol SO2
1mol O2
2mol SO2
1mol O2
2mol SO2 1mol O2
开始
恒温恒压
SO2 a%
O2 b%
SO3 c%
平衡状态
SO2 a%
O2 b%
SO3 c%
平衡状态
SO2 a%
O2 b%
SO3 c%
2SO2 + O2
2SO3
SO2 a%
O2 b%
SO3 c%
探究二
等温等压条件下等效平衡的条件
相同物质的起始物质的量之比相等
等温等压条件下等效平衡的条件
把不同的起始状态,通过化学方程式中的计量数,换算成同一边物质(反应物一边或生成物一边),如果各反应物或生成物的_____________相同,则是等效平衡。
判断方法
物质的量之比
2.恒温、恒压下的等效平衡问题
判断方法:
使用极限转化法将各种情况变换成同一反应物或生成物,然后观察有关物质的物质的量比是否相等。
练习6、在一个1L的密闭容器中,加2molA 1molB ,发生下述反应:
达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的压强和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L(或C的体积分数仍是a%)的是
A、3mol C+1mol D
B、1mol A+0.5mol B+1.5mol C+0.5mol D
C、1mol A+0.5mol B+1.5mol C
D、4mol A+2mol B
ABD
练习7、在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:
3A(气)+2B(气) xC(气)+yD(气)
达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA 、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则X,Y的值分别为( )
A x=3 y=1 B x=4 y=1
C x=5 y =1 D x=10 y=2
C D
﹏
练习9恒温、恒压下,在一个可变容积的容器中发生如下发应:A(气)+B(气) C(气)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时A的物质的量为
(2)若开始时放入3molA和3molB,到达平衡后,生成C物质的量为 mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3a mol,则x= mol,y= mol。
3a
(1-a)mol
2
3-3a
练习10、某温度下,向某密闭容器中加入1molN2和3molH2,使之反应合成NH3,平衡后测得NH3的体积分数为m。若T不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为m,若N2、H2、NH3的加入量用X、Y、Z表示应满足:
(2)恒定T、P:
[1]若X=0、Y=0,则Z 。
[2]若X=0.75,则Y ,Z 。
[3]X、Y、Z应满足的一般条件是 。
>0
=2.25mol
≥0
Y=3X,
Z≥0
探究三
1molBr2
2molH2
A
500℃ 1L
请总结反应前后气体计量数之和相等反应的等效平衡条件。
B
1molH2 2molHBr
500℃
1molH2 2molHBr
1L
1L
C
500℃ 1L
H2
Br2
HBr
1molH2 2molHBr
1molH2 2molHBr
反应前后气体计量数之和相等
反应的等效平衡条件
探究三
反应前后气体计量数之和相等的反应等效平衡的条件
相同物质的起始物质的量之比相等
反应前后气体计量数之和相等
反应的等效平衡条件
把不同的起始状态,通过化学方程式中的计量数,换算成同一边物质(反应物一边或生成物一边),如果各反应物或生成物的_______________相同,则是等效平衡。
判断方法
物质的量之比
总结
等效平衡的条件[xA(g)+yB(g) pC(g)+qD(g)]
等温等容:相同起始物质的物质的量相等
等温等压:相同起始物质的物质的量之比相等
A、x+y≠ p+q
B、x+y = p+q
相同起始物质的物质的量之比相等
应用二
恒温、恒压下,在一个可变容积的容器中发生如下反应: ?A(g)+B(g) C(g) ①若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为______mol。 ②若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为______mol。 ③若开始时放入xmolA、2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3amol,则x=__mol,y=___ __ mol。平衡时,B的物质的量______(选填一个编号)。 (A)大于2mol (B)等于2mol (C)小于2mol (D) 以上都有可能 做出此判断的理由是__________________________________ ④若在③的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是__________。
1-a
3a
2
3(1-a)
D
达到平衡的过程中反应的方向不能确定。
a/(2-a)
等效平衡小结
条件 等效条件 结果
恒温恒容
(气体总体积改变) 投料换算成相同物质表示时量相同 两次平衡时各组分百分量、n、c均相同
恒温恒容
(气体总体积不变) 投料换算成相同物质表示时等比例 两次平衡时各组分百分量相同,n、c同比例变化
恒温恒压 投料换算成相同物质表示时等比例 两次平衡时各组分百分量、c相同,n同比例变化
等效平衡问题
条件 等效条件 结果
恒温恒容
(△n(g)≠0)
恒温恒容
(△n(g)=0)
恒温恒压
等效平衡小结
投料换算成相同物质表示时量相同
两次平衡时各组分百分量、n、c均相同
投料换算成相同物质表示时等比例
两次平衡时各组分百分量相同,n、c同比例变化
投料换算成相同物质表示时等比例
两次平衡时各组分百分量、c相同,n同比例变化
2.在下列平衡体系中,保持温度一定时,改变某物质的浓度,混合气体的颜色会改变;改变压强时,颜色也会改变,但平衡并不移动,这个反应是
A.2NO+O2 2NO2 B.N2O4 2NO2
C.Br2(g)+H2 2HBr
D.6NO+4NH3 5N2+3H2O
3.(04广东)在恒温时,一固定容积的容器内发生如下反应:2NO2(g) N2O4(g),达平衡是,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数
A、不变 B、增大
C、减小 D、无法判断
若改成恒压,又是那个答案 .
C
C
C
例A、B两容器,A容器容积固定,B容器容积可变。一定温度下,在A中加入2molN2和3molH2,当 N2 (g)+3H2 (g) 2NH3 (g)反应达平衡时,生成的NH3的物质的量为m。相同温度下,保持B的容积为A的一半,并加入1molNH3,当B中反应达平衡时要使B中各物质的质量分数与上述A容器中达到平衡时相同,则起始时应加入 molN2 和 molH2
A
B
0.5
0
