浙教版九年级上册科学1.6 几种重要的盐(课件 23张ppt)
文档属性
| 名称 | 浙教版九年级上册科学1.6 几种重要的盐(课件 23张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2020-12-18 00:00:00 | ||
图片预览







文档简介
(共23张PPT)
1.6几种重要的盐
做饭时,我们都要用到食盐,食盐的主要成分是氯化钠。你对氯化钠了解有多少呢?
(1)生活中用做调味品
(2)腌制食品
(3)医疗上,制取生理盐水
(4)雪后公路上撒盐
(5)工业上做化工原料
(6)农业上选种
……
一、氯化钠
粗盐经溶解、沉淀、过滤、蒸发,可制得精盐。
海水、湖水、井水
提纯,除去不溶物
除去可溶物
精盐
蒸发
粗盐
(含泥沙、MgCl2、CaCl2)
海水晒盐
它们的主要成分都是碳酸钙
引入
一、碳酸钙
2.性质:
物理性质:白色固体,难溶于水
化学性质(1)和稀盐酸反应
CaCO3
+
2
HCl
===
CaCl2
+
H2CO3
CO2↑+H2O
1.用途:
做建筑材料、补钙剂
(2)高温分解
CaCO3
===
CaO+
CO2↑
高温
碳酸钠
碳酸氢钠
二、碳酸钠和碳酸氢钠
碳酸钠的用途
用于生产玻璃、造纸、纺织、洗涤剂、生活中可以用来蒸馒头
碳酸氢钠的用途
发酵粉的主要成分之一,治疗胃酸过多症的药剂,干粉灭火器的主要成分。
碳酸钠、碳酸氢钠的用途
碳酸钠+
盐酸
碳酸氢钠+盐酸
现
象
分
析
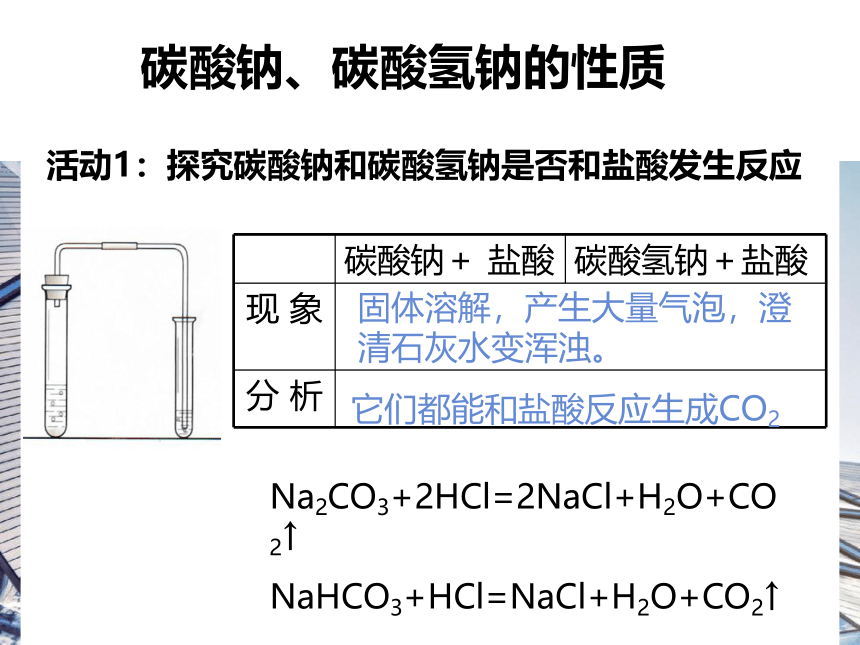
固体溶解,产生大量气泡,澄清石灰水变浑浊。
它们都能和盐酸反应生成CO2
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
碳酸钠、碳酸氢钠的性质
活动1:探究碳酸钠和碳酸氢钠是否和盐酸发生反应
CaCO3+2HCl=CaCl2+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
观察与思考
①观察:三个反应有什么共同特点?
②总结:鉴定碳酸根离子(或碳酸氢根离子)的方法。
碳酸钠、碳酸氢钠的性质
操作
现象
结论
向少量样品中加入稀盐酸。
有无色无味气体生成。
该样品是碳酸盐。
将产生的气体通入澄清石灰水。
澄清石灰水变浑浊。
鉴定碳酸根离子的方法。
碳酸钠、碳酸氢钠的性质
活动2
探究碳酸钠和碳酸氢钠是否和石灰水发生反应
碳酸钠+
石灰水
碳酸氢钠+石灰水
现
象
分
析
产生白色沉淀
无现象
可溶性碳酸盐和石灰水反应产生白色沉淀
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
工业制取烧碱的反应
碳酸钠、碳酸氢钠的性质
三、复分解反应
观察:三个反应有什么共同特点?
(1)HCl+
NaOH==
H2O
+
NaCl
(2)Na2CO3
+2HCl==2NaCl
+
H2CO3
(3)Na2CO3
+
Ca(OH)2==
2NaOH
+
CaCO3↓
两种化合物相互交换成分,生成另外两种化合物的反应,叫复分解反应。
AB+CD=AD+CB
CO2↑+H2O
写出下列反应的化学方程式。
1.实验室制取二氧化碳
2.工业制取烧碱
3.熟石灰处理硫酸厂的废水
1.CaCO3
+2HCl=CaCl2
+
CO2↑+
H2O
2.Na2CO3
+
Ca(OH)2=
2NaOH
+
CaCO3↓
3.Ca(OH)2+H2SO4=
CaSO4+2H2O
复习
探究硫酸铜溶液的性质
氢氧化钠溶液
氯化钡溶液
现象
分别向盛有硫酸铜溶液的试管里滴加氢氧化钠溶液和氯化钡溶液,振荡,观察现象。
产生蓝色沉淀
产生白色沉淀
化学方程式:
CuSO4+2NaOH=
Na2SO4
+
Cu(OH)2↓
CuSO4+BaCl2=
CuCl2+BaSO4
↓
CuSO4+2NaOH=
Na2SO4
+
Cu(OH)2↓
CuSO4+BaCl2=
CuCl2+BaSO4
↓
Na2CO3
+
Ca(OH)2=
2NaOH
+
CaCO3↓
Ca(OH)2+H2SO4=
CaSO4+2H2O CaCO3
+2HCl=CaCl2
+
CO2↑+
H2O
两种化合物相互交换成分,生成物中有沉淀或者气体或者水生成时,复分解反应才能发生。
这些方程式有什么共同点?
复分解反应发生的条件
1.和金属反应
反应条件:金属排在盐中金属前面,盐溶于水。
Fe
+
CuSO4
=
Cu
+
FeSO4
2Al
+3CuSO4
=
3
Cu
+
Al2(SO4)3
盐的化学性质
1.和金属反应2.和酸反应
CaCO3
+2HCl=
BaCl2+H2SO4=
反应条件:有水或者沉淀或者气体生成
CaCl2
+
CO2↑+
H2O
BaSO4
↓
+2HCl
盐酸腐蚀大理石
盐的化学性质
1.和金属反应
2.和酸反应
3.和碱溶液反应
Na2CO3
+Ca(OH)2=
CuSO4+2NaOH=
反应条件:反应物溶于水,生成物中有水或者沉淀或者气体生成。
2NaOH
+
CaCO3↓
Na2SO4
+
Cu(OH)2↓
盐的化学性质
1.和金属反应
2.和酸反应
3.和碱溶液反应
4.和盐溶液反应
CuSO4+BaCl2
=
Na2CO3
+CaCl2
=
反应条件:反应物溶于水,生成物中有沉淀生成。
CuCl2+BaSO4
↓
2NaCl
+
CaCO3↓
盐的化学性质
物质
混合物(多种物质)
纯净物
(一种物质)
单质(一种元素)
化合物(多种元素)
氧化物(H2O)
酸(HCl)
碱(Ca(OH)2)
盐(NaCl)
金属(铁)
非金属(氧气)
物质种类
元素种类
组成元素
最外层电子数
物质的分类
1.复分解反应的条件
两种化合物相互交换成分,有沉淀或者气体或者水生成。
2.盐的化学性质
(1)和金属反应(2)和酸反应
(3)和某些碱反应(4)和某些盐反应
3.物质的分类
我的收获
我的收获
1.碳酸钠、碳酸氢钠、碳酸钙的用途
物
质
俗
名
用途
Na2CO3
纯碱、苏打
用于生产玻璃、造纸、纺织、洗涤剂、蒸馒头等。
NaHCO3
小苏打
发酵粉主要成分之一,
治疗胃酸过多。
CaCO3
大理石、石灰石主要成分
建筑材料、补钙剂,
还可用于实验室制
取二氧化碳。
2.碳酸钠和碳酸氢钠的性质
都可以和盐酸反应,碳酸钠可以和石灰水反应。
3.碳酸根离子的鉴定
取样于试管中,滴加稀盐酸,若有气泡产生,将产生的气体通入澄清石灰水,石灰水变浑浊,证明样品中含有碳酸根离子。
4.复分解反应
AB+CD=AD+CB
我的收获
1.6几种重要的盐
做饭时,我们都要用到食盐,食盐的主要成分是氯化钠。你对氯化钠了解有多少呢?
(1)生活中用做调味品
(2)腌制食品
(3)医疗上,制取生理盐水
(4)雪后公路上撒盐
(5)工业上做化工原料
(6)农业上选种
……
一、氯化钠
粗盐经溶解、沉淀、过滤、蒸发,可制得精盐。
海水、湖水、井水
提纯,除去不溶物
除去可溶物
精盐
蒸发
粗盐
(含泥沙、MgCl2、CaCl2)
海水晒盐
它们的主要成分都是碳酸钙
引入
一、碳酸钙
2.性质:
物理性质:白色固体,难溶于水
化学性质(1)和稀盐酸反应
CaCO3
+
2
HCl
===
CaCl2
+
H2CO3
CO2↑+H2O
1.用途:
做建筑材料、补钙剂
(2)高温分解
CaCO3
===
CaO+
CO2↑
高温
碳酸钠
碳酸氢钠
二、碳酸钠和碳酸氢钠
碳酸钠的用途
用于生产玻璃、造纸、纺织、洗涤剂、生活中可以用来蒸馒头
碳酸氢钠的用途
发酵粉的主要成分之一,治疗胃酸过多症的药剂,干粉灭火器的主要成分。
碳酸钠、碳酸氢钠的用途
碳酸钠+
盐酸
碳酸氢钠+盐酸
现
象
分
析
固体溶解,产生大量气泡,澄清石灰水变浑浊。
它们都能和盐酸反应生成CO2
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
碳酸钠、碳酸氢钠的性质
活动1:探究碳酸钠和碳酸氢钠是否和盐酸发生反应
CaCO3+2HCl=CaCl2+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
观察与思考
①观察:三个反应有什么共同特点?
②总结:鉴定碳酸根离子(或碳酸氢根离子)的方法。
碳酸钠、碳酸氢钠的性质
操作
现象
结论
向少量样品中加入稀盐酸。
有无色无味气体生成。
该样品是碳酸盐。
将产生的气体通入澄清石灰水。
澄清石灰水变浑浊。
鉴定碳酸根离子的方法。
碳酸钠、碳酸氢钠的性质
活动2
探究碳酸钠和碳酸氢钠是否和石灰水发生反应
碳酸钠+
石灰水
碳酸氢钠+石灰水
现
象
分
析
产生白色沉淀
无现象
可溶性碳酸盐和石灰水反应产生白色沉淀
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
工业制取烧碱的反应
碳酸钠、碳酸氢钠的性质
三、复分解反应
观察:三个反应有什么共同特点?
(1)HCl+
NaOH==
H2O
+
NaCl
(2)Na2CO3
+2HCl==2NaCl
+
H2CO3
(3)Na2CO3
+
Ca(OH)2==
2NaOH
+
CaCO3↓
两种化合物相互交换成分,生成另外两种化合物的反应,叫复分解反应。
AB+CD=AD+CB
CO2↑+H2O
写出下列反应的化学方程式。
1.实验室制取二氧化碳
2.工业制取烧碱
3.熟石灰处理硫酸厂的废水
1.CaCO3
+2HCl=CaCl2
+
CO2↑+
H2O
2.Na2CO3
+
Ca(OH)2=
2NaOH
+
CaCO3↓
3.Ca(OH)2+H2SO4=
CaSO4+2H2O
复习
探究硫酸铜溶液的性质
氢氧化钠溶液
氯化钡溶液
现象
分别向盛有硫酸铜溶液的试管里滴加氢氧化钠溶液和氯化钡溶液,振荡,观察现象。
产生蓝色沉淀
产生白色沉淀
化学方程式:
CuSO4+2NaOH=
Na2SO4
+
Cu(OH)2↓
CuSO4+BaCl2=
CuCl2+BaSO4
↓
CuSO4+2NaOH=
Na2SO4
+
Cu(OH)2↓
CuSO4+BaCl2=
CuCl2+BaSO4
↓
Na2CO3
+
Ca(OH)2=
2NaOH
+
CaCO3↓
Ca(OH)2+H2SO4=
CaSO4+2H2O CaCO3
+2HCl=CaCl2
+
CO2↑+
H2O
两种化合物相互交换成分,生成物中有沉淀或者气体或者水生成时,复分解反应才能发生。
这些方程式有什么共同点?
复分解反应发生的条件
1.和金属反应
反应条件:金属排在盐中金属前面,盐溶于水。
Fe
+
CuSO4
=
Cu
+
FeSO4
2Al
+3CuSO4
=
3
Cu
+
Al2(SO4)3
盐的化学性质
1.和金属反应2.和酸反应
CaCO3
+2HCl=
BaCl2+H2SO4=
反应条件:有水或者沉淀或者气体生成
CaCl2
+
CO2↑+
H2O
BaSO4
↓
+2HCl
盐酸腐蚀大理石
盐的化学性质
1.和金属反应
2.和酸反应
3.和碱溶液反应
Na2CO3
+Ca(OH)2=
CuSO4+2NaOH=
反应条件:反应物溶于水,生成物中有水或者沉淀或者气体生成。
2NaOH
+
CaCO3↓
Na2SO4
+
Cu(OH)2↓
盐的化学性质
1.和金属反应
2.和酸反应
3.和碱溶液反应
4.和盐溶液反应
CuSO4+BaCl2
=
Na2CO3
+CaCl2
=
反应条件:反应物溶于水,生成物中有沉淀生成。
CuCl2+BaSO4
↓
2NaCl
+
CaCO3↓
盐的化学性质
物质
混合物(多种物质)
纯净物
(一种物质)
单质(一种元素)
化合物(多种元素)
氧化物(H2O)
酸(HCl)
碱(Ca(OH)2)
盐(NaCl)
金属(铁)
非金属(氧气)
物质种类
元素种类
组成元素
最外层电子数
物质的分类
1.复分解反应的条件
两种化合物相互交换成分,有沉淀或者气体或者水生成。
2.盐的化学性质
(1)和金属反应(2)和酸反应
(3)和某些碱反应(4)和某些盐反应
3.物质的分类
我的收获
我的收获
1.碳酸钠、碳酸氢钠、碳酸钙的用途
物
质
俗
名
用途
Na2CO3
纯碱、苏打
用于生产玻璃、造纸、纺织、洗涤剂、蒸馒头等。
NaHCO3
小苏打
发酵粉主要成分之一,
治疗胃酸过多。
CaCO3
大理石、石灰石主要成分
建筑材料、补钙剂,
还可用于实验室制
取二氧化碳。
2.碳酸钠和碳酸氢钠的性质
都可以和盐酸反应,碳酸钠可以和石灰水反应。
3.碳酸根离子的鉴定
取样于试管中,滴加稀盐酸,若有气泡产生,将产生的气体通入澄清石灰水,石灰水变浑浊,证明样品中含有碳酸根离子。
4.复分解反应
AB+CD=AD+CB
我的收获
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
