人教版九年级上册 第六单元 课题2二氧化碳制取的研究(46张PPT)
文档属性
| 名称 | 人教版九年级上册 第六单元 课题2二氧化碳制取的研究(46张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-23 00:00:00 | ||
图片预览









文档简介
第六单元 碳和碳的氧化物
课题2二氧化碳制取的研究
温故知新:形成化合物最多的元素
1:同种元素可以组成不同的单质吗?
2:常见的碳单质有?常见自然界中最硬的物质?
3:金刚石石墨的结构?性质?用途?物理性质差异大的原因?金刚石变石墨是什么变化?
4:02和O3,CO和CO2,H2O和H2O2化学性质差异大的原因
5:无定型碳有哪些?有吸附性的含碳物质有哪两个?具有吸附性的原因?
6:金刚石、石墨有什么构成?
7:C60由什么构成?
8:古代字画保持时间长的原因
9:碳的化学性质
10:碳在常温下化学性质稳定的四个例子
11:碳完全燃烧和不完全燃烧化学方程式 12:小二实验酒灯注意事项,现象,涉及到的方程式
氧气的制取原理:
【回忆思考】
2KMnO4===K2MnO4+ MnO2+O2
2KClO3===2KCl + O2
2H2O2===2H2O + O2
△
△
MnO2
MnO2
实验室制取气体选取原则是:
①反应条件是否容易达到;
②产生气体的量是多少;
③收集的气体是否纯净;
④装置、操作是否简单和安全;
⑤原料是否易得、价廉。
……
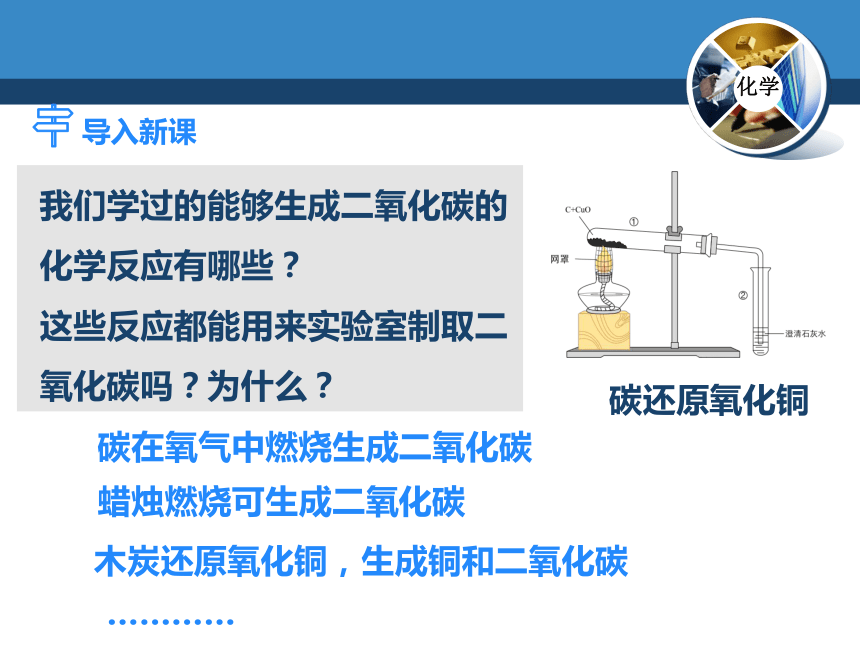
我们学过的能够生成二氧化碳的化学反应有哪些?
这些反应都能用来实验室制取二氧化碳吗?为什么?
碳还原氧化铜
碳在氧气中燃烧生成二氧化碳
蜡烛燃烧可生成二氧化碳
木炭还原氧化铜,生成铜和二氧化碳
…………
导入新课
学习目标
探究实验室里制取二氧化碳的装置。
02
了解实验室制取二氧化碳的反应原理。
01
讲授新课
了解实验室里制取气体的一般思路和方法。
03
含碳酸根离子的化合物
(如Na2CO3 、CaCO3) 能与稀盐酸(HCl)或稀硫酸(H2SO4 )在常温下反应生成CO2气体。
资料信息
探究制取二氧化碳的药品及反应原理
一
上述四个反应都能产生二氧化碳,都适合用来实验室制取二氧化碳吗?
Na2CO3 + 2HCl 2NaCl + CO2↑ + H2O
Na2CO3 + H2SO4 Na2SO4 + CO2↑ + H2O
CaCO3 + 2HCl CaCl2 + CO2↑ + H2O
CaCO3 + H2SO4 CaSO4 + CO2↑ + H2O
NaCl、CaCl2易溶于水、CaSO4微溶于水
原理
探究制取二氧化碳的药品及反应原理
一
探究制取二氧化碳的药品及反应原理
一
实验
现象
碳酸钠和稀盐酸反应
大量气泡,反应很快
碳酸钠和稀硫酸反应
大量气泡,反应很快
大理石和稀盐酸反应
大量气泡,反应速度适中
大理石和稀硫酸反应
少量气泡,反应一会儿就停止
选择制取气体时药品的一般原则:较易反应、反应速度适中、生成的气体纯净、易于收集、操作简便、原料廉价易得等。
探究制取二氧化碳的药品及反应原理
一
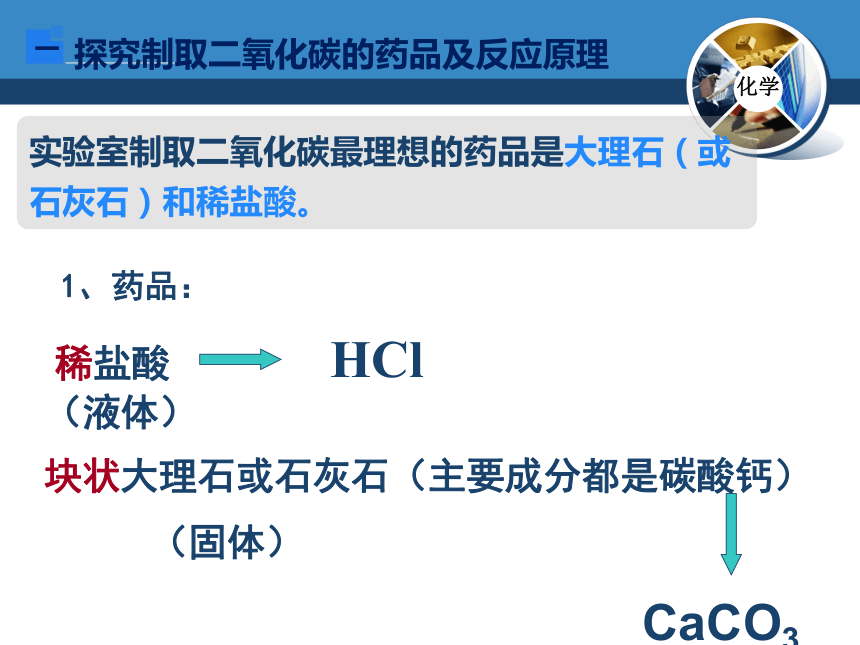
稀盐酸
(液体)
块状大理石或石灰石(主要成分都是碳酸钙)
(固体)
HCl
CaCO3
实验室制取二氧化碳最理想的药品是大理石(或石灰石)和稀盐酸。
1、药品:
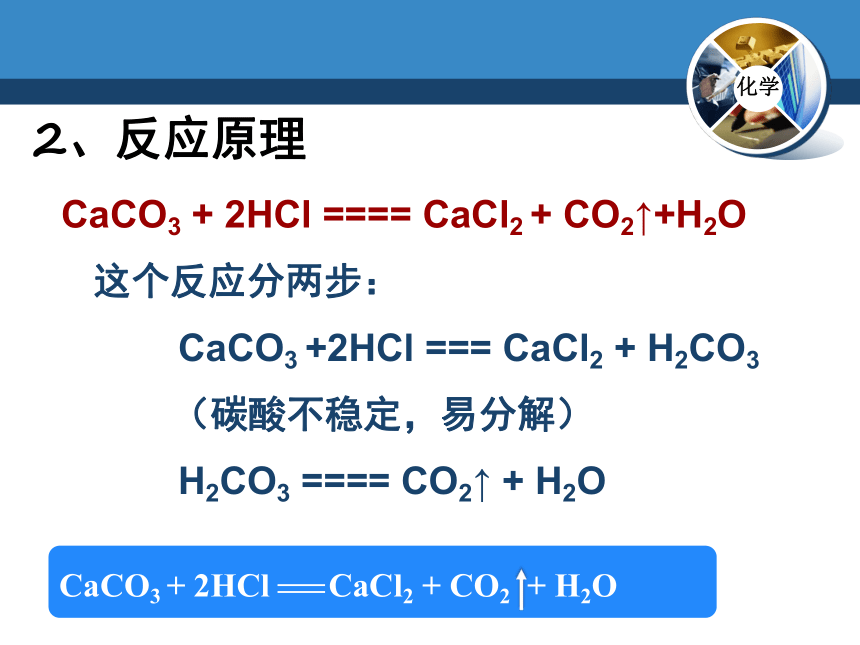
CaCO3 + 2HCl ==== CaCl2 + CO2↑+H2O
这个反应分两步:
CaCO3 +2HCl === CaCl2 + H2CO3
(碳酸不稳定,易分解)
H2CO3 ==== CO2↑ + H2O
2、反应原理
CaCO3 + 2HCl CaCl2 + CO2 + H2O
3、注意事项
不能,因为浓盐酸具有强挥发性,能挥发出HCl气体,使收集的CO2不纯。
1. 实验室制取二氧化碳能不能用浓盐酸代替稀盐酸?
探究制取二氧化碳的药品及反应原理
一
3. 为什么不用碳酸钠粉末和碳酸钙粉末制二氧化碳?
因为碳酸钠粉末和碳酸钙粉末与稀盐酸反应时,速度过快,不利于气体收集。
因为稀硫酸与大理石反应生成微溶于水的硫酸钙,覆盖在大理石表面,阻止了大理石与稀硫酸继续反应。
2. 为什么不用稀硫酸和大理石反应制二氧化碳?
探究制取二氧化碳的药品及反应原理
一
实验室制取二氧化碳的装置
加热高锰酸钾制取氧气
用MnO2在常温下催化H2O2分解制取氧气
用排水法收集氧气
用向上排空气法收集氧气
回忆实验室制取和收集氧气的实验装置
实验室制取气体的装置包括发生装置和收集装置,请结合实验室制取氧气的知识以及课本113—114页的材料,小结确定气体发生装置和收集装置时应考虑的因素。
实验室制取气体的装置的确定
气体发生装置
反应物的状态
反应条件
固体反应物
(是否需加热、催化剂等)
气体收集装置
排空气法(29)
密度比空气大:
向上排气法
密度比空气小:
向下排气法
排水法
(不易溶于水、不与水反应)
固体和液体反应
液体和液体反应
…
实验室制取氧气的发生装置
实验
发生装置
选择依据
反应物状态
反应条件
高锰酸钾
氯酸钾
过氧化氢
固固
加热型
固液
常温型
固体
固体和
液体
常温
加热
探究制取二氧化碳的发生装置
二
装
置
优点
装置简单
装
置
优点
方便添加液体药品
可以控制反应速率
随时控制反应的发生和停止
几种装置的变形,及其优点:
装置简单
注意事项:
长颈漏斗要伸到液面以下,
以防气体从漏斗中逸出,起液封作用。
简易装置
优点:
装置简单
易操作
复杂装置
优点:
方便随时添加稀盐酸
多孔隔板
适用条件:块状固体与液体在常温下反应
发生原理:打开活塞,固液接触,反应开始;
停止原理:关闭活塞,生成的CO2气体使内部压强增大,液体被压回长颈漏斗,液面下降固液分离,反应停止。
几种可控装置:
A
B
C
适用条件:块状固体与液体在常温下反应
发生原理:打开弹簧夹,从长颈漏斗中加入液体至没过容器中的固体,固液接触,反应开始;
停止原理:关闭弹簧夹,容器中生成的CO2气体不能逸出,使内部压强增大,液体被压入长颈漏斗内,液面下降,固液分离,反应停止。
升温法:先向锥形瓶中加水,使长颈漏斗下端没入水中,用弹簧夹夹紧胶皮管,双手紧握锥形瓶,长颈漏斗下端能形成一段水柱,并且一段时间后液面不下降说明气密性良好;
注水法:先向锥形瓶中加水,使长颈漏斗下端没入水中,用弹簧夹夹紧胶皮管,再从长颈漏斗处向其中加水,下端能形成一段稳定的水柱,说明气密性良好;
想一想:第二、第四套装置如何检查装置的气密性?
抽气法:先向锥形瓶中加水,使长颈漏斗下端浸入液面以下,用注射器在胶皮管处往外抽气,长颈漏斗下端管口有气泡冒出,说明气密性良好;
充气法:先向锥形瓶中加水,使长颈漏斗下端浸入液面以下,用注射器在胶皮管处往里充气,长颈漏斗内液面上升,并且一段时间后液面不下降,说明气密性良好;
实验室制取氧气的装置
发生装置
收集装置
发生装置
收集装置
制取二氧化碳该用什么装置呢?
1、发生装置:
固液常温型
装 置
CO2收集装置的选择:
排水法
向下排空法
向上排空法
√
2、收集方法:
向上排空气法
装 置
3、检验方法:
将气体通入澄清的石灰水, 石灰水变浑浊,证明该气体是二氧化碳。
澄清石灰水
4、验满:
燃着的木条放在集气瓶口,若熄灭则已集满
二氧化碳的实验室制法
一、原料及原理
二、装置
三、步骤
我来试试看
下列仪器可供设计制取二氧化碳的装置时选择,你也可以另选或自制仪器,还可利用代用品
1、锥形瓶
2、平底烧瓶
3、烧杯
4、试管
5、集气瓶
6、长颈漏斗
7、双孔导管
8、导管
9、弯导管
10、水槽
11、酒精灯
×
×
×
×
【讨论】
如果要利用所设计的装置制取一瓶二氧化碳,需要哪些步骤?
制取二氧化碳的实验步骤:
向长颈漏斗中加水,使长颈漏斗的下端浸入液面以下,堵住导气管,继续向长颈漏斗加水,发现长颈漏斗中的液面不下降,说明装置的气密性良好
先装入固体,后加液体
导气管插入到集气瓶的底部
用燃着的木条平放在集气瓶口
1、按要求连接好仪器。
2、检查装置的气密性。
3、装入药品。
4、收集气体。
5、验满。
分析:
制取二氧化碳和氧气的发生装置
和收集装置各有什么不同。
制取氧气和二氧化碳装置的比较
类型
类别
制取氧气
制取二氧化碳
原料
原理
发生装置
收集装置
KMnO4
固体
反应条件
加 热
常 温
大理石或石灰石
稀盐酸
(固体)
(液体)
2KMnO4 K2MnO4 +MnO2+O2
CaCO3+2HCl=
CaCl2+H2O+CO2
O2不易溶于水
O2的密度比空气大
CO2的密度比空气大能溶于水
实验室制取气体的思路是什么?
1、药品
2、反应原理
3、装置(发生装置和收集装置)
4、检验(验证和验满)
1、实验室用石灰石(或大理石)与稀盐酸反应来制取二氧化碳。
2、实验室用下述装置来制取和检验二氧化碳:
3、实验室制取气体要注意:
(1)选择适当的反应;
(2)选择合适的实验装置;
(3)需验证所制得的气体
澄清石灰水
4、二氧化碳的工业制法
高温煅烧石灰石(主要成分是碳酸钙)
CaCO3 CaO+CO2
高温
5、家庭制取二氧化碳
2、水垢和醋酸、鸡蛋壳和醋酸、碱面和醋酸
1、含碳酸钙的物质:大理石、石灰石、鸡蛋壳、水垢、珍珠、钟乳石
1、实验室制取二氧化碳,选用的反应物最好的是:
A碳酸钠和稀硫酸 B石灰石和稀硫酸
C大理石和稀盐酸 D石灰石和浓盐酸
2、下列哪个反应可用于实验室制取二氧化碳:
A C+O2 CO2
B C+2CuO 2Cu+CO2
C CaCO3+2HCl CaCl2+H2O+CO2
D CaCO3 CaO+CO2
点燃
高温
高温
3、实验室制备并收集CO2,有以下操作步骤:
①检查装置的气密性 ②连接装置
③加入大理石 ④加入稀盐酸
⑤收集 ⑥验满
其中排列顺序正确的是( )
A.①②③④⑤⑥ B. ②①④③⑤⑥
C.②①③④⑤⑥D.②③④①⑤⑥
C
4、下列气体只能用向上排空气法收集的是 (??? )
A. H2 B.O2 C.CO2 D.O2和CO2
5.检验CO2气体是否收集满的方法是 (????? )
A.将燃着的木条伸入集气瓶内
B.将带火星的木条放在集气瓶口
C.将少量澄清的石灰水倒入集气瓶中、振荡
D.将燃着的木条放在集气瓶口
6.实验室收集CO2的正确方法是
A.排水法 B.向下排空气法
C.向上排空气法 D.排水法和向上排空气法
7.你能举出几种鉴别O2、CO2气体的方法?
课题2二氧化碳制取的研究
温故知新:形成化合物最多的元素
1:同种元素可以组成不同的单质吗?
2:常见的碳单质有?常见自然界中最硬的物质?
3:金刚石石墨的结构?性质?用途?物理性质差异大的原因?金刚石变石墨是什么变化?
4:02和O3,CO和CO2,H2O和H2O2化学性质差异大的原因
5:无定型碳有哪些?有吸附性的含碳物质有哪两个?具有吸附性的原因?
6:金刚石、石墨有什么构成?
7:C60由什么构成?
8:古代字画保持时间长的原因
9:碳的化学性质
10:碳在常温下化学性质稳定的四个例子
11:碳完全燃烧和不完全燃烧化学方程式 12:小二实验酒灯注意事项,现象,涉及到的方程式
氧气的制取原理:
【回忆思考】
2KMnO4===K2MnO4+ MnO2+O2
2KClO3===2KCl + O2
2H2O2===2H2O + O2
△
△
MnO2
MnO2
实验室制取气体选取原则是:
①反应条件是否容易达到;
②产生气体的量是多少;
③收集的气体是否纯净;
④装置、操作是否简单和安全;
⑤原料是否易得、价廉。
……
我们学过的能够生成二氧化碳的化学反应有哪些?
这些反应都能用来实验室制取二氧化碳吗?为什么?
碳还原氧化铜
碳在氧气中燃烧生成二氧化碳
蜡烛燃烧可生成二氧化碳
木炭还原氧化铜,生成铜和二氧化碳
…………
导入新课
学习目标
探究实验室里制取二氧化碳的装置。
02
了解实验室制取二氧化碳的反应原理。
01
讲授新课
了解实验室里制取气体的一般思路和方法。
03
含碳酸根离子的化合物
(如Na2CO3 、CaCO3) 能与稀盐酸(HCl)或稀硫酸(H2SO4 )在常温下反应生成CO2气体。
资料信息
探究制取二氧化碳的药品及反应原理
一
上述四个反应都能产生二氧化碳,都适合用来实验室制取二氧化碳吗?
Na2CO3 + 2HCl 2NaCl + CO2↑ + H2O
Na2CO3 + H2SO4 Na2SO4 + CO2↑ + H2O
CaCO3 + 2HCl CaCl2 + CO2↑ + H2O
CaCO3 + H2SO4 CaSO4 + CO2↑ + H2O
NaCl、CaCl2易溶于水、CaSO4微溶于水
原理
探究制取二氧化碳的药品及反应原理
一
探究制取二氧化碳的药品及反应原理
一
实验
现象
碳酸钠和稀盐酸反应
大量气泡,反应很快
碳酸钠和稀硫酸反应
大量气泡,反应很快
大理石和稀盐酸反应
大量气泡,反应速度适中
大理石和稀硫酸反应
少量气泡,反应一会儿就停止
选择制取气体时药品的一般原则:较易反应、反应速度适中、生成的气体纯净、易于收集、操作简便、原料廉价易得等。
探究制取二氧化碳的药品及反应原理
一
稀盐酸
(液体)
块状大理石或石灰石(主要成分都是碳酸钙)
(固体)
HCl
CaCO3
实验室制取二氧化碳最理想的药品是大理石(或石灰石)和稀盐酸。
1、药品:
CaCO3 + 2HCl ==== CaCl2 + CO2↑+H2O
这个反应分两步:
CaCO3 +2HCl === CaCl2 + H2CO3
(碳酸不稳定,易分解)
H2CO3 ==== CO2↑ + H2O
2、反应原理
CaCO3 + 2HCl CaCl2 + CO2 + H2O
3、注意事项
不能,因为浓盐酸具有强挥发性,能挥发出HCl气体,使收集的CO2不纯。
1. 实验室制取二氧化碳能不能用浓盐酸代替稀盐酸?
探究制取二氧化碳的药品及反应原理
一
3. 为什么不用碳酸钠粉末和碳酸钙粉末制二氧化碳?
因为碳酸钠粉末和碳酸钙粉末与稀盐酸反应时,速度过快,不利于气体收集。
因为稀硫酸与大理石反应生成微溶于水的硫酸钙,覆盖在大理石表面,阻止了大理石与稀硫酸继续反应。
2. 为什么不用稀硫酸和大理石反应制二氧化碳?
探究制取二氧化碳的药品及反应原理
一
实验室制取二氧化碳的装置
加热高锰酸钾制取氧气
用MnO2在常温下催化H2O2分解制取氧气
用排水法收集氧气
用向上排空气法收集氧气
回忆实验室制取和收集氧气的实验装置
实验室制取气体的装置包括发生装置和收集装置,请结合实验室制取氧气的知识以及课本113—114页的材料,小结确定气体发生装置和收集装置时应考虑的因素。
实验室制取气体的装置的确定
气体发生装置
反应物的状态
反应条件
固体反应物
(是否需加热、催化剂等)
气体收集装置
排空气法(29)
密度比空气大:
向上排气法
密度比空气小:
向下排气法
排水法
(不易溶于水、不与水反应)
固体和液体反应
液体和液体反应
…
实验室制取氧气的发生装置
实验
发生装置
选择依据
反应物状态
反应条件
高锰酸钾
氯酸钾
过氧化氢
固固
加热型
固液
常温型
固体
固体和
液体
常温
加热
探究制取二氧化碳的发生装置
二
装
置
优点
装置简单
装
置
优点
方便添加液体药品
可以控制反应速率
随时控制反应的发生和停止
几种装置的变形,及其优点:
装置简单
注意事项:
长颈漏斗要伸到液面以下,
以防气体从漏斗中逸出,起液封作用。
简易装置
优点:
装置简单
易操作
复杂装置
优点:
方便随时添加稀盐酸
多孔隔板
适用条件:块状固体与液体在常温下反应
发生原理:打开活塞,固液接触,反应开始;
停止原理:关闭活塞,生成的CO2气体使内部压强增大,液体被压回长颈漏斗,液面下降固液分离,反应停止。
几种可控装置:
A
B
C
适用条件:块状固体与液体在常温下反应
发生原理:打开弹簧夹,从长颈漏斗中加入液体至没过容器中的固体,固液接触,反应开始;
停止原理:关闭弹簧夹,容器中生成的CO2气体不能逸出,使内部压强增大,液体被压入长颈漏斗内,液面下降,固液分离,反应停止。
升温法:先向锥形瓶中加水,使长颈漏斗下端没入水中,用弹簧夹夹紧胶皮管,双手紧握锥形瓶,长颈漏斗下端能形成一段水柱,并且一段时间后液面不下降说明气密性良好;
注水法:先向锥形瓶中加水,使长颈漏斗下端没入水中,用弹簧夹夹紧胶皮管,再从长颈漏斗处向其中加水,下端能形成一段稳定的水柱,说明气密性良好;
想一想:第二、第四套装置如何检查装置的气密性?
抽气法:先向锥形瓶中加水,使长颈漏斗下端浸入液面以下,用注射器在胶皮管处往外抽气,长颈漏斗下端管口有气泡冒出,说明气密性良好;
充气法:先向锥形瓶中加水,使长颈漏斗下端浸入液面以下,用注射器在胶皮管处往里充气,长颈漏斗内液面上升,并且一段时间后液面不下降,说明气密性良好;
实验室制取氧气的装置
发生装置
收集装置
发生装置
收集装置
制取二氧化碳该用什么装置呢?
1、发生装置:
固液常温型
装 置
CO2收集装置的选择:
排水法
向下排空法
向上排空法
√
2、收集方法:
向上排空气法
装 置
3、检验方法:
将气体通入澄清的石灰水, 石灰水变浑浊,证明该气体是二氧化碳。
澄清石灰水
4、验满:
燃着的木条放在集气瓶口,若熄灭则已集满
二氧化碳的实验室制法
一、原料及原理
二、装置
三、步骤
我来试试看
下列仪器可供设计制取二氧化碳的装置时选择,你也可以另选或自制仪器,还可利用代用品
1、锥形瓶
2、平底烧瓶
3、烧杯
4、试管
5、集气瓶
6、长颈漏斗
7、双孔导管
8、导管
9、弯导管
10、水槽
11、酒精灯
×
×
×
×
【讨论】
如果要利用所设计的装置制取一瓶二氧化碳,需要哪些步骤?
制取二氧化碳的实验步骤:
向长颈漏斗中加水,使长颈漏斗的下端浸入液面以下,堵住导气管,继续向长颈漏斗加水,发现长颈漏斗中的液面不下降,说明装置的气密性良好
先装入固体,后加液体
导气管插入到集气瓶的底部
用燃着的木条平放在集气瓶口
1、按要求连接好仪器。
2、检查装置的气密性。
3、装入药品。
4、收集气体。
5、验满。
分析:
制取二氧化碳和氧气的发生装置
和收集装置各有什么不同。
制取氧气和二氧化碳装置的比较
类型
类别
制取氧气
制取二氧化碳
原料
原理
发生装置
收集装置
KMnO4
固体
反应条件
加 热
常 温
大理石或石灰石
稀盐酸
(固体)
(液体)
2KMnO4 K2MnO4 +MnO2+O2
CaCO3+2HCl=
CaCl2+H2O+CO2
O2不易溶于水
O2的密度比空气大
CO2的密度比空气大能溶于水
实验室制取气体的思路是什么?
1、药品
2、反应原理
3、装置(发生装置和收集装置)
4、检验(验证和验满)
1、实验室用石灰石(或大理石)与稀盐酸反应来制取二氧化碳。
2、实验室用下述装置来制取和检验二氧化碳:
3、实验室制取气体要注意:
(1)选择适当的反应;
(2)选择合适的实验装置;
(3)需验证所制得的气体
澄清石灰水
4、二氧化碳的工业制法
高温煅烧石灰石(主要成分是碳酸钙)
CaCO3 CaO+CO2
高温
5、家庭制取二氧化碳
2、水垢和醋酸、鸡蛋壳和醋酸、碱面和醋酸
1、含碳酸钙的物质:大理石、石灰石、鸡蛋壳、水垢、珍珠、钟乳石
1、实验室制取二氧化碳,选用的反应物最好的是:
A碳酸钠和稀硫酸 B石灰石和稀硫酸
C大理石和稀盐酸 D石灰石和浓盐酸
2、下列哪个反应可用于实验室制取二氧化碳:
A C+O2 CO2
B C+2CuO 2Cu+CO2
C CaCO3+2HCl CaCl2+H2O+CO2
D CaCO3 CaO+CO2
点燃
高温
高温
3、实验室制备并收集CO2,有以下操作步骤:
①检查装置的气密性 ②连接装置
③加入大理石 ④加入稀盐酸
⑤收集 ⑥验满
其中排列顺序正确的是( )
A.①②③④⑤⑥ B. ②①④③⑤⑥
C.②①③④⑤⑥D.②③④①⑤⑥
C
4、下列气体只能用向上排空气法收集的是 (??? )
A. H2 B.O2 C.CO2 D.O2和CO2
5.检验CO2气体是否收集满的方法是 (????? )
A.将燃着的木条伸入集气瓶内
B.将带火星的木条放在集气瓶口
C.将少量澄清的石灰水倒入集气瓶中、振荡
D.将燃着的木条放在集气瓶口
6.实验室收集CO2的正确方法是
A.排水法 B.向下排空气法
C.向上排空气法 D.排水法和向上排空气法
7.你能举出几种鉴别O2、CO2气体的方法?
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
