人教版九年级上册化学课件:10.1第1课时 酸碱指示剂 常见的酸(32张PPT)
文档属性
| 名称 | 人教版九年级上册化学课件:10.1第1课时 酸碱指示剂 常见的酸(32张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 701.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-24 00:00:00 | ||
图片预览









文档简介
第十单元 酸和碱
课题1 常见的酸和碱
第1课时 酸碱指示剂 常见的酸
1.(2019·郴州)下列溶液能使紫色石蕊溶液变成蓝色的是( )
A.澄清石灰水 B.NaCl溶液 C.稀硫酸 D.KNO3溶液
A
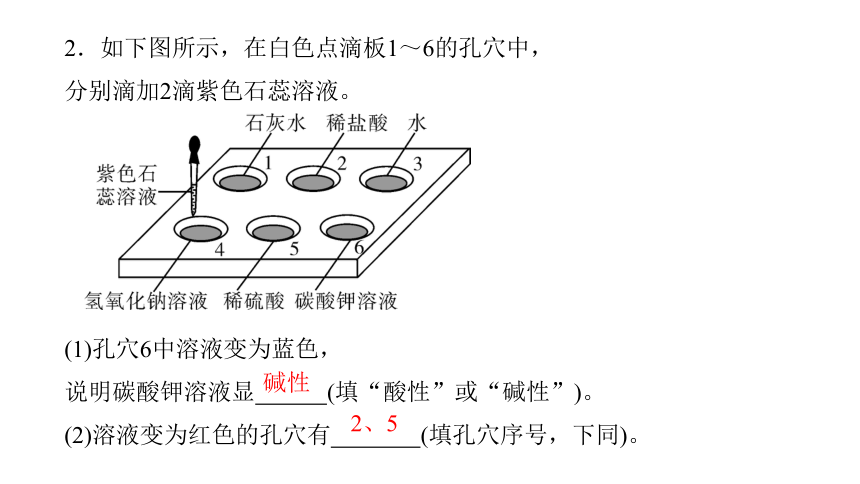
2.如下图所示,在白色点滴板1~6的孔穴中,
分别滴加2滴紫色石蕊溶液。
(1)孔穴6中溶液变为蓝色,
说明碳酸钾溶液显 (填“酸性”或“碱性”)。
(2)溶液变为红色的孔穴有 (填孔穴序号,下同)。
碱性
2、5
(3)作为空白对照实验的孔穴是___。
(4)再向孔穴4中滴加稀硫酸,溶液变为紫色,
是因为硫酸与氢氧化钠反应生成了硫酸钠和水,
反应的化学方程式是___________________________________。
3
2NaOH + H2SO4=== Na2SO4+ 2H2O
3.下列关于浓盐酸的说法错误的是( )
A.易挥发 B.有腐蚀性 C.有较强吸水性 D.密度比水大
4.将浓硫酸和浓盐酸都敞口放置在空气中,一段时间后,
它们发生的相同变化是( )
A.溶质的质量都变小 B.溶液的质量都变大
C.溶剂的质量都变大 D.溶质的质量分数都变小
C
D
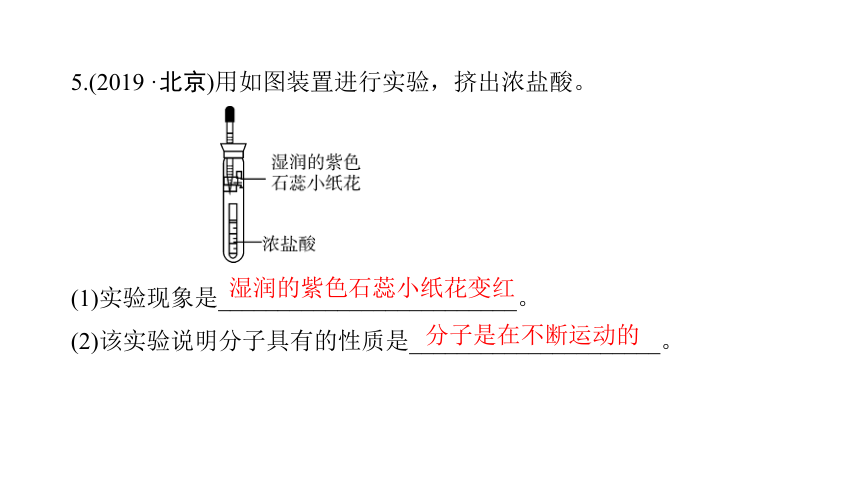
5.(2019·北京)用如图装置进行实验,挤出浓盐酸。
(1)实验现象是_________________________。
(2)该实验说明分子具有的性质是_____________________。
湿润的紫色石蕊小纸花变红
分子是在不断运动的
6.(变式题)现有两瓶失去标签的无色溶液:浓硫酸和浓盐酸。
鉴别方法是:
(1)打开瓶盖,观察到瓶口有“白雾”冒出者为_______。
(2)用玻璃棒蘸取少许滴在火柴梗上,变黑者为_________。
(3)取等体积称重量,重者为_________。
(4)在瓶口上方扇一下,闻气味,有刺激性气味者为_________。
浓盐酸
浓硫酸
浓硫酸
浓盐酸
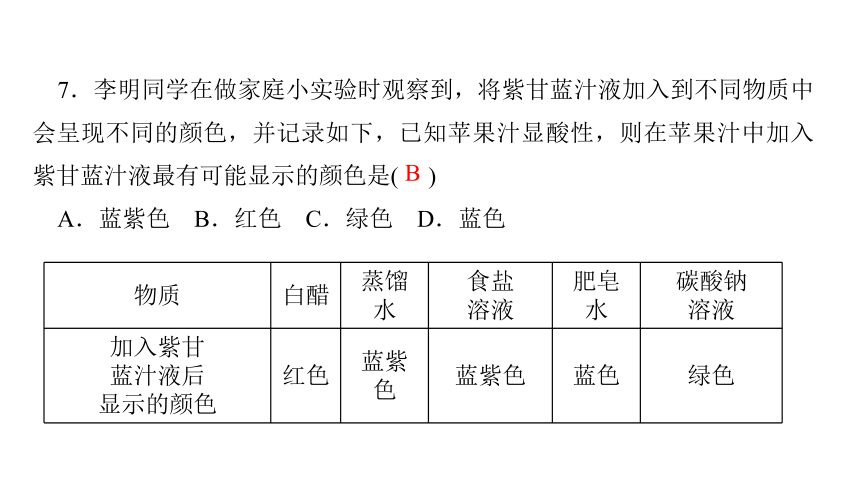
7.李明同学在做家庭小实验时观察到,将紫甘蓝汁液加入到不同物质中会呈现不同的颜色,并记录如下,已知苹果汁显酸性,则在苹果汁中加入紫甘蓝汁液最有可能显示的颜色是( )
A.蓝紫色 B.红色 C.绿色 D.蓝色
物质
白醋
蒸馏水
食盐
溶液
肥皂水
碳酸钠
溶液
加入紫甘
蓝汁液后
显示的颜色
红色
蓝紫色
蓝紫色
蓝色
绿色
B
8.(变式题)实验室里,常用浓硫酸作为干燥剂,
这是利用了浓硫酸的( )
A.吸水性 B.脱水性 C.酸性 D.氧化性
9.浓盐酸和浓硫酸对比,下列叙述正确的是( )
A.两者均具有挥发性
B.两者均具有刺激性气味
C.两者均具有腐蚀性
D.两者均是黏稠状液体
A
C
10.某同学在化学晚会上使用毛笔蘸取一种无色液体在一张白纸上书写“化学魔术”四个字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四个字。该同学所用的两种无色液体可能是( )
A.NaOH溶液、酚酞溶液
B.白醋、酚酞溶液
C.石蕊溶液、酚酞溶液
D.“雪碧”饮料、酚酞溶液
A
11.下图是浓盐酸试剂瓶上标签的部分内容。请回答:
(1)该浓盐酸的溶质是 (填化学式)。
(2)现要配制3%的稀盐酸120 g,需要这种浓盐酸___g。
(3)使用一段时间后,浓盐酸的溶质的质量分数小于36%,
原因是________________。
HCl
10
浓盐酸具有挥发性
12.如图所示是两种稀释浓硫酸的操作,回答下列问题:
(1)B图中加水仪器的名称是____________。
(2)B图锥形瓶内产生的现象是__________________________。
产生这一现象的原因是_________________________________。
(3)上边两幅图中,稀释浓硫酸的操作正确的是 (填序号)。
分液漏斗
液体沸腾,产生大量蒸气
浓硫酸溶于水放出大量的热
A
13.某些植物的花汁可作为酸碱指示剂。
取三种花汁用酒精溶液、稀酸溶液、稀碱溶液检验,颜色如下:
花种类
花汁在酒精
(中性)中的颜色
花汁在稀
酸中的颜色
花汁在稀
碱中的颜色
玫瑰花
粉红
粉红
绿
万寿菊花
黄
黄
黄
大红花
粉红
橙
绿
试回答下列问题:
(1)为检验生活中的食盐水、肥皂水、汽水、石灰水四种物质的酸碱性,
可选择________花汁,不选用其他花汁的原因
是_____________________________________________。
大红花
其他两种在酸、碱、中性溶液中有显示相同的颜色
(2)取所选花汁少许分别滴入上述四种物质中,请将所显颜色填入下表中。
检验物质
食盐水
肥皂水
汽水
石灰水
所显颜色
____
____
___
____
粉红
绿
橙
绿
1.柠檬汁能使紫色石蕊溶液变红色,由此可知柠檬汁( )
A.显碱性 B.显酸性 C.显中性 D.无法确定
B
2.小红学习了酸碱指示剂与常见的酸、碱溶液作用后,归纳总结出如图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,其中颜色不正确的是( )
A.紫色 B.蓝色
C.红色 D.无色
A
3.(2019·平舆县期中)下列物质中,不能用金属跟稀酸反应直接制得的是( )
A.硫酸锌(ZnSO4) B.氯化镁(MgCl2)
C.氯化铁(FeCl3) D.硫酸亚铁(FeSO4)
4.有A、B两种金属,放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示。下列结论合理的是( )
A.金属活动性:A>B
B.生成氢气的质量:A>B
C.反应的硫酸质量:A<B
D.反应的金属质量:A<B
C
B
5.泉州是白蚂蚁灾害的高发地区,白蚂蚁会蛀蚀木头,它分泌的蚁酸是一种酸,能腐蚀很多建筑材料。下列建筑材料最不容易被白蚂蚁腐蚀的是( )
A.钢筋 B.铜制品 C.大理石 D.铝合金
B
6.物质X可发生“X+酸―→化合物+H2O”的反应,则X可能是( )
A.Fe B.CO2 C.H2SO4 D.CuO
7.(2019·驻马店一模)取一定量氧化铁与氧化铜的混合物,向其中加入100 g 14.6%的稀盐酸,恰好完全反应,则混合物中氧元素的质量为____g;
写出氧化铁与稀盐酸反应的化学方程式:__________________________。
D
3.2
Fe2O3+6HCl===2FeCl3+3H2O
8.酸溶液具有相似化学性质的原因是( )
A.酸溶液里都含有水分子
B.酸溶液里都含有氢离子
C.酸溶液里都含有氢元素
D.酸溶液里都含有酸根离子
B
9.小王同学往厨房的纯碱中滴加白醋,发现有气体生成。
已知白醋里含3%~5%的醋酸(CH3COOH),
醋酸与盐酸的化学性质相似,
下列说法不正确的是( )
A.白醋里含有氢离子
B.生成的气体是二氧化碳
C白醋能使紫色石蕊溶液变红
D.白醋与纯碱的反应属于化合反应
D
10.下列物质的变化中,只有加酸才能一步实现的是( )
A.CaCO3―→CO2 B.Zn―→ZnSO4
C.CuO―→CuCl2 D.Fe―→FeCl2
11.(2019·荆州)将某稀硫酸分成两等份,分别向其中加入锌粉或铁粉,
反应结束后剩余的铁比剩余的锌多,产生氢气的质量分别为a g和b g,
则a和b的关系是( )
A.a<b B.a=b
C.a>b D.无法判断
C
B
12.(2019·自贡)氧化铜与稀盐酸发生反应时,容器中溶液总质量随
时间的变化曲线如图所示。下列说法错误的是( )
A.该实验是将稀盐酸逐渐加入到盛有氧化铜的容器中
B.m点表示氧化铜与稀盐酸恰好完全反应
C.m点和n点对应溶液中铜元素的质量不相等
D.m点和n点对应溶液蒸发结晶后得到的固体成分相同
C
13.将稀盐酸分别滴入盛有不同物质的试管中,如图所示。
(1)不能发生反应的是 (填字母,下同)。
(2)有气泡产生的是_______。
(3)有浅绿色溶液生成的是___。
(4)有蓝色溶液生成的是___。
(5)溶液变成红色的是___。
A
B、C
B
D
E
14.利用以下装置对酸的化学性质进行探究。
(1)实验Ⅰ中,在点滴板的a、b孔穴中滴入酸溶液后,
溶液变红的是 (填“a”或“b”)。
使用点滴板的优点之一是_______________。
a
节约药品
15.(2019·平舆县期中)某研究性学习小组的同学做了如下的实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球悬浮于液面,位置如图所示。将从废电池外壳收集来的锌片放入烧杯中,该学生看到的现象
是________________________________,当杯中的盐酸完全反应后,
此时小球所处位置与原来相比 (填“不变”“上浮”或“下沉”)。
其依据是___________________________________________________,
,
,
______________________________________________________,
反应的化学方程式为_______________________。
产生气泡,锌片逐渐溶解,小球移动
上浮
因为锌与盐酸反应生成了氯化锌,溶质的相对分子质量增大
使得溶液的密度增大,漂浮满足的条件为重力等于浮力
由于重力不变
则浮力不变,则应该是排开液体的体积减小,因此应该上浮
Zn+2HCl===ZnCl2+H2↑
课题1 常见的酸和碱
第1课时 酸碱指示剂 常见的酸
1.(2019·郴州)下列溶液能使紫色石蕊溶液变成蓝色的是( )
A.澄清石灰水 B.NaCl溶液 C.稀硫酸 D.KNO3溶液
A
2.如下图所示,在白色点滴板1~6的孔穴中,
分别滴加2滴紫色石蕊溶液。
(1)孔穴6中溶液变为蓝色,
说明碳酸钾溶液显 (填“酸性”或“碱性”)。
(2)溶液变为红色的孔穴有 (填孔穴序号,下同)。
碱性
2、5
(3)作为空白对照实验的孔穴是___。
(4)再向孔穴4中滴加稀硫酸,溶液变为紫色,
是因为硫酸与氢氧化钠反应生成了硫酸钠和水,
反应的化学方程式是___________________________________。
3
2NaOH + H2SO4=== Na2SO4+ 2H2O
3.下列关于浓盐酸的说法错误的是( )
A.易挥发 B.有腐蚀性 C.有较强吸水性 D.密度比水大
4.将浓硫酸和浓盐酸都敞口放置在空气中,一段时间后,
它们发生的相同变化是( )
A.溶质的质量都变小 B.溶液的质量都变大
C.溶剂的质量都变大 D.溶质的质量分数都变小
C
D
5.(2019·北京)用如图装置进行实验,挤出浓盐酸。
(1)实验现象是_________________________。
(2)该实验说明分子具有的性质是_____________________。
湿润的紫色石蕊小纸花变红
分子是在不断运动的
6.(变式题)现有两瓶失去标签的无色溶液:浓硫酸和浓盐酸。
鉴别方法是:
(1)打开瓶盖,观察到瓶口有“白雾”冒出者为_______。
(2)用玻璃棒蘸取少许滴在火柴梗上,变黑者为_________。
(3)取等体积称重量,重者为_________。
(4)在瓶口上方扇一下,闻气味,有刺激性气味者为_________。
浓盐酸
浓硫酸
浓硫酸
浓盐酸
7.李明同学在做家庭小实验时观察到,将紫甘蓝汁液加入到不同物质中会呈现不同的颜色,并记录如下,已知苹果汁显酸性,则在苹果汁中加入紫甘蓝汁液最有可能显示的颜色是( )
A.蓝紫色 B.红色 C.绿色 D.蓝色
物质
白醋
蒸馏水
食盐
溶液
肥皂水
碳酸钠
溶液
加入紫甘
蓝汁液后
显示的颜色
红色
蓝紫色
蓝紫色
蓝色
绿色
B
8.(变式题)实验室里,常用浓硫酸作为干燥剂,
这是利用了浓硫酸的( )
A.吸水性 B.脱水性 C.酸性 D.氧化性
9.浓盐酸和浓硫酸对比,下列叙述正确的是( )
A.两者均具有挥发性
B.两者均具有刺激性气味
C.两者均具有腐蚀性
D.两者均是黏稠状液体
A
C
10.某同学在化学晚会上使用毛笔蘸取一种无色液体在一张白纸上书写“化学魔术”四个字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四个字。该同学所用的两种无色液体可能是( )
A.NaOH溶液、酚酞溶液
B.白醋、酚酞溶液
C.石蕊溶液、酚酞溶液
D.“雪碧”饮料、酚酞溶液
A
11.下图是浓盐酸试剂瓶上标签的部分内容。请回答:
(1)该浓盐酸的溶质是 (填化学式)。
(2)现要配制3%的稀盐酸120 g,需要这种浓盐酸___g。
(3)使用一段时间后,浓盐酸的溶质的质量分数小于36%,
原因是________________。
HCl
10
浓盐酸具有挥发性
12.如图所示是两种稀释浓硫酸的操作,回答下列问题:
(1)B图中加水仪器的名称是____________。
(2)B图锥形瓶内产生的现象是__________________________。
产生这一现象的原因是_________________________________。
(3)上边两幅图中,稀释浓硫酸的操作正确的是 (填序号)。
分液漏斗
液体沸腾,产生大量蒸气
浓硫酸溶于水放出大量的热
A
13.某些植物的花汁可作为酸碱指示剂。
取三种花汁用酒精溶液、稀酸溶液、稀碱溶液检验,颜色如下:
花种类
花汁在酒精
(中性)中的颜色
花汁在稀
酸中的颜色
花汁在稀
碱中的颜色
玫瑰花
粉红
粉红
绿
万寿菊花
黄
黄
黄
大红花
粉红
橙
绿
试回答下列问题:
(1)为检验生活中的食盐水、肥皂水、汽水、石灰水四种物质的酸碱性,
可选择________花汁,不选用其他花汁的原因
是_____________________________________________。
大红花
其他两种在酸、碱、中性溶液中有显示相同的颜色
(2)取所选花汁少许分别滴入上述四种物质中,请将所显颜色填入下表中。
检验物质
食盐水
肥皂水
汽水
石灰水
所显颜色
____
____
___
____
粉红
绿
橙
绿
1.柠檬汁能使紫色石蕊溶液变红色,由此可知柠檬汁( )
A.显碱性 B.显酸性 C.显中性 D.无法确定
B
2.小红学习了酸碱指示剂与常见的酸、碱溶液作用后,归纳总结出如图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,其中颜色不正确的是( )
A.紫色 B.蓝色
C.红色 D.无色
A
3.(2019·平舆县期中)下列物质中,不能用金属跟稀酸反应直接制得的是( )
A.硫酸锌(ZnSO4) B.氯化镁(MgCl2)
C.氯化铁(FeCl3) D.硫酸亚铁(FeSO4)
4.有A、B两种金属,放入等质量分数的稀硫酸中,生成氢气的质量与反应时间的关系如图所示。下列结论合理的是( )
A.金属活动性:A>B
B.生成氢气的质量:A>B
C.反应的硫酸质量:A<B
D.反应的金属质量:A<B
C
B
5.泉州是白蚂蚁灾害的高发地区,白蚂蚁会蛀蚀木头,它分泌的蚁酸是一种酸,能腐蚀很多建筑材料。下列建筑材料最不容易被白蚂蚁腐蚀的是( )
A.钢筋 B.铜制品 C.大理石 D.铝合金
B
6.物质X可发生“X+酸―→化合物+H2O”的反应,则X可能是( )
A.Fe B.CO2 C.H2SO4 D.CuO
7.(2019·驻马店一模)取一定量氧化铁与氧化铜的混合物,向其中加入100 g 14.6%的稀盐酸,恰好完全反应,则混合物中氧元素的质量为____g;
写出氧化铁与稀盐酸反应的化学方程式:__________________________。
D
3.2
Fe2O3+6HCl===2FeCl3+3H2O
8.酸溶液具有相似化学性质的原因是( )
A.酸溶液里都含有水分子
B.酸溶液里都含有氢离子
C.酸溶液里都含有氢元素
D.酸溶液里都含有酸根离子
B
9.小王同学往厨房的纯碱中滴加白醋,发现有气体生成。
已知白醋里含3%~5%的醋酸(CH3COOH),
醋酸与盐酸的化学性质相似,
下列说法不正确的是( )
A.白醋里含有氢离子
B.生成的气体是二氧化碳
C白醋能使紫色石蕊溶液变红
D.白醋与纯碱的反应属于化合反应
D
10.下列物质的变化中,只有加酸才能一步实现的是( )
A.CaCO3―→CO2 B.Zn―→ZnSO4
C.CuO―→CuCl2 D.Fe―→FeCl2
11.(2019·荆州)将某稀硫酸分成两等份,分别向其中加入锌粉或铁粉,
反应结束后剩余的铁比剩余的锌多,产生氢气的质量分别为a g和b g,
则a和b的关系是( )
A.a<b B.a=b
C.a>b D.无法判断
C
B
12.(2019·自贡)氧化铜与稀盐酸发生反应时,容器中溶液总质量随
时间的变化曲线如图所示。下列说法错误的是( )
A.该实验是将稀盐酸逐渐加入到盛有氧化铜的容器中
B.m点表示氧化铜与稀盐酸恰好完全反应
C.m点和n点对应溶液中铜元素的质量不相等
D.m点和n点对应溶液蒸发结晶后得到的固体成分相同
C
13.将稀盐酸分别滴入盛有不同物质的试管中,如图所示。
(1)不能发生反应的是 (填字母,下同)。
(2)有气泡产生的是_______。
(3)有浅绿色溶液生成的是___。
(4)有蓝色溶液生成的是___。
(5)溶液变成红色的是___。
A
B、C
B
D
E
14.利用以下装置对酸的化学性质进行探究。
(1)实验Ⅰ中,在点滴板的a、b孔穴中滴入酸溶液后,
溶液变红的是 (填“a”或“b”)。
使用点滴板的优点之一是_______________。
a
节约药品
15.(2019·平舆县期中)某研究性学习小组的同学做了如下的实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球悬浮于液面,位置如图所示。将从废电池外壳收集来的锌片放入烧杯中,该学生看到的现象
是________________________________,当杯中的盐酸完全反应后,
此时小球所处位置与原来相比 (填“不变”“上浮”或“下沉”)。
其依据是___________________________________________________,
,
,
______________________________________________________,
反应的化学方程式为_______________________。
产生气泡,锌片逐渐溶解,小球移动
上浮
因为锌与盐酸反应生成了氯化锌,溶质的相对分子质量增大
使得溶液的密度增大,漂浮满足的条件为重力等于浮力
由于重力不变
则浮力不变,则应该是排开液体的体积减小,因此应该上浮
Zn+2HCl===ZnCl2+H2↑
同课章节目录
