人教版九年级下册化学课件:8.2金属的化学性质第一课时课件(24张PPT)
文档属性
| 名称 | 人教版九年级下册化学课件:8.2金属的化学性质第一课时课件(24张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-24 00:00:00 | ||
图片预览








文档简介
友情提示:
黄铜(铜锌合金)与黄金的外观极为相似,很难区分,社会上有些不法分子时常以黄铜冒充黄金进行诈骗活动,我们可以用什么方法去拆穿他们的骗局呢?如果你家里的铝壶表面不再光亮,一般不能用钢刷或者清洁球去擦洗它们,这又是为什么呢?
Fe
Al
Mg
Au
第一课时
1.知道镁、铝、铁、铜、金等常见金属与氧气的反应;
2.初步认识常见金属与盐酸、硫酸的置换反应。
3.能用金属活动顺序对有关的置换反应进行简单地判断。
学习目标
3Fe +2O2 Fe3O4
点燃
2Mg + O2 2MgO
点燃
知识再现
我们曾经学过有关金属的哪些反应?
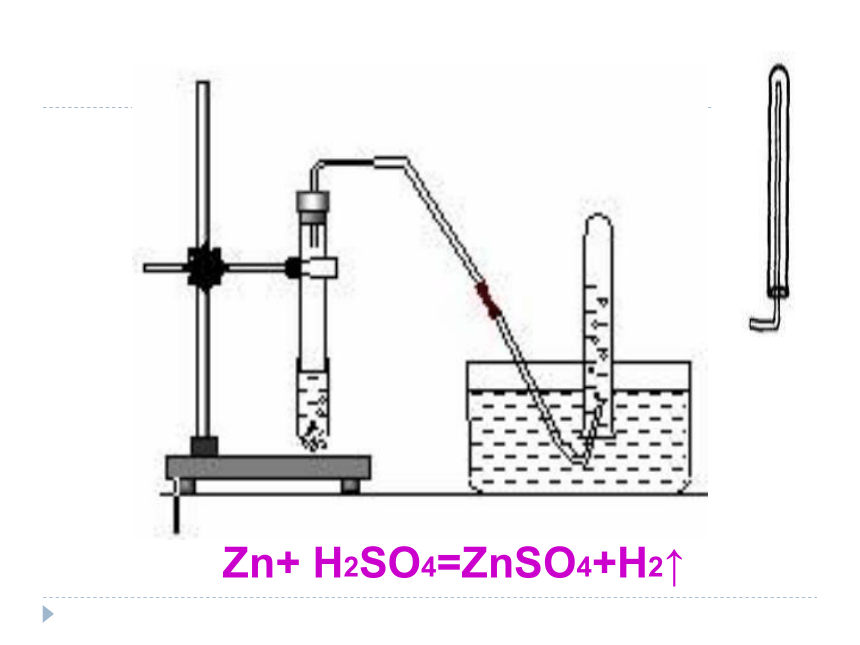
Zn+ H2SO4=ZnSO4+H2↑
镁条和铝片在常温下就能和空气中的氧气发生反应。
铜和铁只在加热或高温时才能与氧气反应
金即使在高温时也不和氧气反应
根据反应条件和反应的剧烈程度,比较一下谁的化学性质更活泼?
化学性质一:能和氧气反应
2Mg+O2===2MgO
2Cu+O2===2CuO
3Fe+2 O2 ===Fe3 O4
点燃
点燃
加热
4Al+3O2===2Al2O3
(白色)
(黑色)
(黑色)
(白色)
判断金属的活动性的方法之一:比较和氧气反应的难易程度和剧烈程度。
镁铝活泼,铁铜较活泼,金很不活泼
归纳总结
1.大多数金属都能与_______反应,
反应剧烈程度 ________(相同,不相同)
氧气
不相同
2.金属的活动性:
说明 _______ 较活泼,________次之,
______很不活泼
Mg、 Al、
Fe、Cu
Au
金属活动性: Mg、Al >Fe、Cu>Au
铝的化学性质活泼,为什么我们通常没有见到铝被锈蚀?
金属铝在常温下发生缓慢氧化:4Al+3O2=2Al2O3; 在铝的表面形成一层致密的氧化铝薄膜,从而保护铝不被腐蚀。
为何不宜用钢刷来擦洗铝制餐具呢?
若用钢刷擦洗铝制品,容易把氧化铝薄膜除掉,从而失去了保护作用。
提出问题:
金属与酸反应现象是否也像金属与氧气反应一样存在差别呢?
我们可以从金属与酸:
来推断金属的活泼程度(活动性)
①能否反应;
②反应的激烈程度;
A组
B组
金属与稀盐酸(HCl)的反应
金属与稀H2SO4的反应
在4支试管里分别放入两小块铜、铁、锌、镁,再依次加入约占试管容积1/4的稀盐酸(或稀硫酸),仔细观察金属表面与溶液的变化,比较反应的剧烈程度。选择反应比较快的用燃着的小木条放在试管口,检验产生的气体。请记录实验现象。
金属与盐酸或稀硫酸的反应
友情提醒:
实验操作要规范,取用稀盐酸或稀硫酸千万要小心哦!
(A组:金属与稀盐酸反应)
金属
现 象
反应的化学方程式
铜
铁
锌
镁
缓慢反应,有气泡产生,溶液由无色变为浅绿色
没有明显变化
很快反应,产生大量的气泡,放出热量.
迅速剧烈反应,产生大量的气泡,放出热量.
Fe+2HCl FeCl2+H2↑
+2
氯化亚铁
Mg+2HCl MgCl2+H2↑
Zn+2HCl ZnCl2+H2 ↑
(B组:金属与硫酸反应)
金属
现 象
反应的化学方程式
铜
铁
锌
镁
没有明显变化
Fe+ H2SO4 FeSO4+ H2↑
+2
硫酸亚铁
Zn+ H2SO4 ZnSO4+ H2↑
Mg+ H2SO4 MgSO4+ H2↑
缓慢反应,有气泡产生,溶液由无色变为浅绿色
很快反应,产生大量的气泡,放出热量.
迅速剧烈反应,产生大量的气泡,放出热量.
盐酸
God Save me!!
无所谓, 慢慢减减肥……
为什么受伤的总是我!晕!
呵呵,挺舒服,我不怕…
谁强谁弱你看清楚了吗?
1、能与盐酸,稀硫酸反应的金属是
它们反应的剧烈程度依次是 > > .
2、不能与盐酸,稀硫酸反应的金属是
3、镁、锌、铁、铜四种金属的活动性顺序
是 > > > .
4、将镁、锌、铁、铜四种金属分为两类:
活泼金属 : .
不活泼金属: .
分类的依据是: .
讨论
Mg Zn Fe
Mg Zn Fe
Cu
Mg Zn Fe Cu
Mg Zn Fe
Cu
它们是否与盐酸、硫酸反应
Mg + 2HCl MgCl2 + H2↑
Zn + 2HCl ZnCl2 + H2↑
Fe + 2HCl FeCl2 + H2↑
思考:从反应物和生成物的物质类别的角度分析,这些反应有什么特点?这一类反应与化合反应,分解反应有何区别。
单质
化合物
化合物
单质
置换反应:
这种由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。 (基本反应类型)
A+BC=__+__
AC
B
以上两个反应属于置换反应吗?为什么?
CO+CuO == Cu+CO2
△
CH4+2O2==CO2+2H2O
点燃
×
×
*
属于化合反应的有:
属于分解反应物有:
属于置换反应的有:
① H2+CuO==Cu+H2O
② S+O2==SO2
③ H2CO3==H2O+CO2↑
④ CO+CuO==Cu+CO2
⑤ Zn+H2SO4==ZnSO4+H2↑
⑥ 3C+2Fe2O3==4Fe+3CO2↑
△
△
点燃
高温
下列反应
②
③
①⑤⑥
金属活动性由强到弱
Zn Fe Sn Pb
(H)
Cu Hg Ag Pt Au
1、在金属活动性顺序里,金属的位置越靠前,它的活动性就越强
2、 在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
K Ca Na Mg Al
怎么读?
第一句
第二句
第三句
怎么用?
用自己的话说一说,你对这两种用法的理解
金属活动性顺序
*
判断下列金属能否与酸反应生成氢气
①Zn+HCl ——
②Mg+H2SO4——
③Cu+HCl——
④Fe+ H2SO4——
⑤Ag+ H2SO4——
课堂小结:
一. 金属与氧气的反应
4Al+3O2=2Al2O3
2Mg+O2=2MgO
3Fe+2 O2 点燃 Fe3 O4
二.金属与稀盐酸、稀硫酸反应
Fe + 2HCl = FeCl2 + H2 ↑
Fe + H2 SO4 = Fe SO4 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Zn + H2 SO4 = Zn SO4 + H2 ↑
Mg + 2HCl = MgCl2 + H2 ↑
Mg + H2 SO4 = Mg SO4 + H2 ↑
三.置换反应:由单质和化合物反应,生成单质和化合物 的反应。
四.金属活动性顺序:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性,由强逐渐减弱。
比较金属活动性强弱的方法(一)
比较金属活动性强弱的方法(二)
1.小兰家中收藏一件清末的铝制佛像,至今仍保存十分完好。该佛像未锈蚀的主要原因是( )
A.铝不易发生化学反应
B.铝的氧化物容易发生化学反应
C.铝不易被氧化
D.铝易被氧化,但氧化铝具有保护内部铝的作用。
2、下列金属中,常温下就易和氧气反应的是( )
A.铝 B.铂 C.铁 D.铜
3、下列有关金属的说法正确的是
A、铝在空气中能生成一层致密的氧化物保护膜
B、铜的化学性质不活泼,在潮湿的空气中也不会生锈
C、铁生锈是铁与氧气作用的结果
D、铝的抗腐蚀性能比铁好,说明铝没有铁活泼
4、“真金不怕火炼”是说明了
A、真金在高温下不融化 B、真金不用火炼
C、真金遇火不变色 D、金的化学性质不活泼,在高温下不与氧气反应
课堂练习
1.下列关于金属的说法正确的是( )
A.各种金属在常温下都不能与氧气反应
B.各种金属在高温下都能与氧气反应
C.根据金属与氧气反应的难易程度可以初步比较 金属的活动性
D.各种金属都能与盐酸发生置换反应
2、将生铁投入足量的稀盐酸中,充分反应后过滤,滤纸上的物质主要是( )
A、盐酸 B、铁 C、碳 D、氯化亚铁
3、某金属放在稀硫酸中,不产生气泡,该金属可能是
A、Cu B、Zn C、Al D、Mg
课堂检测
4、为适应火车提速,我国一些铁路线上原有的短轨已全部连接为超长轨。工程技术人员常用如下反应来焊接钢轨间的缝隙:2Al + Fe2O3 Al2O3 + 2Fe。有关此反应的下列说法中正确的是( )
A.该反应属于化合反应
B.该反应属于分解反应
C.该反应属于置换反应
D.该反应中铁元素的化合价升高
5、鉴别下列物质,要求写出实验操作、现象和结论。
(1)铁和铜
(2)真金和“假金”(铜锌合金)
市场上很多不法分子利用黄铜(铜、锌合金)来冒充黄金牟取暴利。请你设计实验,鉴别区分戒指是黄金还是黄铜。
黄铜戒指
黄金戒指
性质
黄铜
黄金
设计实验
硬度
密度
化学性质一
化学性质二
其中的Cu在加热时能和氧气反应生成黑色的氧化铜
大
小
大
其中的Zn能和稀盐酸或稀硫酸反应生成氢气
小
不和酸反应
高温下也不和氧气反应
将戒指与黄铜相互刻画,软的是黄金
测戒指的密度,然后与纯金的密度比较。
用火烧烤片刻,变黑的是黄铜,不变色的是黄金。
将戒指投入到稀盐酸或稀硫酸中观察,表面有气泡冒出的是黄铜,不反应的是黄金。
鉴别区分物质,就要熟悉物质的性质!
黄铜(铜锌合金)与黄金的外观极为相似,很难区分,社会上有些不法分子时常以黄铜冒充黄金进行诈骗活动,我们可以用什么方法去拆穿他们的骗局呢?如果你家里的铝壶表面不再光亮,一般不能用钢刷或者清洁球去擦洗它们,这又是为什么呢?
Fe
Al
Mg
Au
第一课时
1.知道镁、铝、铁、铜、金等常见金属与氧气的反应;
2.初步认识常见金属与盐酸、硫酸的置换反应。
3.能用金属活动顺序对有关的置换反应进行简单地判断。
学习目标
3Fe +2O2 Fe3O4
点燃
2Mg + O2 2MgO
点燃
知识再现
我们曾经学过有关金属的哪些反应?
Zn+ H2SO4=ZnSO4+H2↑
镁条和铝片在常温下就能和空气中的氧气发生反应。
铜和铁只在加热或高温时才能与氧气反应
金即使在高温时也不和氧气反应
根据反应条件和反应的剧烈程度,比较一下谁的化学性质更活泼?
化学性质一:能和氧气反应
2Mg+O2===2MgO
2Cu+O2===2CuO
3Fe+2 O2 ===Fe3 O4
点燃
点燃
加热
4Al+3O2===2Al2O3
(白色)
(黑色)
(黑色)
(白色)
判断金属的活动性的方法之一:比较和氧气反应的难易程度和剧烈程度。
镁铝活泼,铁铜较活泼,金很不活泼
归纳总结
1.大多数金属都能与_______反应,
反应剧烈程度 ________(相同,不相同)
氧气
不相同
2.金属的活动性:
说明 _______ 较活泼,________次之,
______很不活泼
Mg、 Al、
Fe、Cu
Au
金属活动性: Mg、Al >Fe、Cu>Au
铝的化学性质活泼,为什么我们通常没有见到铝被锈蚀?
金属铝在常温下发生缓慢氧化:4Al+3O2=2Al2O3; 在铝的表面形成一层致密的氧化铝薄膜,从而保护铝不被腐蚀。
为何不宜用钢刷来擦洗铝制餐具呢?
若用钢刷擦洗铝制品,容易把氧化铝薄膜除掉,从而失去了保护作用。
提出问题:
金属与酸反应现象是否也像金属与氧气反应一样存在差别呢?
我们可以从金属与酸:
来推断金属的活泼程度(活动性)
①能否反应;
②反应的激烈程度;
A组
B组
金属与稀盐酸(HCl)的反应
金属与稀H2SO4的反应
在4支试管里分别放入两小块铜、铁、锌、镁,再依次加入约占试管容积1/4的稀盐酸(或稀硫酸),仔细观察金属表面与溶液的变化,比较反应的剧烈程度。选择反应比较快的用燃着的小木条放在试管口,检验产生的气体。请记录实验现象。
金属与盐酸或稀硫酸的反应
友情提醒:
实验操作要规范,取用稀盐酸或稀硫酸千万要小心哦!
(A组:金属与稀盐酸反应)
金属
现 象
反应的化学方程式
铜
铁
锌
镁
缓慢反应,有气泡产生,溶液由无色变为浅绿色
没有明显变化
很快反应,产生大量的气泡,放出热量.
迅速剧烈反应,产生大量的气泡,放出热量.
Fe+2HCl FeCl2+H2↑
+2
氯化亚铁
Mg+2HCl MgCl2+H2↑
Zn+2HCl ZnCl2+H2 ↑
(B组:金属与硫酸反应)
金属
现 象
反应的化学方程式
铜
铁
锌
镁
没有明显变化
Fe+ H2SO4 FeSO4+ H2↑
+2
硫酸亚铁
Zn+ H2SO4 ZnSO4+ H2↑
Mg+ H2SO4 MgSO4+ H2↑
缓慢反应,有气泡产生,溶液由无色变为浅绿色
很快反应,产生大量的气泡,放出热量.
迅速剧烈反应,产生大量的气泡,放出热量.
盐酸
God Save me!!
无所谓, 慢慢减减肥……
为什么受伤的总是我!晕!
呵呵,挺舒服,我不怕…
谁强谁弱你看清楚了吗?
1、能与盐酸,稀硫酸反应的金属是
它们反应的剧烈程度依次是 > > .
2、不能与盐酸,稀硫酸反应的金属是
3、镁、锌、铁、铜四种金属的活动性顺序
是 > > > .
4、将镁、锌、铁、铜四种金属分为两类:
活泼金属 : .
不活泼金属: .
分类的依据是: .
讨论
Mg Zn Fe
Mg Zn Fe
Cu
Mg Zn Fe Cu
Mg Zn Fe
Cu
它们是否与盐酸、硫酸反应
Mg + 2HCl MgCl2 + H2↑
Zn + 2HCl ZnCl2 + H2↑
Fe + 2HCl FeCl2 + H2↑
思考:从反应物和生成物的物质类别的角度分析,这些反应有什么特点?这一类反应与化合反应,分解反应有何区别。
单质
化合物
化合物
单质
置换反应:
这种由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。 (基本反应类型)
A+BC=__+__
AC
B
以上两个反应属于置换反应吗?为什么?
CO+CuO == Cu+CO2
△
CH4+2O2==CO2+2H2O
点燃
×
×
*
属于化合反应的有:
属于分解反应物有:
属于置换反应的有:
① H2+CuO==Cu+H2O
② S+O2==SO2
③ H2CO3==H2O+CO2↑
④ CO+CuO==Cu+CO2
⑤ Zn+H2SO4==ZnSO4+H2↑
⑥ 3C+2Fe2O3==4Fe+3CO2↑
△
△
点燃
高温
下列反应
②
③
①⑤⑥
金属活动性由强到弱
Zn Fe Sn Pb
(H)
Cu Hg Ag Pt Au
1、在金属活动性顺序里,金属的位置越靠前,它的活动性就越强
2、 在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。
K Ca Na Mg Al
怎么读?
第一句
第二句
第三句
怎么用?
用自己的话说一说,你对这两种用法的理解
金属活动性顺序
*
判断下列金属能否与酸反应生成氢气
①Zn+HCl ——
②Mg+H2SO4——
③Cu+HCl——
④Fe+ H2SO4——
⑤Ag+ H2SO4——
课堂小结:
一. 金属与氧气的反应
4Al+3O2=2Al2O3
2Mg+O2=2MgO
3Fe+2 O2 点燃 Fe3 O4
二.金属与稀盐酸、稀硫酸反应
Fe + 2HCl = FeCl2 + H2 ↑
Fe + H2 SO4 = Fe SO4 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Zn + H2 SO4 = Zn SO4 + H2 ↑
Mg + 2HCl = MgCl2 + H2 ↑
Mg + H2 SO4 = Mg SO4 + H2 ↑
三.置换反应:由单质和化合物反应,生成单质和化合物 的反应。
四.金属活动性顺序:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性,由强逐渐减弱。
比较金属活动性强弱的方法(一)
比较金属活动性强弱的方法(二)
1.小兰家中收藏一件清末的铝制佛像,至今仍保存十分完好。该佛像未锈蚀的主要原因是( )
A.铝不易发生化学反应
B.铝的氧化物容易发生化学反应
C.铝不易被氧化
D.铝易被氧化,但氧化铝具有保护内部铝的作用。
2、下列金属中,常温下就易和氧气反应的是( )
A.铝 B.铂 C.铁 D.铜
3、下列有关金属的说法正确的是
A、铝在空气中能生成一层致密的氧化物保护膜
B、铜的化学性质不活泼,在潮湿的空气中也不会生锈
C、铁生锈是铁与氧气作用的结果
D、铝的抗腐蚀性能比铁好,说明铝没有铁活泼
4、“真金不怕火炼”是说明了
A、真金在高温下不融化 B、真金不用火炼
C、真金遇火不变色 D、金的化学性质不活泼,在高温下不与氧气反应
课堂练习
1.下列关于金属的说法正确的是( )
A.各种金属在常温下都不能与氧气反应
B.各种金属在高温下都能与氧气反应
C.根据金属与氧气反应的难易程度可以初步比较 金属的活动性
D.各种金属都能与盐酸发生置换反应
2、将生铁投入足量的稀盐酸中,充分反应后过滤,滤纸上的物质主要是( )
A、盐酸 B、铁 C、碳 D、氯化亚铁
3、某金属放在稀硫酸中,不产生气泡,该金属可能是
A、Cu B、Zn C、Al D、Mg
课堂检测
4、为适应火车提速,我国一些铁路线上原有的短轨已全部连接为超长轨。工程技术人员常用如下反应来焊接钢轨间的缝隙:2Al + Fe2O3 Al2O3 + 2Fe。有关此反应的下列说法中正确的是( )
A.该反应属于化合反应
B.该反应属于分解反应
C.该反应属于置换反应
D.该反应中铁元素的化合价升高
5、鉴别下列物质,要求写出实验操作、现象和结论。
(1)铁和铜
(2)真金和“假金”(铜锌合金)
市场上很多不法分子利用黄铜(铜、锌合金)来冒充黄金牟取暴利。请你设计实验,鉴别区分戒指是黄金还是黄铜。
黄铜戒指
黄金戒指
性质
黄铜
黄金
设计实验
硬度
密度
化学性质一
化学性质二
其中的Cu在加热时能和氧气反应生成黑色的氧化铜
大
小
大
其中的Zn能和稀盐酸或稀硫酸反应生成氢气
小
不和酸反应
高温下也不和氧气反应
将戒指与黄铜相互刻画,软的是黄金
测戒指的密度,然后与纯金的密度比较。
用火烧烤片刻,变黑的是黄铜,不变色的是黄金。
将戒指投入到稀盐酸或稀硫酸中观察,表面有气泡冒出的是黄铜,不反应的是黄金。
鉴别区分物质,就要熟悉物质的性质!
同课章节目录
