人教版九年级化学下册 第九单元 溶液复习测试题(word版,含答案)
文档属性
| 名称 | 人教版九年级化学下册 第九单元 溶液复习测试题(word版,含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 343.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-24 10:30:13 | ||
图片预览

文档简介
第九单元复习测试题
(时间:70分钟
满分:100分)
可能用到的相对原子质量:H-1
C-12
O-16
Cl-35.5
Ca-40
一、单项选择题(本大题包括10小题,每小题2分,共20分,每小题只有一个选项符合题意)
1.名称中有“水”字的物质可能是溶液,下列有“水”字的物质属于溶液的是(
)
A.硬水
B.油水
C.泥水
D.蒸馏水
2.衣服、餐具上的油污可以用洗涤剂洗掉,因为洗涤剂(
)
A.可以软化水
B.具有乳化功能
C.可以沉降杂质
D.溶于水时放热
3.下列关于溶液的叙述正确的是(
)
A.溶液一定是无色、透明的液体
B.溶液中各部分性质不一定相同
C.在溶液中进行的化学反应其速率较快
D.溶液和浊液的不同取决于被分散物质的状态
4.一定温度下,向如图所示烧杯中加入一定量水,仅有部分晶体溶解。所得溶液与原溶液相比,说法正确的是(
)
A.溶剂的质量增加,溶液颜色变浅
B.溶质溶解度不变,溶液颜色变深
C.溶质的质量增加,溶液颜色变深
D.溶质溶解度不变,溶液颜色不变
5.下表为甲、乙、丙三种物质的溶解度,请结合表中信息判断下列说法正确的是( )
温度/℃
0
10
20
t
30
40
50
溶解度/g
甲
13.3
20.9
31.6
39.1
45.8
63.9
85.5
乙
29.4
33.3
37.2
39.1
41.1
45.8
50.4
丙
35.7
35.8
36.0
36.2
36.3
36.6
37.0
A.三种物质的溶解度大小为:甲>乙>丙
B.随着温度变化,甲的溶解度变化最小
C.30℃时,100g饱和丙溶液中,溶质质量为36.3g
D.分别将50℃时甲、乙的饱和溶液降温至t℃,两种溶液的浓度相等
6.某溶液的溶质质量分数为10%,下面有关的说法正确的是(
)
①在100份质量的溶液中含有10份质量的溶质
②在110份质量的溶液中含有10份质量的溶质
③在100份质量的溶剂中含有10份质量的溶质
④在90份质量的溶剂中溶有10份质量的溶质
A.①④
B.①②
C.③④
D.②③
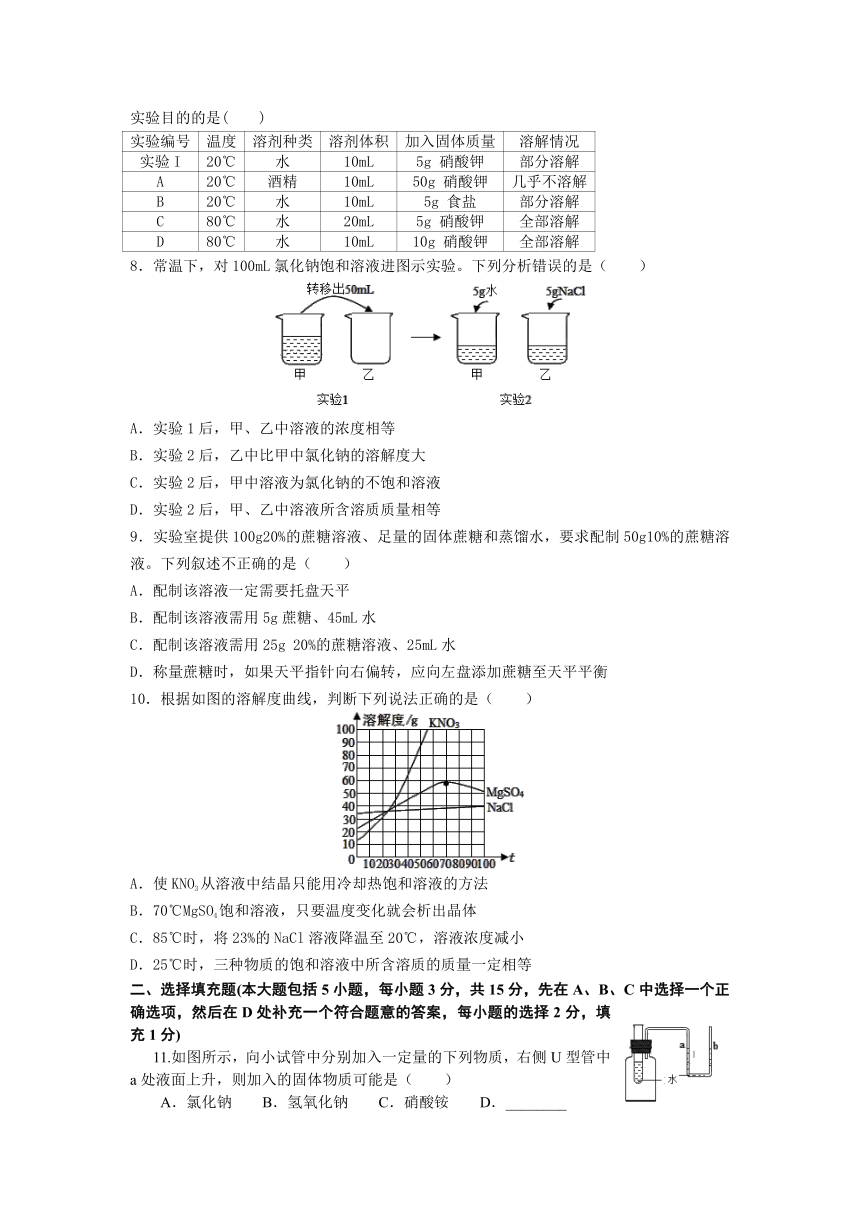
7.
为确定某一因素对物质溶解性的影响,A、B、C、D四个实验中能与实验I作为一组达到实验目的的是(
)
实验编号
温度
溶剂种类
溶剂体积
加入固体质量
溶解情况
实验I
20℃
水
10mL
5g
硝酸钾
部分溶解
A
20℃
酒精
10mL
50g
硝酸钾
几乎不溶解
B
20℃
水
10mL
5g
食盐
部分溶解
C
80℃
水
20mL
5g
硝酸钾
全部溶解
D
80℃
水
10mL
10g
硝酸钾
全部溶解
8.常温下,对100mL氯化钠饱和溶液进图示实验。下列分析错误的是( )
A.实验1后,甲、乙中溶液的浓度相等
B.实验2后,乙中比甲中氯化钠的溶解度大
C.实验2后,甲中溶液为氯化钠的不饱和溶液
D.实验2后,甲、乙中溶液所含溶质质量相等
9.实验室提供100g20%的蔗糖溶液、足量的固体蔗糖和蒸馏水,要求配制50g10%的蔗糖溶液。下列叙述不正确的是(
)
A.配制该溶液一定需要托盘天平
B.配制该溶液需用5g蔗糖、45mL水
C.配制该溶液需用25g
20%的蔗糖溶液、25mL水
D.称量蔗糖时,如果天平指针向右偏转,应向左盘添加蔗糖至天平平衡
10.根据如图的溶解度曲线,判断下列说法正确的是(
)
A.使KNO3从溶液中结晶只能用冷却热饱和溶液的方法
B.70℃MgSO4饱和溶液,只要温度变化就会析出晶体
C.85℃时,将23%的NaCl溶液降温至20℃,溶液浓度减小
D.25℃时,三种物质的饱和溶液中所含溶质的质量一定相等
二、选择填充题(本大题包括5小题,每小题3分,共15分,先在A、B、C中选择一个正确选项,然后在D处补充一个符合题意的答案,每小题的选择2分,填充1分)
11.如图所示,向小试管中分别加入一定量的下列物质,右侧U型管中a处液面上升,则加入的固体物质可能是( )
A.氯化钠
B.氢氧化钠
C.硝酸铵
D.________
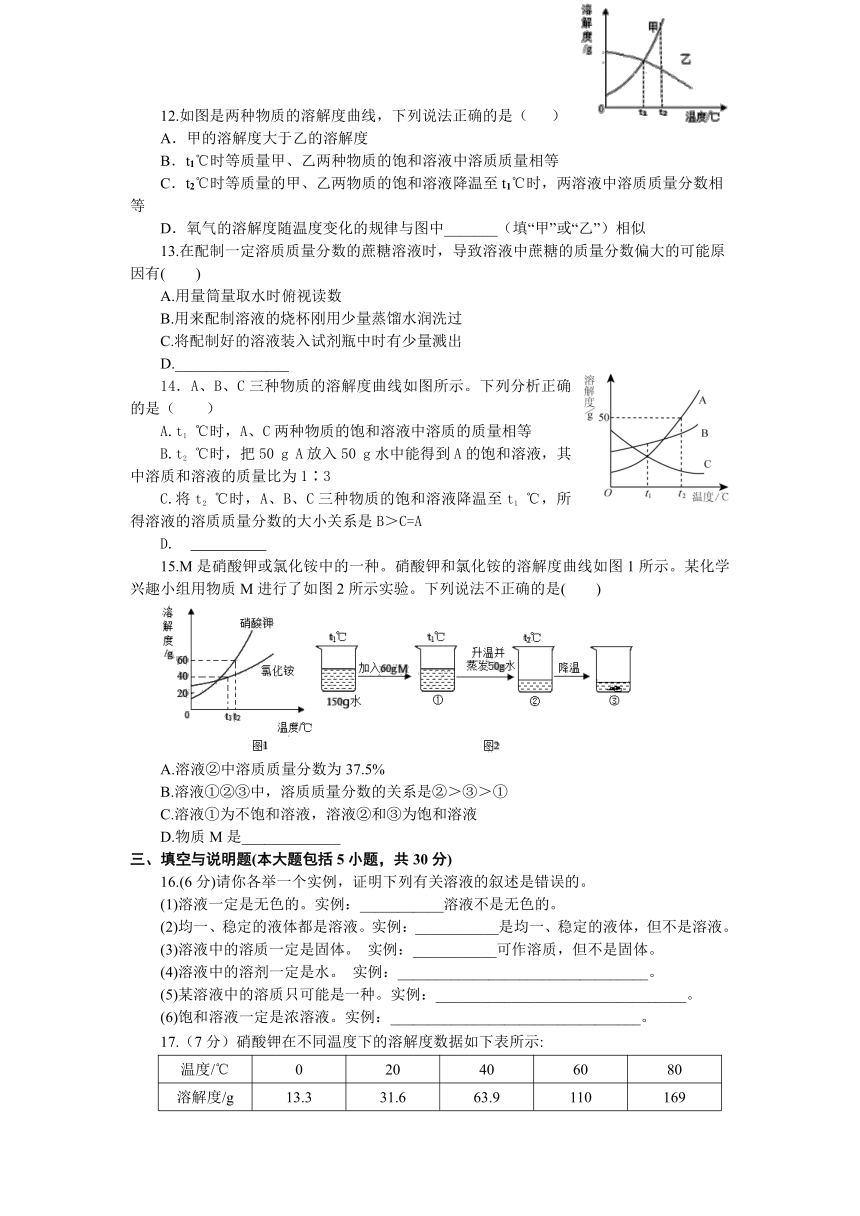
12.如图是两种物质的溶解度曲线,下列说法正确的是(
)
A.甲的溶解度大于乙的溶解度
B.t1℃时等质量甲、乙两种物质的饱和溶液中溶质质量相等
C.t2℃时等质量的甲、乙两物质的饱和溶液降温至t1℃时,两溶液中溶质质量分数相等
D.氧气的溶解度随温度变化的规律与图中_______(填“甲”或“乙”)相似
13.在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有(
)
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.将配制好的溶液装入试剂瓶中时有少量溅出
D._______________
14.A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是(
)
A.t1
℃时,A、C两种物质的饱和溶液中溶质的质量相等
B.t2
℃时,把50
g
A放入50
g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶3
C.将t2
℃时,A、B、C三种物质的饱和溶液降温至t1
℃,所得溶液的溶质质量分数的大小关系是B>C=A
D.
15.M是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组用物质M进行了如图2所示实验。下列说法不正确的是(
)
A.溶液②中溶质质量分数为37.5%
B.溶液①②③中,溶质质量分数的关系是②>③>①
C.溶液①为不饱和溶液,溶液②和③为饱和溶液
D.物质M是_____________
三、填空与说明题(本大题包括5小题,共30分)
16.(6分)请你各举一个实例,证明下列有关溶液的叙述是错误的。
(1)溶液一定是无色的。实例:___________溶液不是无色的。
(2)均一、稳定的液体都是溶液。实例:___________是均一、稳定的液体,但不是溶液。
(3)溶液中的溶质一定是固体。
实例:___________可作溶质,但不是固体。
(4)溶液中的溶剂一定是水。
实例:_________________________________。
(5)某溶液中的溶质只可能是一种。实例:_________________________________。
(6)饱和溶液一定是浓溶液。实例:_________________________________。
17.(7分)硝酸钾在不同温度下的溶解度数据如下表所示:
温度/℃
0
20
40
60
80
溶解度/g
13.3
31.6
63.9
110
169
回答下列问题:
(1)硝酸钾溶于水时吸收热量,使溶液的温度
。
(2)在60℃时,硝酸钾的溶解度是110g。这句话的含义是__________。
(3)0℃时,硝酸钾饱和溶液中溶质的质量分数是
(精确到0.1%);20℃时,将18g硝酸钾加入到50g水中,充分溶解后,所得溶液的质量是
g;80℃时,将269g硝酸钾饱和溶液降温到60℃,析出晶体的质量是
g。
(4)将40℃的硝酸钾饱和溶液变为不饱和溶液,可采取的措施是
或
。
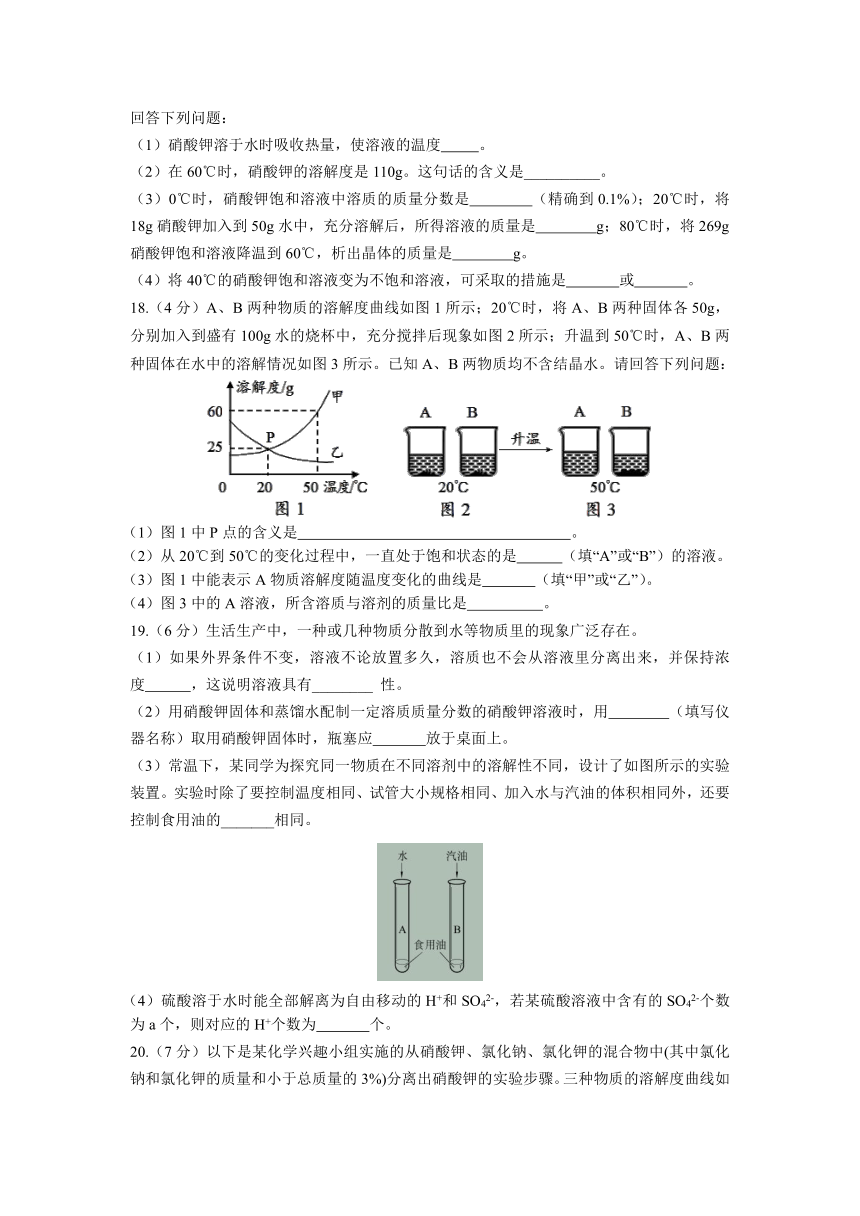
18.(4分)A、B两种物质的溶解度曲线如图1所示;20℃时,将A、B两种固体各50g,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图2所示;升温到50℃时,A、B两种固体在水中的溶解情况如图3所示。已知A、B两物质均不含结晶水。请回答下列问题:
(1)图1中P点的含义是
。
(2)从20℃到50℃的变化过程中,一直处于饱和状态的是
(填“A”或“B”)的溶液。
(3)图1中能表示A物质溶解度随温度变化的曲线是
(填“甲”或“乙”)。
(4)图3中的A溶液,所含溶质与溶剂的质量比是
。
19.(6分)生活生产中,一种或几种物质分散到水等物质里的现象广泛存在。
(1)如果外界条件不变,溶液不论放置多久,溶质也不会从溶液里分离出来,并保持浓度
,这说明溶液具有________
性。
(2)用硝酸钾固体和蒸馏水配制一定溶质质量分数的硝酸钾溶液时,用
(填写仪器名称)取用硝酸钾固体时,瓶塞应
放于桌面上。
(3)常温下,某同学为探究同一物质在不同溶剂中的溶解性不同,设计了如图所示的实验装置。实验时除了要控制温度相同、试管大小规格相同、加入水与汽油的体积相同外,还要控制食用油的_______相同。
(4)硫酸溶于水时能全部解离为自由移动的H+和SO42-,若某硫酸溶液中含有的SO42-个数为a个,则对应的H+个数为
个。
20.(7分)以下是某化学兴趣小组实施的从硝酸钾、氯化钠、氯化钾的混合物中(其中氯化钠和氯化钾的质量和小于总质量的3%)分离出硝酸钾的实验步骤。三种物质的溶解度曲线如图所示。
Ⅰ.用托盘天平称得样品的总质量为87.5g;
Ⅱ.配制成80℃左右的饱和溶液;
Ⅲ.将热饱和溶液冷却至室温(20℃)后进行过滤,并用少量水洗涤2~3次;
Ⅳ.取出过滤器中的固体,干燥后分装。
请回答以下问题:
(1)用天平称取87.5g样品时,游码位于_______g位置(1g以下用游码)。
(2)某同学发现,无论将称量物还是砝码放置于托盘中时,天平均不发生偏转,原因是_______。
A.天平未放置于水平桌面上
B.天平没有调零
C.托盘下的垫圈未取下
D.游码未归零
(3)将这些样品制成80℃左右的热饱和溶液,约需水_______
(填字母)。
A.12.5mL
B.50
mL
C.100
mL
D.112.5mL
(4)该实验中,玻璃棒除了用于搅拌和引流外,还用于_______。
(5)步骤Ⅲ中,只能用少量水洗涤固体的原因是_______;过滤并洗涤后,氯化钾存在于_______中。
(6)如果实验中热饱和溶液未完全冷却至室温就过滤,将会影响晶体产量,理由是_______。
四、实验与探究题(本大题包括3小题,共25分)
21.(10分)为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验。(提示:本实验所用汽油与KMnO4、碘均不发生化学反应)
【实验l】KMnO4晶体在不同溶剂中的溶解实验
根据实验步骤、实验操作图示填写相关实验现象.
实验步骤
实验操作图示
实验操作及现象
步骤1
振荡后静置:(1)A试管中晶体全部溶解,溶液呈_______色;B试管中晶体不溶解,汽油不变色。
步骤2
将步骤1中A试管内溶液倒人B试管中,振荡后静置:(2)B试管中观察到的现象为______________。
【实验2】碘在不同溶剂中的溶解实验
根据实验操作图示回答相关问题.
实验操作图示
实验结论或解释
(3)由图2所示现象可知:碘_______(选填“不”、“微”或“易”)溶于水(4)图3所示试管中液体分层。上层紫红色溶液的名称是_________,该溶液中的溶质是________,溶剂是________;说明碘在汽油中的溶解性比在水中_______(选填“强”或“弱”)。
【反思与应用】
(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体__________(选填“分层”或“小分层”)。
②“从稀碘水中提取碘”是“海带提碘”工艺中的一个重要步骤,其原理类似【实验2]中第二步操作。工业实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是____________________。
22.(8分)某实验小组进行物质溶解实验,20℃时,分别称取2.5g、5.0g、7.5gNaOH固体,分别加入3个小烧杯中(均盛有50mL水),均完全溶解。通过数字化实验仪器测得它们在溶解过程中溶液温度的变化情况如图所示。依据该实验,你能获得哪些有关NaOH在水中溶解的实验结论?请按示例,再回答出两点。
证据1:曲线均呈上升趋势;结论1:NaOH在水中溶解时放出热量。
证据2:
;
结论2:
。
证据3:
;
结论3:
。
23.(7分)实验室用氯化钠固体配制50g质量分数10%的氯化钠溶液,可供选择的部分仪器如图,请按要求回答:
(1)不需要的仪器是_______(填字母)。
(2)使用称量仪器的第一步是_______(写出操作过程);需要称取_______g氯化钠固体,将称好的氯化钠固体倒入仪器_______(填字母)中。
(3)量取所需水的体积时应选用_______mL(填“10”、“50”或“100”)的仪器_______(填字母)。
(4)通过溶解,将配制好的溶液装入仪器_______
(填字母)中,并贴上标签。
五、计算题(本大题包括1小题,共10分)
24.因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用钙片,某补钙药剂说明书的部分信息如图1所示。现将100g盐酸五等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与关系图如图2。请根据有关信息回答问题。
实验次数
第一次
第三次
第四次
加入盐酸的质量/g
20
20
20
剩余固体的质量/g
35
a
20
(1)该品牌补钙药剂中CaCO3的质量分数是
,a的数值为
。
(2)该盐酸中溶质的质量分数是多少?(写出计算过程,最后结果精确至0.1%)
参
考
答
案
1.A
2.B
3.C
4.D
5.D
6.A
7.D
8.B
9.D
10.C
11.C
冰(合理即可)
12.B
乙
13.A
向烧杯中倾倒量取的水时,有水洒出(合理即可)
14.B
将C的饱和溶液变为不饱和溶液,可采用降温的方法(合理即可)
15.B
氯化铵
16.(1)高锰酸钾
(2)水
(3)CO2
(4)碘酒中的溶剂是酒精
(5)汽水中有柠檬酸、蔗糖等溶质(合理答案均可)
(6)澄清的石灰水是饱和溶液,但却是稀溶液
17.(1)升高
(2)在60℃时,100g水里最多能溶解110g硝酸钾(3)11.7%
65.8
59(4)加水
升温
18.
(1)20℃时A、B两种物质溶解度相等(2)B
(3)甲(4)1:2
19.(1)不变
稳定
(2)药匙
倒
(3)体积(4)2a
20.(1)0.5(2)C
(3)B
(4)转移固体
(5)晶体易溶于水,洗涤用水越少,晶体损失越小
滤液(6)硝酸钾饱和溶液在较高温度下结晶时,析出的晶体较少
21.(1)紫(紫红、红)
(2)液体分层,上层为无色,下层为紫红色,试管底部无固体残留
(3)微
(4)碘的汽油溶液
碘
汽油
强
(5)①不分层
②与水不互溶,碘在这种液体中的溶解度远大于在水中的溶解度
22.证据2:2.5g氢氧化钠溶于水时,温度上升最小;7.5g氢氧化钠溶于水时,温度上升最大。结论2:相同条件下,溶解的氢氧化钠越多,放出的热量越多。
证据3:20℃时,7.5g氢氧化钠能完全溶解在50mL水中;结论3:氢氧化钠易溶于水
23.(1)C
(2)游码置零,调节天平平衡
5
F(3)50
A
(4)D
24.(1)50%
25(2)1.58%
(时间:70分钟
满分:100分)
可能用到的相对原子质量:H-1
C-12
O-16
Cl-35.5
Ca-40
一、单项选择题(本大题包括10小题,每小题2分,共20分,每小题只有一个选项符合题意)
1.名称中有“水”字的物质可能是溶液,下列有“水”字的物质属于溶液的是(
)
A.硬水
B.油水
C.泥水
D.蒸馏水
2.衣服、餐具上的油污可以用洗涤剂洗掉,因为洗涤剂(
)
A.可以软化水
B.具有乳化功能
C.可以沉降杂质
D.溶于水时放热
3.下列关于溶液的叙述正确的是(
)
A.溶液一定是无色、透明的液体
B.溶液中各部分性质不一定相同
C.在溶液中进行的化学反应其速率较快
D.溶液和浊液的不同取决于被分散物质的状态
4.一定温度下,向如图所示烧杯中加入一定量水,仅有部分晶体溶解。所得溶液与原溶液相比,说法正确的是(
)
A.溶剂的质量增加,溶液颜色变浅
B.溶质溶解度不变,溶液颜色变深
C.溶质的质量增加,溶液颜色变深
D.溶质溶解度不变,溶液颜色不变
5.下表为甲、乙、丙三种物质的溶解度,请结合表中信息判断下列说法正确的是( )
温度/℃
0
10
20
t
30
40
50
溶解度/g
甲
13.3
20.9
31.6
39.1
45.8
63.9
85.5
乙
29.4
33.3
37.2
39.1
41.1
45.8
50.4
丙
35.7
35.8
36.0
36.2
36.3
36.6
37.0
A.三种物质的溶解度大小为:甲>乙>丙
B.随着温度变化,甲的溶解度变化最小
C.30℃时,100g饱和丙溶液中,溶质质量为36.3g
D.分别将50℃时甲、乙的饱和溶液降温至t℃,两种溶液的浓度相等
6.某溶液的溶质质量分数为10%,下面有关的说法正确的是(
)
①在100份质量的溶液中含有10份质量的溶质
②在110份质量的溶液中含有10份质量的溶质
③在100份质量的溶剂中含有10份质量的溶质
④在90份质量的溶剂中溶有10份质量的溶质
A.①④
B.①②
C.③④
D.②③
7.
为确定某一因素对物质溶解性的影响,A、B、C、D四个实验中能与实验I作为一组达到实验目的的是(
)
实验编号
温度
溶剂种类
溶剂体积
加入固体质量
溶解情况
实验I
20℃
水
10mL
5g
硝酸钾
部分溶解
A
20℃
酒精
10mL
50g
硝酸钾
几乎不溶解
B
20℃
水
10mL
5g
食盐
部分溶解
C
80℃
水
20mL
5g
硝酸钾
全部溶解
D
80℃
水
10mL
10g
硝酸钾
全部溶解
8.常温下,对100mL氯化钠饱和溶液进图示实验。下列分析错误的是( )
A.实验1后,甲、乙中溶液的浓度相等
B.实验2后,乙中比甲中氯化钠的溶解度大
C.实验2后,甲中溶液为氯化钠的不饱和溶液
D.实验2后,甲、乙中溶液所含溶质质量相等
9.实验室提供100g20%的蔗糖溶液、足量的固体蔗糖和蒸馏水,要求配制50g10%的蔗糖溶液。下列叙述不正确的是(
)
A.配制该溶液一定需要托盘天平
B.配制该溶液需用5g蔗糖、45mL水
C.配制该溶液需用25g
20%的蔗糖溶液、25mL水
D.称量蔗糖时,如果天平指针向右偏转,应向左盘添加蔗糖至天平平衡
10.根据如图的溶解度曲线,判断下列说法正确的是(
)
A.使KNO3从溶液中结晶只能用冷却热饱和溶液的方法
B.70℃MgSO4饱和溶液,只要温度变化就会析出晶体
C.85℃时,将23%的NaCl溶液降温至20℃,溶液浓度减小
D.25℃时,三种物质的饱和溶液中所含溶质的质量一定相等
二、选择填充题(本大题包括5小题,每小题3分,共15分,先在A、B、C中选择一个正确选项,然后在D处补充一个符合题意的答案,每小题的选择2分,填充1分)
11.如图所示,向小试管中分别加入一定量的下列物质,右侧U型管中a处液面上升,则加入的固体物质可能是( )
A.氯化钠
B.氢氧化钠
C.硝酸铵
D.________
12.如图是两种物质的溶解度曲线,下列说法正确的是(
)
A.甲的溶解度大于乙的溶解度
B.t1℃时等质量甲、乙两种物质的饱和溶液中溶质质量相等
C.t2℃时等质量的甲、乙两物质的饱和溶液降温至t1℃时,两溶液中溶质质量分数相等
D.氧气的溶解度随温度变化的规律与图中_______(填“甲”或“乙”)相似
13.在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有(
)
A.用量筒量取水时俯视读数
B.用来配制溶液的烧杯刚用少量蒸馏水润洗过
C.将配制好的溶液装入试剂瓶中时有少量溅出
D._______________
14.A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是(
)
A.t1
℃时,A、C两种物质的饱和溶液中溶质的质量相等
B.t2
℃时,把50
g
A放入50
g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1∶3
C.将t2
℃时,A、B、C三种物质的饱和溶液降温至t1
℃,所得溶液的溶质质量分数的大小关系是B>C=A
D.
15.M是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组用物质M进行了如图2所示实验。下列说法不正确的是(
)
A.溶液②中溶质质量分数为37.5%
B.溶液①②③中,溶质质量分数的关系是②>③>①
C.溶液①为不饱和溶液,溶液②和③为饱和溶液
D.物质M是_____________
三、填空与说明题(本大题包括5小题,共30分)
16.(6分)请你各举一个实例,证明下列有关溶液的叙述是错误的。
(1)溶液一定是无色的。实例:___________溶液不是无色的。
(2)均一、稳定的液体都是溶液。实例:___________是均一、稳定的液体,但不是溶液。
(3)溶液中的溶质一定是固体。
实例:___________可作溶质,但不是固体。
(4)溶液中的溶剂一定是水。
实例:_________________________________。
(5)某溶液中的溶质只可能是一种。实例:_________________________________。
(6)饱和溶液一定是浓溶液。实例:_________________________________。
17.(7分)硝酸钾在不同温度下的溶解度数据如下表所示:
温度/℃
0
20
40
60
80
溶解度/g
13.3
31.6
63.9
110
169
回答下列问题:
(1)硝酸钾溶于水时吸收热量,使溶液的温度
。
(2)在60℃时,硝酸钾的溶解度是110g。这句话的含义是__________。
(3)0℃时,硝酸钾饱和溶液中溶质的质量分数是
(精确到0.1%);20℃时,将18g硝酸钾加入到50g水中,充分溶解后,所得溶液的质量是
g;80℃时,将269g硝酸钾饱和溶液降温到60℃,析出晶体的质量是
g。
(4)将40℃的硝酸钾饱和溶液变为不饱和溶液,可采取的措施是
或
。
18.(4分)A、B两种物质的溶解度曲线如图1所示;20℃时,将A、B两种固体各50g,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图2所示;升温到50℃时,A、B两种固体在水中的溶解情况如图3所示。已知A、B两物质均不含结晶水。请回答下列问题:
(1)图1中P点的含义是
。
(2)从20℃到50℃的变化过程中,一直处于饱和状态的是
(填“A”或“B”)的溶液。
(3)图1中能表示A物质溶解度随温度变化的曲线是
(填“甲”或“乙”)。
(4)图3中的A溶液,所含溶质与溶剂的质量比是
。
19.(6分)生活生产中,一种或几种物质分散到水等物质里的现象广泛存在。
(1)如果外界条件不变,溶液不论放置多久,溶质也不会从溶液里分离出来,并保持浓度
,这说明溶液具有________
性。
(2)用硝酸钾固体和蒸馏水配制一定溶质质量分数的硝酸钾溶液时,用
(填写仪器名称)取用硝酸钾固体时,瓶塞应
放于桌面上。
(3)常温下,某同学为探究同一物质在不同溶剂中的溶解性不同,设计了如图所示的实验装置。实验时除了要控制温度相同、试管大小规格相同、加入水与汽油的体积相同外,还要控制食用油的_______相同。
(4)硫酸溶于水时能全部解离为自由移动的H+和SO42-,若某硫酸溶液中含有的SO42-个数为a个,则对应的H+个数为
个。
20.(7分)以下是某化学兴趣小组实施的从硝酸钾、氯化钠、氯化钾的混合物中(其中氯化钠和氯化钾的质量和小于总质量的3%)分离出硝酸钾的实验步骤。三种物质的溶解度曲线如图所示。
Ⅰ.用托盘天平称得样品的总质量为87.5g;
Ⅱ.配制成80℃左右的饱和溶液;
Ⅲ.将热饱和溶液冷却至室温(20℃)后进行过滤,并用少量水洗涤2~3次;
Ⅳ.取出过滤器中的固体,干燥后分装。
请回答以下问题:
(1)用天平称取87.5g样品时,游码位于_______g位置(1g以下用游码)。
(2)某同学发现,无论将称量物还是砝码放置于托盘中时,天平均不发生偏转,原因是_______。
A.天平未放置于水平桌面上
B.天平没有调零
C.托盘下的垫圈未取下
D.游码未归零
(3)将这些样品制成80℃左右的热饱和溶液,约需水_______
(填字母)。
A.12.5mL
B.50
mL
C.100
mL
D.112.5mL
(4)该实验中,玻璃棒除了用于搅拌和引流外,还用于_______。
(5)步骤Ⅲ中,只能用少量水洗涤固体的原因是_______;过滤并洗涤后,氯化钾存在于_______中。
(6)如果实验中热饱和溶液未完全冷却至室温就过滤,将会影响晶体产量,理由是_______。
四、实验与探究题(本大题包括3小题,共25分)
21.(10分)为了探究相同条件下同种溶质在不同溶剂中的溶解性,某兴趣小组同学进行如下两组实验。(提示:本实验所用汽油与KMnO4、碘均不发生化学反应)
【实验l】KMnO4晶体在不同溶剂中的溶解实验
根据实验步骤、实验操作图示填写相关实验现象.
实验步骤
实验操作图示
实验操作及现象
步骤1
振荡后静置:(1)A试管中晶体全部溶解,溶液呈_______色;B试管中晶体不溶解,汽油不变色。
步骤2
将步骤1中A试管内溶液倒人B试管中,振荡后静置:(2)B试管中观察到的现象为______________。
【实验2】碘在不同溶剂中的溶解实验
根据实验操作图示回答相关问题.
实验操作图示
实验结论或解释
(3)由图2所示现象可知:碘_______(选填“不”、“微”或“易”)溶于水(4)图3所示试管中液体分层。上层紫红色溶液的名称是_________,该溶液中的溶质是________,溶剂是________;说明碘在汽油中的溶解性比在水中_______(选填“强”或“弱”)。
【反思与应用】
(5)①碘易溶于酒精。若【实验2】中汽油用酒精代替,振荡后静置,最终所得液体__________(选填“分层”或“小分层”)。
②“从稀碘水中提取碘”是“海带提碘”工艺中的一个重要步骤,其原理类似【实验2]中第二步操作。工业实际生产时使用其他挥发性液体代替汽油,这种挥发性液体必须具备的条件是____________________。
22.(8分)某实验小组进行物质溶解实验,20℃时,分别称取2.5g、5.0g、7.5gNaOH固体,分别加入3个小烧杯中(均盛有50mL水),均完全溶解。通过数字化实验仪器测得它们在溶解过程中溶液温度的变化情况如图所示。依据该实验,你能获得哪些有关NaOH在水中溶解的实验结论?请按示例,再回答出两点。
证据1:曲线均呈上升趋势;结论1:NaOH在水中溶解时放出热量。
证据2:
;
结论2:
。
证据3:
;
结论3:
。
23.(7分)实验室用氯化钠固体配制50g质量分数10%的氯化钠溶液,可供选择的部分仪器如图,请按要求回答:
(1)不需要的仪器是_______(填字母)。
(2)使用称量仪器的第一步是_______(写出操作过程);需要称取_______g氯化钠固体,将称好的氯化钠固体倒入仪器_______(填字母)中。
(3)量取所需水的体积时应选用_______mL(填“10”、“50”或“100”)的仪器_______(填字母)。
(4)通过溶解,将配制好的溶液装入仪器_______
(填字母)中,并贴上标签。
五、计算题(本大题包括1小题,共10分)
24.因缺钙而导致骨质疏松、佝偻病等的患者应在医生的指导下服用钙片,某补钙药剂说明书的部分信息如图1所示。现将100g盐酸五等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与关系图如图2。请根据有关信息回答问题。
实验次数
第一次
第三次
第四次
加入盐酸的质量/g
20
20
20
剩余固体的质量/g
35
a
20
(1)该品牌补钙药剂中CaCO3的质量分数是
,a的数值为
。
(2)该盐酸中溶质的质量分数是多少?(写出计算过程,最后结果精确至0.1%)
参
考
答
案
1.A
2.B
3.C
4.D
5.D
6.A
7.D
8.B
9.D
10.C
11.C
冰(合理即可)
12.B
乙
13.A
向烧杯中倾倒量取的水时,有水洒出(合理即可)
14.B
将C的饱和溶液变为不饱和溶液,可采用降温的方法(合理即可)
15.B
氯化铵
16.(1)高锰酸钾
(2)水
(3)CO2
(4)碘酒中的溶剂是酒精
(5)汽水中有柠檬酸、蔗糖等溶质(合理答案均可)
(6)澄清的石灰水是饱和溶液,但却是稀溶液
17.(1)升高
(2)在60℃时,100g水里最多能溶解110g硝酸钾(3)11.7%
65.8
59(4)加水
升温
18.
(1)20℃时A、B两种物质溶解度相等(2)B
(3)甲(4)1:2
19.(1)不变
稳定
(2)药匙
倒
(3)体积(4)2a
20.(1)0.5(2)C
(3)B
(4)转移固体
(5)晶体易溶于水,洗涤用水越少,晶体损失越小
滤液(6)硝酸钾饱和溶液在较高温度下结晶时,析出的晶体较少
21.(1)紫(紫红、红)
(2)液体分层,上层为无色,下层为紫红色,试管底部无固体残留
(3)微
(4)碘的汽油溶液
碘
汽油
强
(5)①不分层
②与水不互溶,碘在这种液体中的溶解度远大于在水中的溶解度
22.证据2:2.5g氢氧化钠溶于水时,温度上升最小;7.5g氢氧化钠溶于水时,温度上升最大。结论2:相同条件下,溶解的氢氧化钠越多,放出的热量越多。
证据3:20℃时,7.5g氢氧化钠能完全溶解在50mL水中;结论3:氢氧化钠易溶于水
23.(1)C
(2)游码置零,调节天平平衡
5
F(3)50
A
(4)D
24.(1)50%
25(2)1.58%
同课章节目录
