2.4 化学反应的调控 课件(13张ppt)
文档属性
| 名称 | 2.4 化学反应的调控 课件(13张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2020-12-25 00:00:00 | ||
图片预览





文档简介
化学反应的调控
【学习目标】
1. 了解如何应用化学反应速率和化学平衡原理分析合
成氨的适宜条件;
2. 了解应用化学反应原理分析化工生产条件的思路和
方法,体验实际生产条件的选择与理论分析的差异;
3. 认识化学反应速率和化学平衡的调控在工业生产中
的重要作用。
工业合成氨是人类科学技术的一项重大突破,其反应
如下:
?
在实际工业生产过程中如何选择反应的条件?
【温故知新】
影响化学反应速率和平衡移动的因素有哪些?
速率
平衡移动
温度
压强
浓度
催化剂
温度
压强
浓度
一、合成氨的适宜条件选择
增大
升高
增大
降低
增大
增大
使用
无影响
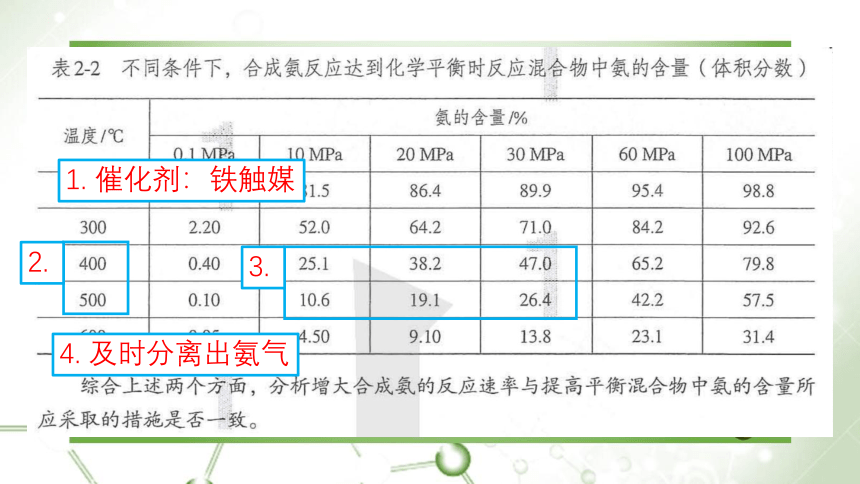
【思考与讨论】---P44
1. 催化剂:铁触媒
2.
3.
4. 及时分离出氨气
【思考1】合成氨时压强越大越好,为何不采用比30MPa更大的压强?
【思考2】合成氨采用低温时可提高转化率,但为何未采用更低的温度?
【思考3】合成氨工业采用迅速冷却法,使气态氨变成液态氨后及时从混合物中分离出去的目的是什么?
【小结】
提高温度
增大压强
增大浓度
催化剂
加快合成
氨的速率
增大压强
分离氨气
利于氨
的合成
二、实际化工生产适宜条件的选择
1. 分析反应的特点
2. 综合考虑影响化学反应速率和化学平衡的因素,同
时结合化工生产的动力、材料、设备、催化剂活性等
因素实行生产。
【拓展探究】
1.根据化学理论和以上的数据综合分析,为了使SO2尽可能转化为SO3,可控制的条件是什么?
2.在实际生产中,选定400~500℃作为参考温度,其原因是什么?
3.根据上表中的数据分析,制取SO3时为什么不采用高压?
4.在生产中,通入过量的空气的目的是什么?
5.尾气中的必须回收的目的是什么?
【问题思考】
考虑环境保护和社会利益
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}外界
条件
有利于增大反应速率的条件控制
有利于平衡正向移动的条件控制
综合分析结果
浓度
增大反应物的浓度
增大反应物的浓度,减小生成物的浓度
不断地补充反应物、及时分离出生成物
催化剂
加合适的催化剂
不需要
加合适的催化剂
温度
高温
△H< 0
低温
兼顾速率和平衡,考虑催化剂的适宜温度
△H> 0
高温
在设备条件允许的前提下,尽量采用高温并考虑催化剂的活性
压强
高压(有气体参加)
△V< 0
高压
在设备允许条件下,尽量采取高压
△V> 0
低压
兼顾速率和平衡,选取适宜的压强
【总结】工业生产中选择适宜生产条件的原则
谢谢大家
【学习目标】
1. 了解如何应用化学反应速率和化学平衡原理分析合
成氨的适宜条件;
2. 了解应用化学反应原理分析化工生产条件的思路和
方法,体验实际生产条件的选择与理论分析的差异;
3. 认识化学反应速率和化学平衡的调控在工业生产中
的重要作用。
工业合成氨是人类科学技术的一项重大突破,其反应
如下:
?
在实际工业生产过程中如何选择反应的条件?
【温故知新】
影响化学反应速率和平衡移动的因素有哪些?
速率
平衡移动
温度
压强
浓度
催化剂
温度
压强
浓度
一、合成氨的适宜条件选择
增大
升高
增大
降低
增大
增大
使用
无影响
【思考与讨论】---P44
1. 催化剂:铁触媒
2.
3.
4. 及时分离出氨气
【思考1】合成氨时压强越大越好,为何不采用比30MPa更大的压强?
【思考2】合成氨采用低温时可提高转化率,但为何未采用更低的温度?
【思考3】合成氨工业采用迅速冷却法,使气态氨变成液态氨后及时从混合物中分离出去的目的是什么?
【小结】
提高温度
增大压强
增大浓度
催化剂
加快合成
氨的速率
增大压强
分离氨气
利于氨
的合成
二、实际化工生产适宜条件的选择
1. 分析反应的特点
2. 综合考虑影响化学反应速率和化学平衡的因素,同
时结合化工生产的动力、材料、设备、催化剂活性等
因素实行生产。
【拓展探究】
1.根据化学理论和以上的数据综合分析,为了使SO2尽可能转化为SO3,可控制的条件是什么?
2.在实际生产中,选定400~500℃作为参考温度,其原因是什么?
3.根据上表中的数据分析,制取SO3时为什么不采用高压?
4.在生产中,通入过量的空气的目的是什么?
5.尾气中的必须回收的目的是什么?
【问题思考】
考虑环境保护和社会利益
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}外界
条件
有利于增大反应速率的条件控制
有利于平衡正向移动的条件控制
综合分析结果
浓度
增大反应物的浓度
增大反应物的浓度,减小生成物的浓度
不断地补充反应物、及时分离出生成物
催化剂
加合适的催化剂
不需要
加合适的催化剂
温度
高温
△H< 0
低温
兼顾速率和平衡,考虑催化剂的适宜温度
△H> 0
高温
在设备条件允许的前提下,尽量采用高温并考虑催化剂的活性
压强
高压(有气体参加)
△V< 0
高压
在设备允许条件下,尽量采取高压
△V> 0
低压
兼顾速率和平衡,选取适宜的压强
【总结】工业生产中选择适宜生产条件的原则
谢谢大家
