氯气的性质(一)
图片预览






文档简介
(共18张PPT)
氯气的性质(一)
专题2第一单元氯、溴、碘及其化合物
舍勒 【瑞典】 1742一1786
18世纪,人们致力于采矿事业, 瑞典化学家舍勒 也把精力放在了软锰矿(主要成分是MnO2)的研究上。
1774年的一天当他把软锰矿粉末和浓盐酸混合加热时,惊奇的看到一种黄绿色的气体冒出。这种气体立即引起了舍勒的兴趣,并对它进行了研究。这种呛人的气体不但能使染料褪色,还有许多奇特的性质。
到了1807年,英国化学家戴维对这种气体进行了细致的研究,并于1810年11月在英国皇家学会上正式定名确认上述黄绿色气体是由一种新元素组成,英文定名为“Chlorine”,希腊文的意思是“绿色的”。
启示:
要用发现的眼光看待事物,要有执着的热情对待学习
自来水用氯气消毒
游泳池
漂白粉
漂粉精
含氯制品
一.物理性质:
色:
态:
味:
溶:
熔:
密:
毒性:
黄绿色
气体
有刺激性气味
比空气大(ρ1/ ρ2 =M1 / M2)
1:2溶解于水中
有毒
易液化
氯气
液氯
固态氯
101KPa,-34.6℃
101KPa,-101℃
相比较其他气体较高
思考:
用什么方法和物质来挖掘氯气的化学性质?
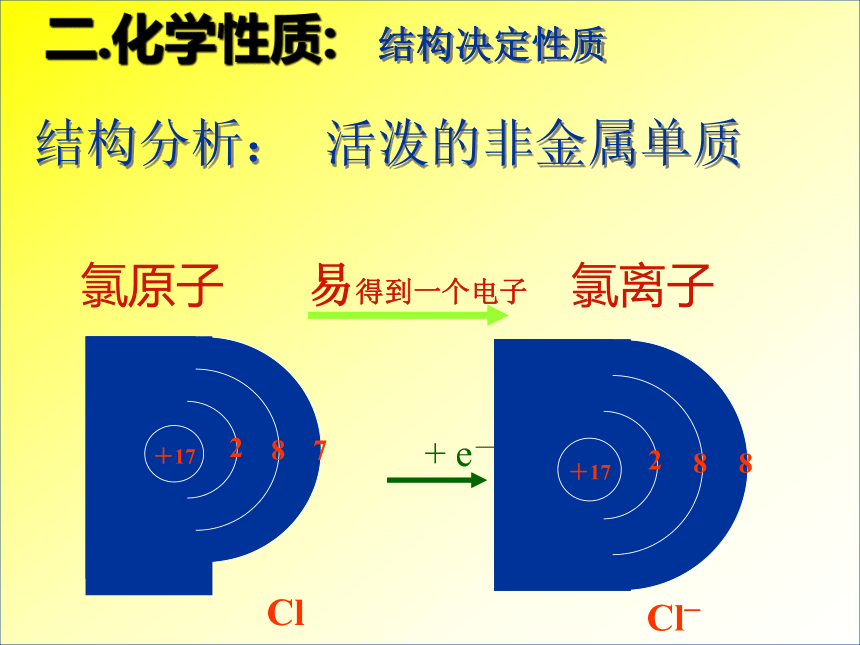
氯原子 易得到一个电子 氯离子
结构分析:
活泼的非金属单质
+17
2
8
8
Cl
Cl_
+ e-
+17
2
8
7
二.化学性质:
结构决定性质
①钠与氯气的反应
1.与金属单质反应
现象:剧烈燃烧,黄色火焰,生成大量白烟。
2Na+Cl2 2NaCl
二.化学性质:
②铁与氯气的反应
2Fe + 3Cl2 2FeCl3
点燃
+3
现象:剧烈燃烧,棕褐色的烟
二.化学性质:
信息提示 :
1.已知氧化性强的物质和金属能发生反应
2. 铁离子的化合价有+3和+2,氧化性强的
物质和其反应生成高价化合物,弱的物质生成低价化合物
2.比较氯气与盐酸的氧化性
1.氯气的氧化性强吗?它与变价金属反应的时候产物是低价还是高价?
③ 铜与氯气的反应
现象:剧烈燃烧,生成棕黄色的烟。
Cu+Cl2 CuCl2
点燃
氯化铜溶解在水里,成为蓝绿色的氯化铜溶液。
2. 氯气与非金属单质的反应
现象:安静的燃烧,火焰呈苍白色,瓶口有白雾产生
现象:释放大量的热,发生爆炸。
氢气在氯气中燃烧
氢气与氯气混合光照
H2+Cl2 2HCl
点燃或
光照
①与H2反应
思考:H2与Cl2 在点燃和光照的条件下都能反应生成HCl,那么工业制盐酸采用什么条件?(点燃还是光照?)
现象:产生了大量白色烟雾
2P + 3Cl2 2 PCl3
2P + 5Cl2 2 PCl5
(固体)
(液体)
点燃
点燃
拓展了解:
Cl2不足,产物为液态,现象:白雾
Cl2足量,产物为固态,现象:白烟
②磷在氯气中燃烧
课堂小结:氯气的性质:
2、氯气与铁反应
1、氯气与钠反应
3、氯气与铜反应
4、氯气与氢气反应
燃烧
光照
5、氯气与磷反应
物理性质
化学性质:
1.下列各组物质反应时,生成白烟的是( )
A.氢气在氯气中燃烧 B.钠在氯气中燃烧
C.铜丝在氯气中燃烧 D.铁丝在氯气中燃烧
B
2.下列氯化物中,不能用金属和氯气直接反应制的是( )
A.CuCl2 B.FeCl2 C.NaCl D.AlCl3
B
3、氯气有毒,第一次世界大战中第一次把氯气用于战场,毒气弹爆炸后,氯气随风飘散。在战场上能有效防御氯气的方法是 ( )
A、人畜躲到地势低洼处
B、人畜躲到地势较高处
C、人畜多饮豆浆和牛奶
D、可用肥皂水或尿液湿软布蒙面
B D
谢谢大家!
再见
氯气的性质(一)
专题2第一单元氯、溴、碘及其化合物
舍勒 【瑞典】 1742一1786
18世纪,人们致力于采矿事业, 瑞典化学家舍勒 也把精力放在了软锰矿(主要成分是MnO2)的研究上。
1774年的一天当他把软锰矿粉末和浓盐酸混合加热时,惊奇的看到一种黄绿色的气体冒出。这种气体立即引起了舍勒的兴趣,并对它进行了研究。这种呛人的气体不但能使染料褪色,还有许多奇特的性质。
到了1807年,英国化学家戴维对这种气体进行了细致的研究,并于1810年11月在英国皇家学会上正式定名确认上述黄绿色气体是由一种新元素组成,英文定名为“Chlorine”,希腊文的意思是“绿色的”。
启示:
要用发现的眼光看待事物,要有执着的热情对待学习
自来水用氯气消毒
游泳池
漂白粉
漂粉精
含氯制品
一.物理性质:
色:
态:
味:
溶:
熔:
密:
毒性:
黄绿色
气体
有刺激性气味
比空气大(ρ1/ ρ2 =M1 / M2)
1:2溶解于水中
有毒
易液化
氯气
液氯
固态氯
101KPa,-34.6℃
101KPa,-101℃
相比较其他气体较高
思考:
用什么方法和物质来挖掘氯气的化学性质?
氯原子 易得到一个电子 氯离子
结构分析:
活泼的非金属单质
+17
2
8
8
Cl
Cl_
+ e-
+17
2
8
7
二.化学性质:
结构决定性质
①钠与氯气的反应
1.与金属单质反应
现象:剧烈燃烧,黄色火焰,生成大量白烟。
2Na+Cl2 2NaCl
二.化学性质:
②铁与氯气的反应
2Fe + 3Cl2 2FeCl3
点燃
+3
现象:剧烈燃烧,棕褐色的烟
二.化学性质:
信息提示 :
1.已知氧化性强的物质和金属能发生反应
2. 铁离子的化合价有+3和+2,氧化性强的
物质和其反应生成高价化合物,弱的物质生成低价化合物
2.比较氯气与盐酸的氧化性
1.氯气的氧化性强吗?它与变价金属反应的时候产物是低价还是高价?
③ 铜与氯气的反应
现象:剧烈燃烧,生成棕黄色的烟。
Cu+Cl2 CuCl2
点燃
氯化铜溶解在水里,成为蓝绿色的氯化铜溶液。
2. 氯气与非金属单质的反应
现象:安静的燃烧,火焰呈苍白色,瓶口有白雾产生
现象:释放大量的热,发生爆炸。
氢气在氯气中燃烧
氢气与氯气混合光照
H2+Cl2 2HCl
点燃或
光照
①与H2反应
思考:H2与Cl2 在点燃和光照的条件下都能反应生成HCl,那么工业制盐酸采用什么条件?(点燃还是光照?)
现象:产生了大量白色烟雾
2P + 3Cl2 2 PCl3
2P + 5Cl2 2 PCl5
(固体)
(液体)
点燃
点燃
拓展了解:
Cl2不足,产物为液态,现象:白雾
Cl2足量,产物为固态,现象:白烟
②磷在氯气中燃烧
课堂小结:氯气的性质:
2、氯气与铁反应
1、氯气与钠反应
3、氯气与铜反应
4、氯气与氢气反应
燃烧
光照
5、氯气与磷反应
物理性质
化学性质:
1.下列各组物质反应时,生成白烟的是( )
A.氢气在氯气中燃烧 B.钠在氯气中燃烧
C.铜丝在氯气中燃烧 D.铁丝在氯气中燃烧
B
2.下列氯化物中,不能用金属和氯气直接反应制的是( )
A.CuCl2 B.FeCl2 C.NaCl D.AlCl3
B
3、氯气有毒,第一次世界大战中第一次把氯气用于战场,毒气弹爆炸后,氯气随风飘散。在战场上能有效防御氯气的方法是 ( )
A、人畜躲到地势低洼处
B、人畜躲到地势较高处
C、人畜多饮豆浆和牛奶
D、可用肥皂水或尿液湿软布蒙面
B D
谢谢大家!
再见
