2012高三备考精品资源系列:沉淀溶解平衡
文档属性
| 名称 | 2012高三备考精品资源系列:沉淀溶解平衡 |

|
|
| 格式 | zip | ||
| 文件大小 | 96.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-11-19 00:00:00 | ||
图片预览



文档简介
沉淀溶解平衡2012备考
1. 已知25℃时,电离常数Ka(HF)=3.6×10-4mol/L,溶度积常数Ksp(CaF2)=1.46×10-10mol3/L3。现向1L 0.2mol/LHF溶液中加入1L 0.2mol/LCaCl2溶液,则下列说法中,正确的是
A.25℃时,0.1 mol/LHF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中,Ksp(CaF2)=
D.该体系中有CaF2沉淀产生
2. 已知Ksp(AgCl )=1.8×10-10,Ksp(AgI)=1.0×10-16。下列关于不溶物之间转化的说法中错误的是
A.AgCl不溶于水,不能转化为AgI
B.两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物
C.AgI比AgCl更难溶于水,所以,AgCl可以转化为AgI
D.常温下AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于 EQ \F(1,) ×10-11 mol·L-1
3. 在已知AgCl和Ag2CrO4 的溶度积分别为1.8×10-10mol-2和2.0×10-12mol3·L-3。若用难溶盐在溶液中的浓度来表示其溶解度,则下列叙述正确的是
A.AgCl和Ag2CrO4 的溶解度相等
B.AgCl的溶解度大于Ag2CrO4
C.两者类型不同,不能直接由Ksp的大小来判断其溶解能力的大小
D.都是难溶盐,溶解度无意义
4. 当固体AgCl放在较浓的KI溶液中振荡时,部分AgCl转化为AgI,其原因是.
A.AgI比AgCl稳定 B.氯的非金属性比碘强
C.I-的还原性比Cl-强 D.AgI的溶解度比AgCl小
5. 25℃时,现向1L 0.2mol·L-1HF溶液中加入1L 0.2mol·L-1CaCl2溶液,则下列说法中,正确的是
A.25℃时,0.1mol·L-1HF 溶液中pH=1 B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中没有沉淀产生 D.该体系中HF与CaCl2反应产生沉淀
6. 在2mL物质的量浓度相等的NaCl和NaI溶液中滴入几滴AgNO3溶液,发生的反应为.
A.只有AgCl沉淀生成
B.只有AgI沉淀生成
C.生成等物质的量的AgCl和AgI沉淀
D.两种沉淀都有,但以AgI为主
7. 已知25℃时,AgI饱和溶液中c (Ag+)为1.22×10—8mol/L,AgCl的饱和溶液中c (Ag+)为1.25×10—5mol/L。若在5mL含有KCl和KI各为0.01mol/L的溶液中,加入8mL0.01mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
A.c (K+)>c (NO3—) >c (Cl—) >c (Ag+)>c (I—)
B.c (K+)>c (NO3—) >c (Ag+) >c (Cl—)>c (I—)
C.c (NO3—)>c (K+)>c (Ag+) >c (Cl—)>c (I—)
D.c (K+)>c (NO3—) >c (Ag+) = c (Cl—) + c (I—)
8. 常温下,AgCl、AgBr、AgI的溶度积常数(Ksp)依次为1.8×10-10mol2·L-2、5.0×10-13mol2·L-2、8.3×10-17mol2·L-2。下列有关说法错误的是
A.常温下在水中溶解能力AgCl>AgBr>AgI
B.在AgCl饱和液中加入足量浓NaBr溶液有AgBr沉淀生成
C.在AgBr饱和溶液中加入足量浓NaCl溶液不可能有AgCl沉淀生成
D.在AgI饱和液中加入NaI固体有AgI沉淀析出
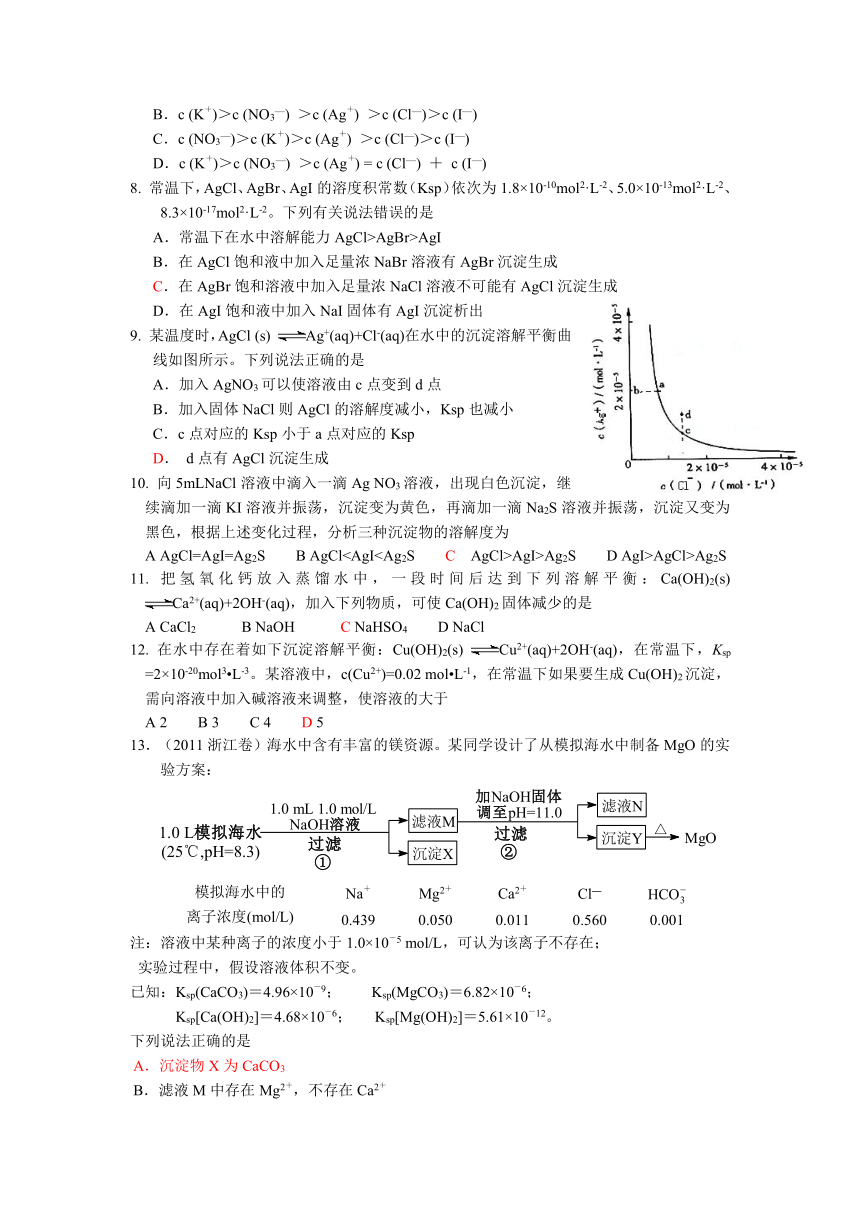
9. 某温度时,AgCl (s) Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.加入AgNO3可以使溶液由c点变到d点
B.加入固体NaCl则AgCl的溶解度减小,Ksp也减小
C.c点对应的Ksp小于a点对应的Ksp
D. d点有AgCl沉淀生成
10. 向5mLNaCl溶液中滴入一滴Ag NO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴加一滴Na2S溶液并振荡,沉淀又变为黑色,根据上述变化过程,分析三种沉淀物的溶解度为
A AgCl=AgI=Ag2S B AgClAgI>Ag2S D AgI>AgCl>Ag2S
11. 把氢氧化钙放入蒸馏水中,一段时间后达到下列溶解平衡:Ca(OH)2(s) Ca2+(aq)+2OH-(aq),加入下列物质,可使Ca(OH)2固体减少的是
A CaCl2 B NaOH C NaHSO4 D NaCl
12. 在水中存在着如下沉淀溶解平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),在常温下,Ksp =2×10-20mol3 L-3。某溶液中,c(Cu2+)=0.02 mol L-1,在常温下如果要生成Cu(OH)2沉淀,需向溶液中加入碱溶液来调整,使溶液的大于
A 2 B 3 C 4 D 5
13.(2011浙江卷)海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
模拟海水中的离子浓度(mol/L) Na+ Mg2+ Ca2+ Cl―
0.439 0.050 0.011 0.560 0.001
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9; Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6; Ksp[Mg(OH)2]=5.61×10-12。
下列说法正确的是
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
14.(2008·山东)某温度时,BaSO4在水中的沉淀溶解平衡曲线如下图所示。下列说法正确的是
提示:BaSO4(s) Ba2+(aq)+SO42 -(aq)的平衡常数:Ksp = c(Ba2+)·c(SO42 -),称为溶度积常数。
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
15.(2009福建)在一定条件下,Na2CO3溶液存在水解平衡:CO32 -+H2OHCO3- +OH-。下列说法正确的是
A.稀释溶液,水解平衡常数增大 B.通入CO2,平衡朝正反应方向移动
C.升高温度,减小 D.加入NaOH固体,溶液pH减小
16.(2009·广东卷,18,4分)硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下。下列说法正确的是
A.温度一定时,Ksp(SrSO4)随c(SO42 -)的增大而减小
B.三个不同温度中,313 K时Ksp(SrSO4)最大
C.283 K时,图中a点对应的溶液是不饱和溶液
D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
17.(2009·理综 )已知:25 ℃时,Ksp[Mg(OH)2] = 5.61×10-12,Ksp[MgF2] = 7.42×10-11。下列说法正确的是
A.25 ℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.25 ℃时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大
C.25 ℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小
D.25 ℃时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2
18.已知:25°C时, Ksp(Mg(OH)2)=5.61×10-12, Ksp(MgF2)=7.42×10-11。下列说法正确的是
A.25°C时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的C(Mg2+)大
B.25°C时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,C(Mg2+)增大
C.25°C时,Mg(OH)2固体在20ml0.01 mol·L-1氨水中的Ksp比在20mL0.01 mol·L-1 NH4Cl 溶液中的Ksp小
D.25°C时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2
19. 在1 mol L-1 CuSO4溶液中含有少量的Fe3+杂质,pH值控制在 范围才能除去Fe3+,使[Fe3+]≤10-5 mol L-1。已知:Fe(OH)3的Ksp = 2.6×10-39mol4 L-4,Cu(OH)2的Ksp = 5.6×10-20mol3 L-3
20. 已知在室温时,Mg(OH)2的溶度积Ksp=5.6×10-12 (mol/L)3,求室温下Mg(OH)2饱和溶液中Mg 2+和OH-的物质的量浓度
21. 一定温度下,难溶电解质在饱和溶液中各离子浓度幂的乘积是一个常数,这个常数称为该难溶电解质的溶度积,用符号Ksp表示。
即:AmBn(s) mAn+(aq)+nBm-(aq) [An+]m·[Bm-]n=Ksp
已知:某温度时,Ksp(AgCl)=[Ag+][Cl-] =1.8×10-10
Ksp(Ag2CrO4)=[Ag+]2[CrO2- 4] =1.1×10-12
试求:
(1)此温度下AgCl饱和溶液和Ag2CrO4饱和溶液的物质的量浓度,并比较两者的大小。
(2)此温度下,在0.010mo1·L-1的AgNO3溶液中,AgCl与Ag2CrO4分别能达到的最大物质的量浓度,并比较两者的大小。
22.(1)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃的恒温,致使混合溶液
的pH=7,则Ba(OH)2和盐酸的体积比为__________________。
(2)已知AnBm的离子积为[c(Am+)]n[c(Bn-)]m,若某温度下Ca(OH)2的溶解度为0.74g,设饱和溶液的密度为1g/mL,其离子积约为______________。
23. (2011新课标卷)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色请氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________________mol·L-1(Kap[Cu(OH)2]=2.2×10-20)。
若在0.1mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是_______________mol·L-1。
24.(2011天津卷)工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生
很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
其中第①步存在平衡:
(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr2O72-和CrO42-的浓度相同
b.2v (Cr2O72-) =v (CrO42-)
c.溶液的颜色不变
(3)第②步中,还原1mol Cr2O72-离子,需要 mol的FeSO·7HO。
(4)第③步生成的Cr(OH)在溶液中存在以下沉淀溶解平衡:
Cr(OH) (s)Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)的溶度积Kap= 10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
25.(2008江苏)工业上制备BaCl2的工艺流程图如下:
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s)4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s)2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(3)反应C(s) + CO2(g)2CO(g)的△H2= kJ·mol-1。
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是 , 。
26.运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂 反应的ΔH(填“增大”“减小”或“不改变”)。
(2)O2 (g)= O+2(g)+e- H1= 1175.7 kJ·mol-1
PtF6(g)+ e-1 PtF6-(g) H2= - 771.1 kJ·mol-1
O2+PtF6-(s)=O2+(g)+PtF6- H3=482.2 kJ·mol-1
则反应O2(g)+ PtF6 (g) = O2+PtF6- (s)的H=_____________ kJ·mol-1。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为_______ _____。
已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4*)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________。
27.(2010江苏卷)以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp[Mg(OH)2]=1.8×10-11,若溶液中c(OH-)=3.0×10-6mol·L-1,则溶液中c(Mg2*)= 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。
(3)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下CO20.896L,通过计算确定碱式碳酸镁的化学式 。
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数 (填 “升高”、“降低”或“不变”)。
28.已知25℃时,Ksp[Cu(OH)2]=2×10-20。
(1)某CuSO4溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于________。
(2)要使0.2 mol·L-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为________。
29. 29. 下列说法中正确的是
A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小
C.AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI)
D.硬水中含有较多的Ca2+、Mg2+、HCO、SO,加热煮沸可以完全除去其中的Ca2+、Mg2+
20c(Mg2+)=1.12×10-4 mol/L ;c(OH-)=2.24×10-4 mol/L
21.①AgCl(s)Ag+(aq)+Cl-(aq)
Ag2CrO4(s) 2Ag+(aq)+CrO42-(aq)
2x x
(2x)2·x=Ksp
∴ c(AgCl)<c(Ag2CrO4)
②在0.010 mol·L-1 AgNO3溶液中,c(Ag+)=0.010 mol·L-1
AgCl(s) Ag+(aq) + Cl-(aq)
溶解平衡时: 0.010+x x
(0.010+x)·x=1.8×10-10 ∵ x很小,∴ 0.010+x ≈0.010
x=1.8×10-8(mol·L-1)
c(AgCl)= 1.8×10-8(mol·L-1)
Ag2CrO4(s) 2Ag+(aq) + CrO2-4(aq)
溶解平衡时: 0.010+x x
(0.010+2x)2·x=1.1×10-12 ∵ x很小,∴ 0.010+2x≈0.010
x=1.1×10-8(mol·L-1) ∴ c(Ag2CrO4)=1.1×10-8 (mol·L-1)
21.①AgCl(s)Ag+(aq)+Cl-(aq)
Ag2CrO4(s) 2Ag+(aq)+CrO42-(aq)
2x x
(2x)2·x=Ksp
∴ c(AgCl)<c(Ag2CrO4)
②在0.010 mol·L-1 AgNO3溶液中,c(Ag+)=0.010 mol·L-1
AgCl(s) Ag+(aq) + Cl-(aq)
溶解平衡时: 0.010+x x
(0.010+x)·x=1.8×10-10 ∵ x很小,∴ 0.010+x ≈0.010
x=1.8×10-8(mol·L-1)
c(AgCl)= 1.8×10-8(mol·L-1)
Ag2CrO4(s) 2Ag+(aq) + CrO2-4(aq)
溶解平衡时: 0.010+x x
(0.010+2x)2·x=1.1×10-12 ∵ x很小,∴ 0.010+2x≈0.010
x=1.1×10-8(mol·L-1) ∴ c(Ag2CrO4)=1.1×10-8 (mol·L-1)
∴ c(AgCl)>c(Ag2CrO4)
22. (1) 10-14 10-12 (2) 2 :9 (3) 4×10-3
25.答案:(1)
(可不写)
(2)2.7×
(3)172.5
(4)使得到充分的还原(或提高 的产量)
①②为吸热反应,碳和氧气反应放热维持反应所需高温
26答案:w(1)向左 不改变 (2)-77.6 (3)Cu(OH)2 Cu2++2NH3·H2O=Cu(OH)2 ↓+2NH4+
(4)中 Kb=10-9/( (a-0.01)mol·L-1.
27【答案】
(1)2.0mol.L-1
(2)NH4Cl
(3)Mg(OH)24MgCO34H2O
(4)升高
28答案:(1)5 (2)6
水氯
镁石
溶 解
过滤
热水解
沉淀镁
预氨化
碱式
碳酸镁
H2O
NH3
NH3、NH4HCO3
滤液
A
B
10-6
10-7
10-7 10-6 c(H+)mol/L
c(OH-) mol/L
1. 已知25℃时,电离常数Ka(HF)=3.6×10-4mol/L,溶度积常数Ksp(CaF2)=1.46×10-10mol3/L3。现向1L 0.2mol/LHF溶液中加入1L 0.2mol/LCaCl2溶液,则下列说法中,正确的是
A.25℃时,0.1 mol/LHF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中,Ksp(CaF2)=
D.该体系中有CaF2沉淀产生
2. 已知Ksp(AgCl )=1.8×10-10,Ksp(AgI)=1.0×10-16。下列关于不溶物之间转化的说法中错误的是
A.AgCl不溶于水,不能转化为AgI
B.两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物
C.AgI比AgCl更难溶于水,所以,AgCl可以转化为AgI
D.常温下AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于 EQ \F(1,) ×10-11 mol·L-1
3. 在已知AgCl和Ag2CrO4 的溶度积分别为1.8×10-10mol-2和2.0×10-12mol3·L-3。若用难溶盐在溶液中的浓度来表示其溶解度,则下列叙述正确的是
A.AgCl和Ag2CrO4 的溶解度相等
B.AgCl的溶解度大于Ag2CrO4
C.两者类型不同,不能直接由Ksp的大小来判断其溶解能力的大小
D.都是难溶盐,溶解度无意义
4. 当固体AgCl放在较浓的KI溶液中振荡时,部分AgCl转化为AgI,其原因是.
A.AgI比AgCl稳定 B.氯的非金属性比碘强
C.I-的还原性比Cl-强 D.AgI的溶解度比AgCl小
5. 25℃时,现向1L 0.2mol·L-1HF溶液中加入1L 0.2mol·L-1CaCl2溶液,则下列说法中,正确的是
A.25℃时,0.1mol·L-1HF 溶液中pH=1 B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中没有沉淀产生 D.该体系中HF与CaCl2反应产生沉淀
6. 在2mL物质的量浓度相等的NaCl和NaI溶液中滴入几滴AgNO3溶液,发生的反应为.
A.只有AgCl沉淀生成
B.只有AgI沉淀生成
C.生成等物质的量的AgCl和AgI沉淀
D.两种沉淀都有,但以AgI为主
7. 已知25℃时,AgI饱和溶液中c (Ag+)为1.22×10—8mol/L,AgCl的饱和溶液中c (Ag+)为1.25×10—5mol/L。若在5mL含有KCl和KI各为0.01mol/L的溶液中,加入8mL0.01mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
A.c (K+)>c (NO3—) >c (Cl—) >c (Ag+)>c (I—)
B.c (K+)>c (NO3—) >c (Ag+) >c (Cl—)>c (I—)
C.c (NO3—)>c (K+)>c (Ag+) >c (Cl—)>c (I—)
D.c (K+)>c (NO3—) >c (Ag+) = c (Cl—) + c (I—)
8. 常温下,AgCl、AgBr、AgI的溶度积常数(Ksp)依次为1.8×10-10mol2·L-2、5.0×10-13mol2·L-2、8.3×10-17mol2·L-2。下列有关说法错误的是
A.常温下在水中溶解能力AgCl>AgBr>AgI
B.在AgCl饱和液中加入足量浓NaBr溶液有AgBr沉淀生成
C.在AgBr饱和溶液中加入足量浓NaCl溶液不可能有AgCl沉淀生成
D.在AgI饱和液中加入NaI固体有AgI沉淀析出
9. 某温度时,AgCl (s) Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.加入AgNO3可以使溶液由c点变到d点
B.加入固体NaCl则AgCl的溶解度减小,Ksp也减小
C.c点对应的Ksp小于a点对应的Ksp
D. d点有AgCl沉淀生成
10. 向5mLNaCl溶液中滴入一滴Ag NO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴加一滴Na2S溶液并振荡,沉淀又变为黑色,根据上述变化过程,分析三种沉淀物的溶解度为
A AgCl=AgI=Ag2S B AgCl
11. 把氢氧化钙放入蒸馏水中,一段时间后达到下列溶解平衡:Ca(OH)2(s) Ca2+(aq)+2OH-(aq),加入下列物质,可使Ca(OH)2固体减少的是
A CaCl2 B NaOH C NaHSO4 D NaCl
12. 在水中存在着如下沉淀溶解平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),在常温下,Ksp =2×10-20mol3 L-3。某溶液中,c(Cu2+)=0.02 mol L-1,在常温下如果要生成Cu(OH)2沉淀,需向溶液中加入碱溶液来调整,使溶液的大于
A 2 B 3 C 4 D 5
13.(2011浙江卷)海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
模拟海水中的离子浓度(mol/L) Na+ Mg2+ Ca2+ Cl―
0.439 0.050 0.011 0.560 0.001
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9; Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6; Ksp[Mg(OH)2]=5.61×10-12。
下列说法正确的是
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
14.(2008·山东)某温度时,BaSO4在水中的沉淀溶解平衡曲线如下图所示。下列说法正确的是
提示:BaSO4(s) Ba2+(aq)+SO42 -(aq)的平衡常数:Ksp = c(Ba2+)·c(SO42 -),称为溶度积常数。
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
15.(2009福建)在一定条件下,Na2CO3溶液存在水解平衡:CO32 -+H2OHCO3- +OH-。下列说法正确的是
A.稀释溶液,水解平衡常数增大 B.通入CO2,平衡朝正反应方向移动
C.升高温度,减小 D.加入NaOH固体,溶液pH减小
16.(2009·广东卷,18,4分)硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下。下列说法正确的是
A.温度一定时,Ksp(SrSO4)随c(SO42 -)的增大而减小
B.三个不同温度中,313 K时Ksp(SrSO4)最大
C.283 K时,图中a点对应的溶液是不饱和溶液
D.283 K下的SrSO4饱和溶液升温到363 K后变为不饱和溶液
17.(2009·理综 )已知:25 ℃时,Ksp[Mg(OH)2] = 5.61×10-12,Ksp[MgF2] = 7.42×10-11。下列说法正确的是
A.25 ℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.25 ℃时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大
C.25 ℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小
D.25 ℃时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2
18.已知:25°C时, Ksp(Mg(OH)2)=5.61×10-12, Ksp(MgF2)=7.42×10-11。下列说法正确的是
A.25°C时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的C(Mg2+)大
B.25°C时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,C(Mg2+)增大
C.25°C时,Mg(OH)2固体在20ml0.01 mol·L-1氨水中的Ksp比在20mL0.01 mol·L-1 NH4Cl 溶液中的Ksp小
D.25°C时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2
19. 在1 mol L-1 CuSO4溶液中含有少量的Fe3+杂质,pH值控制在 范围才能除去Fe3+,使[Fe3+]≤10-5 mol L-1。已知:Fe(OH)3的Ksp = 2.6×10-39mol4 L-4,Cu(OH)2的Ksp = 5.6×10-20mol3 L-3
20. 已知在室温时,Mg(OH)2的溶度积Ksp=5.6×10-12 (mol/L)3,求室温下Mg(OH)2饱和溶液中Mg 2+和OH-的物质的量浓度
21. 一定温度下,难溶电解质在饱和溶液中各离子浓度幂的乘积是一个常数,这个常数称为该难溶电解质的溶度积,用符号Ksp表示。
即:AmBn(s) mAn+(aq)+nBm-(aq) [An+]m·[Bm-]n=Ksp
已知:某温度时,Ksp(AgCl)=[Ag+][Cl-] =1.8×10-10
Ksp(Ag2CrO4)=[Ag+]2[CrO2- 4] =1.1×10-12
试求:
(1)此温度下AgCl饱和溶液和Ag2CrO4饱和溶液的物质的量浓度,并比较两者的大小。
(2)此温度下,在0.010mo1·L-1的AgNO3溶液中,AgCl与Ag2CrO4分别能达到的最大物质的量浓度,并比较两者的大小。
22.(1)将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃的恒温,致使混合溶液
的pH=7,则Ba(OH)2和盐酸的体积比为__________________。
(2)已知AnBm的离子积为[c(Am+)]n[c(Bn-)]m,若某温度下Ca(OH)2的溶解度为0.74g,设饱和溶液的密度为1g/mL,其离子积约为______________。
23. (2011新课标卷)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色请氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________________mol·L-1(Kap[Cu(OH)2]=2.2×10-20)。
若在0.1mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是_______________mol·L-1。
24.(2011天津卷)工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生
很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
其中第①步存在平衡:
(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr2O72-和CrO42-的浓度相同
b.2v (Cr2O72-) =v (CrO42-)
c.溶液的颜色不变
(3)第②步中,还原1mol Cr2O72-离子,需要 mol的FeSO·7HO。
(4)第③步生成的Cr(OH)在溶液中存在以下沉淀溶解平衡:
Cr(OH) (s)Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)的溶度积Kap= 10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
25.(2008江苏)工业上制备BaCl2的工艺流程图如下:
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s)4CO(g) + BaS(s) △H1 = 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s)2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,= 。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
(3)反应C(s) + CO2(g)2CO(g)的△H2= kJ·mol-1。
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是 , 。
26.运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应反应N2(g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);,使用催化剂 反应的ΔH(填“增大”“减小”或“不改变”)。
(2)O2 (g)= O+2(g)+e- H1= 1175.7 kJ·mol-1
PtF6(g)+ e-1 PtF6-(g) H2= - 771.1 kJ·mol-1
O2+PtF6-(s)=O2+(g)+PtF6- H3=482.2 kJ·mol-1
则反应O2(g)+ PtF6 (g) = O2+PtF6- (s)的H=_____________ kJ·mol-1。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为_______ _____。
已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4*)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________。
27.(2010江苏卷)以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的Ksp[Mg(OH)2]=1.8×10-11,若溶液中c(OH-)=3.0×10-6mol·L-1,则溶液中c(Mg2*)= 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。
(3)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下CO20.896L,通过计算确定碱式碳酸镁的化学式 。
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数 (填 “升高”、“降低”或“不变”)。
28.已知25℃时,Ksp[Cu(OH)2]=2×10-20。
(1)某CuSO4溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于________。
(2)要使0.2 mol·L-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为________。
29. 29. 下列说法中正确的是
A.饱和石灰水中加入一定量生石灰,温度明显升高,所得溶液的pH增大
B.AgCl悬浊液中存在平衡:AgCl(s) Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小
C.AgCl悬浊液中加入KI溶液,白色沉淀变成黄色,证明此条件下Ksp(AgCl)>Ksp(AgI)
D.硬水中含有较多的Ca2+、Mg2+、HCO、SO,加热煮沸可以完全除去其中的Ca2+、Mg2+
20c(Mg2+)=1.12×10-4 mol/L ;c(OH-)=2.24×10-4 mol/L
21.①AgCl(s)Ag+(aq)+Cl-(aq)
Ag2CrO4(s) 2Ag+(aq)+CrO42-(aq)
2x x
(2x)2·x=Ksp
∴ c(AgCl)<c(Ag2CrO4)
②在0.010 mol·L-1 AgNO3溶液中,c(Ag+)=0.010 mol·L-1
AgCl(s) Ag+(aq) + Cl-(aq)
溶解平衡时: 0.010+x x
(0.010+x)·x=1.8×10-10 ∵ x很小,∴ 0.010+x ≈0.010
x=1.8×10-8(mol·L-1)
c(AgCl)= 1.8×10-8(mol·L-1)
Ag2CrO4(s) 2Ag+(aq) + CrO2-4(aq)
溶解平衡时: 0.010+x x
(0.010+2x)2·x=1.1×10-12 ∵ x很小,∴ 0.010+2x≈0.010
x=1.1×10-8(mol·L-1) ∴ c(Ag2CrO4)=1.1×10-8 (mol·L-1)
21.①AgCl(s)Ag+(aq)+Cl-(aq)
Ag2CrO4(s) 2Ag+(aq)+CrO42-(aq)
2x x
(2x)2·x=Ksp
∴ c(AgCl)<c(Ag2CrO4)
②在0.010 mol·L-1 AgNO3溶液中,c(Ag+)=0.010 mol·L-1
AgCl(s) Ag+(aq) + Cl-(aq)
溶解平衡时: 0.010+x x
(0.010+x)·x=1.8×10-10 ∵ x很小,∴ 0.010+x ≈0.010
x=1.8×10-8(mol·L-1)
c(AgCl)= 1.8×10-8(mol·L-1)
Ag2CrO4(s) 2Ag+(aq) + CrO2-4(aq)
溶解平衡时: 0.010+x x
(0.010+2x)2·x=1.1×10-12 ∵ x很小,∴ 0.010+2x≈0.010
x=1.1×10-8(mol·L-1) ∴ c(Ag2CrO4)=1.1×10-8 (mol·L-1)
∴ c(AgCl)>c(Ag2CrO4)
22. (1) 10-14 10-12 (2) 2 :9 (3) 4×10-3
25.答案:(1)
(可不写)
(2)2.7×
(3)172.5
(4)使得到充分的还原(或提高 的产量)
①②为吸热反应,碳和氧气反应放热维持反应所需高温
26答案:w(1)向左 不改变 (2)-77.6 (3)Cu(OH)2 Cu2++2NH3·H2O=Cu(OH)2 ↓+2NH4+
(4)中 Kb=10-9/( (a-0.01)mol·L-1.
27【答案】
(1)2.0mol.L-1
(2)NH4Cl
(3)Mg(OH)24MgCO34H2O
(4)升高
28答案:(1)5 (2)6
水氯
镁石
溶 解
过滤
热水解
沉淀镁
预氨化
碱式
碳酸镁
H2O
NH3
NH3、NH4HCO3
滤液
A
B
10-6
10-7
10-7 10-6 c(H+)mol/L
c(OH-) mol/L
