【原】化学:第二章 烃和卤代烃复习课件(莒南)(人教版选修5)
文档属性
| 名称 | 【原】化学:第二章 烃和卤代烃复习课件(莒南)(人教版选修5) |  | |
| 格式 | rar | ||
| 文件大小 | 483.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-11-20 08:39:34 | ||
图片预览






文档简介
(共31张PPT)
复习课
新课标人教版高中化学选修5
第二章 烃和卤代烃
一、基础知识回顾
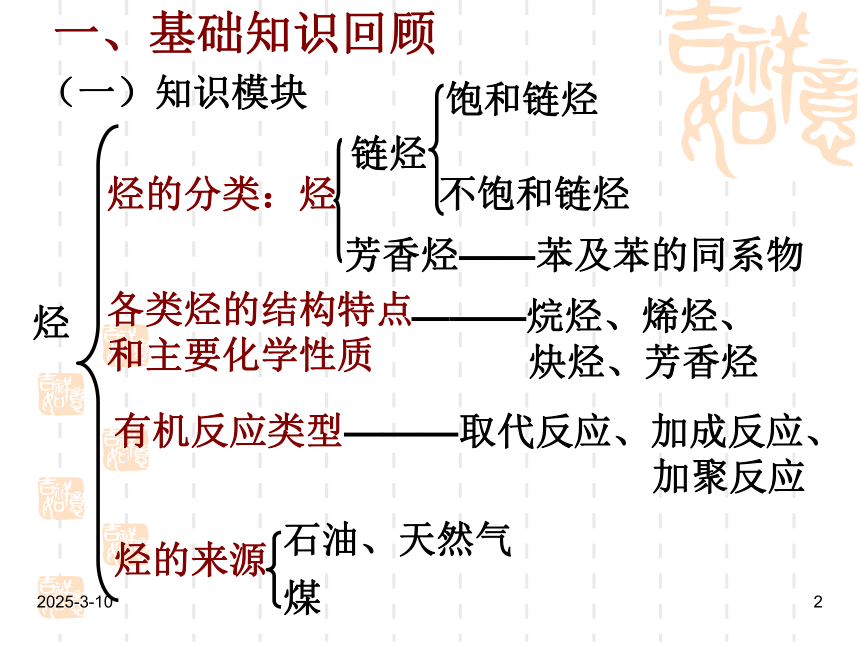
(一)知识模块
烃
烃的分类:烃
饱和链烃
不饱和链烃
链烃
芳香烃——苯及苯的同系物
各类烃的结构特点和主要化学性质
有机反应类型
———烷烃、烯烃、
炔烃、芳香烃
———取代反应、加成反应、
加聚反应
烃的来源
石油、天然气
煤
思考:
1.我们学过的烷烃(乙烷)、乙烯、乙炔、苯的组成、结构之间有什么规律性?
2.各种烃的结构如何决定它们的性质?
1、烃的物理性质:
①密度:所有烃的密度都比水小
②状态:常温下,碳原子数小于等于4的气态
③熔沸点:碳原子数越多,熔、沸点越高 ;
碳原子数相同,支链越多,熔沸点越低;
④含碳量规律:
烷烃<烯烃<炔烃<苯的同系物
烷烃(CnH2n+2):随n值增大,含碳量增大
烯烃(CnH2n) :n值增大,碳的含量为定值;
炔烃(CnH2n-2) :随n值增大,含碳量减小
苯及其同系物:(CnH2n-6):随n值增大含碳量减小
(二)、烃的重要性质:
分类 通式 官能团 化学性质
烷烃 CnH2n+2 特点:
C—C
烯烃(环烷烃) CnH2n 一个C=C
炔烃(二烯烃) CnH2n-2 一个C≡C
苯及其同系物 CnH2n-6 一个苯基
卤代烃 CnH2n+1X —X
2.各类烃及卤代烃的结构特点和化学性质
稳定,取代、氧化、
裂化
加成、加聚、氧化
加成、加聚、氧化
取代、加成(H2)、
氧化
水解→醇
消去→烯烃
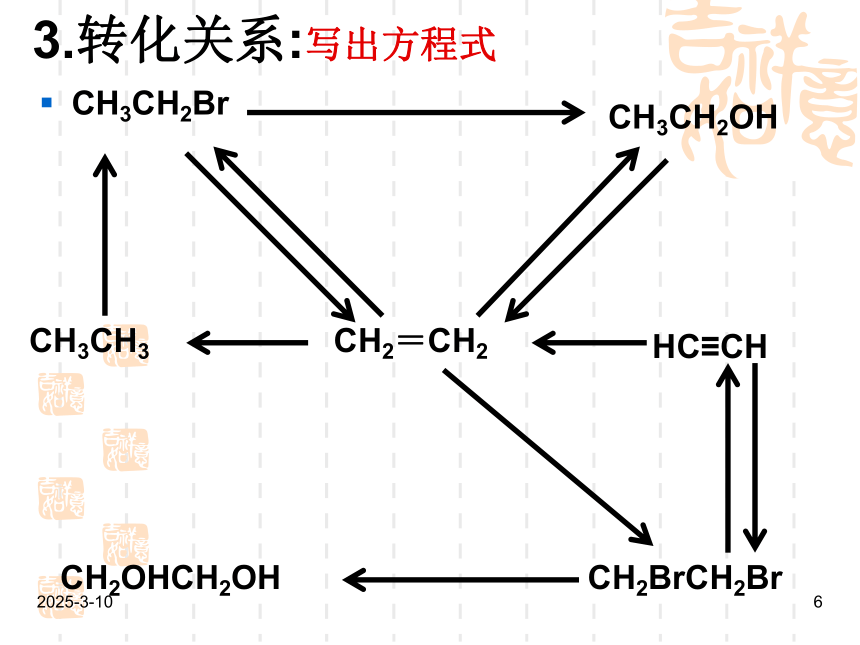
3.转化关系:写出方程式
CH3CH2Br
CH3CH2OH
CH3CH3
HC≡CH
CH2=CH2
CH2BrCH2Br
CH2OHCH2OH
二、有机化学的主要反应类型
1、取代反应 2、加成反应
3、消去反应 4、氧化反应
5、还原反应 6、聚合反应
7、酯化反应 8、水解反应
9、裂化反应
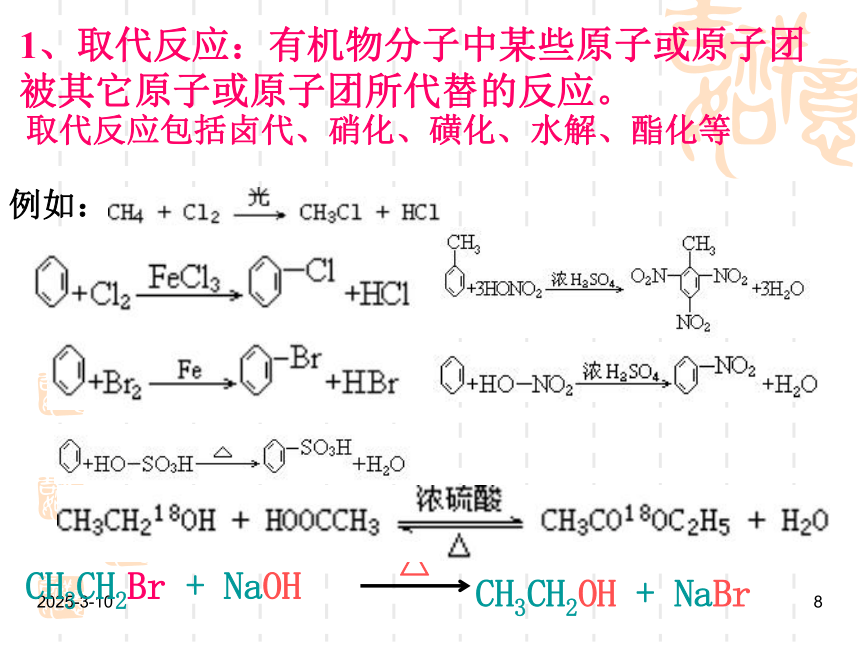
1、取代反应:有机物分子中某些原子或原子团
被其它原子或原子团所代替的反应。
取代反应包括卤代、硝化、磺化、水解、酯化等
例如:
CH3CH2Br + NaOH
CH3CH2OH + NaBr
△
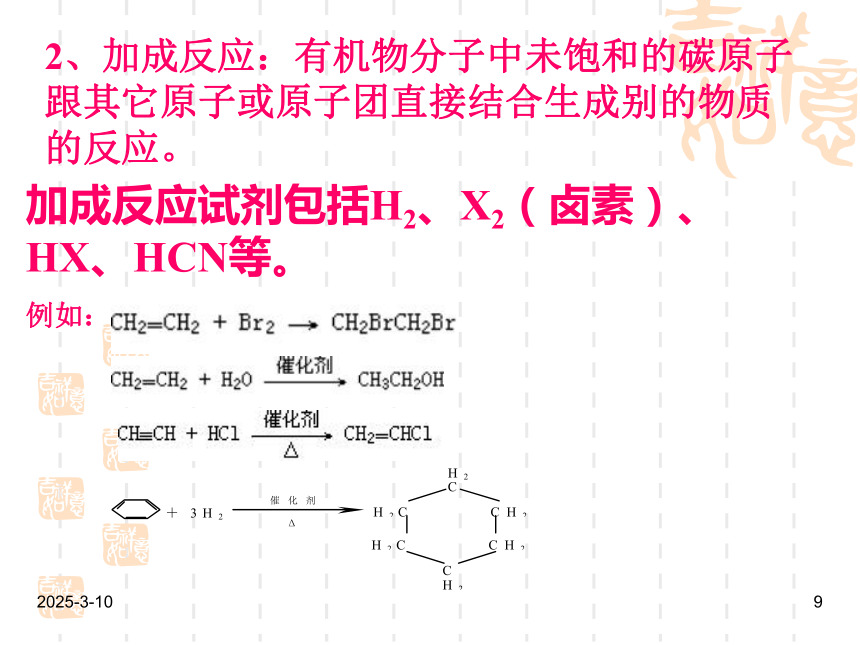
2、加成反应:有机物分子中未饱和的碳原子跟其它原子或原子团直接结合生成别的物质的反应。
加成反应试剂包括H2、X2(卤素)、HX、HCN等。
例如:
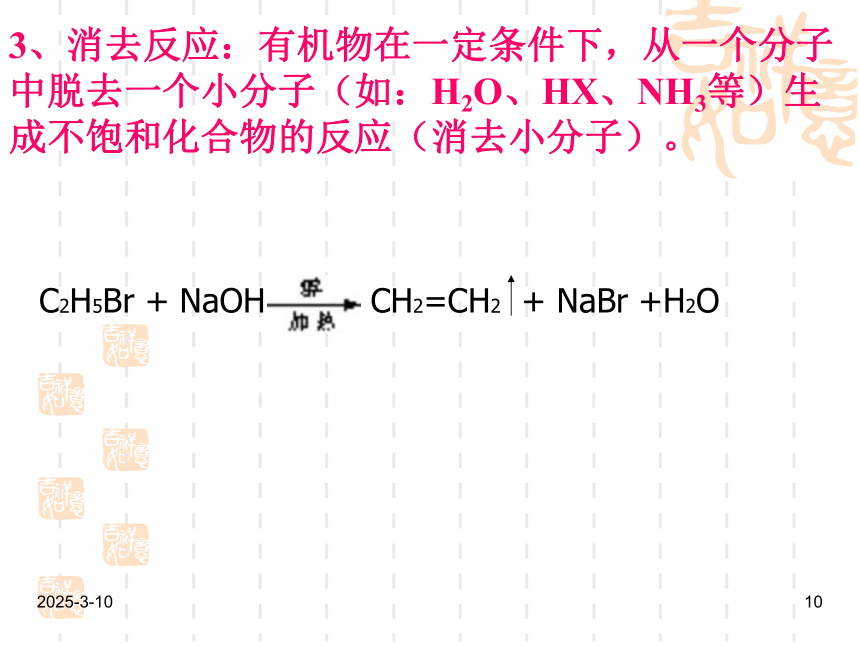
3、消去反应:有机物在一定条件下,从一个分子中脱去一个小分子(如:H2O、HX、NH3等)生成不饱和化合物的反应(消去小分子)。
C2H5Br + NaOH CH2=CH2 + NaBr +H2O
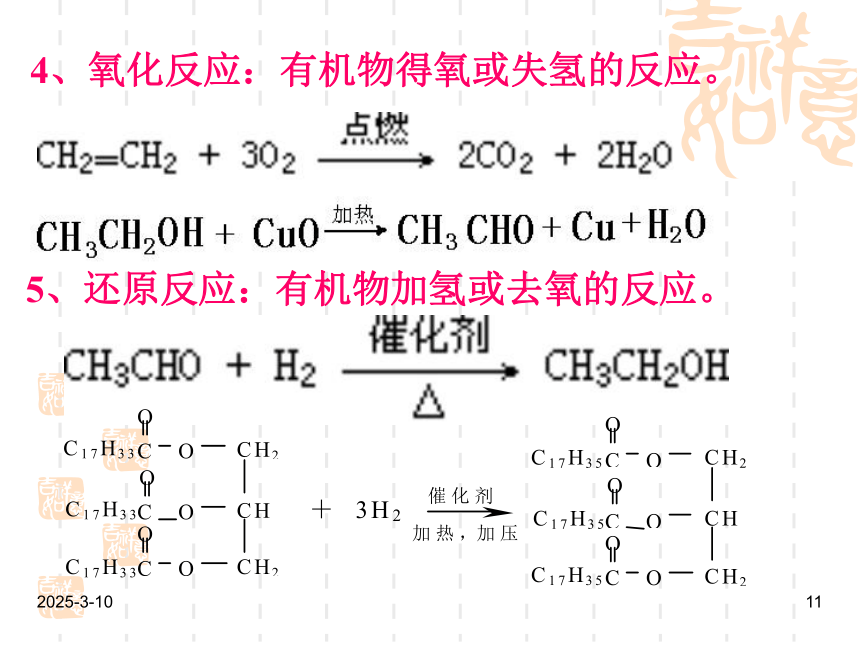
4、氧化反应:有机物得氧或失氢的反应。
5、还原反应:有机物加氢或去氧的反应。
(1)加聚反应:通过加成反应聚合成高分子化合物的反应(加成聚合)。主要为含双键的单体聚合。
6、聚合反应:单体间通过缩合反应生成高分子化合物,同时生成小分子(H2O、NH3、HX等)的反应。
7、酯化反应(属于取代反应):酸(有机羧酸、无机含氧酸)与醇作用生成酯和水的反应。
8、水解反应:有机物在一定条件下跟水作用
生成两种或多种物质的反应。
水解反应包括卤代烃水解、酯水解、糖(除单糖外)水解、蛋白质水解等。
9、裂化反应:在一定温度下,把相对分子质量大、沸点高的长链烃断裂为相对分子质量小、沸点低的短链烃的反应。
(1)甲烷的制备;
(2)乙烯的制备;
(3)乙炔的制备;
三、有关实验内容
(一)几种有机气体的制备
甲烷的实验室制法:
1.药品:无水醋酸钠(CH3COONa)和碱石灰;
2.发生和收集装置:
使用“固+固
气
”型的物质制备发生装置.
(与实验室制氧气,氨气的装置相同)
由于甲烷不溶于水,可用排水法收集.
3.碱石灰的作用:反应物,干燥
乙烯的实验室制法:
1. 发生装置及收集方法:
(1).选用“液+液 气”的物质制备装置.(与实验室制氯气,氯化氢的装置相同)
(2)用排水法收集.
2.实验注意事项:
(1).V(乙醇)/V(浓硫酸)=1:3;
(2)烧瓶中加入啐瓷片防止爆沸;
(3)迅速升温至170 0c.
乙炔的实验室制法:
1.发生装置:“固+液 气”的制取装置;
2.收集方法:排水法;
3.注意事项:
(1)可用饱和食盐水代替水,以得到平稳气流.
(2)不能使用启普发生器,
(3)产物气体中因含有AsH3,PH3而有特殊气味.
(二)、几个重要实验
溴乙烷水解
与氢氧化钠溶液共热:
你认为哪一套装置更好?它的优点有哪些?
溴乙烷与氢氧化钠共热实验的注意事项:
1.反应物:
2.反应条件:
3.产物检验步骤
4.此反应
溴乙烷+氢氧化钠溶液;
共热
叫做水解反应,属于取代反应!
①取水解后上层清液少许加入稀硝酸至酸性
②再加入硝酸银溶液
③因为Ag++OH—=AgOH(白色)↓
2AgOH=Ag2O(褐色)+H2O;
褐色掩蔽AgBr的浅黄色,使产物检验实验失败。所以必须用硝酸酸化!
CH3CH2Br + HOH
CH3CH2Br + NaOH
CH3CH2OH + HBr
CH3CH2OH + NaBr
NaOH△
NaOH+HBr=NaBr+H2O
△
反应:
AgNO3+NaBr=AgBr↓+NaNO3
水解反应取代反应
溴乙烷消去反应:
C2H5Br与NaOH的醇溶液共热实验的注意事项:
1.反应物:
2.反应条件:
3.反应方程式
4.产物检验
溴乙烷+氢氧化钠的醇溶液;
共热
CH2=CH2+Br2→CH2BrCH2Br
KMnO4 褪色
CH2=CH2
将产生的气体通入溴水或酸性高锰酸钾溶液中,二者均褪色。
CH2-CH2+NaOH CH2=CH2 +NaBr+H2O
H Br
醇
Δ
复习课
新课标人教版高中化学选修5
第二章 烃和卤代烃
一、基础知识回顾
(一)知识模块
烃
烃的分类:烃
饱和链烃
不饱和链烃
链烃
芳香烃——苯及苯的同系物
各类烃的结构特点和主要化学性质
有机反应类型
———烷烃、烯烃、
炔烃、芳香烃
———取代反应、加成反应、
加聚反应
烃的来源
石油、天然气
煤
思考:
1.我们学过的烷烃(乙烷)、乙烯、乙炔、苯的组成、结构之间有什么规律性?
2.各种烃的结构如何决定它们的性质?
1、烃的物理性质:
①密度:所有烃的密度都比水小
②状态:常温下,碳原子数小于等于4的气态
③熔沸点:碳原子数越多,熔、沸点越高 ;
碳原子数相同,支链越多,熔沸点越低;
④含碳量规律:
烷烃<烯烃<炔烃<苯的同系物
烷烃(CnH2n+2):随n值增大,含碳量增大
烯烃(CnH2n) :n值增大,碳的含量为定值;
炔烃(CnH2n-2) :随n值增大,含碳量减小
苯及其同系物:(CnH2n-6):随n值增大含碳量减小
(二)、烃的重要性质:
分类 通式 官能团 化学性质
烷烃 CnH2n+2 特点:
C—C
烯烃(环烷烃) CnH2n 一个C=C
炔烃(二烯烃) CnH2n-2 一个C≡C
苯及其同系物 CnH2n-6 一个苯基
卤代烃 CnH2n+1X —X
2.各类烃及卤代烃的结构特点和化学性质
稳定,取代、氧化、
裂化
加成、加聚、氧化
加成、加聚、氧化
取代、加成(H2)、
氧化
水解→醇
消去→烯烃
3.转化关系:写出方程式
CH3CH2Br
CH3CH2OH
CH3CH3
HC≡CH
CH2=CH2
CH2BrCH2Br
CH2OHCH2OH
二、有机化学的主要反应类型
1、取代反应 2、加成反应
3、消去反应 4、氧化反应
5、还原反应 6、聚合反应
7、酯化反应 8、水解反应
9、裂化反应
1、取代反应:有机物分子中某些原子或原子团
被其它原子或原子团所代替的反应。
取代反应包括卤代、硝化、磺化、水解、酯化等
例如:
CH3CH2Br + NaOH
CH3CH2OH + NaBr
△
2、加成反应:有机物分子中未饱和的碳原子跟其它原子或原子团直接结合生成别的物质的反应。
加成反应试剂包括H2、X2(卤素)、HX、HCN等。
例如:
3、消去反应:有机物在一定条件下,从一个分子中脱去一个小分子(如:H2O、HX、NH3等)生成不饱和化合物的反应(消去小分子)。
C2H5Br + NaOH CH2=CH2 + NaBr +H2O
4、氧化反应:有机物得氧或失氢的反应。
5、还原反应:有机物加氢或去氧的反应。
(1)加聚反应:通过加成反应聚合成高分子化合物的反应(加成聚合)。主要为含双键的单体聚合。
6、聚合反应:单体间通过缩合反应生成高分子化合物,同时生成小分子(H2O、NH3、HX等)的反应。
7、酯化反应(属于取代反应):酸(有机羧酸、无机含氧酸)与醇作用生成酯和水的反应。
8、水解反应:有机物在一定条件下跟水作用
生成两种或多种物质的反应。
水解反应包括卤代烃水解、酯水解、糖(除单糖外)水解、蛋白质水解等。
9、裂化反应:在一定温度下,把相对分子质量大、沸点高的长链烃断裂为相对分子质量小、沸点低的短链烃的反应。
(1)甲烷的制备;
(2)乙烯的制备;
(3)乙炔的制备;
三、有关实验内容
(一)几种有机气体的制备
甲烷的实验室制法:
1.药品:无水醋酸钠(CH3COONa)和碱石灰;
2.发生和收集装置:
使用“固+固
气
”型的物质制备发生装置.
(与实验室制氧气,氨气的装置相同)
由于甲烷不溶于水,可用排水法收集.
3.碱石灰的作用:反应物,干燥
乙烯的实验室制法:
1. 发生装置及收集方法:
(1).选用“液+液 气”的物质制备装置.(与实验室制氯气,氯化氢的装置相同)
(2)用排水法收集.
2.实验注意事项:
(1).V(乙醇)/V(浓硫酸)=1:3;
(2)烧瓶中加入啐瓷片防止爆沸;
(3)迅速升温至170 0c.
乙炔的实验室制法:
1.发生装置:“固+液 气”的制取装置;
2.收集方法:排水法;
3.注意事项:
(1)可用饱和食盐水代替水,以得到平稳气流.
(2)不能使用启普发生器,
(3)产物气体中因含有AsH3,PH3而有特殊气味.
(二)、几个重要实验
溴乙烷水解
与氢氧化钠溶液共热:
你认为哪一套装置更好?它的优点有哪些?
溴乙烷与氢氧化钠共热实验的注意事项:
1.反应物:
2.反应条件:
3.产物检验步骤
4.此反应
溴乙烷+氢氧化钠溶液;
共热
叫做水解反应,属于取代反应!
①取水解后上层清液少许加入稀硝酸至酸性
②再加入硝酸银溶液
③因为Ag++OH—=AgOH(白色)↓
2AgOH=Ag2O(褐色)+H2O;
褐色掩蔽AgBr的浅黄色,使产物检验实验失败。所以必须用硝酸酸化!
CH3CH2Br + HOH
CH3CH2Br + NaOH
CH3CH2OH + HBr
CH3CH2OH + NaBr
NaOH△
NaOH+HBr=NaBr+H2O
△
反应:
AgNO3+NaBr=AgBr↓+NaNO3
水解反应取代反应
溴乙烷消去反应:
C2H5Br与NaOH的醇溶液共热实验的注意事项:
1.反应物:
2.反应条件:
3.反应方程式
4.产物检验
溴乙烷+氢氧化钠的醇溶液;
共热
CH2=CH2+Br2→CH2BrCH2Br
KMnO4 褪色
CH2=CH2
将产生的气体通入溴水或酸性高锰酸钾溶液中,二者均褪色。
CH2-CH2+NaOH CH2=CH2 +NaBr+H2O
H Br
醇
Δ
