人教版化学九年级上第七单元《燃料及其利用》测试题(含答案)
文档属性
| 名称 | 人教版化学九年级上第七单元《燃料及其利用》测试题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 266.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-04 00:00:00 | ||
图片预览




文档简介
《燃料及其利用》测试题
一、单选题
1.下列说法中正确的是( )
A.用活性炭可除去水中的色素和有异味的物质
B.人类利用的能量,都是通过化学反应获得的
C.灯帽盖灭酒精灯,是因为降低了可燃物温度
D.铁丝在氧气中燃烧,火星四射,生成红色固体
2.下列做法正确的是(
)
A.用活性炭净水器降低自来水的硬度
B.用干粉灭火器来扑灭汽油着火
C.用炉具清洁剂来除去衣服上的油污
D.用食醋涂抹蚊虫叮咬后的皮肤
3.近期,济南的天空常常出现美丽的泉城蓝,环境治理,成效明显。为了让天空更蓝,让泉城更美,下列做法中,不合理的是
A.把秸秆还田,禁止焚烧处理
B.将垃圾进行分类投放
C.短距离出行时,尽量步行或骑自行车
D.将工厂污水直接排入小清河
4.燃烧是一类重要的化学变化,下列关于燃烧的叙述正确的是(
)
A.燃烧一定有火焰
B.物质在有限的空间内燃烧,一定会发生爆炸
C.物质跟氧气的反应就是燃烧
D.使可燃物温度降低到着火点以下,可以灭火
5.2016年,170多个国家领导人齐聚纽约共同签署气候变化问题(巴黎协定)旨在全球控制碳排放,使全球经济可持续发展。下列在经济发展中某地区制定的措施违法了该项协定的是(
)
A.大力发展公共交通,减少私家车使用
B.开发风能和电能
C.植树造林
D.大力引进和发展大型火力发电厂
6.加油站、面粉加工厂、纺织厂、矿井都应粘贴的安全标志是( )
7.如图是金刚石、石墨的结构示意图,下列说法不正确的是
A.它们的化学式都可以用“C”表示
B.石墨转化成金刚石是物理变化
C.物理性质有很大差异的原因是原子的排列方式不同
D.化学性质相似是因为都是由碳原子直接构成的
8.安全意识是人类生存所必须具有的基本素质之一,下列实验操作比较安全的是
A.用鼻子凑到容器口直接嗅闻气体的气味
B.用嘴品尝药品的味道
C.进入久未开启的菜窖、干涸的深井和深洞前,要做灯火试验
D.发现家里煤气泄漏时,应立即打开排气扇
9.木柴燃烧时,要把木柴架空一些才能燃烧得更旺一些,这是因为(
)
A.木柴是可燃物
B.温度易达到着火点
C.散热的速率快
D.使柴火和空气充分接触
10.在汽车加油站见到的油罐车上,所贴的危险化学品图标是(
)
A.B.
C.
D.
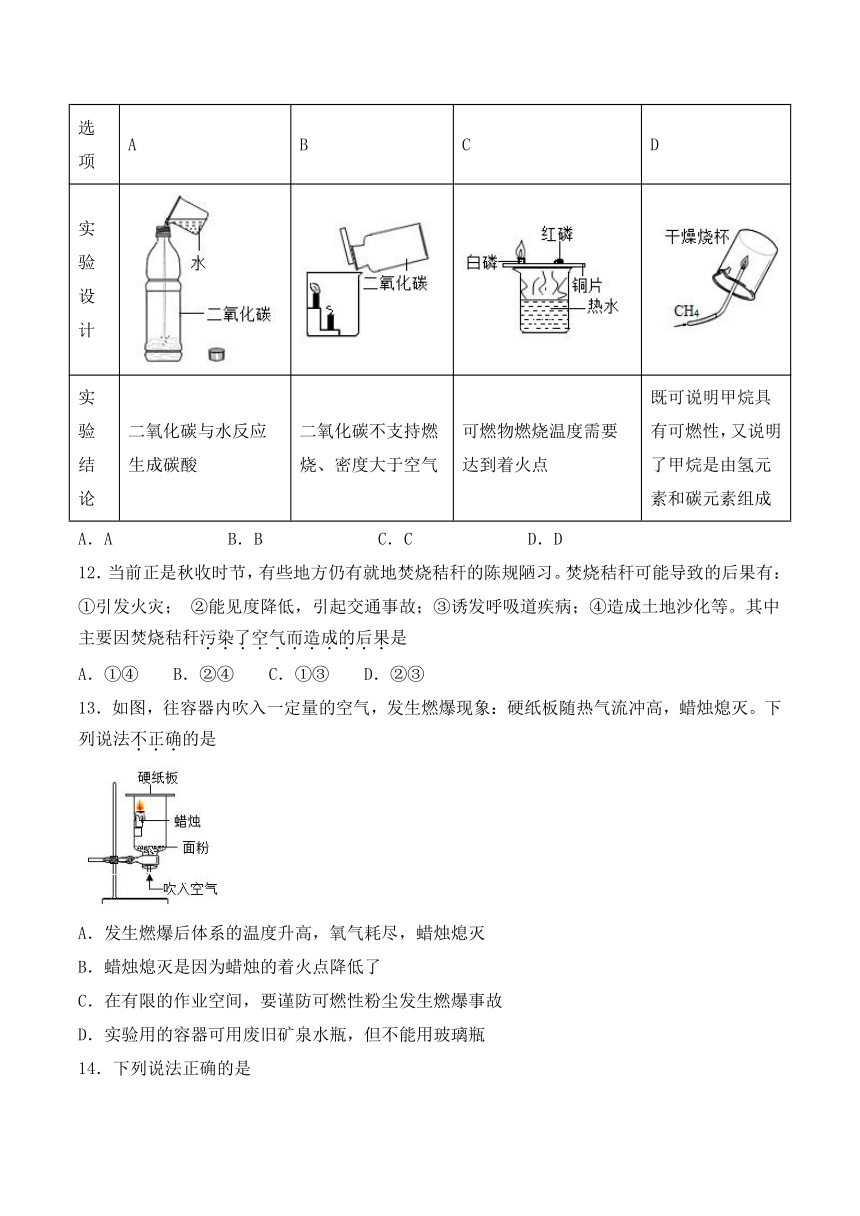
11.依据下列实验所得到的结论准确的是
选项
A
B
C
D
实验设计
实验结论
二氧化碳与水反应生成碳酸
二氧化碳不支持燃烧、密度大于空气
可燃物燃烧温度需要达到着火点
既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
A.A
B.B
C.C
D.D
12.当前正是秋收时节,有些地方仍有就地焚烧秸秆的陈规陋习。焚烧秸秆可能导致的后果有:①引发火灾;
②能见度降低,引起交通事故;③诱发呼吸道疾病;④造成土地沙化等。其中主要因焚烧秸秆污染了空气而造成的后果是
A.①④
B.②④
C.①③
D.②③
13.如图,往容器内吹入一定量的空气,发生燃爆现象:硬纸板随热气流冲高,蜡烛熄灭。下列说法不正确的是
A.发生燃爆后体系的温度升高,氧气耗尽,蜡烛熄灭
B.蜡烛熄灭是因为蜡烛的着火点降低了
C.在有限的作业空间,要谨防可燃性粉尘发生燃爆事故
D.实验用的容器可用废旧矿泉水瓶,但不能用玻璃瓶
14.下列说法正确的是
A.水能灭火是由于和易燃物接触后,吸收了大量的热,从而把易燃物的着火点升高了
B.可燃物燃烧,需要与氧气接触,同时温度要达到可燃物的着火点
C.夏天,可燃物易着火是由于可燃物在夏天的着火点降低了
D.浸在沸水中的白磷不能燃烧,是因为温度没有达到白磷的着火点
二、填空题
15.能源、环境与人类的生活和社会经济发展密切相关。
(1)目前化石能源是人类的主要能源,煤、石油和_____是常见的三大化石能源。
(2)2016年12月中下旬我国出现了大面积的雾霾天气,目前普遍认为雾霾与PM2.5有密切关系。PM2.5主要来自化石燃料的燃烧和扬尘,对人体健康和空气质量的影响很大。请你就减少雾霾发生提出一条建议_______________。
(3)为减少污染、提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳与水的反应,其微观示意图如图所示,该反应生成物的分子个数比为_______。
(4)研究发现NH3燃烧的产物没有污染,产物为水和一种单质,且释放大量能量,有一定应用前景。请写出NH3燃烧的化学方程式______________________。
16.空气、水是我们赖以生存的重要资源。
(1)2020新冠病毒疫情爆发后,佩戴口罩可以有效预防病毒传播,利用的化学原理是___。
(2)环境问题越来越受到人们的关注,现在使用脱硫煤能减少__的排放,减轻酸雨的危害。
(3)饮用硬水对健康有害,生活中常用_____________方法降低水的硬度。
(4)自来水厂常用的一种消毒剂有效成分是次氯酸钙(化学式为Ca(C1O)2),它可发生如下的反应:,则X的化学式为_________________。
(5)电解水可制氢气。通电一段时间后,如图所示。电极X为电源的__________极。氢气作为新能源,其主要优点为__________(填序号)。
A
制取成本低
B
燃烧产物无污染
C
制备原料为水,来源广
D
贮存方便、安全
17.阅读下列资料,完成本题
1777年,英国化学家卡文迪许用金属锌和稀盐酸制得氢气,并把氢气收集到一个倒置在水槽中的装满水的瓶中.最初,氢气被用于飞艇和载人气球.1973年“兴登堡”号飞艇因为火花引起燃烧,从此,人们改用氦气填充飞艇.工业上氢气主要用来和氮气反应制取氨气;还可以用来制备金属,如三氧化钨和氢气加热得到水和金属钨.氢气燃烧时放出大量热,是等质量汽油燃烧放热的倍;氢气燃烧后的产物是水,不会造成污染,因此,氢气正在成为新兴的能源.工业上,人们常用水和高温的焦炭反应制得一氧化碳和氢气.
(1)物质的性质决定物质的应用,本文中介绍了一些氢气的应用知识,请写出相对应的氢气性质.(用文字表述)用倒置在水槽中的装满水的瓶子收集氢气:_;氢气被用于飞艇和载人气球:__;氢气正在成为新兴的能源:__.
(2)文中分别介绍了一种氢气的实验室制法和工业制法,请写出相应的化学方程式.工业:________;实验室:___.
(3)配平下列反应化学方程式
①___N2+___H2___NH3
②___WO3+___H2___W+___H2O
18.随着经济的发展,能源和环境成为人们关注的焦点.
(1)煤、石油和
常称为化石燃料,属于
(填“可”或“不可”)再生能源
(2)对金属资源的保护,可以采取的措施是
(一条即可)
(3)“火患猛于虎”我们不能忘记生活中那些惨痛的教训.新闻媒体报道的一些娱乐场所发生的多起火灾事故,均是由于随意丢弃未熄灭的烟头所导致.在这些事故中,从燃烧的条件考虑,烟头所起的作用是
;钋对上述事件,作为青少年,你应该怎么做
.
19.空气、水、燃料是人类赖以生存的自然资源.
(1)人类时刻都离不开空气,是因为空气中的氧气能
,空气属于
(填物质类别)。
(2)为了保护环境,用煤作燃料的煤炉要适当增加进风口,将煤粉吹起使之剧烈燃烧,请解释这种做法有利于节能的原因是
。
(3)自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
图乙所示反应的基本类型为
;
写出图甲所示反应的化学方程式
。
三、推断题
20.已知A、D均为无色无味的气体,B、C为黑色粉末,E为单质。A、B、C、D、E、F六种物质之间的转化关系如下图所示。请回答:
(1)B、D的化学式分别为____________、____________;
(2)反应②、③的化学方程式分别为________、________
(3)①③这两个反应说明A和C具有相同的化学性质为________(填:“可燃性”或“稳定性”或“还原性”或“氧化性”)。
21.ABCDE为初中常见到物质,B和E组成元素相同,它们之间存在如图所示的转化关系,请根据信息和图示回答问题(反应条件和部分生成物已略去)。
(1)A的化学式_____,D的化学式_____。
(2)写出E转化为C的化学方程式_____。
四、实验题
22.同学们已经学习了有关金属的一些知识,对金属的活动性顺序也有了一定的认识。请运用所学知识参与以下探究并回答相关问题:
(实验一)将4枚洁净无锈的铁钉分别放入图中a、b、c、d4支试管中。
上述实验中,______试管中的铁钉最易生锈。设计如图d实验的目的是______。铁生锈的主要原因是铁与_______、______等物质发生了复杂的化学反应。
(实验二)为了探究Fe、Cu、Al三种金属的活动性顺序,小宁同学做了如图所示的实验.
(1)实验时,为了除去铝和铁表面的氧化物或污物,在插入溶液前应将_____。
(2)实验时观察到的主要现象是_____。得出的结论是_____。写出其中一种金属与硫酸铜溶液反应的化学方程式______。
(3)小成同学认为小宁同学设计的实验不能达到实验目的,原因是____,因此另设计一个实验,才能得出正确的结论。请你设计一个实验并完成下表:
操作
现象
结论
____
____
三种金属活动性由强到弱的顺序是:Al、Fe、Cu
23.达州盛产天然气,有“中国气都”之称的美誉。天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与:
(提出问题):甲烷燃烧后生成哪些物质?
(查阅资料):含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
(猜想与假设):
甲
CO2
H2O
;
乙
CO
H2O;
丙
NH3
CO2
H2O;
丁
CO2
CO
H2O
。
你认为______同学的猜想是错误的,理由是_____________________________________。
(实验探究):为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:
二、A、B装置的顺序能否颠倒?(填“能"或“否”)_______。
三、实验中用纯净O2而不用空气的原因是____________________________________。
四、实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断_______同学猜想成立。
五、请写出B中澄清石灰水变浑浊、C中红色粉末变成黑色的化学方程式:
_______________________________________、
_______________________________________。
(反思与交流):为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是_____________________________________。
五、计算题
24.随着经济发展,能源和环境日益成为人们关注的焦点。
(1)煤、石油和_______通常成为化石燃料,燃煤发电时,将煤块粉碎成煤粉的目的是__________。
(2)人类目前所消耗的能源主要来自化石能源,化石能源的大量使用会产生CO2、SO2、NO2、CO等气体和粉尘,其中在大气中的含量不断上升,导致温室效应增强,全球气候变暖的是________,能形成酸雨的是_________(只写出一种)。
(3)氢能是一种既高效又干净的新能源。根据化学方程式,试计算4g氢气在氧气中燃烧,生成水的质量是多少________?(写出计算过程)
25.利用化学反应2Na+H22NaH可实现氢气的存储,计算230
g金属钠最多可吸收氢气的质量。
参考答案
1.A
2.B
3.D
4.D
5.D
6.D
7.B
8.C
9.D
10.C
11.C
12.D
13.B
14.B
15.
天然气
减少化石燃料燃烧(或开发新能源,出行时尽量乘坐公交车等)
1:1
4NH3+3O22N2+6H2O
16.过滤
SO2
煮沸
CO2
正
BC
17.氢气难溶于水
氢气的密度比空气小
氢气可燃性
1
3
2
1
3
1
3
18.(1)天然气;不可;(2)防止金属制品生锈.
(3)使可燃物的温度达到着火点;禁止吸烟.
19.(1)供给呼吸;混合物;(2)使煤粉与氧气充分接触;(3)分解反应;H2O+Cl2═HCl+HClO.
20.CuO
CO2
CO2+Ca(OH)2═CaCO3↓+H2O
还原性
21.C
CaCO3
CO2+H2O=H2CO3
22.a
探究铁在的干燥的空气(没有水)中是否容易生锈
氧气
水
金属表面打磨光亮
铝和铁表面均覆盖一层红色的物质
铝和铁的金属活动性比铜强
Fe+CuSO4=Cu+FeSO4(或2Al+3CuSO4=Al2(SO4)3+3Cu)
无法比较铝和铁的金属活动性
将相同状态的Fe、Cu、Al分别放入相同条件下的稀盐酸
Al、Fe表面有气泡产生且与稀盐酸反应时Al比Fe剧烈。Cu无明显现象发生
23.丙
质量守恒定律或化学反应前后元素的种类不变或反应前不含氮元素
否
空气中含有CO2
和H2O(干扰对产物的鉴别)
丁
CO2+Ca(OH)2=CaCO3↓+H2O
Fe2O3+3CO2Fe+3CO2
氧气充足
24.(1)天然气;增大与氧气接触面积,使燃烧更充分(2)CO2;SO2或NO2(3)36g
25.10
g
一、单选题
1.下列说法中正确的是( )
A.用活性炭可除去水中的色素和有异味的物质
B.人类利用的能量,都是通过化学反应获得的
C.灯帽盖灭酒精灯,是因为降低了可燃物温度
D.铁丝在氧气中燃烧,火星四射,生成红色固体
2.下列做法正确的是(
)
A.用活性炭净水器降低自来水的硬度
B.用干粉灭火器来扑灭汽油着火
C.用炉具清洁剂来除去衣服上的油污
D.用食醋涂抹蚊虫叮咬后的皮肤
3.近期,济南的天空常常出现美丽的泉城蓝,环境治理,成效明显。为了让天空更蓝,让泉城更美,下列做法中,不合理的是
A.把秸秆还田,禁止焚烧处理
B.将垃圾进行分类投放
C.短距离出行时,尽量步行或骑自行车
D.将工厂污水直接排入小清河
4.燃烧是一类重要的化学变化,下列关于燃烧的叙述正确的是(
)
A.燃烧一定有火焰
B.物质在有限的空间内燃烧,一定会发生爆炸
C.物质跟氧气的反应就是燃烧
D.使可燃物温度降低到着火点以下,可以灭火
5.2016年,170多个国家领导人齐聚纽约共同签署气候变化问题(巴黎协定)旨在全球控制碳排放,使全球经济可持续发展。下列在经济发展中某地区制定的措施违法了该项协定的是(
)
A.大力发展公共交通,减少私家车使用
B.开发风能和电能
C.植树造林
D.大力引进和发展大型火力发电厂
6.加油站、面粉加工厂、纺织厂、矿井都应粘贴的安全标志是( )
7.如图是金刚石、石墨的结构示意图,下列说法不正确的是
A.它们的化学式都可以用“C”表示
B.石墨转化成金刚石是物理变化
C.物理性质有很大差异的原因是原子的排列方式不同
D.化学性质相似是因为都是由碳原子直接构成的
8.安全意识是人类生存所必须具有的基本素质之一,下列实验操作比较安全的是
A.用鼻子凑到容器口直接嗅闻气体的气味
B.用嘴品尝药品的味道
C.进入久未开启的菜窖、干涸的深井和深洞前,要做灯火试验
D.发现家里煤气泄漏时,应立即打开排气扇
9.木柴燃烧时,要把木柴架空一些才能燃烧得更旺一些,这是因为(
)
A.木柴是可燃物
B.温度易达到着火点
C.散热的速率快
D.使柴火和空气充分接触
10.在汽车加油站见到的油罐车上,所贴的危险化学品图标是(
)
A.B.
C.
D.
11.依据下列实验所得到的结论准确的是
选项
A
B
C
D
实验设计
实验结论
二氧化碳与水反应生成碳酸
二氧化碳不支持燃烧、密度大于空气
可燃物燃烧温度需要达到着火点
既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
A.A
B.B
C.C
D.D
12.当前正是秋收时节,有些地方仍有就地焚烧秸秆的陈规陋习。焚烧秸秆可能导致的后果有:①引发火灾;
②能见度降低,引起交通事故;③诱发呼吸道疾病;④造成土地沙化等。其中主要因焚烧秸秆污染了空气而造成的后果是
A.①④
B.②④
C.①③
D.②③
13.如图,往容器内吹入一定量的空气,发生燃爆现象:硬纸板随热气流冲高,蜡烛熄灭。下列说法不正确的是
A.发生燃爆后体系的温度升高,氧气耗尽,蜡烛熄灭
B.蜡烛熄灭是因为蜡烛的着火点降低了
C.在有限的作业空间,要谨防可燃性粉尘发生燃爆事故
D.实验用的容器可用废旧矿泉水瓶,但不能用玻璃瓶
14.下列说法正确的是
A.水能灭火是由于和易燃物接触后,吸收了大量的热,从而把易燃物的着火点升高了
B.可燃物燃烧,需要与氧气接触,同时温度要达到可燃物的着火点
C.夏天,可燃物易着火是由于可燃物在夏天的着火点降低了
D.浸在沸水中的白磷不能燃烧,是因为温度没有达到白磷的着火点
二、填空题
15.能源、环境与人类的生活和社会经济发展密切相关。
(1)目前化石能源是人类的主要能源,煤、石油和_____是常见的三大化石能源。
(2)2016年12月中下旬我国出现了大面积的雾霾天气,目前普遍认为雾霾与PM2.5有密切关系。PM2.5主要来自化石燃料的燃烧和扬尘,对人体健康和空气质量的影响很大。请你就减少雾霾发生提出一条建议_______________。
(3)为减少污染、提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳与水的反应,其微观示意图如图所示,该反应生成物的分子个数比为_______。
(4)研究发现NH3燃烧的产物没有污染,产物为水和一种单质,且释放大量能量,有一定应用前景。请写出NH3燃烧的化学方程式______________________。
16.空气、水是我们赖以生存的重要资源。
(1)2020新冠病毒疫情爆发后,佩戴口罩可以有效预防病毒传播,利用的化学原理是___。
(2)环境问题越来越受到人们的关注,现在使用脱硫煤能减少__的排放,减轻酸雨的危害。
(3)饮用硬水对健康有害,生活中常用_____________方法降低水的硬度。
(4)自来水厂常用的一种消毒剂有效成分是次氯酸钙(化学式为Ca(C1O)2),它可发生如下的反应:,则X的化学式为_________________。
(5)电解水可制氢气。通电一段时间后,如图所示。电极X为电源的__________极。氢气作为新能源,其主要优点为__________(填序号)。
A
制取成本低
B
燃烧产物无污染
C
制备原料为水,来源广
D
贮存方便、安全
17.阅读下列资料,完成本题
1777年,英国化学家卡文迪许用金属锌和稀盐酸制得氢气,并把氢气收集到一个倒置在水槽中的装满水的瓶中.最初,氢气被用于飞艇和载人气球.1973年“兴登堡”号飞艇因为火花引起燃烧,从此,人们改用氦气填充飞艇.工业上氢气主要用来和氮气反应制取氨气;还可以用来制备金属,如三氧化钨和氢气加热得到水和金属钨.氢气燃烧时放出大量热,是等质量汽油燃烧放热的倍;氢气燃烧后的产物是水,不会造成污染,因此,氢气正在成为新兴的能源.工业上,人们常用水和高温的焦炭反应制得一氧化碳和氢气.
(1)物质的性质决定物质的应用,本文中介绍了一些氢气的应用知识,请写出相对应的氢气性质.(用文字表述)用倒置在水槽中的装满水的瓶子收集氢气:_;氢气被用于飞艇和载人气球:__;氢气正在成为新兴的能源:__.
(2)文中分别介绍了一种氢气的实验室制法和工业制法,请写出相应的化学方程式.工业:________;实验室:___.
(3)配平下列反应化学方程式
①___N2+___H2___NH3
②___WO3+___H2___W+___H2O
18.随着经济的发展,能源和环境成为人们关注的焦点.
(1)煤、石油和
常称为化石燃料,属于
(填“可”或“不可”)再生能源
(2)对金属资源的保护,可以采取的措施是
(一条即可)
(3)“火患猛于虎”我们不能忘记生活中那些惨痛的教训.新闻媒体报道的一些娱乐场所发生的多起火灾事故,均是由于随意丢弃未熄灭的烟头所导致.在这些事故中,从燃烧的条件考虑,烟头所起的作用是
;钋对上述事件,作为青少年,你应该怎么做
.
19.空气、水、燃料是人类赖以生存的自然资源.
(1)人类时刻都离不开空气,是因为空气中的氧气能
,空气属于
(填物质类别)。
(2)为了保护环境,用煤作燃料的煤炉要适当增加进风口,将煤粉吹起使之剧烈燃烧,请解释这种做法有利于节能的原因是
。
(3)自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
图乙所示反应的基本类型为
;
写出图甲所示反应的化学方程式
。
三、推断题
20.已知A、D均为无色无味的气体,B、C为黑色粉末,E为单质。A、B、C、D、E、F六种物质之间的转化关系如下图所示。请回答:
(1)B、D的化学式分别为____________、____________;
(2)反应②、③的化学方程式分别为________、________
(3)①③这两个反应说明A和C具有相同的化学性质为________(填:“可燃性”或“稳定性”或“还原性”或“氧化性”)。
21.ABCDE为初中常见到物质,B和E组成元素相同,它们之间存在如图所示的转化关系,请根据信息和图示回答问题(反应条件和部分生成物已略去)。
(1)A的化学式_____,D的化学式_____。
(2)写出E转化为C的化学方程式_____。
四、实验题
22.同学们已经学习了有关金属的一些知识,对金属的活动性顺序也有了一定的认识。请运用所学知识参与以下探究并回答相关问题:
(实验一)将4枚洁净无锈的铁钉分别放入图中a、b、c、d4支试管中。
上述实验中,______试管中的铁钉最易生锈。设计如图d实验的目的是______。铁生锈的主要原因是铁与_______、______等物质发生了复杂的化学反应。
(实验二)为了探究Fe、Cu、Al三种金属的活动性顺序,小宁同学做了如图所示的实验.
(1)实验时,为了除去铝和铁表面的氧化物或污物,在插入溶液前应将_____。
(2)实验时观察到的主要现象是_____。得出的结论是_____。写出其中一种金属与硫酸铜溶液反应的化学方程式______。
(3)小成同学认为小宁同学设计的实验不能达到实验目的,原因是____,因此另设计一个实验,才能得出正确的结论。请你设计一个实验并完成下表:
操作
现象
结论
____
____
三种金属活动性由强到弱的顺序是:Al、Fe、Cu
23.达州盛产天然气,有“中国气都”之称的美誉。天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与:
(提出问题):甲烷燃烧后生成哪些物质?
(查阅资料):含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。
(猜想与假设):
甲
CO2
H2O
;
乙
CO
H2O;
丙
NH3
CO2
H2O;
丁
CO2
CO
H2O
。
你认为______同学的猜想是错误的,理由是_____________________________________。
(实验探究):为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:
二、A、B装置的顺序能否颠倒?(填“能"或“否”)_______。
三、实验中用纯净O2而不用空气的原因是____________________________________。
四、实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断_______同学猜想成立。
五、请写出B中澄清石灰水变浑浊、C中红色粉末变成黑色的化学方程式:
_______________________________________、
_______________________________________。
(反思与交流):为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是_____________________________________。
五、计算题
24.随着经济发展,能源和环境日益成为人们关注的焦点。
(1)煤、石油和_______通常成为化石燃料,燃煤发电时,将煤块粉碎成煤粉的目的是__________。
(2)人类目前所消耗的能源主要来自化石能源,化石能源的大量使用会产生CO2、SO2、NO2、CO等气体和粉尘,其中在大气中的含量不断上升,导致温室效应增强,全球气候变暖的是________,能形成酸雨的是_________(只写出一种)。
(3)氢能是一种既高效又干净的新能源。根据化学方程式,试计算4g氢气在氧气中燃烧,生成水的质量是多少________?(写出计算过程)
25.利用化学反应2Na+H22NaH可实现氢气的存储,计算230
g金属钠最多可吸收氢气的质量。
参考答案
1.A
2.B
3.D
4.D
5.D
6.D
7.B
8.C
9.D
10.C
11.C
12.D
13.B
14.B
15.
天然气
减少化石燃料燃烧(或开发新能源,出行时尽量乘坐公交车等)
1:1
4NH3+3O22N2+6H2O
16.过滤
SO2
煮沸
CO2
正
BC
17.氢气难溶于水
氢气的密度比空气小
氢气可燃性
1
3
2
1
3
1
3
18.(1)天然气;不可;(2)防止金属制品生锈.
(3)使可燃物的温度达到着火点;禁止吸烟.
19.(1)供给呼吸;混合物;(2)使煤粉与氧气充分接触;(3)分解反应;H2O+Cl2═HCl+HClO.
20.CuO
CO2
CO2+Ca(OH)2═CaCO3↓+H2O
还原性
21.C
CaCO3
CO2+H2O=H2CO3
22.a
探究铁在的干燥的空气(没有水)中是否容易生锈
氧气
水
金属表面打磨光亮
铝和铁表面均覆盖一层红色的物质
铝和铁的金属活动性比铜强
Fe+CuSO4=Cu+FeSO4(或2Al+3CuSO4=Al2(SO4)3+3Cu)
无法比较铝和铁的金属活动性
将相同状态的Fe、Cu、Al分别放入相同条件下的稀盐酸
Al、Fe表面有气泡产生且与稀盐酸反应时Al比Fe剧烈。Cu无明显现象发生
23.丙
质量守恒定律或化学反应前后元素的种类不变或反应前不含氮元素
否
空气中含有CO2
和H2O(干扰对产物的鉴别)
丁
CO2+Ca(OH)2=CaCO3↓+H2O
Fe2O3+3CO2Fe+3CO2
氧气充足
24.(1)天然气;增大与氧气接触面积,使燃烧更充分(2)CO2;SO2或NO2(3)36g
25.10
g
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
