人教版化学九年级下册第九单元 溶液测试题(含答案)
文档属性
| 名称 | 人教版化学九年级下册第九单元 溶液测试题(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 235.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-04 00:00:00 | ||
图片预览


文档简介
《溶液》测试题
一、单选题
1.洗涤在生活、生产中不可缺少。下列洗涤方法中利用了乳化原理的是()
A.用汽油洗去手上的油污
B.用洗洁精洗去餐具上的油污
C.用酒精洗去试管中的碘
D.用水洗去手上的泥灰
2.如图是a、b、
c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是
A.a的溶解度大于b的溶解度
B.P点表示t1°C时b、c两物质溶解度相等
C.将t1°C饱和的c溶液升温到t2°C,得到的是不饱和溶液
D.将t2°C,a、b、c三种物质的饱和溶液降温到t1°C时,所得溶液中溶质质量分数由大到小的顺序为:
b>a>c
3.下列对溶液的叙述,正确的是
A.无色透明的液体一定是溶液
B.水是一切溶液的溶剂
C.溶液中只能含有一种溶质
D.将饱和溶液降温后,不一定有晶体析出
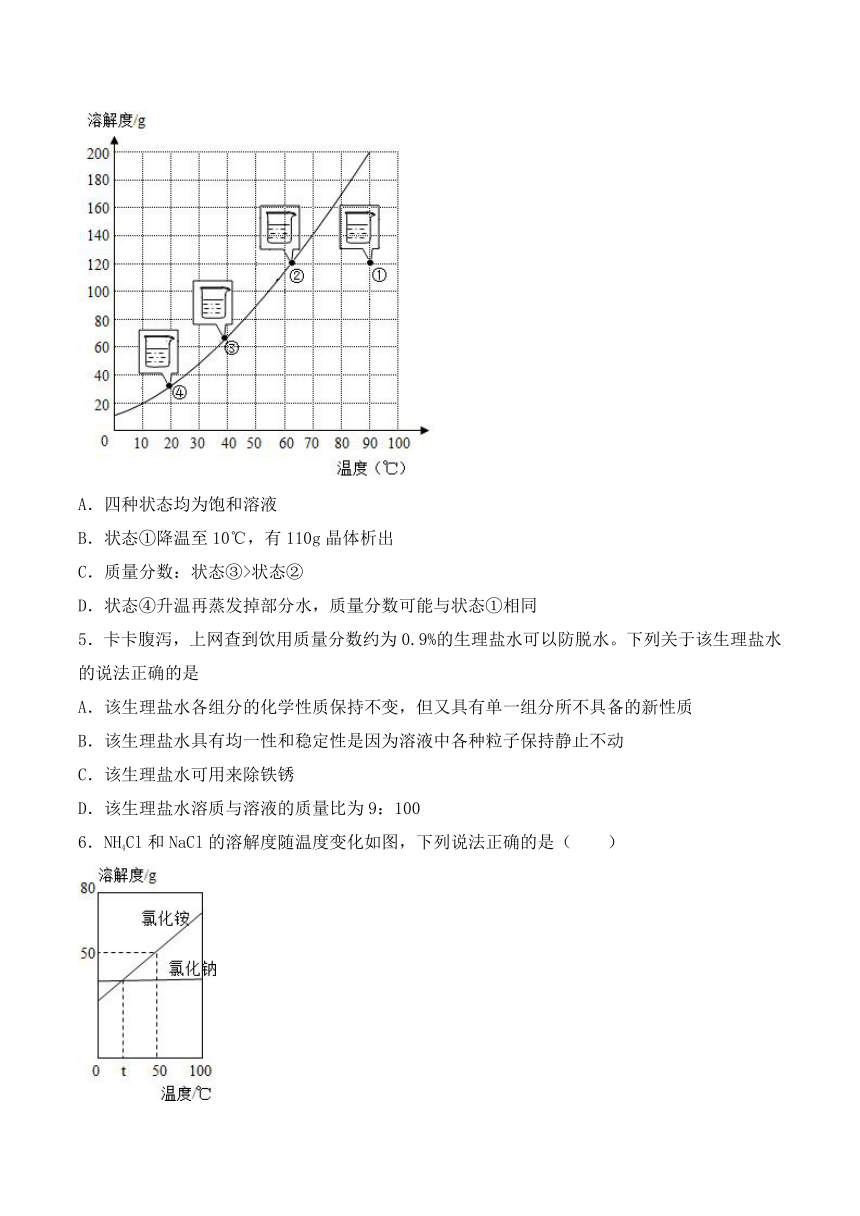
4.某固体物质的溶解度曲线如图所示,在100g水中加入120g固体,充分搅拌,在不同温度下存在①②③④四种状态。对这四种状态的描述正确的是( )
A.四种状态均为饱和溶液
B.状态①降温至10℃,有110g晶体析出
C.质量分数:状态③>状态②
D.状态④升温再蒸发掉部分水,质量分数可能与状态①相同
5.卡卡腹泻,上网查到饮用质量分数约为0.9%的生理盐水可以防脱水。下列关于该生理盐水的说法正确的是
A.该生理盐水各组分的化学性质保持不变,但又具有单一组分所不具备的新性质
B.该生理盐水具有均一性和稳定性是因为溶液中各种粒子保持静止不动
C.该生理盐水可用来除铁锈
D.该生理盐水溶质与溶液的质量比为9:100
6.NH4Cl和NaCl的溶解度随温度变化如图,下列说法正确的是( )
A.NH4Cl的溶解度一定大于NaCl
B.将NaCl溶液降温一定会有NaCl固体析出
C.50℃时NH4Cl饱和溶液的溶质质量分数为50%
D.将t℃时,NH4Cl和NaCl的饱和溶液加热至50℃,两溶液的溶质质量分数相等
7.
取70g某温度下的氯化钾饱和溶液,将其恒温蒸发10g水,析出4g氯化钾固体,则剩余溶液中所含溶质质量为
A.16g
B.20g
C.24g
D.56g
8.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏大的是
①称量的氯化钠固体中含有不溶性杂质;②用量筒量取水时俯视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.①②
B.②③
C.②④
D.③④
9.生活中处处蕴含着化学知识,下列说法错误的是
A.用碳素笔书写档案是利用了碳在常温下化学性质稳定
B.用洗洁精除油污利用的原理是乳化油污
C.用完煤气后关闭阀门利用的灭火原理是将可燃物清除
D.用石墨作电池的电极是利用了石墨质地坚硬的性质
10.下列关于溶液的说法中,正确的是( )
A.溶液一定是均一、稳定的混合物
B.溶液中的溶质只能是固体,不能是液体或气体
C.某温度下的饱和溶液不能再溶解任何物质
D.氢氧化钠溶解在水中会使溶液温度降低
11.常熟地处江南,水资源总量较丰富,下列有关水的说法正确的是
A.自然界的水中硬水属于混合物,软水属于纯净物
B.水由氢原子和氧原子构成
C.水中加入一定量的蔗糖可以明显增强其导电性
D.自来水生产过程中加入明矶的作用是凝聚水中悬浮颗粒,促进其沉降
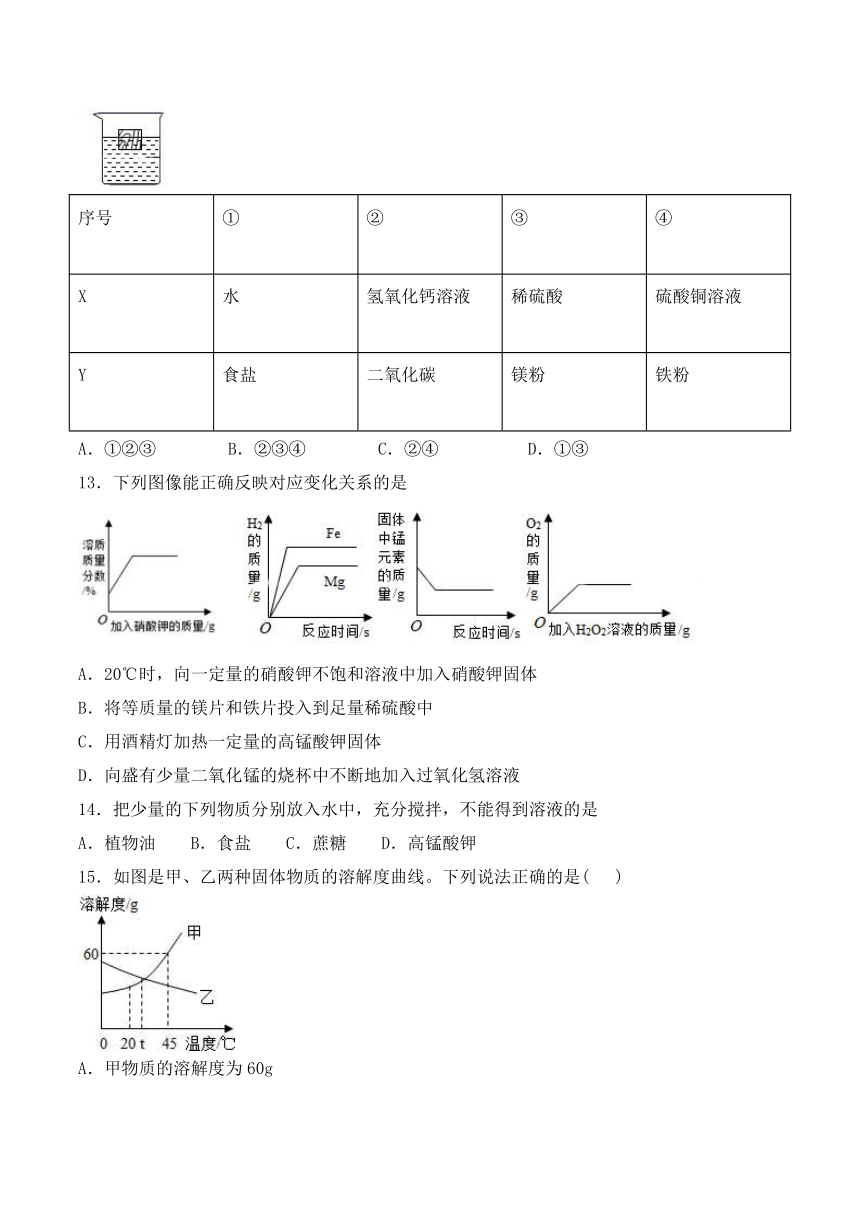
12.如图所示,一木块漂浮于X上,向X中缓缓加入(或通入)少量物质Y后,木块逐渐上浮,则X与Y可能是(溶液的体积变化忽略不计)
序号
①
②
③
④
X
水
氢氧化钙溶液
稀硫酸
硫酸铜溶液
Y
食盐
二氧化碳
镁粉
铁粉
A.①②③
B.②③④
C.②④
D.①③
13.下列图像能正确反映对应变化关系的是
A.20℃时,向一定量的硝酸钾不饱和溶液中加入硝酸钾固体
B.将等质量的镁片和铁片投入到足量稀硫酸中
C.用酒精灯加热一定量的高锰酸钾固体
D.向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液
14.把少量的下列物质分别放入水中,充分搅拌,不能得到溶液的是
A.植物油
B.食盐
C.蔗糖
D.高锰酸钾
15.如图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是(
)
A.甲物质的溶解度为60g
B.升高温度可使不饱和的甲溶液变为饱和
C.t℃时,甲、乙两物质的溶解度相等
D.乙物质的溶解度随温度的升高而增大
二、填空题
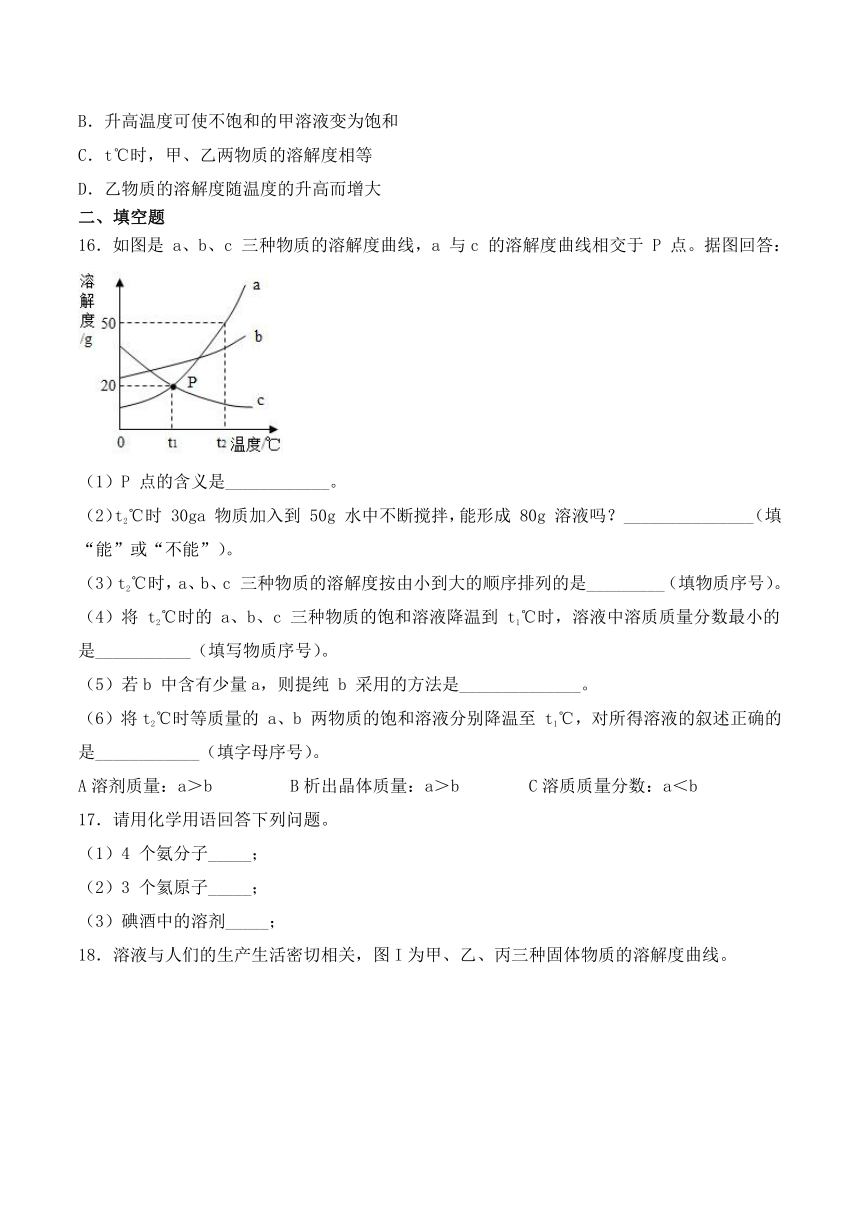
16.如图是
a、b、c
三种物质的溶解度曲线,a
与c
的溶解度曲线相交于
P
点。据图回答:
(1)P
点的含义是____________。
(2)t2℃时
30ga
物质加入到
50g
水中不断搅拌,能形成
80g
溶液吗?_______________(填“能”或“不能”)。
(3)t2℃时,a、b、c
三种物质的溶解度按由小到大的顺序排列的是_________(填物质序号)。
(4)将
t2℃时的
a、b、c
三种物质的饱和溶液降温到
t1℃时,溶液中溶质质量分数最小的是___________(填写物质序号)。
(5)若b
中含有少量a,则提纯
b
采用的方法是______________。
(6)将t2℃时等质量的
a、b
两物质的饱和溶液分别降温至
t1℃,对所得溶液的叙述正确的是____________(填字母序号)。
A溶剂质量:a>b
B析出晶体质量:a>b
C溶质质量分数:a<b
17.请用化学用语回答下列问题。
(1)4
个氨分子_____;
(2)3
个氦原子_____;
(3)碘酒中的溶剂_____;
18.溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。
(1)t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是____。
(2)某同学按图所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是___(填字母)。
(3)t3℃时要把150g甲物质的饱和溶液中稀释成质量分数为20%的溶液,需加入水的质量为____克。
19.水是生命之源,请回答有关水的下列问题:
(1)电解水实验如图所示:
①与②中所得气体的体积比约为_____。该反应的微观示意图如下,请在方框内补全相应微粒的示意图_____。
(2)“生命吸管”是一种便携式户外净水器。其净水原理如下图:
①过滤网可去除_____(填“可溶性”或“难溶性”)杂质。
②抗菌活性复合滤料中有活性炭、离子交换树脂等。活性炭所起的是_____作用。离子交换树脂能去除原水中的钙离子,钙离子的符号是_____。
(3)如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
①p点的含义是_____。
②室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的并NH4NO3并搅拌,试管内可观察到的现象是_____。
③将t3℃时A、B、C三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的由大到小的关系是_____。
20.水是一种重要的物质,在实验室和日常生活中有着十分重要的作用.请根据下列提示简要回答相关问题:
(1)根据图1和图2回答下列问题.
①分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母序号)________;
A
水分子不断运动
B
水分子之间间隔不变
C
氢、氧原子不发生改变
D
水分子可以保持水的物理性质
②图2的试管A中的气体的化学式是________,试管B中气体的检验方法是________;电解水的化学方程式为________。
(2)硬水会给生产和生活带来许多不便,生活中可用________的方法降低它的硬度;
(3)农业和园林浇灌植物时,将大水漫灌改为喷灌、滴灌的目的是________;
(4)生活离不开水,净化水的知识在日常生活中有着广泛的应用.
①用纱网可将茶叶与茶水分离,便于饮用,其应用的分离方法在化学上称为________.
②自来水厂用二氧化氯消毒杀菌,二氧化氯的化学式为________.
③自来水厂主要通过
①吸附沉淀(用明矾)
②投药消毒(用漂白粉等)
③静置沉淀
④过滤等对自然水进行净化,其合理的步骤顺序是________(填序号);
(5)实验室有一瓶质量分数为36%的浓盐酸,现要配制200g7.3%的稀盐酸,实验步骤有________、________、________装瓶贴标签等.
(6)用该稀盐酸100g和6g含杂质的铁粉完全反应,得到溶液的溶质质量分数是多少________?(杂质不和盐酸反应,也不溶于水)(计算结果保留一位小数)
三、推断题
21.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。其流程简图和部分物质的溶解度曲线如下:
已知:①母液中有一种铵态氮肥
②
请回答下列问题:
(1)操作a的名称是_____。
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是_____,从图2中还能获得的一条信息是_____。
(3)图1中得到的母液中一定含有的阳离子是_____
(填离子符号),
流程中可以循环使用的物质是_____。
(4)从图2可以看出温度高于60°C,NaHCO3的溶解度曲线“消失”了,其原因可能是_____。
22.A~H是初中化学中的常见物质,A、B、C含有相同的金属元素,B固体的溶解度随温度的升高而减小;C、D、E为氧化物;
F、H为非金属单质,G、I为金属单质且I单质显红色。图中“﹣”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物或生成物已略去。
(1)写化学式:B_____、E_____。
(2)写出D﹣F反应的化学方程式_____,该反应过程_____热量(填“放出”或“吸收”)。
(3)写出G→I反应的化学方程式_____,该反应的基本类型是_____。
四、实验题
23.实验室配制50g16%的氯化钠溶液的操作如下图所示。
请回答:
步骤①中玻璃棒的作用是_____;该实验的正确操作顺序为_____(填序号)。
24.小丽在配制一定溶质质量分数的氯化钠溶液时,计算所需氯化钠的质量和水的体积后,进行了如图所示的实验:
请回答:
(1)操作中不规范的步骤是_____(填序号)。
(2)改正后,图示实验中正确的操作顺序是_____(填字号)。
(3)⑤中玻璃棒作用是_____。
(4)小丽发现图示实验操作步骤不完整,应补充的是_____。
五、计算题
25.“黄铜”是铜锌合金,具有较机械性能,比纯铜耐腐蚀,街头许多“金色”饰品就是用它来制作的。现将20g黄铜投入100g稀硫酸中,恰好完全反应,剩余的溶液和残余固体总质量为119.8g。已知:Zn+H2
SO4==ZnSO4+
H2↑。
请计算:
(1)产生氢气的质量为________g。
(2)这种黄铜中铜的质量分数为多少?
(3)所用稀硫酸的溶质质量分数是多少?
26.有一瓶标签破损的稀盐酸如图1,为测定其溶质质量分数,取出25g稀盐酸样品,加入足量铝片(表面被氧化)。使其充分反应,生成氢气的质量与反应的稀盐酸溶液的质量关系如图2。请计算该稀盐酸溶液的溶质质量分数___________,并在新标签的横线上填写稀盐酸溶液的溶质质量分数。
参考答案
1.B
2.D
3.D
4.D
5.A
6.D
7.A
8.B
9.D
10.A
11.D
12.D
13.A
14.A
15.C
16.t1℃时,a、c的溶解度相等
不能
c<
b<
a
c
蒸发结晶
BC
17.4NH3
3He
C2H5OH
18.丙>乙>甲
B
100
19.1∶2
难溶性
吸附
Ca2+
t2℃时A和B的溶解度相等
有固体析出
B>A>C
20.AC
H2
带火星的木条复燃
2H2O2H2↑+O2↑
煮沸
节约用水
过滤
ClO2
③①④②
计算
量取
稀释
12.0%
21.过滤
此温度下碳酸氢钠的溶解度较小
氯化铵的溶解度受温度的影响较大
Na+、NH4+
CO2
温度高于60℃时,碳酸氢钠开始分解
22.Ca(OH)2;
H2O;
CO2+C2CO;
吸收;
Fe+CuSO4=Cu+FeSO4;
置换反应;
23.加快溶解
②③①
24.③
②①④③⑤
搅拌,加速溶解
装瓶贴标签
25.(1)0.2;(2)67.5%;(3)9.8%
26.4.9%;
一、单选题
1.洗涤在生活、生产中不可缺少。下列洗涤方法中利用了乳化原理的是()
A.用汽油洗去手上的油污
B.用洗洁精洗去餐具上的油污
C.用酒精洗去试管中的碘
D.用水洗去手上的泥灰
2.如图是a、b、
c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是
A.a的溶解度大于b的溶解度
B.P点表示t1°C时b、c两物质溶解度相等
C.将t1°C饱和的c溶液升温到t2°C,得到的是不饱和溶液
D.将t2°C,a、b、c三种物质的饱和溶液降温到t1°C时,所得溶液中溶质质量分数由大到小的顺序为:
b>a>c
3.下列对溶液的叙述,正确的是
A.无色透明的液体一定是溶液
B.水是一切溶液的溶剂
C.溶液中只能含有一种溶质
D.将饱和溶液降温后,不一定有晶体析出
4.某固体物质的溶解度曲线如图所示,在100g水中加入120g固体,充分搅拌,在不同温度下存在①②③④四种状态。对这四种状态的描述正确的是( )
A.四种状态均为饱和溶液
B.状态①降温至10℃,有110g晶体析出
C.质量分数:状态③>状态②
D.状态④升温再蒸发掉部分水,质量分数可能与状态①相同
5.卡卡腹泻,上网查到饮用质量分数约为0.9%的生理盐水可以防脱水。下列关于该生理盐水的说法正确的是
A.该生理盐水各组分的化学性质保持不变,但又具有单一组分所不具备的新性质
B.该生理盐水具有均一性和稳定性是因为溶液中各种粒子保持静止不动
C.该生理盐水可用来除铁锈
D.该生理盐水溶质与溶液的质量比为9:100
6.NH4Cl和NaCl的溶解度随温度变化如图,下列说法正确的是( )
A.NH4Cl的溶解度一定大于NaCl
B.将NaCl溶液降温一定会有NaCl固体析出
C.50℃时NH4Cl饱和溶液的溶质质量分数为50%
D.将t℃时,NH4Cl和NaCl的饱和溶液加热至50℃,两溶液的溶质质量分数相等
7.
取70g某温度下的氯化钾饱和溶液,将其恒温蒸发10g水,析出4g氯化钾固体,则剩余溶液中所含溶质质量为
A.16g
B.20g
C.24g
D.56g
8.实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏大的是
①称量的氯化钠固体中含有不溶性杂质;②用量筒量取水时俯视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A.①②
B.②③
C.②④
D.③④
9.生活中处处蕴含着化学知识,下列说法错误的是
A.用碳素笔书写档案是利用了碳在常温下化学性质稳定
B.用洗洁精除油污利用的原理是乳化油污
C.用完煤气后关闭阀门利用的灭火原理是将可燃物清除
D.用石墨作电池的电极是利用了石墨质地坚硬的性质
10.下列关于溶液的说法中,正确的是( )
A.溶液一定是均一、稳定的混合物
B.溶液中的溶质只能是固体,不能是液体或气体
C.某温度下的饱和溶液不能再溶解任何物质
D.氢氧化钠溶解在水中会使溶液温度降低
11.常熟地处江南,水资源总量较丰富,下列有关水的说法正确的是
A.自然界的水中硬水属于混合物,软水属于纯净物
B.水由氢原子和氧原子构成
C.水中加入一定量的蔗糖可以明显增强其导电性
D.自来水生产过程中加入明矶的作用是凝聚水中悬浮颗粒,促进其沉降
12.如图所示,一木块漂浮于X上,向X中缓缓加入(或通入)少量物质Y后,木块逐渐上浮,则X与Y可能是(溶液的体积变化忽略不计)
序号
①
②
③
④
X
水
氢氧化钙溶液
稀硫酸
硫酸铜溶液
Y
食盐
二氧化碳
镁粉
铁粉
A.①②③
B.②③④
C.②④
D.①③
13.下列图像能正确反映对应变化关系的是
A.20℃时,向一定量的硝酸钾不饱和溶液中加入硝酸钾固体
B.将等质量的镁片和铁片投入到足量稀硫酸中
C.用酒精灯加热一定量的高锰酸钾固体
D.向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液
14.把少量的下列物质分别放入水中,充分搅拌,不能得到溶液的是
A.植物油
B.食盐
C.蔗糖
D.高锰酸钾
15.如图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是(
)
A.甲物质的溶解度为60g
B.升高温度可使不饱和的甲溶液变为饱和
C.t℃时,甲、乙两物质的溶解度相等
D.乙物质的溶解度随温度的升高而增大
二、填空题
16.如图是
a、b、c
三种物质的溶解度曲线,a
与c
的溶解度曲线相交于
P
点。据图回答:
(1)P
点的含义是____________。
(2)t2℃时
30ga
物质加入到
50g
水中不断搅拌,能形成
80g
溶液吗?_______________(填“能”或“不能”)。
(3)t2℃时,a、b、c
三种物质的溶解度按由小到大的顺序排列的是_________(填物质序号)。
(4)将
t2℃时的
a、b、c
三种物质的饱和溶液降温到
t1℃时,溶液中溶质质量分数最小的是___________(填写物质序号)。
(5)若b
中含有少量a,则提纯
b
采用的方法是______________。
(6)将t2℃时等质量的
a、b
两物质的饱和溶液分别降温至
t1℃,对所得溶液的叙述正确的是____________(填字母序号)。
A溶剂质量:a>b
B析出晶体质量:a>b
C溶质质量分数:a<b
17.请用化学用语回答下列问题。
(1)4
个氨分子_____;
(2)3
个氦原子_____;
(3)碘酒中的溶剂_____;
18.溶液与人们的生产生活密切相关,图I为甲、乙、丙三种固体物质的溶解度曲线。
(1)t1℃时甲、乙、丙三种物质的溶解度由大到小的顺序是____。
(2)某同学按图所示进行实验,得到相应温度下的A、B、C三种溶液,其中属于饱和溶液的是___(填字母)。
(3)t3℃时要把150g甲物质的饱和溶液中稀释成质量分数为20%的溶液,需加入水的质量为____克。
19.水是生命之源,请回答有关水的下列问题:
(1)电解水实验如图所示:
①与②中所得气体的体积比约为_____。该反应的微观示意图如下,请在方框内补全相应微粒的示意图_____。
(2)“生命吸管”是一种便携式户外净水器。其净水原理如下图:
①过滤网可去除_____(填“可溶性”或“难溶性”)杂质。
②抗菌活性复合滤料中有活性炭、离子交换树脂等。活性炭所起的是_____作用。离子交换树脂能去除原水中的钙离子,钙离子的符号是_____。
(3)如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
①p点的含义是_____。
②室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的并NH4NO3并搅拌,试管内可观察到的现象是_____。
③将t3℃时A、B、C三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的由大到小的关系是_____。
20.水是一种重要的物质,在实验室和日常生活中有着十分重要的作用.请根据下列提示简要回答相关问题:
(1)根据图1和图2回答下列问题.
①分析图1可知,在水蒸发的过程中,下列说法正确的是(填字母序号)________;
A
水分子不断运动
B
水分子之间间隔不变
C
氢、氧原子不发生改变
D
水分子可以保持水的物理性质
②图2的试管A中的气体的化学式是________,试管B中气体的检验方法是________;电解水的化学方程式为________。
(2)硬水会给生产和生活带来许多不便,生活中可用________的方法降低它的硬度;
(3)农业和园林浇灌植物时,将大水漫灌改为喷灌、滴灌的目的是________;
(4)生活离不开水,净化水的知识在日常生活中有着广泛的应用.
①用纱网可将茶叶与茶水分离,便于饮用,其应用的分离方法在化学上称为________.
②自来水厂用二氧化氯消毒杀菌,二氧化氯的化学式为________.
③自来水厂主要通过
①吸附沉淀(用明矾)
②投药消毒(用漂白粉等)
③静置沉淀
④过滤等对自然水进行净化,其合理的步骤顺序是________(填序号);
(5)实验室有一瓶质量分数为36%的浓盐酸,现要配制200g7.3%的稀盐酸,实验步骤有________、________、________装瓶贴标签等.
(6)用该稀盐酸100g和6g含杂质的铁粉完全反应,得到溶液的溶质质量分数是多少________?(杂质不和盐酸反应,也不溶于水)(计算结果保留一位小数)
三、推断题
21.我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。其流程简图和部分物质的溶解度曲线如下:
已知:①母液中有一种铵态氮肥
②
请回答下列问题:
(1)操作a的名称是_____。
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是_____,从图2中还能获得的一条信息是_____。
(3)图1中得到的母液中一定含有的阳离子是_____
(填离子符号),
流程中可以循环使用的物质是_____。
(4)从图2可以看出温度高于60°C,NaHCO3的溶解度曲线“消失”了,其原因可能是_____。
22.A~H是初中化学中的常见物质,A、B、C含有相同的金属元素,B固体的溶解度随温度的升高而减小;C、D、E为氧化物;
F、H为非金属单质,G、I为金属单质且I单质显红色。图中“﹣”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物或生成物已略去。
(1)写化学式:B_____、E_____。
(2)写出D﹣F反应的化学方程式_____,该反应过程_____热量(填“放出”或“吸收”)。
(3)写出G→I反应的化学方程式_____,该反应的基本类型是_____。
四、实验题
23.实验室配制50g16%的氯化钠溶液的操作如下图所示。
请回答:
步骤①中玻璃棒的作用是_____;该实验的正确操作顺序为_____(填序号)。
24.小丽在配制一定溶质质量分数的氯化钠溶液时,计算所需氯化钠的质量和水的体积后,进行了如图所示的实验:
请回答:
(1)操作中不规范的步骤是_____(填序号)。
(2)改正后,图示实验中正确的操作顺序是_____(填字号)。
(3)⑤中玻璃棒作用是_____。
(4)小丽发现图示实验操作步骤不完整,应补充的是_____。
五、计算题
25.“黄铜”是铜锌合金,具有较机械性能,比纯铜耐腐蚀,街头许多“金色”饰品就是用它来制作的。现将20g黄铜投入100g稀硫酸中,恰好完全反应,剩余的溶液和残余固体总质量为119.8g。已知:Zn+H2
SO4==ZnSO4+
H2↑。
请计算:
(1)产生氢气的质量为________g。
(2)这种黄铜中铜的质量分数为多少?
(3)所用稀硫酸的溶质质量分数是多少?
26.有一瓶标签破损的稀盐酸如图1,为测定其溶质质量分数,取出25g稀盐酸样品,加入足量铝片(表面被氧化)。使其充分反应,生成氢气的质量与反应的稀盐酸溶液的质量关系如图2。请计算该稀盐酸溶液的溶质质量分数___________,并在新标签的横线上填写稀盐酸溶液的溶质质量分数。
参考答案
1.B
2.D
3.D
4.D
5.A
6.D
7.A
8.B
9.D
10.A
11.D
12.D
13.A
14.A
15.C
16.t1℃时,a、c的溶解度相等
不能
c<
b<
a
c
蒸发结晶
BC
17.4NH3
3He
C2H5OH
18.丙>乙>甲
B
100
19.1∶2
难溶性
吸附
Ca2+
t2℃时A和B的溶解度相等
有固体析出
B>A>C
20.AC
H2
带火星的木条复燃
2H2O2H2↑+O2↑
煮沸
节约用水
过滤
ClO2
③①④②
计算
量取
稀释
12.0%
21.过滤
此温度下碳酸氢钠的溶解度较小
氯化铵的溶解度受温度的影响较大
Na+、NH4+
CO2
温度高于60℃时,碳酸氢钠开始分解
22.Ca(OH)2;
H2O;
CO2+C2CO;
吸收;
Fe+CuSO4=Cu+FeSO4;
置换反应;
23.加快溶解
②③①
24.③
②①④③⑤
搅拌,加速溶解
装瓶贴标签
25.(1)0.2;(2)67.5%;(3)9.8%
26.4.9%;
同课章节目录
