2021年人教版初中九年级化学第二学期课题 2 金属的化学性质同步练习卷(无答案)
文档属性
| 名称 | 2021年人教版初中九年级化学第二学期课题 2 金属的化学性质同步练习卷(无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 170.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-05 00:00:00 | ||
图片预览




文档简介
2021年人教版初中九年级化学第二学期第8单元《8.2金属的化学性质》同步练习卷
一.选择题(共18小题)
1.推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是( )
A.稀有气体可作保护气,可做保护气的一定是稀有气体
B.单质是由一种元素组成的物质,由一种元素组成的物质一定是单质
C.性质活泼的金属在空气中容易被腐蚀,铝在空气中不易被腐蚀是因为其性质不活泼
D.人类需要的大部分能量是由化学反应产生的,但不是所有化学反应都放出热量
2.某同学为验证镁、铜、银三种金属的活动性顺序,以下四种实验方案中能达到目的的是( )
A.Mg丝、Cu丝、AgNO3溶液
B.Mg丝、Cu丝、Ag丝、稀盐酸
C.MgSO4溶液、CuSO4溶液、Ag丝
D.Mg丝、Ag丝、CuSO4溶液
3.下列关于资源、能源、环保方面的叙述正确的是( )
A.空气中的各种成分作为原料广泛用于生产化工产品、运输等领域
B.地表的咸水约占地球总水量的96.5%
C.地球上的金属资源都是以金属矿物的形式存在的
D.煤、石油、沼气都属于化石燃料
4.下列有关资源、能源的叙述错误的是( )
A.金属资源广泛地存在于地壳和海洋中,地壳中铁元素含量最高
B.利用石油中各成分的沸点不同,将它们分离,可得到汽油、煤油、石蜡等不同的产品
C.稀土金属有“工业的维生素”的美誉,是不可再生的重要战略资源
D.开发利用太阳能、核能、氢能、风能、地热能等能源,可适当节省化石燃料
5.CO和C分别跟CuO反应,若生成等质量的Cu,则反应中消耗的CO和C的质量比为(假定CO全部用于还原CuO)( )
A.1:1
B.7:3
C.14:3
D.1:2
6.我国古代的湿法冶金术是世界闻名的,我国在世界上最先应用湿法冶炼的金属是( )
A.Fe
B.Cu
C.Ag
D.Hg
7.下列不属于金属材料的是( )
A.不锈钢菜刀
B.铝合金
C.铜导线
D.氧化铁
8.下列不属于金属材料的是( )
A.东汉晚期马踏飞燕的青铜
B.
纳米铜
C.河北沧州铁狮子的生铁
D.
铁矿石
9.关于物质的用途,下列说法错误的是( )
A.CO炼铁时表现还原性,发生了还原反应
B.活性炭净水利用了其吸附性
C.氮气作保护气利用了其稳定性
D.洗洁精洗涤油污体现了其乳化作用
10.下列实验现象描述正确的是( )
A.磷在氧气中燃烧,产生大量白色烟雾
B.硫在空气中燃烧,发出明亮的蓝紫色火焰
C.一氧化碳通入灼热的氧化铁,红棕色粉末变黑
D.铁钉加入氯化铜溶液中,表面有红色的铜生成
11.下列关于金属材料的说法中,不正确的是( )
A.生铁、硬铝、黄铜都属于合金
B.铜有良好的导电性,因而大量用于制作电线
C.己生锈的铁不具有回收的价值
D.通过高炉炼得的铁含有杂质
12.下列关于铁的说法正确的是( )
A.工业炼铁得到含碳量较低的钢
B.自然界大部分的铁以单质形式存在
C.铁是地壳中含量最丰富的金属元素
D.合金许多性能和组成它们的纯金属不同
13.金属冶炼工业中常用化学性质比较活泼的金属还原出相对不活泼的金属.如:用铝和二氧化锰在高温下反应,可以制取金属锰.反应的化学方程式为:aAl+bMnO2cAl2O3+dMn下列说法中,错误的是( )
A.b=3
B.MnO2中锰元素质量分数为63.2%
C.Al2O3中铝、氧元素的质量比为9:8
D.在上述反应中,MnO2起催化作用
14.距今2000余年前的西汉时期,就有“曾青得铁则化为铜”的记述,这是现代湿法冶金技术的先驱,从现代的科学观点理解,“曾青”应赋予的最恰当的涵义是( )
A.铜单质
B.硫酸铜溶液
C.铜的化合物
D.可溶性铜盐的溶液
15.用1000t含铁56%的赤铁矿石(主要成分是氧化铁),理论上可以炼出含铁96%的生铁的质量是( )
A.583.3
t
B.560
t
C.408.3
t
D.392
t
16.钢铁厂购进含氧化铁80%的赤铁矿1000t,可以炼取含杂质4%的生铁的质量( )
A.560t
B.583t
C.800t
D.1400t
17.下列化学反应中属于置换反应的是( )
A.3Fe+2O2
Fe3O4
B.CO+CuO
Cu+CO2
C.Zn+CuSO4=ZnSO4+Cu
D.SO2+2NaOH=Na2SO3+H2O
18.下列实验方案可行的是( )
①将NaCl和KNO3的混合物溶于水,再用过滤的方法将它们分离
②往铜盐溶液中加入铁粉获得少量铜
③将氧气、二氧化碳的混合气体通过盛有足量灼热的铜网的试管获得纯净二氧化碳
④用稀盐酸除去混在铜粉中的镁粉和铝粉.
A.②③④
B.②④
C.③④
D.①③④
二.填空题(共10小题)
19.镁在空气中燃烧生成氧化镁和氮化镁(其中氮为﹣3价),氮化镁与水反应生成氢氧化镁和氨气.
(1)写出氮化镁与水反应的化学方程式
;
(2)12克镁在空气中燃烧所生成的产物的总质量
(填>、<或等于多少克);
(3)已知氮化镁是一种黄色的固体.根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更易与空气中的①
化合,理由是生成物②
.
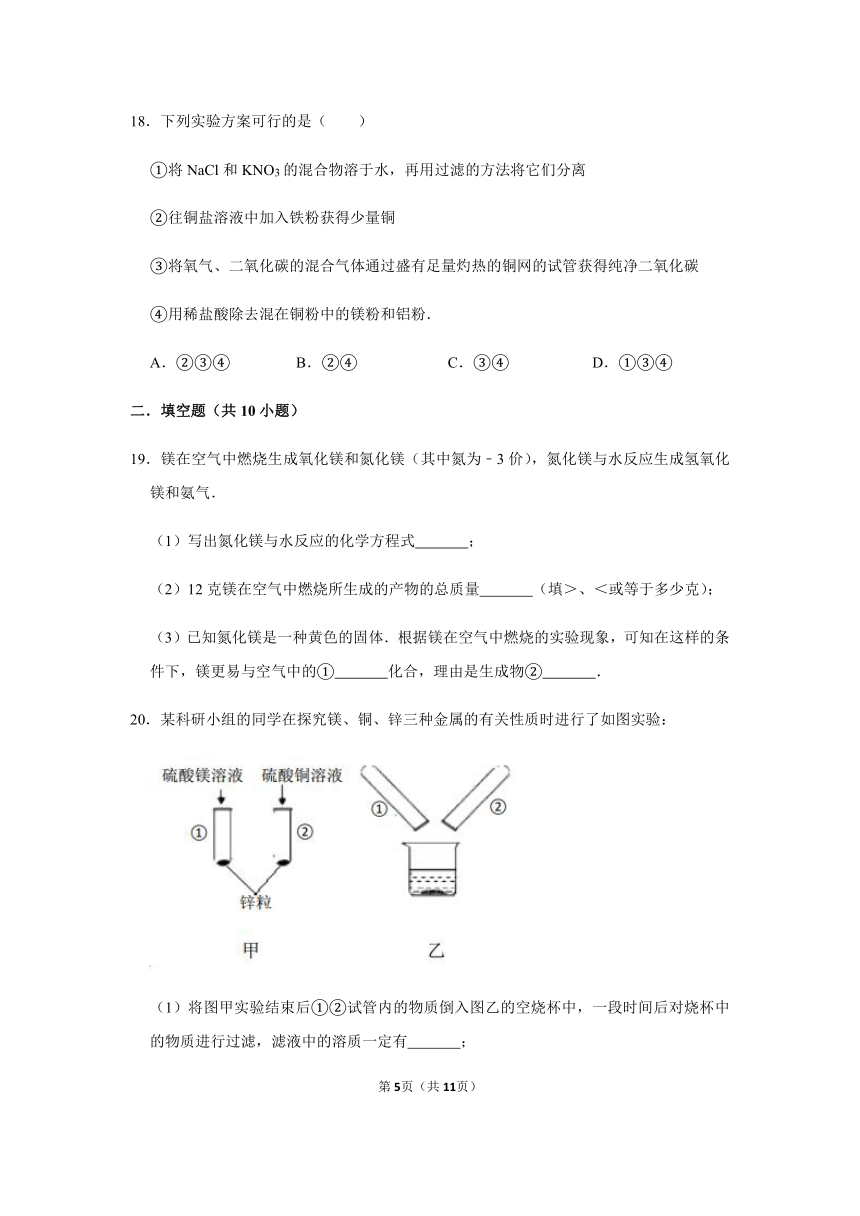
20.某科研小组的同学在探究镁、铜、锌三种金属的有关性质时进行了如图实验:
(1)将图甲实验结束后①②试管内的物质倒入图乙的空烧杯中,一段时间后对烧杯中的物质进行过滤,滤液中的溶质一定有
;
(2)若要验证镁、锌、铜金属活动性顺序,还可以用一种试剂直接与三种金属反应就能达到目的,该试剂可以是
。
21.使用密度小、强度大的镁合金能减轻汽车自重,从而减少汽油消耗和废气排放。
(1)镁元素在自然界中是以
(填“单质”或“化合物”)形式存在。
(2)工业制镁的一种原理是2MgO+Si+2CaO2Mg↑+Ca2SiO4,抽走容器中的空气对反应有促进作用,且能防止空气中的物质与Mg反应使产品混有
(填化学式)。
(3)制镁的原料MgO可从海水中获得。小华利用镁与盐酸反应后的废液,模拟从海水中获取MgO的过程,实验如下:
步骤1:向上述废液中,边搅拌边分批加入CaO,至MgCl2完全沉淀为止,过滤得Mg(OH)2固体。共消耗8.4g
CaO。
步骤2:将Mg(OH)2固体加热分解为MgO和水,所得MgO的质量为4.0g。
①步骤2中Mg(OH)2分解的化学方程式为
。
②通过所得MgO的质量计算上述废液中含MgCl2的质量m=
g。
③分析实验数据,可知步骤Ⅰ中反生的化学反应有:
CaO+H2O═Ca(OH)2;Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓;
。
22.钛(Ti)因为具有神奇的性能而被人们关注,常温下不和金属、盐酸和稀硫酸反应,加热时,即可与许多常见金属单质反应.钛是航空、宇航、军工、电力等方面的必需原料,地壳中含钛矿石称金红石(TiO2),目前大规模生产钛的方法是:
第一步:金红石、炭粉混合在高温条件下通入氯气得TiCl4和一种可燃性气体,该步发生反应的化学方程式为:
.
第二步:在氩气的气氛下,用过量的镁在加热条件下与TiCl4反应制得金属钛
①此反应的化学方程式为:
②由上述所得产物中获得纯净的金属钛,其主要实验步骤是:
往产物中加入足量的
充分反应后,再进行过滤、洗涤、烘干便可得金属钛.有关反应的化学方程式为
.
23.空气中体积分数最大的气体是
,世界年产量最高的金属是
。
24.某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示.请回答有关问题:
(1)实验开始时,应
(填“先加热再通CO”或“先通CO再加热”),目的是
.
(2)实验进行一段时间后,玻璃管A中出现的现象为
,反应方程式
B试管的现象为
,反应方程式为
.
25.赤铁矿是一种常用的炼铁矿石,其主要成分是Fe2O3。
(1)Fe2O3属于
(填序号)。
A.单质
B.化合物
C.氧化物
(2)工业上用一氧化碳和赤铁矿炼铁,反应的化学方程式为
。
26.工业上用铝土矿(含有
Al2O3和
SiO2,不考虑其它杂质)制取金属铝的基本流程如图所示:
(1)通过该流程可得出SiO2的性质有
(填序号)。
A.难溶于水
B.不能与稀硫酸反应
C.能与氢氧化钠溶液反应
(2)铝土矿中氧化铝与稀硫酸反应生成硫酸铝和水的化学方程式为
。
(3)操作I的名称为
。
(4)铝合金材料具有较好的抗腐蚀性,反应的化学方程式为
。
27.某钢铁厂每天需消耗4900t含Fe2O376%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是
t。
28.下列属于置换反应的是
.
A.3CO+Fe2O32Fe+3CO2
B.CH4+2O3CO2+2H2O
C.H2+CuOCu+H2O
D.
.
三.实验探究题(共3小题)
29.用如图装置进行实验。取3个玻璃注射器分别放入等量锌片、铜片、镁片,再各吸入足量的稀硫酸,迅速固定在铁架台上,并保持注射器的活塞始终不动。下方各放置一个小烧杯,观察到如下现象。
(1)注射器①中产生气泡,反应的化学方程式为
。
(2)注射器②中无明显现象,原因是
。
(3)注射器③中发生剧烈反应,注射器中的液体被压入小烧杯中,反应很快停止。出现这现象的原因包括
(填字母序号)。
A.镁片与稀硫酸反应产生大量氢气
B.注射器③内压强迅速增大
C.压强差使液体流入烧杯中,使反应物分离
30.验证金属Cu、Mg、Zn和Ag活动性顺序的四个实验如下,根据实验回答下列问题:
(1)上述四个实验,没有必要做的实验是
;
(2)实验三中,发生反应的化学方程式为
;
(3)实验一发生变化过程中,镁条表面不仅出现红色固体,还有气泡产生,这种气体是无色无味的,密度较小。请你猜想该气体是
;
(4)将四个实验后的所有物质倒入一个烧杯内,过滤,得到无色滤液和固体,在固体中加稀盐酸有气泡,则固体中可能含有的金属是
。
31.“低碳生活,绿色出行”。学校建议同学们骑自行车出行。请回答下列问题
①图中所标示的各部件中,属于金属材料的是
(序号)
②自行车车架一般用生铁制造,某些部件为不锈钢。工业上常以赤铁矿(主要成分为Fe2O3)为原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式:
。
③车架表面喷漆不仅美观,而且可有效防止其与
接触而生锈。防止公共自行车链条生锈的有效措施是
。
④自行车轮圈一般用铝合金制造,这是因为铝合金既轻便又耐用。铝制品比较耐腐蚀的原因是
。
⑤天气太热,建议同学们车胎气压不能太高试用。用分子、原子的相关知识解释
。有些同学带的碳酸饮料,其中溶有二氧化碳气体,当打开汽水瓶盖时,汽水会自动喷出来,原因是
有的同学们带了“摇摇冰”的罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动使它们混合,罐内饮料温度就会降低。这种固体物质可能是
(填字母)
A.生石灰B.烧碱C.食盐D.硝酸铵
⑥为防止旅途中皮肤的以外擦伤感染,常备有碘酒,碘酒中的溶剂是
(写化学式)。
⑦同学们准备将垃圾分类处理,其中属于不可回收垃圾的是
(填字母)。
A.废纸
B.果皮
C.
饮料罐
D.废弃塑料。
四.计算题(共1小题)
32.向AgNO3溶液中加入一定质量的Zn和Cu的混合粉末,充分反应后过滤,得到滤渣和蓝色滤液。
(1)分析溶液质量变化的情况。
(2)若向滤液中加入稀盐酸,有沉淀产生,写出溶液中溶质的成分。
第1页(共1页)
一.选择题(共18小题)
1.推理和归纳是化学学习和研究中常用的思维方法,下列推理正确的是( )
A.稀有气体可作保护气,可做保护气的一定是稀有气体
B.单质是由一种元素组成的物质,由一种元素组成的物质一定是单质
C.性质活泼的金属在空气中容易被腐蚀,铝在空气中不易被腐蚀是因为其性质不活泼
D.人类需要的大部分能量是由化学反应产生的,但不是所有化学反应都放出热量
2.某同学为验证镁、铜、银三种金属的活动性顺序,以下四种实验方案中能达到目的的是( )
A.Mg丝、Cu丝、AgNO3溶液
B.Mg丝、Cu丝、Ag丝、稀盐酸
C.MgSO4溶液、CuSO4溶液、Ag丝
D.Mg丝、Ag丝、CuSO4溶液
3.下列关于资源、能源、环保方面的叙述正确的是( )
A.空气中的各种成分作为原料广泛用于生产化工产品、运输等领域
B.地表的咸水约占地球总水量的96.5%
C.地球上的金属资源都是以金属矿物的形式存在的
D.煤、石油、沼气都属于化石燃料
4.下列有关资源、能源的叙述错误的是( )
A.金属资源广泛地存在于地壳和海洋中,地壳中铁元素含量最高
B.利用石油中各成分的沸点不同,将它们分离,可得到汽油、煤油、石蜡等不同的产品
C.稀土金属有“工业的维生素”的美誉,是不可再生的重要战略资源
D.开发利用太阳能、核能、氢能、风能、地热能等能源,可适当节省化石燃料
5.CO和C分别跟CuO反应,若生成等质量的Cu,则反应中消耗的CO和C的质量比为(假定CO全部用于还原CuO)( )
A.1:1
B.7:3
C.14:3
D.1:2
6.我国古代的湿法冶金术是世界闻名的,我国在世界上最先应用湿法冶炼的金属是( )
A.Fe
B.Cu
C.Ag
D.Hg
7.下列不属于金属材料的是( )
A.不锈钢菜刀
B.铝合金
C.铜导线
D.氧化铁
8.下列不属于金属材料的是( )
A.东汉晚期马踏飞燕的青铜
B.
纳米铜
C.河北沧州铁狮子的生铁
D.
铁矿石
9.关于物质的用途,下列说法错误的是( )
A.CO炼铁时表现还原性,发生了还原反应
B.活性炭净水利用了其吸附性
C.氮气作保护气利用了其稳定性
D.洗洁精洗涤油污体现了其乳化作用
10.下列实验现象描述正确的是( )
A.磷在氧气中燃烧,产生大量白色烟雾
B.硫在空气中燃烧,发出明亮的蓝紫色火焰
C.一氧化碳通入灼热的氧化铁,红棕色粉末变黑
D.铁钉加入氯化铜溶液中,表面有红色的铜生成
11.下列关于金属材料的说法中,不正确的是( )
A.生铁、硬铝、黄铜都属于合金
B.铜有良好的导电性,因而大量用于制作电线
C.己生锈的铁不具有回收的价值
D.通过高炉炼得的铁含有杂质
12.下列关于铁的说法正确的是( )
A.工业炼铁得到含碳量较低的钢
B.自然界大部分的铁以单质形式存在
C.铁是地壳中含量最丰富的金属元素
D.合金许多性能和组成它们的纯金属不同
13.金属冶炼工业中常用化学性质比较活泼的金属还原出相对不活泼的金属.如:用铝和二氧化锰在高温下反应,可以制取金属锰.反应的化学方程式为:aAl+bMnO2cAl2O3+dMn下列说法中,错误的是( )
A.b=3
B.MnO2中锰元素质量分数为63.2%
C.Al2O3中铝、氧元素的质量比为9:8
D.在上述反应中,MnO2起催化作用
14.距今2000余年前的西汉时期,就有“曾青得铁则化为铜”的记述,这是现代湿法冶金技术的先驱,从现代的科学观点理解,“曾青”应赋予的最恰当的涵义是( )
A.铜单质
B.硫酸铜溶液
C.铜的化合物
D.可溶性铜盐的溶液
15.用1000t含铁56%的赤铁矿石(主要成分是氧化铁),理论上可以炼出含铁96%的生铁的质量是( )
A.583.3
t
B.560
t
C.408.3
t
D.392
t
16.钢铁厂购进含氧化铁80%的赤铁矿1000t,可以炼取含杂质4%的生铁的质量( )
A.560t
B.583t
C.800t
D.1400t
17.下列化学反应中属于置换反应的是( )
A.3Fe+2O2
Fe3O4
B.CO+CuO
Cu+CO2
C.Zn+CuSO4=ZnSO4+Cu
D.SO2+2NaOH=Na2SO3+H2O
18.下列实验方案可行的是( )
①将NaCl和KNO3的混合物溶于水,再用过滤的方法将它们分离
②往铜盐溶液中加入铁粉获得少量铜
③将氧气、二氧化碳的混合气体通过盛有足量灼热的铜网的试管获得纯净二氧化碳
④用稀盐酸除去混在铜粉中的镁粉和铝粉.
A.②③④
B.②④
C.③④
D.①③④
二.填空题(共10小题)
19.镁在空气中燃烧生成氧化镁和氮化镁(其中氮为﹣3价),氮化镁与水反应生成氢氧化镁和氨气.
(1)写出氮化镁与水反应的化学方程式
;
(2)12克镁在空气中燃烧所生成的产物的总质量
(填>、<或等于多少克);
(3)已知氮化镁是一种黄色的固体.根据镁在空气中燃烧的实验现象,可知在这样的条件下,镁更易与空气中的①
化合,理由是生成物②
.
20.某科研小组的同学在探究镁、铜、锌三种金属的有关性质时进行了如图实验:
(1)将图甲实验结束后①②试管内的物质倒入图乙的空烧杯中,一段时间后对烧杯中的物质进行过滤,滤液中的溶质一定有
;
(2)若要验证镁、锌、铜金属活动性顺序,还可以用一种试剂直接与三种金属反应就能达到目的,该试剂可以是
。
21.使用密度小、强度大的镁合金能减轻汽车自重,从而减少汽油消耗和废气排放。
(1)镁元素在自然界中是以
(填“单质”或“化合物”)形式存在。
(2)工业制镁的一种原理是2MgO+Si+2CaO2Mg↑+Ca2SiO4,抽走容器中的空气对反应有促进作用,且能防止空气中的物质与Mg反应使产品混有
(填化学式)。
(3)制镁的原料MgO可从海水中获得。小华利用镁与盐酸反应后的废液,模拟从海水中获取MgO的过程,实验如下:
步骤1:向上述废液中,边搅拌边分批加入CaO,至MgCl2完全沉淀为止,过滤得Mg(OH)2固体。共消耗8.4g
CaO。
步骤2:将Mg(OH)2固体加热分解为MgO和水,所得MgO的质量为4.0g。
①步骤2中Mg(OH)2分解的化学方程式为
。
②通过所得MgO的质量计算上述废液中含MgCl2的质量m=
g。
③分析实验数据,可知步骤Ⅰ中反生的化学反应有:
CaO+H2O═Ca(OH)2;Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓;
。
22.钛(Ti)因为具有神奇的性能而被人们关注,常温下不和金属、盐酸和稀硫酸反应,加热时,即可与许多常见金属单质反应.钛是航空、宇航、军工、电力等方面的必需原料,地壳中含钛矿石称金红石(TiO2),目前大规模生产钛的方法是:
第一步:金红石、炭粉混合在高温条件下通入氯气得TiCl4和一种可燃性气体,该步发生反应的化学方程式为:
.
第二步:在氩气的气氛下,用过量的镁在加热条件下与TiCl4反应制得金属钛
①此反应的化学方程式为:
②由上述所得产物中获得纯净的金属钛,其主要实验步骤是:
往产物中加入足量的
充分反应后,再进行过滤、洗涤、烘干便可得金属钛.有关反应的化学方程式为
.
23.空气中体积分数最大的气体是
,世界年产量最高的金属是
。
24.某化学兴趣小组用一氧化碳与氧化铁的反应来探究炼铁的原理,装置如下图所示.请回答有关问题:
(1)实验开始时,应
(填“先加热再通CO”或“先通CO再加热”),目的是
.
(2)实验进行一段时间后,玻璃管A中出现的现象为
,反应方程式
B试管的现象为
,反应方程式为
.
25.赤铁矿是一种常用的炼铁矿石,其主要成分是Fe2O3。
(1)Fe2O3属于
(填序号)。
A.单质
B.化合物
C.氧化物
(2)工业上用一氧化碳和赤铁矿炼铁,反应的化学方程式为
。
26.工业上用铝土矿(含有
Al2O3和
SiO2,不考虑其它杂质)制取金属铝的基本流程如图所示:
(1)通过该流程可得出SiO2的性质有
(填序号)。
A.难溶于水
B.不能与稀硫酸反应
C.能与氢氧化钠溶液反应
(2)铝土矿中氧化铝与稀硫酸反应生成硫酸铝和水的化学方程式为
。
(3)操作I的名称为
。
(4)铝合金材料具有较好的抗腐蚀性,反应的化学方程式为
。
27.某钢铁厂每天需消耗4900t含Fe2O376%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是
t。
28.下列属于置换反应的是
.
A.3CO+Fe2O32Fe+3CO2
B.CH4+2O3CO2+2H2O
C.H2+CuOCu+H2O
D.
.
三.实验探究题(共3小题)
29.用如图装置进行实验。取3个玻璃注射器分别放入等量锌片、铜片、镁片,再各吸入足量的稀硫酸,迅速固定在铁架台上,并保持注射器的活塞始终不动。下方各放置一个小烧杯,观察到如下现象。
(1)注射器①中产生气泡,反应的化学方程式为
。
(2)注射器②中无明显现象,原因是
。
(3)注射器③中发生剧烈反应,注射器中的液体被压入小烧杯中,反应很快停止。出现这现象的原因包括
(填字母序号)。
A.镁片与稀硫酸反应产生大量氢气
B.注射器③内压强迅速增大
C.压强差使液体流入烧杯中,使反应物分离
30.验证金属Cu、Mg、Zn和Ag活动性顺序的四个实验如下,根据实验回答下列问题:
(1)上述四个实验,没有必要做的实验是
;
(2)实验三中,发生反应的化学方程式为
;
(3)实验一发生变化过程中,镁条表面不仅出现红色固体,还有气泡产生,这种气体是无色无味的,密度较小。请你猜想该气体是
;
(4)将四个实验后的所有物质倒入一个烧杯内,过滤,得到无色滤液和固体,在固体中加稀盐酸有气泡,则固体中可能含有的金属是
。
31.“低碳生活,绿色出行”。学校建议同学们骑自行车出行。请回答下列问题
①图中所标示的各部件中,属于金属材料的是
(序号)
②自行车车架一般用生铁制造,某些部件为不锈钢。工业上常以赤铁矿(主要成分为Fe2O3)为原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式:
。
③车架表面喷漆不仅美观,而且可有效防止其与
接触而生锈。防止公共自行车链条生锈的有效措施是
。
④自行车轮圈一般用铝合金制造,这是因为铝合金既轻便又耐用。铝制品比较耐腐蚀的原因是
。
⑤天气太热,建议同学们车胎气压不能太高试用。用分子、原子的相关知识解释
。有些同学带的碳酸饮料,其中溶有二氧化碳气体,当打开汽水瓶盖时,汽水会自动喷出来,原因是
有的同学们带了“摇摇冰”的罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动使它们混合,罐内饮料温度就会降低。这种固体物质可能是
(填字母)
A.生石灰B.烧碱C.食盐D.硝酸铵
⑥为防止旅途中皮肤的以外擦伤感染,常备有碘酒,碘酒中的溶剂是
(写化学式)。
⑦同学们准备将垃圾分类处理,其中属于不可回收垃圾的是
(填字母)。
A.废纸
B.果皮
C.
饮料罐
D.废弃塑料。
四.计算题(共1小题)
32.向AgNO3溶液中加入一定质量的Zn和Cu的混合粉末,充分反应后过滤,得到滤渣和蓝色滤液。
(1)分析溶液质量变化的情况。
(2)若向滤液中加入稀盐酸,有沉淀产生,写出溶液中溶质的成分。
第1页(共1页)
同课章节目录
