2021年人教版化学九年级第二学期课题 2 金属的化学性质同步练习卷带答案
文档属性
| 名称 | 2021年人教版化学九年级第二学期课题 2 金属的化学性质同步练习卷带答案 |

|
|
| 格式 | zip | ||
| 文件大小 | 133.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-05 00:00:00 | ||
图片预览




文档简介
2021年人教版化学九年级第二学期第8单元《8.2金属的化学性质》同步练习卷带答案
一.选择题(共30小题)
1.在自然界中以游离态存在的金属元素是( )
A.金
B.镁
C.铝
D.铁
2.向Zn(NO3)2和Cu(NO3)2混合溶液中加入一定量的铁粉,充分反应后,过滤。向滤渣中再加入稀盐酸,有气体放出。下列说法正确的是( )
A.滤渣中一定有锌
B.滤渣中一定有铜
C.所得溶液中一定有Zn2+、Cu2+
D.所得溶液中一定有Cu2+、Fe2+
3.把X、Y、Z三种金属分别放入稀盐酸中,X、Y溶解并有气泡产生,Z不反应,取过量X放入Y(NO3)2和Z(NO3)2的混合溶液中充分反应后过滤,经检验,滤渣中只有X、Z.则X、Y、Z三种金属的活动性由强到弱的顺序是( )
A.X>Y>Z
B.Y>Z>X
C.Y>X>Z
D.X>Z>Y
4.不法分子常常用金光闪闪的“金元宝”(铜锌合金)当作黄金来蒙骗人们,下列鉴别方法中错误的是( )
A.加盐酸
B.测密度
C.用火烧
D.看颜色
5.向AgNO3溶液中加入一定质量的Al、Cu的混合粉末,充分反应后过滤,得到滤渣和蓝色滤液.关于该滤渣和滤液的下列四种说法中,正确的是( )
A.向滤渣中加入稀盐酸,一定有气泡产生
B.向滤液中加入足量的铁粉,一定有三种金属剩余
C.滤渣中一定含有Ag,可能含有铜
D.滤液中一定含有Cu(NO3)2,一定不含AgNO3,不一定含有A1(NO3)3
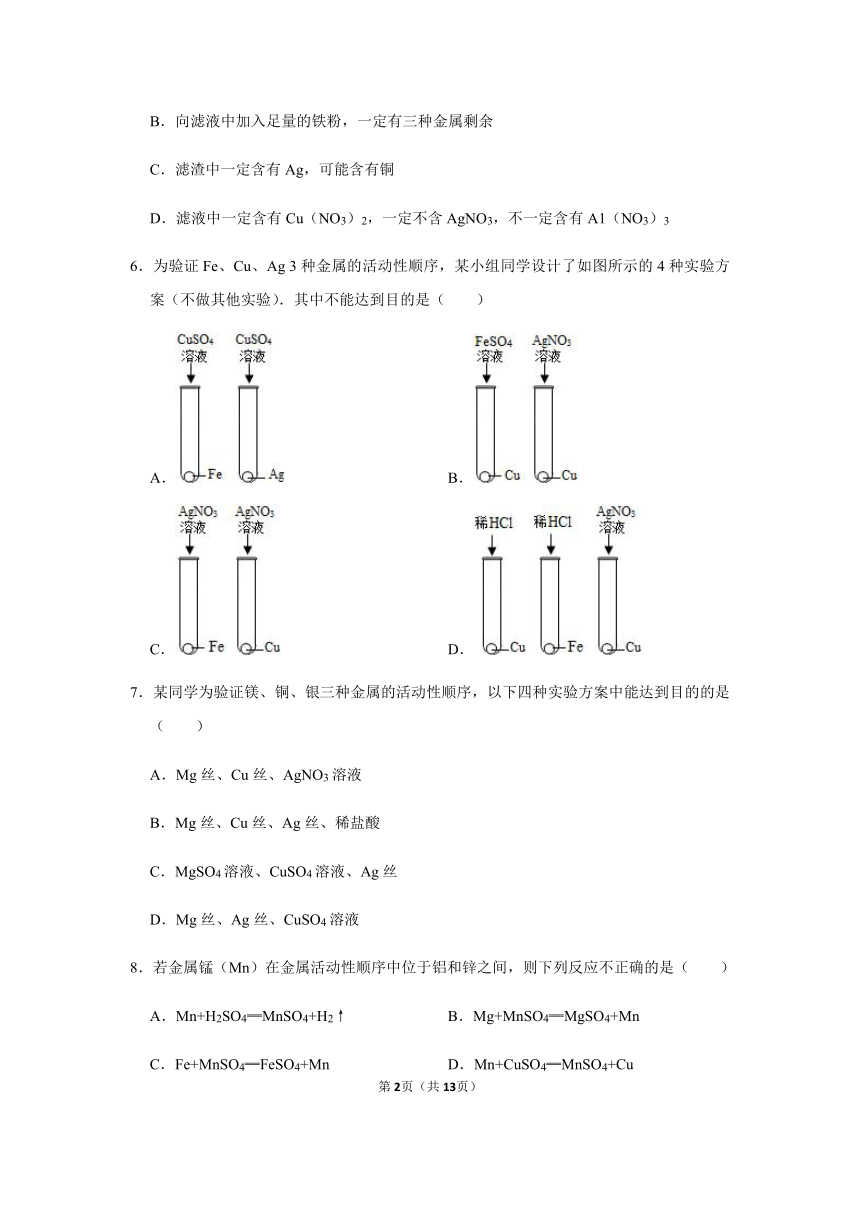
6.为验证Fe、Cu、Ag
3种金属的活动性顺序,某小组同学设计了如图所示的4种实验方案(不做其他实验).其中不能达到目的是( )
A.
B.
C.
D.
7.某同学为验证镁、铜、银三种金属的活动性顺序,以下四种实验方案中能达到目的的是( )
A.Mg丝、Cu丝、AgNO3溶液
B.Mg丝、Cu丝、Ag丝、稀盐酸
C.MgSO4溶液、CuSO4溶液、Ag丝
D.Mg丝、Ag丝、CuSO4溶液
8.若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
A.Mn+H2SO4═MnSO4+H2↑
B.Mg+MnSO4═MgSO4+Mn
C.Fe+MnSO4═FeSO4+Mn
D.Mn+CuSO4═MnSO4+Cu
9.有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性顺序由弱到强的是( )
A.丙<丁<甲<乙
B.乙<甲<丁<丙
C.丁<甲<乙<丙
D.丙<乙<甲<丁
10.向AgNO3、Zn(NO3)2的混合溶液中加入一定量铁粉,充分反应后,过滤,向滤液中滴入NaCl溶液,有白色沉淀产生.则下列对滤渣成分的判断中,正确的是( )
A.一定有Fe和Ag
B.一定有Zn和Ag
C.只有Ag
D.只有Fe
11.在Fe(NO3)2和AgNO3的混合溶液中,加入一定量锌粉,充分反应后过滤,得到滤渣和滤液。下列说法中正确的是( )
A.若滤液为浅绿色,则滤渣中一定有锌
B.滤液中一定有Zn(NO3)2,滤渣中一定有银
C.若滤液中有AgNO3,则滤渣中一定有铁
D.若取少量滤渣,加入稀盐酸,产生气泡,则滤渣的组成有三种情况
12.关于铁与稀硫酸的反应,以下说法错误的是( )
A.生成硫酸铁和氢气
B.属于置换反应
C.溶液变浅绿色
D.溶液的质量一定增加
13.下列实验对应的图象不正确的是( )
A.将等质量的锌和铁分别与足量的盐酸反应
B.向盐酸和氯化钙的混合溶液中加入过量的碳酸钠溶液
C.向澄清石灰水中通入适量的CO2气体至与氢氧化钙恰好完全反应
D.一定温度下,向一定量的饱和NaCl溶液中不断加入蔗糖晶体
14.有X、Y、Z
3种金属,将X和Y浸入稀硫酸中,X溶解,Y不溶解;将Y浸入Z的硝酸盐溶液中,Y的表面有Z析出.则X、Y、Z的金属活动性由强到弱的顺序为( )
A.X、Y、Z
B.Z、X、Y
C.X、Z、Y
D.Y、Z、X
15.为验证Fe、Cu、Ag三种金属的活动性是依次减弱的,某化学兴趣小组设计了如图所示的四个实验。其中不必进行的是( )
A.
B.
C.
D.
16.现有X、Y、Z三种金属,将X、Y分别放入稀硫酸中,结果Y表面产生气泡,X表面无明显现象;另取X放入Z的盐溶液中,结果X表面有Z析出.则X、Y、Z三种金属的活动性顺序是( )
A.Y>X>Z
B.X>Y>Z
C.X>Z>Y
D.Y>Z>X
17.向含有AgNO3、Zn(NO3)2的混合溶液中加入一定量的铜粉,充分反应后,过滤,向滤液中滴入NaCl溶液,有白色沉淀产生。则下列对滤渣和滤液成分的判断中,正确的是( )
A.滤渣中只有Cu和Ag
B.滤渣中只有单质Ag
C.滤液中只有Cu2+和Zn2+
D.滤液中只有Ag+和Zn2+
18.向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液,关于该滤渣和滤液有下列四种说法(已知HCl+AgNO3═AgCl↓+HNO3):
①向滤渣中加入稀盐酸,一定有气泡产生.
②向滤液中加入稀盐酸,一定有沉淀产生.
③滤渣中一定含有Ag.
④滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Al(NO3)3.
以上说法中正确的个数是( )
A.0个
B.1个
C.2个
D.3个
19.所含溶质质量、溶液体积都相等的稀硫酸分别与足量的颗粒大小和形状几乎相同的镁、铁、锌三种金属反应,下列图象能正确表示生成氢气质量与反应时之间关系的是( )
A.
B.
C.
D.
20.垃圾分类回收有利于保护环境、节约资源。下列可回收垃圾中属于金属材料的是( )
A.玻璃瓶
B.塑料袋
C.易拉罐
D.废报纸
21.对于木炭,一氧化碳和氢气分别跟氧化铜的反应(在适当条件下)下列叙述正确的是( )
A.都是还原剂
B.都是置换反应
C.都有二氧化碳生成
D.都有红色物质生成
22.下列实验方案中,设计合理的是( )
A.证明铜粉中混有银粉:将混合物与稀盐酸混合,观察是否产生气泡
B.制取少量NaOH溶液:将适量的Na2CO3溶液与Ca(OH)2溶液混合,过滤
C.分离氯化钠和氯化钙:加入碳酸钠溶液,充分反应后,过滤,蒸发
D.除去NaCl溶液中混有的少量盐酸:加入过量的CaCO3,充分反应后过滤
23.人们可从铁钛矿(主要成分是FeTiO3)制取金属钛(Ti),其在一定条件下的主要反应有:
①FeTiO3+H2═Fe+TiO2+H2O;②TiO2+2C+2Cl2═X+2CO;③TiCl4+2Mg═2MgCl2+Ti。
下列叙述不正确的是( )
A.反应①中的H2被氧化
B.反应②Cl2中的氯元素为﹣1价
C.反应②中X为TiCl4
D.反应③说明Mg的金属活动性比Ti强
24.根据实验装置图,以下说法中正确的是( )
A.a处固体由黑色逐渐变为红棕色
B.该实验可验证CO的氧化性
C.实验结束后应先停止加热,待玻璃管冷却后再停止通CO
D.在整个实验过程中,c处的尾气可不做处理直接排放到空气中
25.下列有关工业炼铁的叙述中,不正确的是( )
A.炼铁用的设备是高炉
B.炼铁的原料是焦炭、石灰石、铁矿石
C.炼铁得到的生铁仍为混合物
D.炼铁是用空气中的氧气将铁矿石中的杂质氧化除去
26.目前钢铁是人类用量最大的金属材料,每年人们都要从矿物中冶炼出大量的铁.炼铁的主要反应原理可表示为:Fe2O3+3CO2Fe+3CO2.下列对该反应的分析正确的是( )
A.该反应属于置换反应
B.一氧化碳发生了还原反应
C.Fe2O3在反应中提供了氧,具有氧化性
D.该反应属于复分解反应
27.下列化学反应属于置换反应的是( )
A.Mg+2HCl═MgCl2+H2↑
B.C+O2
CO2
C.CO+CuOCu+CO2
D.2KClO3
2KCl+3O2↑
28.下列实验用如图表示合理的是( )
A.向锌铜合金中加入慢慢加入足量的稀硫酸;Y轴表示剩余固体的质量
B.高温灼烧氧化铁和足量炭粉的混合物;Y轴表示剩余固体中氧元素的质量
C.往碳酸钙中慢慢加入足量盐酸;Y轴表示产生气体的质量
D.往澄清石灰水中不断通入CO2;Y轴表示生成沉淀的质量
29.化学小组的同学探究金属中可能有的杂质.取6克锌片(含有杂质)放在足量的盐酸中充分反应,收到的氢气是0.1mol,可以初步估算锌片中的杂质是( )
A.Cu
B.Fe
C.C
D.Ag
30.用Zn、CuO、稀H2SO4作原料制取Cu,有两种途径:①ZnH2Cu
②CuOCuSO4Cu,若用这两种方法制得的铜的质量相等,下列叙述符合实验结果的是( )
A.消耗相同质量的氧化铜
B.消耗相同质量的锌
C.消耗相同质量的稀硫酸
D.生成硫酸锌的质量相同
二.填空题(共2小题)
31.某化学兴趣小组对一包含有铜、银、锰的混合金属粉末进行了分离,获得了一种金属和一种盐的晶体.他们将三种金属随意编号为A、B、C,并设计了如下流程:
(1)金属B是
(填元素符号),操作a的名称是
.
(2)已知A的硫酸盐中A元素显+2价,请写出①、②反应的化学方程式:
①
②
.
32.含有铝粉l.8g、锌粉6.5g、铁粉11.2g、铜粉3.8g的混合物与一定质量的稀硫酸充分反应后,有6.6g金属剩余,则生成氢气的总质量为
g;其中产生氢气质量最多的反应的化学方程式为
。
三.实验探究题(共2小题)
33.验证金属Cu、Mg、Zn和Ag活动性顺序的四个实验如下,根据实验回答下列问题:
(1)上述四个实验,没有必要做的实验是
;
(2)实验三中,发生反应的化学方程式为
;
(3)实验一发生变化过程中,镁条表面不仅出现红色固体,还有气泡产生,这种气体是无色无味的,密度较小。请你猜想该气体是
;
(4)将四个实验后的所有物质倒入一个烧杯内,过滤,得到无色滤液和固体,在固体中加稀盐酸有气泡,则固体中可能含有的金属是
。
34.某研究性学习小组利用草酸晶体分解制取纯净、干燥的一氧化碳并用来还原氧化铁。查阅资料:
草酸晶体(H2C2O4?2H2O)在浓H2SO4作用下加热分解产生H2O、CO和CO2.同学们设计了如图所示的实验装置,请回答下列问题:
(1)图中A是制取一氧化碳的气体发生装置。
①装置A中,方便添加浓硫酸的仪器名称是
;装置B中,提供热源的仪器名称是
。
②装置B中发生反应的化学方程式为
。
(2)将E、F、G3个装置按一定顺序接入到方框中。
①正确的导管接口顺序是:a→
→h。
②方框中的G装置是否可以省略?并说明理由
。
(3)一氧化碳还原氧化铁。
①实验前,要先通入CO,目的是除去装置
(填写装置下方字母序号)中的空气。
②观察到
时,熄灭B处的酒精喷灯,等到
时,再熄灭D处的酒精灯。
参考答案
一.选择题(共30小题)
1.A;
2.B;
3.C;
4.D;
5.C;
6.C;
7.D;
8.C;
9.A;
10.C;
11.B;
12.A;
13.D;
14.A;
15.C;
16.A;
17.B;
18.B;
19.B;
20.C;
21.A;
22.B;
23.B;
24.C;
25.D;
26.C;
27.A;
28.B;
29.B;
30.A;
二.填空题(共2小题)
31.Cu;蒸发;Mn+H2SO4═MnSO4+H2↑;Cu+2AgNO3═Cu(NO3)2+2Ag;
32.0.7;Fe+H2SO4=FeSO4+H2↑;
三.实验探究题(共2小题)
33.实验一;Cu+2AgNO3═Cu(NO3)2+2Ag;氢气;镁;
34.分液漏斗;酒精喷灯;Fe2O3+3CO2Fe+3CO2;f→g→d→e→b→c;不能,G装置是除去混合气中二氧化碳;B;B中的红色粉末变成黑色;装置冷却到室温;
第1页(共1页)
一.选择题(共30小题)
1.在自然界中以游离态存在的金属元素是( )
A.金
B.镁
C.铝
D.铁
2.向Zn(NO3)2和Cu(NO3)2混合溶液中加入一定量的铁粉,充分反应后,过滤。向滤渣中再加入稀盐酸,有气体放出。下列说法正确的是( )
A.滤渣中一定有锌
B.滤渣中一定有铜
C.所得溶液中一定有Zn2+、Cu2+
D.所得溶液中一定有Cu2+、Fe2+
3.把X、Y、Z三种金属分别放入稀盐酸中,X、Y溶解并有气泡产生,Z不反应,取过量X放入Y(NO3)2和Z(NO3)2的混合溶液中充分反应后过滤,经检验,滤渣中只有X、Z.则X、Y、Z三种金属的活动性由强到弱的顺序是( )
A.X>Y>Z
B.Y>Z>X
C.Y>X>Z
D.X>Z>Y
4.不法分子常常用金光闪闪的“金元宝”(铜锌合金)当作黄金来蒙骗人们,下列鉴别方法中错误的是( )
A.加盐酸
B.测密度
C.用火烧
D.看颜色
5.向AgNO3溶液中加入一定质量的Al、Cu的混合粉末,充分反应后过滤,得到滤渣和蓝色滤液.关于该滤渣和滤液的下列四种说法中,正确的是( )
A.向滤渣中加入稀盐酸,一定有气泡产生
B.向滤液中加入足量的铁粉,一定有三种金属剩余
C.滤渣中一定含有Ag,可能含有铜
D.滤液中一定含有Cu(NO3)2,一定不含AgNO3,不一定含有A1(NO3)3
6.为验证Fe、Cu、Ag
3种金属的活动性顺序,某小组同学设计了如图所示的4种实验方案(不做其他实验).其中不能达到目的是( )
A.
B.
C.
D.
7.某同学为验证镁、铜、银三种金属的活动性顺序,以下四种实验方案中能达到目的的是( )
A.Mg丝、Cu丝、AgNO3溶液
B.Mg丝、Cu丝、Ag丝、稀盐酸
C.MgSO4溶液、CuSO4溶液、Ag丝
D.Mg丝、Ag丝、CuSO4溶液
8.若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
A.Mn+H2SO4═MnSO4+H2↑
B.Mg+MnSO4═MgSO4+Mn
C.Fe+MnSO4═FeSO4+Mn
D.Mn+CuSO4═MnSO4+Cu
9.有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性顺序由弱到强的是( )
A.丙<丁<甲<乙
B.乙<甲<丁<丙
C.丁<甲<乙<丙
D.丙<乙<甲<丁
10.向AgNO3、Zn(NO3)2的混合溶液中加入一定量铁粉,充分反应后,过滤,向滤液中滴入NaCl溶液,有白色沉淀产生.则下列对滤渣成分的判断中,正确的是( )
A.一定有Fe和Ag
B.一定有Zn和Ag
C.只有Ag
D.只有Fe
11.在Fe(NO3)2和AgNO3的混合溶液中,加入一定量锌粉,充分反应后过滤,得到滤渣和滤液。下列说法中正确的是( )
A.若滤液为浅绿色,则滤渣中一定有锌
B.滤液中一定有Zn(NO3)2,滤渣中一定有银
C.若滤液中有AgNO3,则滤渣中一定有铁
D.若取少量滤渣,加入稀盐酸,产生气泡,则滤渣的组成有三种情况
12.关于铁与稀硫酸的反应,以下说法错误的是( )
A.生成硫酸铁和氢气
B.属于置换反应
C.溶液变浅绿色
D.溶液的质量一定增加
13.下列实验对应的图象不正确的是( )
A.将等质量的锌和铁分别与足量的盐酸反应
B.向盐酸和氯化钙的混合溶液中加入过量的碳酸钠溶液
C.向澄清石灰水中通入适量的CO2气体至与氢氧化钙恰好完全反应
D.一定温度下,向一定量的饱和NaCl溶液中不断加入蔗糖晶体
14.有X、Y、Z
3种金属,将X和Y浸入稀硫酸中,X溶解,Y不溶解;将Y浸入Z的硝酸盐溶液中,Y的表面有Z析出.则X、Y、Z的金属活动性由强到弱的顺序为( )
A.X、Y、Z
B.Z、X、Y
C.X、Z、Y
D.Y、Z、X
15.为验证Fe、Cu、Ag三种金属的活动性是依次减弱的,某化学兴趣小组设计了如图所示的四个实验。其中不必进行的是( )
A.
B.
C.
D.
16.现有X、Y、Z三种金属,将X、Y分别放入稀硫酸中,结果Y表面产生气泡,X表面无明显现象;另取X放入Z的盐溶液中,结果X表面有Z析出.则X、Y、Z三种金属的活动性顺序是( )
A.Y>X>Z
B.X>Y>Z
C.X>Z>Y
D.Y>Z>X
17.向含有AgNO3、Zn(NO3)2的混合溶液中加入一定量的铜粉,充分反应后,过滤,向滤液中滴入NaCl溶液,有白色沉淀产生。则下列对滤渣和滤液成分的判断中,正确的是( )
A.滤渣中只有Cu和Ag
B.滤渣中只有单质Ag
C.滤液中只有Cu2+和Zn2+
D.滤液中只有Ag+和Zn2+
18.向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液,关于该滤渣和滤液有下列四种说法(已知HCl+AgNO3═AgCl↓+HNO3):
①向滤渣中加入稀盐酸,一定有气泡产生.
②向滤液中加入稀盐酸,一定有沉淀产生.
③滤渣中一定含有Ag.
④滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Al(NO3)3.
以上说法中正确的个数是( )
A.0个
B.1个
C.2个
D.3个
19.所含溶质质量、溶液体积都相等的稀硫酸分别与足量的颗粒大小和形状几乎相同的镁、铁、锌三种金属反应,下列图象能正确表示生成氢气质量与反应时之间关系的是( )
A.
B.
C.
D.
20.垃圾分类回收有利于保护环境、节约资源。下列可回收垃圾中属于金属材料的是( )
A.玻璃瓶
B.塑料袋
C.易拉罐
D.废报纸
21.对于木炭,一氧化碳和氢气分别跟氧化铜的反应(在适当条件下)下列叙述正确的是( )
A.都是还原剂
B.都是置换反应
C.都有二氧化碳生成
D.都有红色物质生成
22.下列实验方案中,设计合理的是( )
A.证明铜粉中混有银粉:将混合物与稀盐酸混合,观察是否产生气泡
B.制取少量NaOH溶液:将适量的Na2CO3溶液与Ca(OH)2溶液混合,过滤
C.分离氯化钠和氯化钙:加入碳酸钠溶液,充分反应后,过滤,蒸发
D.除去NaCl溶液中混有的少量盐酸:加入过量的CaCO3,充分反应后过滤
23.人们可从铁钛矿(主要成分是FeTiO3)制取金属钛(Ti),其在一定条件下的主要反应有:
①FeTiO3+H2═Fe+TiO2+H2O;②TiO2+2C+2Cl2═X+2CO;③TiCl4+2Mg═2MgCl2+Ti。
下列叙述不正确的是( )
A.反应①中的H2被氧化
B.反应②Cl2中的氯元素为﹣1价
C.反应②中X为TiCl4
D.反应③说明Mg的金属活动性比Ti强
24.根据实验装置图,以下说法中正确的是( )
A.a处固体由黑色逐渐变为红棕色
B.该实验可验证CO的氧化性
C.实验结束后应先停止加热,待玻璃管冷却后再停止通CO
D.在整个实验过程中,c处的尾气可不做处理直接排放到空气中
25.下列有关工业炼铁的叙述中,不正确的是( )
A.炼铁用的设备是高炉
B.炼铁的原料是焦炭、石灰石、铁矿石
C.炼铁得到的生铁仍为混合物
D.炼铁是用空气中的氧气将铁矿石中的杂质氧化除去
26.目前钢铁是人类用量最大的金属材料,每年人们都要从矿物中冶炼出大量的铁.炼铁的主要反应原理可表示为:Fe2O3+3CO2Fe+3CO2.下列对该反应的分析正确的是( )
A.该反应属于置换反应
B.一氧化碳发生了还原反应
C.Fe2O3在反应中提供了氧,具有氧化性
D.该反应属于复分解反应
27.下列化学反应属于置换反应的是( )
A.Mg+2HCl═MgCl2+H2↑
B.C+O2
CO2
C.CO+CuOCu+CO2
D.2KClO3
2KCl+3O2↑
28.下列实验用如图表示合理的是( )
A.向锌铜合金中加入慢慢加入足量的稀硫酸;Y轴表示剩余固体的质量
B.高温灼烧氧化铁和足量炭粉的混合物;Y轴表示剩余固体中氧元素的质量
C.往碳酸钙中慢慢加入足量盐酸;Y轴表示产生气体的质量
D.往澄清石灰水中不断通入CO2;Y轴表示生成沉淀的质量
29.化学小组的同学探究金属中可能有的杂质.取6克锌片(含有杂质)放在足量的盐酸中充分反应,收到的氢气是0.1mol,可以初步估算锌片中的杂质是( )
A.Cu
B.Fe
C.C
D.Ag
30.用Zn、CuO、稀H2SO4作原料制取Cu,有两种途径:①ZnH2Cu
②CuOCuSO4Cu,若用这两种方法制得的铜的质量相等,下列叙述符合实验结果的是( )
A.消耗相同质量的氧化铜
B.消耗相同质量的锌
C.消耗相同质量的稀硫酸
D.生成硫酸锌的质量相同
二.填空题(共2小题)
31.某化学兴趣小组对一包含有铜、银、锰的混合金属粉末进行了分离,获得了一种金属和一种盐的晶体.他们将三种金属随意编号为A、B、C,并设计了如下流程:
(1)金属B是
(填元素符号),操作a的名称是
.
(2)已知A的硫酸盐中A元素显+2价,请写出①、②反应的化学方程式:
①
②
.
32.含有铝粉l.8g、锌粉6.5g、铁粉11.2g、铜粉3.8g的混合物与一定质量的稀硫酸充分反应后,有6.6g金属剩余,则生成氢气的总质量为
g;其中产生氢气质量最多的反应的化学方程式为
。
三.实验探究题(共2小题)
33.验证金属Cu、Mg、Zn和Ag活动性顺序的四个实验如下,根据实验回答下列问题:
(1)上述四个实验,没有必要做的实验是
;
(2)实验三中,发生反应的化学方程式为
;
(3)实验一发生变化过程中,镁条表面不仅出现红色固体,还有气泡产生,这种气体是无色无味的,密度较小。请你猜想该气体是
;
(4)将四个实验后的所有物质倒入一个烧杯内,过滤,得到无色滤液和固体,在固体中加稀盐酸有气泡,则固体中可能含有的金属是
。
34.某研究性学习小组利用草酸晶体分解制取纯净、干燥的一氧化碳并用来还原氧化铁。查阅资料:
草酸晶体(H2C2O4?2H2O)在浓H2SO4作用下加热分解产生H2O、CO和CO2.同学们设计了如图所示的实验装置,请回答下列问题:
(1)图中A是制取一氧化碳的气体发生装置。
①装置A中,方便添加浓硫酸的仪器名称是
;装置B中,提供热源的仪器名称是
。
②装置B中发生反应的化学方程式为
。
(2)将E、F、G3个装置按一定顺序接入到方框中。
①正确的导管接口顺序是:a→
→h。
②方框中的G装置是否可以省略?并说明理由
。
(3)一氧化碳还原氧化铁。
①实验前,要先通入CO,目的是除去装置
(填写装置下方字母序号)中的空气。
②观察到
时,熄灭B处的酒精喷灯,等到
时,再熄灭D处的酒精灯。
参考答案
一.选择题(共30小题)
1.A;
2.B;
3.C;
4.D;
5.C;
6.C;
7.D;
8.C;
9.A;
10.C;
11.B;
12.A;
13.D;
14.A;
15.C;
16.A;
17.B;
18.B;
19.B;
20.C;
21.A;
22.B;
23.B;
24.C;
25.D;
26.C;
27.A;
28.B;
29.B;
30.A;
二.填空题(共2小题)
31.Cu;蒸发;Mn+H2SO4═MnSO4+H2↑;Cu+2AgNO3═Cu(NO3)2+2Ag;
32.0.7;Fe+H2SO4=FeSO4+H2↑;
三.实验探究题(共2小题)
33.实验一;Cu+2AgNO3═Cu(NO3)2+2Ag;氢气;镁;
34.分液漏斗;酒精喷灯;Fe2O3+3CO2Fe+3CO2;f→g→d→e→b→c;不能,G装置是除去混合气中二氧化碳;B;B中的红色粉末变成黑色;装置冷却到室温;
第1页(共1页)
同课章节目录
