第五单元 化学方程式 复习学案
图片预览



文档简介
复习:化学方程式
学习目标
1、理解质量守恒定律的宏观概念和微观解释,明晰化学反应前后的“变与不变”;
2、清晰化学方程式的意义与读法;
3、掌握化学方程式的书写步骤,学会至少1种配平方法。
教学内容
堂前测试:
1、在化学反应前后,一定发生了变化的是( )
A.分子的种类 B.分子的个数 C.元素的种类 D.原子的数目
2、食盐(NaCl)不仅可以做调味品,还是一种重要的化工原料。电解饱和食盐水,不可能得到的产物是( )
A.H2???????????????????????? B.Cl2??????????????????????? C.NaOH D.Na2CO3
3、关于化学方程式4P+5O2 2P2O5,获得信息不正确的是( )
A.磷和氧气在点燃的条件下生成五氧化二磷
B.该反应属于化合反应
C.参加反应的磷和氧气质量总和等于生成的五氧化二磷质量
D.点燃条件下,每30份质量的磷和41份质量的氧气反应生成71份质量的五氧化二磷
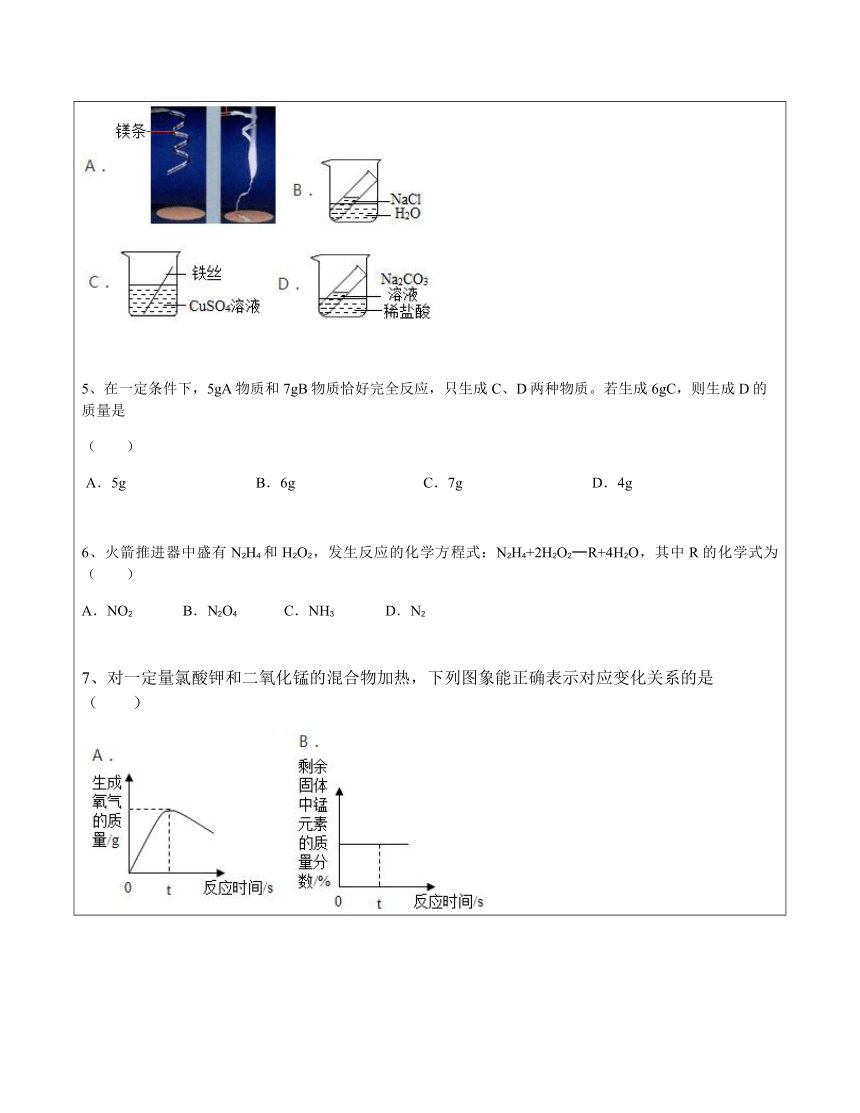
4、下列实验能够直接用于验证质量守恒定律的是( )
5、在一定条件下,5gA物质和7gB物质恰好完全反应,只生成C、D两种物质。若生成6gC,则生成D的质量是
( )
A.5g B.6g C.7g D.4g
6、火箭推进器中盛有N2H4和H2O2,发生反应的化学方程式:N2H4+2H2O2═R+4H2O,其中R的化学式为( )
A.NO2 B.N2O4 C.NH3 D.N2
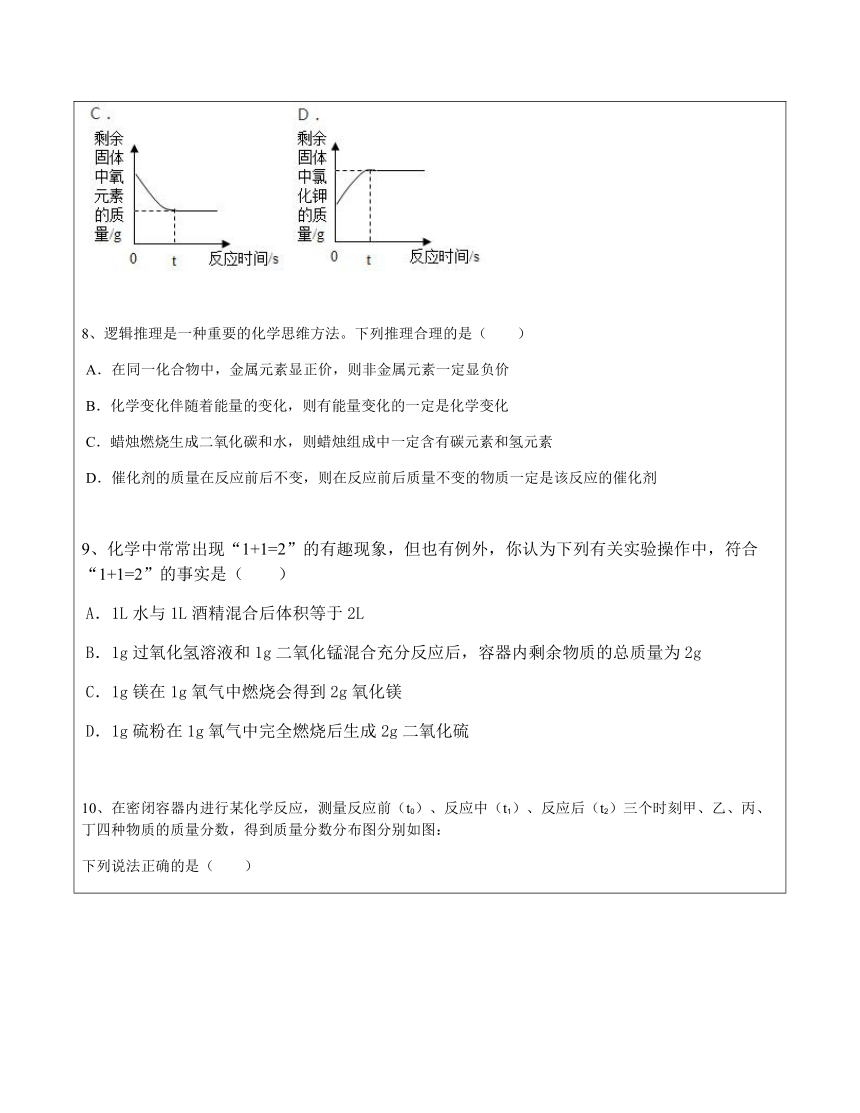
7、对一定量氯酸钾和二氧化锰的混合物加热,下列图象能正确表示对应变化关系的是( )
8、逻辑推理是一种重要的化学思维方法。下列推理合理的是( )
A.在同一化合物中,金属元素显正价,则非金属元素一定显负价
B.化学变化伴随着能量的变化,则有能量变化的一定是化学变化
C.蜡烛燃烧生成二氧化碳和水,则蜡烛组成中一定含有碳元素和氢元素
D.催化剂的质量在反应前后不变,则在反应前后质量不变的物质一定是该反应的催化剂
9、化学中常常出现“1+1=2”的有趣现象,但也有例外,你认为下列有关实验操作中,符合“1+1=2”的事实是( )
A.1L水与1L酒精混合后体积等于2L
B.1g过氧化氢溶液和1g二氧化锰混合充分反应后,容器内剩余物质的总质量为2g
C.1g镁在1g氧气中燃烧会得到2g氧化镁
D.1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫
10、在密闭容器内进行某化学反应,测量反应前(t0)、反应中(t1)、反应后(t2)三个时刻甲、乙、丙、丁四种物质的质量分数,得到质量分数分布图分别如图:
下列说法正确的是( )
A.该反应的类型为化合反应
B.该反应中,参加反应的甲和生成的丁的质量比为20:11
C.t2时刻,还有乙存在,所以乙是催化剂
D.t1时刻,乙和丙的质量比为7:16
本讲重要知识点:
知识点一:
质量守恒定律:
1、内容:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
说明:质量守恒定律只适用于化学变化,不适用于物理变化;只解释化学变化中质量变化,不能解释体积之间的变化。
2、微观解释质量守恒的原因:化学反应的过程,实质上是原子重新组合的过程。
而在化学反应前后,原子的种类、数目、质量均保持不变(原子的“三不变”)。
234315099060
3、化学反应前后 (1)一定不变 宏观:反应物生成物总质量不变;元素种类不变
微观:原子的种类、数目、质量不变
228600099060
(2)一定改变 宏观:物质的种类一定变
微观:分子种类一定变
可能改变:分子总数可能变
练习:
1、在化学反应A+2B═C+2D中,已知16gA与64gB恰好完全反应,生成C和D的质量比为11:9,又知B的相对分子质量为32,则D的相对分子质量为( )
A.9 B.12 C.18 D.36
2、在化学反应前后,肯定不会变化的是(?? )
①原子的数目? ②分子的数目? ③元素的种类? ④物质的质量总和 ⑤物质的种类 ⑥物质的体积?
⑦物质的状态
②④⑤? ?????? ??B.①③④?? ???? ????C.①③④⑥???? ?? ??D.①③⑦
3、在2A+B=2C+4D的反应中,14gA与48gB恰好完全反应生成44gC.若A的相对分子质量为28,则D的相对分子质量为( )
A.36 B.72 C.18 D.64
知识点二:
化学方程式:
例:C+O2点燃 CO2
定义:用化学式来表示化学反应的式子叫做化学方程式。
读法:
1.宏观:碳和氧气在点燃的条件下反应生成二氧化碳 ;
2.微观:每 1 个碳原子和 1 个氧分子在点燃的条件下反应生成 1 个二氧化碳分子;
3.质量关系:每 12 份质量的碳和 32 份质量的氧气在点燃 的条件下反应生成 44份质量的二氧化碳。
各种符号的读法:“+ ”读作“和”或“跟”,“===”读作“反应生成”。
化学方程式的书写步骤:
1.翻译:正确书写反应物与生成物的化学式(注意左反应物右生成物);
2.配平:配上适当的化学计量数(一般为整数);
3.标注:
①注明反应发生的外加条件(如加热、点燃、催化剂、高温、通电等);
②用等号把反应物与生成物连接起来;
③生成物中不同于反应物状态的气体和沉淀用“↑”和“↓”标明。
☆化学方程式配平方法☆:
1.最小公倍数法
方法是: 找左右两边各出现一次且原子数变化较大的元素;求该元素原子个数的最小公倍数;用该最小公倍数除以各自的原子个数,所得的值就是对应物质的计量数。
2.设“1”法
思路是:从组成或原子数较复杂的化学式入手,令其计量数为“1”;推求其它化学式计量数。
课堂练习:
相对原子质量:H-1;C-12;N-14;O-16
一、选择题:
1、在化学反应前后,一定发生了变化的是( )
A.分子的种类 B.分子的个数 C.元素的种类 D.原子的数目
2、食盐(NaCl)不仅可以做调味品,还是一种重要的化工原料。电解饱和食盐水,不可能得到的产物是( )
A.H2?????????????? B.Cl2?????????????? C.NaOH D.Na2CO3
3、关于化学方程式4P+5O22P2O5,获得信息不正确的是( )
A.磷和氧气在点燃的条件下生成五氧化二磷
B.该反应属于化合反应
C.参加反应的磷和氧气质量总和等于生成的五氧化二磷质量
D.点燃条件下,每30份质量的磷和41份质量的氧气反应生成71份质量的五氧化二磷
4、某年5月初,我市某县一副县长酒后驾车将受到法律追究。交警常用一种“酒精检测仪”检查司机是否酒后驾车。其反应原理为C2H5OH + 4CrO3 + 6H2SO4 = 2X + 2CO2↑+9H2O,反应中红色的CrO3转化为绿色的化合物X,则X的化学式为( )
A、Cr2O3 B、CrSO3 C、Cr2(SO4)3 D、Cr2S3
5、如图是某化学反应的微观示意图,其中不同的圆球代表不同原子。下列说法中正确的是( )
364807524130(反应前) (反应后)
(反应前) (反应后)
A.该反应涉及到四种原子
B.该反应属于分解反应
C.参加反应的两种分子的个数比为1∶1
D.该反应前后所有元素的化合价都没有变化
6、 在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表所示。关于此反应下列认识不正确的是( )
物质
甲[
乙
丙
丁
反应前质量/g
1
20
15
2
反应后质量/g
m
29
0
8
A、m的值是1 B、甲可能是该反应的催化剂
C、该反应是分解反应 D、反应中乙、丁的质量比是29:8
填空题:
1、某同学写了以下化学方程式:
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
①未配平的是 ;??②化学式写错的是 ;??③反应条件写错的是 ;④未注明反应条件的是 ;?⑤“↑”使用不当的是 。
2、(1)硫在氧气中燃烧的化学方程式是:S+O2SO2.表示了参与反应的各物质之间的质量关系,即在点燃条件下,每 份质量的硫与 份质量的氧气恰好完全反应生成 份质量的二氧化硫。
(2)化学反应前后必定不发生改变的是 (填字母)
①原子数目②分子数目③元素种类④物质种类⑤原子种类⑥物质的总质量
A.①④⑥B.①③⑤⑥C.①②⑥D.②③⑤
(3)某纯净物X在空气中完全燃烧,反应的化学方程式为2X+3O22CO2+4H2O,则X的化学式为 。
(4)密闭容器中有甲、乙两种物质各10g,加热一段时间后测得容器中各物质的质量如下表所示:
物质
甲
乙
丙
丁
反应后质量g
1.5
X
0.8
2.2
下列选项正确的是 。
A.该反应为化合反应
B.X=54
C.丙、丁一定是单质
D.甲一定是化合物
课后作业:
1、氢气燃烧生成水的反应中,发生变化的是( )
A、分子种类 B、原子种类
C、元素种类 D、物质总质量
2、在一密闭容器中放入X、Y、Z、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识正确的是( )
物质
X
Y
Z
Q
反应前质量/g
20
2
1
37
反应后质量/g
15
32
1
未知
A、物质Y一定是单质
B、反应后物质Q的质量为12g
C、反应过程中X、Q的质量比为9:4
D、物质Z一定的该反应的催化剂
3、在一定条件下,5gA物质和7gB物质恰好完全反应,只生成C、D两种物质。若生成6gC,则生成D的质量是( )
A.5g B.6g C.7g D.4g
4、火箭推进器中盛有N2H4和H2O2,发生反应的化学方程式:N2H4+2H2O2═R+4H2O,其中R的化学式为( )
A.NO2 B.N2O4 C.NH3 D.N2
5、下列有关反应的化学方程式正确的是( )
A.过氧化氢在二氧化锰的催化下分解:H2O2=H2↑+O2↑
B.实验室用氯酸钾制取氧气:2KClO32KCl+3O2
C.碳在氧气中燃烧生成二氧化碳:C+O2CO2↑
D.磷在氧气中燃烧生成五氧化二磷:4P+5O22P2O5
学习目标
1、理解质量守恒定律的宏观概念和微观解释,明晰化学反应前后的“变与不变”;
2、清晰化学方程式的意义与读法;
3、掌握化学方程式的书写步骤,学会至少1种配平方法。
教学内容
堂前测试:
1、在化学反应前后,一定发生了变化的是( )
A.分子的种类 B.分子的个数 C.元素的种类 D.原子的数目
2、食盐(NaCl)不仅可以做调味品,还是一种重要的化工原料。电解饱和食盐水,不可能得到的产物是( )
A.H2???????????????????????? B.Cl2??????????????????????? C.NaOH D.Na2CO3
3、关于化学方程式4P+5O2 2P2O5,获得信息不正确的是( )
A.磷和氧气在点燃的条件下生成五氧化二磷
B.该反应属于化合反应
C.参加反应的磷和氧气质量总和等于生成的五氧化二磷质量
D.点燃条件下,每30份质量的磷和41份质量的氧气反应生成71份质量的五氧化二磷
4、下列实验能够直接用于验证质量守恒定律的是( )
5、在一定条件下,5gA物质和7gB物质恰好完全反应,只生成C、D两种物质。若生成6gC,则生成D的质量是
( )
A.5g B.6g C.7g D.4g
6、火箭推进器中盛有N2H4和H2O2,发生反应的化学方程式:N2H4+2H2O2═R+4H2O,其中R的化学式为( )
A.NO2 B.N2O4 C.NH3 D.N2
7、对一定量氯酸钾和二氧化锰的混合物加热,下列图象能正确表示对应变化关系的是( )
8、逻辑推理是一种重要的化学思维方法。下列推理合理的是( )
A.在同一化合物中,金属元素显正价,则非金属元素一定显负价
B.化学变化伴随着能量的变化,则有能量变化的一定是化学变化
C.蜡烛燃烧生成二氧化碳和水,则蜡烛组成中一定含有碳元素和氢元素
D.催化剂的质量在反应前后不变,则在反应前后质量不变的物质一定是该反应的催化剂
9、化学中常常出现“1+1=2”的有趣现象,但也有例外,你认为下列有关实验操作中,符合“1+1=2”的事实是( )
A.1L水与1L酒精混合后体积等于2L
B.1g过氧化氢溶液和1g二氧化锰混合充分反应后,容器内剩余物质的总质量为2g
C.1g镁在1g氧气中燃烧会得到2g氧化镁
D.1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫
10、在密闭容器内进行某化学反应,测量反应前(t0)、反应中(t1)、反应后(t2)三个时刻甲、乙、丙、丁四种物质的质量分数,得到质量分数分布图分别如图:
下列说法正确的是( )
A.该反应的类型为化合反应
B.该反应中,参加反应的甲和生成的丁的质量比为20:11
C.t2时刻,还有乙存在,所以乙是催化剂
D.t1时刻,乙和丙的质量比为7:16
本讲重要知识点:
知识点一:
质量守恒定律:
1、内容:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
说明:质量守恒定律只适用于化学变化,不适用于物理变化;只解释化学变化中质量变化,不能解释体积之间的变化。
2、微观解释质量守恒的原因:化学反应的过程,实质上是原子重新组合的过程。
而在化学反应前后,原子的种类、数目、质量均保持不变(原子的“三不变”)。
234315099060
3、化学反应前后 (1)一定不变 宏观:反应物生成物总质量不变;元素种类不变
微观:原子的种类、数目、质量不变
228600099060
(2)一定改变 宏观:物质的种类一定变
微观:分子种类一定变
可能改变:分子总数可能变
练习:
1、在化学反应A+2B═C+2D中,已知16gA与64gB恰好完全反应,生成C和D的质量比为11:9,又知B的相对分子质量为32,则D的相对分子质量为( )
A.9 B.12 C.18 D.36
2、在化学反应前后,肯定不会变化的是(?? )
①原子的数目? ②分子的数目? ③元素的种类? ④物质的质量总和 ⑤物质的种类 ⑥物质的体积?
⑦物质的状态
②④⑤? ?????? ??B.①③④?? ???? ????C.①③④⑥???? ?? ??D.①③⑦
3、在2A+B=2C+4D的反应中,14gA与48gB恰好完全反应生成44gC.若A的相对分子质量为28,则D的相对分子质量为( )
A.36 B.72 C.18 D.64
知识点二:
化学方程式:
例:C+O2点燃 CO2
定义:用化学式来表示化学反应的式子叫做化学方程式。
读法:
1.宏观:碳和氧气在点燃的条件下反应生成二氧化碳 ;
2.微观:每 1 个碳原子和 1 个氧分子在点燃的条件下反应生成 1 个二氧化碳分子;
3.质量关系:每 12 份质量的碳和 32 份质量的氧气在点燃 的条件下反应生成 44份质量的二氧化碳。
各种符号的读法:“+ ”读作“和”或“跟”,“===”读作“反应生成”。
化学方程式的书写步骤:
1.翻译:正确书写反应物与生成物的化学式(注意左反应物右生成物);
2.配平:配上适当的化学计量数(一般为整数);
3.标注:
①注明反应发生的外加条件(如加热、点燃、催化剂、高温、通电等);
②用等号把反应物与生成物连接起来;
③生成物中不同于反应物状态的气体和沉淀用“↑”和“↓”标明。
☆化学方程式配平方法☆:
1.最小公倍数法
方法是: 找左右两边各出现一次且原子数变化较大的元素;求该元素原子个数的最小公倍数;用该最小公倍数除以各自的原子个数,所得的值就是对应物质的计量数。
2.设“1”法
思路是:从组成或原子数较复杂的化学式入手,令其计量数为“1”;推求其它化学式计量数。
课堂练习:
相对原子质量:H-1;C-12;N-14;O-16
一、选择题:
1、在化学反应前后,一定发生了变化的是( )
A.分子的种类 B.分子的个数 C.元素的种类 D.原子的数目
2、食盐(NaCl)不仅可以做调味品,还是一种重要的化工原料。电解饱和食盐水,不可能得到的产物是( )
A.H2?????????????? B.Cl2?????????????? C.NaOH D.Na2CO3
3、关于化学方程式4P+5O22P2O5,获得信息不正确的是( )
A.磷和氧气在点燃的条件下生成五氧化二磷
B.该反应属于化合反应
C.参加反应的磷和氧气质量总和等于生成的五氧化二磷质量
D.点燃条件下,每30份质量的磷和41份质量的氧气反应生成71份质量的五氧化二磷
4、某年5月初,我市某县一副县长酒后驾车将受到法律追究。交警常用一种“酒精检测仪”检查司机是否酒后驾车。其反应原理为C2H5OH + 4CrO3 + 6H2SO4 = 2X + 2CO2↑+9H2O,反应中红色的CrO3转化为绿色的化合物X,则X的化学式为( )
A、Cr2O3 B、CrSO3 C、Cr2(SO4)3 D、Cr2S3
5、如图是某化学反应的微观示意图,其中不同的圆球代表不同原子。下列说法中正确的是( )
364807524130(反应前) (反应后)
(反应前) (反应后)
A.该反应涉及到四种原子
B.该反应属于分解反应
C.参加反应的两种分子的个数比为1∶1
D.该反应前后所有元素的化合价都没有变化
6、 在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表所示。关于此反应下列认识不正确的是( )
物质
甲[
乙
丙
丁
反应前质量/g
1
20
15
2
反应后质量/g
m
29
0
8
A、m的值是1 B、甲可能是该反应的催化剂
C、该反应是分解反应 D、反应中乙、丁的质量比是29:8
填空题:
1、某同学写了以下化学方程式:
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
①未配平的是 ;??②化学式写错的是 ;??③反应条件写错的是 ;④未注明反应条件的是 ;?⑤“↑”使用不当的是 。
2、(1)硫在氧气中燃烧的化学方程式是:S+O2SO2.表示了参与反应的各物质之间的质量关系,即在点燃条件下,每 份质量的硫与 份质量的氧气恰好完全反应生成 份质量的二氧化硫。
(2)化学反应前后必定不发生改变的是 (填字母)
①原子数目②分子数目③元素种类④物质种类⑤原子种类⑥物质的总质量
A.①④⑥B.①③⑤⑥C.①②⑥D.②③⑤
(3)某纯净物X在空气中完全燃烧,反应的化学方程式为2X+3O22CO2+4H2O,则X的化学式为 。
(4)密闭容器中有甲、乙两种物质各10g,加热一段时间后测得容器中各物质的质量如下表所示:
物质
甲
乙
丙
丁
反应后质量g
1.5
X
0.8
2.2
下列选项正确的是 。
A.该反应为化合反应
B.X=54
C.丙、丁一定是单质
D.甲一定是化合物
课后作业:
1、氢气燃烧生成水的反应中,发生变化的是( )
A、分子种类 B、原子种类
C、元素种类 D、物质总质量
2、在一密闭容器中放入X、Y、Z、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识正确的是( )
物质
X
Y
Z
Q
反应前质量/g
20
2
1
37
反应后质量/g
15
32
1
未知
A、物质Y一定是单质
B、反应后物质Q的质量为12g
C、反应过程中X、Q的质量比为9:4
D、物质Z一定的该反应的催化剂
3、在一定条件下,5gA物质和7gB物质恰好完全反应,只生成C、D两种物质。若生成6gC,则生成D的质量是( )
A.5g B.6g C.7g D.4g
4、火箭推进器中盛有N2H4和H2O2,发生反应的化学方程式:N2H4+2H2O2═R+4H2O,其中R的化学式为( )
A.NO2 B.N2O4 C.NH3 D.N2
5、下列有关反应的化学方程式正确的是( )
A.过氧化氢在二氧化锰的催化下分解:H2O2=H2↑+O2↑
B.实验室用氯酸钾制取氧气:2KClO32KCl+3O2
C.碳在氧气中燃烧生成二氧化碳:C+O2CO2↑
D.磷在氧气中燃烧生成五氧化二磷:4P+5O22P2O5
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
