苏教版(2019)必修第一册高中化学专题4硫及环境保护-第三单元防治二氧化硫对环境的污染巩固练习
文档属性
| 名称 | 苏教版(2019)必修第一册高中化学专题4硫及环境保护-第三单元防治二氧化硫对环境的污染巩固练习 |

|
|
| 格式 | docx | ||
| 文件大小 | 283.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-16 00:00:00 | ||
图片预览




文档简介
苏教版(2019)必修第一册高中化学专题4硫及环境保护-第三单元防治二氧化硫对环境的污染巩固练习
一、单选题
1.下列关于物质或离子检验的叙述正确的是
A.灼烧某白色粉末,火焰呈黄色,证明原粉末中有K+
B.将某气体通入品红溶液,溶液褪色,证明原气体中含有SO2
C.某溶液中滴入足量稀盐酸后无明显现象,再滴入BaCl2溶液产生白色沉淀,证明原溶液中一定有
D.将某气体通入澄清石灰水,溶液变浑浊,证明原气体一定是CO2
2.联合国气候变化大会于2009年12月7~18日在哥本哈根召开。中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%。有效“减碳”的手段之一是节能。下列制氢方法最节能的是
A.电解水制氢:2H2O2H2↑+O2↑
B.高温使水分解制氢:2H2O2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O2H2↑+O2↑
D.天然气制氢:CH4+H2OCO+3H2
3.酸雨形成的主要原因是( )
A.汽车排出大量尾气 B.自然界中硫化物分解
C.工业上大量燃烧含硫燃料 D.可燃冰燃烧
4.随着工业的发展,大气中CO2的浓度不断增加,如何减少CO2排放已成为全世界关注的热点,低碳经济和低碳生活成为热门话题,以下做法与低碳要求相违背的是 ( )
A.控制高能耗企业上马 B.尽量不使用一次性筷子
C.提倡骑自行车、乘共交车出行 D.多挖煤,多发电,加快经济发展
5.下列不属于空气质量日报监测的物质是( )
A.二氧化硫 B.氮氧化物 C.总悬浮颗粒物 D.二氧化碳
6.除去CO2中SO2的气体,不能选用的试剂为
A.KMnO4溶液 B.NaHCO3溶液 C.NaOH溶液 D.双氧水
7.制备相同质量的硝酸铜,从经济效益和环保角度考虑,最适宜采用的方法是
A.Cu+HNO3(浓)→Cu(NO3)2 B.Cu+HNO3(稀)→Cu(NO3)2
C.Cu+AgNO3→Cu(NO3)2 D.
8.为了除去混入CO2中的SO2,最好将混合气体通入下列哪种溶液中
A.饱和烧碱溶液 B.饱和小苏打溶液 C.饱和纯碱溶液 D.浓硫酸
9.香烟烟雾中含有CO、CO2、SO2、H2O等气体,用①无水CuSO4 ②澄清石灰水③红热CuO ④生石灰 ⑤品红溶液 ⑥酸性高锰酸钾溶液等药品可将其一一检出,检测时香烟烟雾通入药品的正确顺序是
A.①⑤②①④③ B.①⑤⑥②④③ C.③④②⑥⑤① D.②⑤①④③⑥
10.近年来,人类生产、生活所产生的污染使灰霾天气逐渐增多。灰霾粒子的平均直径在1000nm~2000nm。下列有关说法正确的是
A.灰霾可能来自汽车尾气 B.灰霾属于胶体
C.灰霾形成的是非常稳定的体系 D.戴口罩不能阻止呼入灰霾粒子
11.下列溶液中不能够区分SO2和CO2气体的是( )
A.品红溶液 B.H2S溶液 C.澄清石灰水 D.KMnO4溶液
12.下图是某燃煤发电厂处理废气的装置示意图。下列说法正确的是
A.使用此装置处理过的废气就不会对大气造成污染了
B.装置内发生的反应有化合、分解、置换和氧化还原反应
C.整个过程的反应可表示为2SO2+2CaCO3+O2=2CaSO4+2CO2
D.可用澄清的石灰水检验经过处理的废气是否达标
13.下列各组名词或现象中,三者间没有逐级因果关系的是
A.汽车尾气——光化学污染——咳嗽和气喘者增多
B.含磷洗衣粉——水体富营养化——水栖生物大量死亡
C.人口增多——空气中CO2浓度增大——温室效应
D.氟氯烃——臭氧空洞——皮肤癌患者增多
14.下列有关二氧化硫说法中正确的是
A.二氧化硫可用于抑制酒类中细菌生长,可在葡萄酒中微量添加
B.二氧化硫能使品红褪色,加热后不恢复到红色
C.二氧化硫使酸性高锰酸钾褪色,体现了二氧化硫的漂白性
D.二氧化硫属于碱性氧化物,可以用NaOH溶液吸收
15.关于硫化氢气体在空气中完全燃烧的产物,下列叙述正确的是
①具有臭鸡蛋气味的气体 ②是淡黄色的固体
③是无色有刺激性气味的气体 ④是造成酸雨的主要物质
A.② B.③ C.①④ D.③④
二、填空题
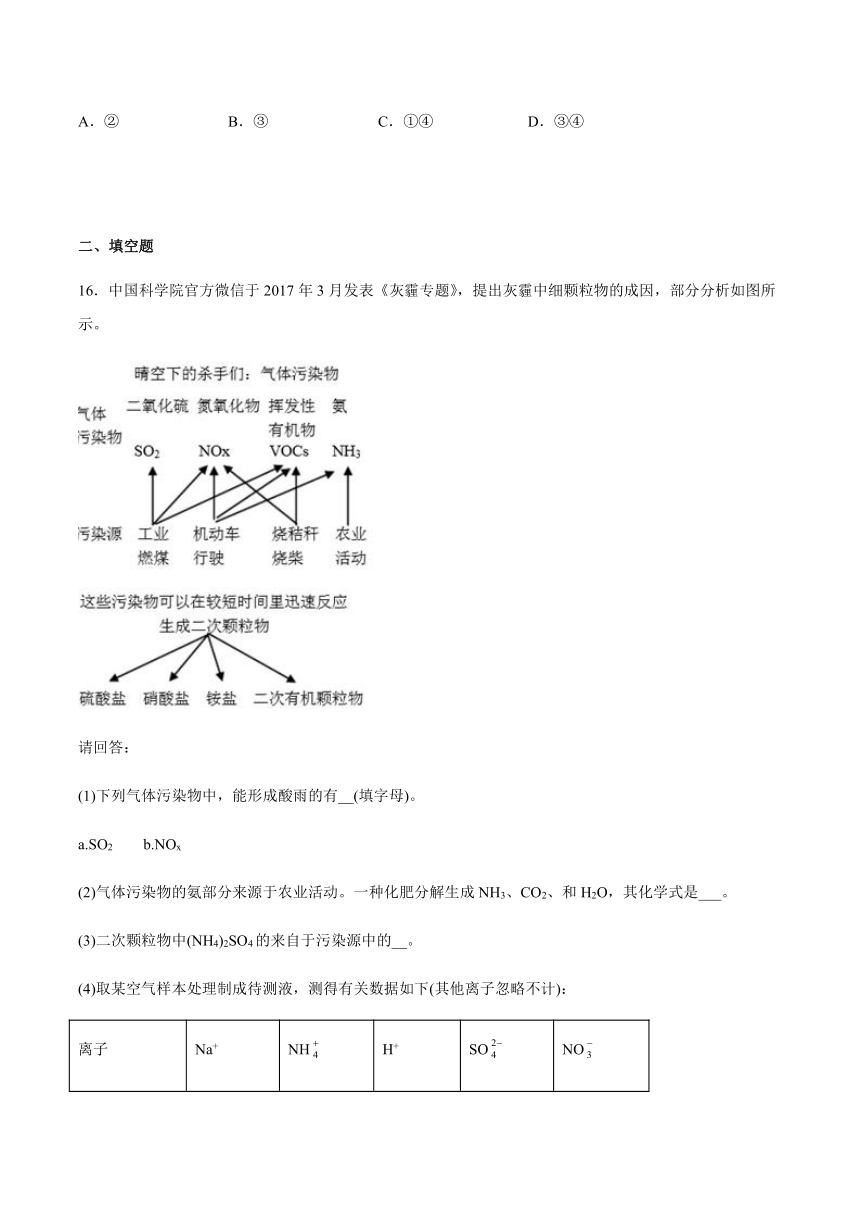
16.中国科学院官方微信于2017年3月发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如图所示。
请回答:
(1)下列气体污染物中,能形成酸雨的有__(填字母)。
a.SO2 b.NOx
(2)气体污染物的氨部分来源于农业活动。一种化肥分解生成NH3、CO2、和H2O,其化学式是___。
(3)二次颗粒物中(NH4)2SO4的来自于污染源中的__。
(4)取某空气样本处理制成待测液,测得有关数据如下(其他离子忽略不计):
离子
Na+
NH
H+
SO
NO
浓度(mol/L)
6×10-6
2×10-5
8.4×10-5
4×10-5
y
表中y=__。
17.为更有效地处理工业废气中的,减少大气污染,科学家们不断地对相关反应进行研究。
(1)按每年全国发电燃煤8亿吨,煤中硫的质量分数以2%计,若不经过脱硫处理,则会有____________亿吨排放到大气中(假设S全部转化为)。
(2)下列物质中,不能吸收的是____________(填标号)。
a.氨水 b.酸性溶液
c.生石灰 d.NaCl溶液
(3)某工厂采用溶液吸收废气中的及用和制备的过程如图所示:
①“吸收”过程中,溶液中和的物质的量之比变__________(填“大”或“小”)。
②“制备”过程中,溶液B中发生反应的化学方程式是_________________________。
③检验产品中含有少量的方法为取少量产品加水溶解,_________________________(将实验操作和现象补充完整)。
18.的排放是造成酸雨的主要因素。形成酸雨的原理之一如图所示:
(1)酸雨的pH____________(填“>”“<”或“=”)5.6.
(2)反应b的化学方程式为_________________________。
(3)D物质的化学式为_________________________。
(4)若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出反应的离子方程式:____________。
19.掌握化学的基本概念和研究方法才能学好化学。按要求回答下列问题:
(1)下列是对碱、酸、盐、氧化物的分类列表:
碱
酸
盐
氧化物
第一组
第二组
第三组
表中每组均有物质分类错误,三组中对应分类错误的物质分别是_________、_________、_________。(填化学式)
(2)固体不能导电,而溶液可以导电,原因是_________________________。
(3)依据下列两个反应,按要求填空。
Ⅰ.
Ⅱ.
反应Ⅰ和反应Ⅱ中,只作氧化剂的反应是________(填“Ⅰ”或“Ⅱ”);反应Ⅱ中,每生成标准状况下,反应中转移________电子;和都能使澄清石灰水变浑浊,请设计一种方法检验、混合气体中的:_____________。
20.(1)材料是人类赖以生存和发展的重要物质基础。
①水泥是最常用的建筑材料,它属于________(填字母)。
a. 金属材料 b. 无机非金属材料 c. 有机高分子材料
②下列硅酸盐产品的生产原料中不需要石灰石的是________(填字母)。
a. 陶瓷 b. 水泥 c. 玻璃
③高岭土是烧制瓷器的重要原料,其组成可以表示为Al2Si2Ox(OH)y,其中x,y的数值分别是________(填字母)。
a. 5、4 b. 6、3 c. 7、2
④下列物品的构成材料中主要是合成高分子材料的是________(填字母)。
a. 宣纸 b. 羊毛衫 c. 保鲜膜
⑤橡胶是制造轮胎的主要原料,天然橡胶是________结构(填“线型”或“体型”),需经过硫化处理改变其结构,增强其机械强度。
(2)某品牌果冻标签如图所示。回答下列问题:
①食品添加剂中,属于无机盐的是______(填化学式)。
②属于着色剂的是诱惑红和______;属于防腐剂的是______。
③配料表中白砂糖的成分是蔗糖,请写出蔗糖在人体内水解的化学方程式______。
(3)化学与科学技术、生产生活及环境保护等密切相关。
①2016年12月我省启动了保卫碧水蓝天的“263”行动,减少煤炭消费总量,减少雾霾天气的发生。形成硫酸型酸雨的主要气体是______;严格整治畜禽养殖场污染,主要是为减少______和P等元素及化学需氧量对水体的污染。
②目前正在推广用尿素水解液来消除柴油汽车尾气中的氮氧化物。写出尿素水解液中的NH3与NO在催化剂作用下,反应生成无污染物质的化学方程式____________________________________________________。
③阿司匹林作为一种药物,主要具有______作用;Mg2Si3O8·nH2O(三硅酸镁)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2 ·H2O等物质的化学方程式___________________________________________。
三、原理综合题
21.某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5?(直径≤2.5?um的悬浮颗粒物,已知1μm=1×10-6 m),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系___________?(填?“属于"或“不属于)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子
K+
Na+
Cl-
浓度/mol/L
4×10-6
6×10-6
2×10-5
4×10-5
3×10-5
2×10-5
根据表中数据判断待测试样为___________(填“酸”或“碱”)性。
(3)煤燃烧排放的烟气含有SO2和NOx形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱碱,脱硝,效果非常好。完成下列对烟气脱氮过程的离子方程式。___________
____+?______NO+____=______Cl-+_____+_______。
(4)洗涤含SO2的烟气,以下物质可作洗涤剂的是___________?(填字母)
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(5)汽车燃油不完全燃烧时产生CO,目前在汽车尾气系统中安装催化转化器,可将CO和NO转化为两种无污染的气体,其化学反应方程式为___________。
四、实验题
22.两个化学兴趣小组进行了以下探究活动:
第一组:为研究铁质材料与热浓硫酸的反应,称取铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。甲同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。分析上述实验中SO2体积分数的结果。甲同学认为气体Y中还可能含有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
(1)写出产生CO2的化学方程式_____________。
(2)装置A中试剂的作用是______,反应的离子方程式________。
(3)如果气体Y中含有H2,预计实验现象应是____________。
(4)简述确认气体Y中含有CO2的实验现象__________。
第二组:拟用下列装置定量分析空气中SO2的含量:
(5)KMnO4溶液中导管末端做成球状多孔结构的作用是________。
(6)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L。若从气体通入到紫色恰好褪去,用时5分钟。则此次取样处的空气中二氧化硫含量为___g/L
23.如图是中学化学实验中常见的制备气体并进行某些物质的检验和性质实验的装置,A是制备气体的装置,C、D、E、F中盛装的液体可能相同,也可能不同。试回答:
如果A中的固体物质是碳,分液漏斗中盛装的是浓硫酸,试写出发生的化学反应方程式:____,若要检验生成的产物,则B、C、D、E、F中应分别加入的试剂为__、__、__、__、__,E中试剂所起的作用__。
参考答案
1.C2.C3.C4.D5.D6.C7.D8.B9.B10.A11.C12.C13.C14.A15.D
16.ab NH4HCO3或(NH4)2CO3 工业燃煤、机动车行驶、农业活动 3×10-5
17.0.32 d 小 先加过量盐酸,充分振荡,再加氯化钡溶液,有白色沉淀产生
18.<
19. 固体中没有自由移动的离子,而在溶液中有自由移动的离子,所以溶液可以导电而固体不导电 Ⅰ 0.2 先将混合气体通入足量的酸性高锰酸钾溶液(或溴水)中,溶液颜色变浅,再通过澄清石灰水,石灰水变浑浊,则证明混合气体中含有
20.b a a c 线型 KCl 柠檬黄 山梨酸钾 C12H22O11(蔗糖) +H2OC6H12O6(葡萄糖)+C6H12O6(果糖) SO2 N(氮) 6NO + 4NH3 5N2 + 6H2O 解热镇痛 Mg2Si3O8?nH2O+4HCl = 2MgCl2 +3SiO2?H2O + (n-1)H2O
21.不属于 酸 3+ 4NO+4OH-=3Cl-+4+2H2O ac 2CO+2NO2CO2+N2
22.C+2H2SO4(浓)CO2↑+2SO2↑+2H2O 除去混合气体中的SO2 5SO2+2+2H2O=5+2Mn2++4H+ E中固体由黑变红和F中固体由白变蓝 B中品红不褪色且C中澄清石灰水变浑浊 增大接触面积,有利于SO2的充分吸收
23.C+2H2SO4(浓)CO2↑+2SO2↑+2H2O 无水CuSO4 品红溶液 足量的酸性KMnO4溶液 品红溶液 澄清石灰水 检验SO2是否已被除尽
一、单选题
1.下列关于物质或离子检验的叙述正确的是
A.灼烧某白色粉末,火焰呈黄色,证明原粉末中有K+
B.将某气体通入品红溶液,溶液褪色,证明原气体中含有SO2
C.某溶液中滴入足量稀盐酸后无明显现象,再滴入BaCl2溶液产生白色沉淀,证明原溶液中一定有
D.将某气体通入澄清石灰水,溶液变浑浊,证明原气体一定是CO2
2.联合国气候变化大会于2009年12月7~18日在哥本哈根召开。中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%。有效“减碳”的手段之一是节能。下列制氢方法最节能的是
A.电解水制氢:2H2O2H2↑+O2↑
B.高温使水分解制氢:2H2O2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O2H2↑+O2↑
D.天然气制氢:CH4+H2OCO+3H2
3.酸雨形成的主要原因是( )
A.汽车排出大量尾气 B.自然界中硫化物分解
C.工业上大量燃烧含硫燃料 D.可燃冰燃烧
4.随着工业的发展,大气中CO2的浓度不断增加,如何减少CO2排放已成为全世界关注的热点,低碳经济和低碳生活成为热门话题,以下做法与低碳要求相违背的是 ( )
A.控制高能耗企业上马 B.尽量不使用一次性筷子
C.提倡骑自行车、乘共交车出行 D.多挖煤,多发电,加快经济发展
5.下列不属于空气质量日报监测的物质是( )
A.二氧化硫 B.氮氧化物 C.总悬浮颗粒物 D.二氧化碳
6.除去CO2中SO2的气体,不能选用的试剂为
A.KMnO4溶液 B.NaHCO3溶液 C.NaOH溶液 D.双氧水
7.制备相同质量的硝酸铜,从经济效益和环保角度考虑,最适宜采用的方法是
A.Cu+HNO3(浓)→Cu(NO3)2 B.Cu+HNO3(稀)→Cu(NO3)2
C.Cu+AgNO3→Cu(NO3)2 D.
8.为了除去混入CO2中的SO2,最好将混合气体通入下列哪种溶液中
A.饱和烧碱溶液 B.饱和小苏打溶液 C.饱和纯碱溶液 D.浓硫酸
9.香烟烟雾中含有CO、CO2、SO2、H2O等气体,用①无水CuSO4 ②澄清石灰水③红热CuO ④生石灰 ⑤品红溶液 ⑥酸性高锰酸钾溶液等药品可将其一一检出,检测时香烟烟雾通入药品的正确顺序是
A.①⑤②①④③ B.①⑤⑥②④③ C.③④②⑥⑤① D.②⑤①④③⑥
10.近年来,人类生产、生活所产生的污染使灰霾天气逐渐增多。灰霾粒子的平均直径在1000nm~2000nm。下列有关说法正确的是
A.灰霾可能来自汽车尾气 B.灰霾属于胶体
C.灰霾形成的是非常稳定的体系 D.戴口罩不能阻止呼入灰霾粒子
11.下列溶液中不能够区分SO2和CO2气体的是( )
A.品红溶液 B.H2S溶液 C.澄清石灰水 D.KMnO4溶液
12.下图是某燃煤发电厂处理废气的装置示意图。下列说法正确的是
A.使用此装置处理过的废气就不会对大气造成污染了
B.装置内发生的反应有化合、分解、置换和氧化还原反应
C.整个过程的反应可表示为2SO2+2CaCO3+O2=2CaSO4+2CO2
D.可用澄清的石灰水检验经过处理的废气是否达标
13.下列各组名词或现象中,三者间没有逐级因果关系的是
A.汽车尾气——光化学污染——咳嗽和气喘者增多
B.含磷洗衣粉——水体富营养化——水栖生物大量死亡
C.人口增多——空气中CO2浓度增大——温室效应
D.氟氯烃——臭氧空洞——皮肤癌患者增多
14.下列有关二氧化硫说法中正确的是
A.二氧化硫可用于抑制酒类中细菌生长,可在葡萄酒中微量添加
B.二氧化硫能使品红褪色,加热后不恢复到红色
C.二氧化硫使酸性高锰酸钾褪色,体现了二氧化硫的漂白性
D.二氧化硫属于碱性氧化物,可以用NaOH溶液吸收
15.关于硫化氢气体在空气中完全燃烧的产物,下列叙述正确的是
①具有臭鸡蛋气味的气体 ②是淡黄色的固体
③是无色有刺激性气味的气体 ④是造成酸雨的主要物质
A.② B.③ C.①④ D.③④
二、填空题
16.中国科学院官方微信于2017年3月发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如图所示。
请回答:
(1)下列气体污染物中,能形成酸雨的有__(填字母)。
a.SO2 b.NOx
(2)气体污染物的氨部分来源于农业活动。一种化肥分解生成NH3、CO2、和H2O,其化学式是___。
(3)二次颗粒物中(NH4)2SO4的来自于污染源中的__。
(4)取某空气样本处理制成待测液,测得有关数据如下(其他离子忽略不计):
离子
Na+
NH
H+
SO
NO
浓度(mol/L)
6×10-6
2×10-5
8.4×10-5
4×10-5
y
表中y=__。
17.为更有效地处理工业废气中的,减少大气污染,科学家们不断地对相关反应进行研究。
(1)按每年全国发电燃煤8亿吨,煤中硫的质量分数以2%计,若不经过脱硫处理,则会有____________亿吨排放到大气中(假设S全部转化为)。
(2)下列物质中,不能吸收的是____________(填标号)。
a.氨水 b.酸性溶液
c.生石灰 d.NaCl溶液
(3)某工厂采用溶液吸收废气中的及用和制备的过程如图所示:
①“吸收”过程中,溶液中和的物质的量之比变__________(填“大”或“小”)。
②“制备”过程中,溶液B中发生反应的化学方程式是_________________________。
③检验产品中含有少量的方法为取少量产品加水溶解,_________________________(将实验操作和现象补充完整)。
18.的排放是造成酸雨的主要因素。形成酸雨的原理之一如图所示:
(1)酸雨的pH____________(填“>”“<”或“=”)5.6.
(2)反应b的化学方程式为_________________________。
(3)D物质的化学式为_________________________。
(4)若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出反应的离子方程式:____________。
19.掌握化学的基本概念和研究方法才能学好化学。按要求回答下列问题:
(1)下列是对碱、酸、盐、氧化物的分类列表:
碱
酸
盐
氧化物
第一组
第二组
第三组
表中每组均有物质分类错误,三组中对应分类错误的物质分别是_________、_________、_________。(填化学式)
(2)固体不能导电,而溶液可以导电,原因是_________________________。
(3)依据下列两个反应,按要求填空。
Ⅰ.
Ⅱ.
反应Ⅰ和反应Ⅱ中,只作氧化剂的反应是________(填“Ⅰ”或“Ⅱ”);反应Ⅱ中,每生成标准状况下,反应中转移________电子;和都能使澄清石灰水变浑浊,请设计一种方法检验、混合气体中的:_____________。
20.(1)材料是人类赖以生存和发展的重要物质基础。
①水泥是最常用的建筑材料,它属于________(填字母)。
a. 金属材料 b. 无机非金属材料 c. 有机高分子材料
②下列硅酸盐产品的生产原料中不需要石灰石的是________(填字母)。
a. 陶瓷 b. 水泥 c. 玻璃
③高岭土是烧制瓷器的重要原料,其组成可以表示为Al2Si2Ox(OH)y,其中x,y的数值分别是________(填字母)。
a. 5、4 b. 6、3 c. 7、2
④下列物品的构成材料中主要是合成高分子材料的是________(填字母)。
a. 宣纸 b. 羊毛衫 c. 保鲜膜
⑤橡胶是制造轮胎的主要原料,天然橡胶是________结构(填“线型”或“体型”),需经过硫化处理改变其结构,增强其机械强度。
(2)某品牌果冻标签如图所示。回答下列问题:
①食品添加剂中,属于无机盐的是______(填化学式)。
②属于着色剂的是诱惑红和______;属于防腐剂的是______。
③配料表中白砂糖的成分是蔗糖,请写出蔗糖在人体内水解的化学方程式______。
(3)化学与科学技术、生产生活及环境保护等密切相关。
①2016年12月我省启动了保卫碧水蓝天的“263”行动,减少煤炭消费总量,减少雾霾天气的发生。形成硫酸型酸雨的主要气体是______;严格整治畜禽养殖场污染,主要是为减少______和P等元素及化学需氧量对水体的污染。
②目前正在推广用尿素水解液来消除柴油汽车尾气中的氮氧化物。写出尿素水解液中的NH3与NO在催化剂作用下,反应生成无污染物质的化学方程式____________________________________________________。
③阿司匹林作为一种药物,主要具有______作用;Mg2Si3O8·nH2O(三硅酸镁)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2 ·H2O等物质的化学方程式___________________________________________。
三、原理综合题
21.某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5?(直径≤2.5?um的悬浮颗粒物,已知1μm=1×10-6 m),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系___________?(填?“属于"或“不属于)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子
K+
Na+
Cl-
浓度/mol/L
4×10-6
6×10-6
2×10-5
4×10-5
3×10-5
2×10-5
根据表中数据判断待测试样为___________(填“酸”或“碱”)性。
(3)煤燃烧排放的烟气含有SO2和NOx形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱碱,脱硝,效果非常好。完成下列对烟气脱氮过程的离子方程式。___________
____+?______NO+____=______Cl-+_____+_______。
(4)洗涤含SO2的烟气,以下物质可作洗涤剂的是___________?(填字母)
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(5)汽车燃油不完全燃烧时产生CO,目前在汽车尾气系统中安装催化转化器,可将CO和NO转化为两种无污染的气体,其化学反应方程式为___________。
四、实验题
22.两个化学兴趣小组进行了以下探究活动:
第一组:为研究铁质材料与热浓硫酸的反应,称取铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。甲同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O=2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。分析上述实验中SO2体积分数的结果。甲同学认为气体Y中还可能含有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
(1)写出产生CO2的化学方程式_____________。
(2)装置A中试剂的作用是______,反应的离子方程式________。
(3)如果气体Y中含有H2,预计实验现象应是____________。
(4)简述确认气体Y中含有CO2的实验现象__________。
第二组:拟用下列装置定量分析空气中SO2的含量:
(5)KMnO4溶液中导管末端做成球状多孔结构的作用是________。
(6)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L。若从气体通入到紫色恰好褪去,用时5分钟。则此次取样处的空气中二氧化硫含量为___g/L
23.如图是中学化学实验中常见的制备气体并进行某些物质的检验和性质实验的装置,A是制备气体的装置,C、D、E、F中盛装的液体可能相同,也可能不同。试回答:
如果A中的固体物质是碳,分液漏斗中盛装的是浓硫酸,试写出发生的化学反应方程式:____,若要检验生成的产物,则B、C、D、E、F中应分别加入的试剂为__、__、__、__、__,E中试剂所起的作用__。
参考答案
1.C2.C3.C4.D5.D6.C7.D8.B9.B10.A11.C12.C13.C14.A15.D
16.ab NH4HCO3或(NH4)2CO3 工业燃煤、机动车行驶、农业活动 3×10-5
17.0.32 d 小 先加过量盐酸,充分振荡,再加氯化钡溶液,有白色沉淀产生
18.<
19. 固体中没有自由移动的离子,而在溶液中有自由移动的离子,所以溶液可以导电而固体不导电 Ⅰ 0.2 先将混合气体通入足量的酸性高锰酸钾溶液(或溴水)中,溶液颜色变浅,再通过澄清石灰水,石灰水变浑浊,则证明混合气体中含有
20.b a a c 线型 KCl 柠檬黄 山梨酸钾 C12H22O11(蔗糖) +H2OC6H12O6(葡萄糖)+C6H12O6(果糖) SO2 N(氮) 6NO + 4NH3 5N2 + 6H2O 解热镇痛 Mg2Si3O8?nH2O+4HCl = 2MgCl2 +3SiO2?H2O + (n-1)H2O
21.不属于 酸 3+ 4NO+4OH-=3Cl-+4+2H2O ac 2CO+2NO2CO2+N2
22.C+2H2SO4(浓)CO2↑+2SO2↑+2H2O 除去混合气体中的SO2 5SO2+2+2H2O=5+2Mn2++4H+ E中固体由黑变红和F中固体由白变蓝 B中品红不褪色且C中澄清石灰水变浑浊 增大接触面积,有利于SO2的充分吸收
23.C+2H2SO4(浓)CO2↑+2SO2↑+2H2O 无水CuSO4 品红溶液 足量的酸性KMnO4溶液 品红溶液 澄清石灰水 检验SO2是否已被除尽
