2020—2021学年人教版高中化学有机化学基础第五章《进入合成有机高分子化合物的时代》单元测试卷 含解析
文档属性
| 名称 | 2020—2021学年人教版高中化学有机化学基础第五章《进入合成有机高分子化合物的时代》单元测试卷 含解析 |

|
|
| 格式 | docx | ||
| 文件大小 | 204.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-19 00:00:00 | ||
图片预览



文档简介
第五章《进入合成有机高分子化合物的时代》单元测试卷
一、单选题(共15小题)
1.下列关于生产、生活中的化学问题的叙述中,正确的是( )
A.
在使用或生产易燃、易爆物的工厂车间,最好不穿化纤类工作服
B.
糯米中的淀粉一经发生水解反应就酿造成酒
C.
食用植物油的主要成分是高级饱和脂肪酸的甘油酯,是人体内不可缺少的重要营养物质
D.
市场销售的洗涤灵的主要成分是对十二烷基苯磺酸钠,它能洗去餐具上的油污,发生的主要是化学变化
2.下列说法不正确的是( )
A.
贝采里乌斯提出了有机化学概念,维勒打破了无机物和有机物的界限,范特霍夫提出了有机化合物的三维结构
B.
同位素示踪法、红外光谱法都是科学家经常使用的研究化学反应历程的手段之一
C.
分光光度计通过测定溶液颜色分析反应物(或生成物)浓度变化,从而确定化学反应速率
D.
科学家将蛋白质的结构层次分为四级进行研究,蛋白质的二级结构主要依靠肽链中﹣NH﹣上的氢原子与羰基上的氧原子形成氢键而实现的
3.下列有关新型高分子材料的说法中不正确的是( )
A.
高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿造业等
B.
复合材料一般是以一种材料作为基体,另一种材料作为增强体
C.
导电塑料是应用于电子工业的一种新型有机高分子材料
D.
合成高分子材料制成的人工器官都受到人体的排斥作用,难以达到生理相容的程度
4.当航天飞机返回地球大气层时,由于空气的剧烈摩擦,飞机尖端的温度可达1000℃以上,为了防止高温将它烧毁,科学家给航天飞机的相应部位安装了可靠的保护层,制作保护层的材料是( )
A.
塑料
B.
合成纤维
C.
新型陶瓷和碳纤维的复合材料
D.
镁铝合金
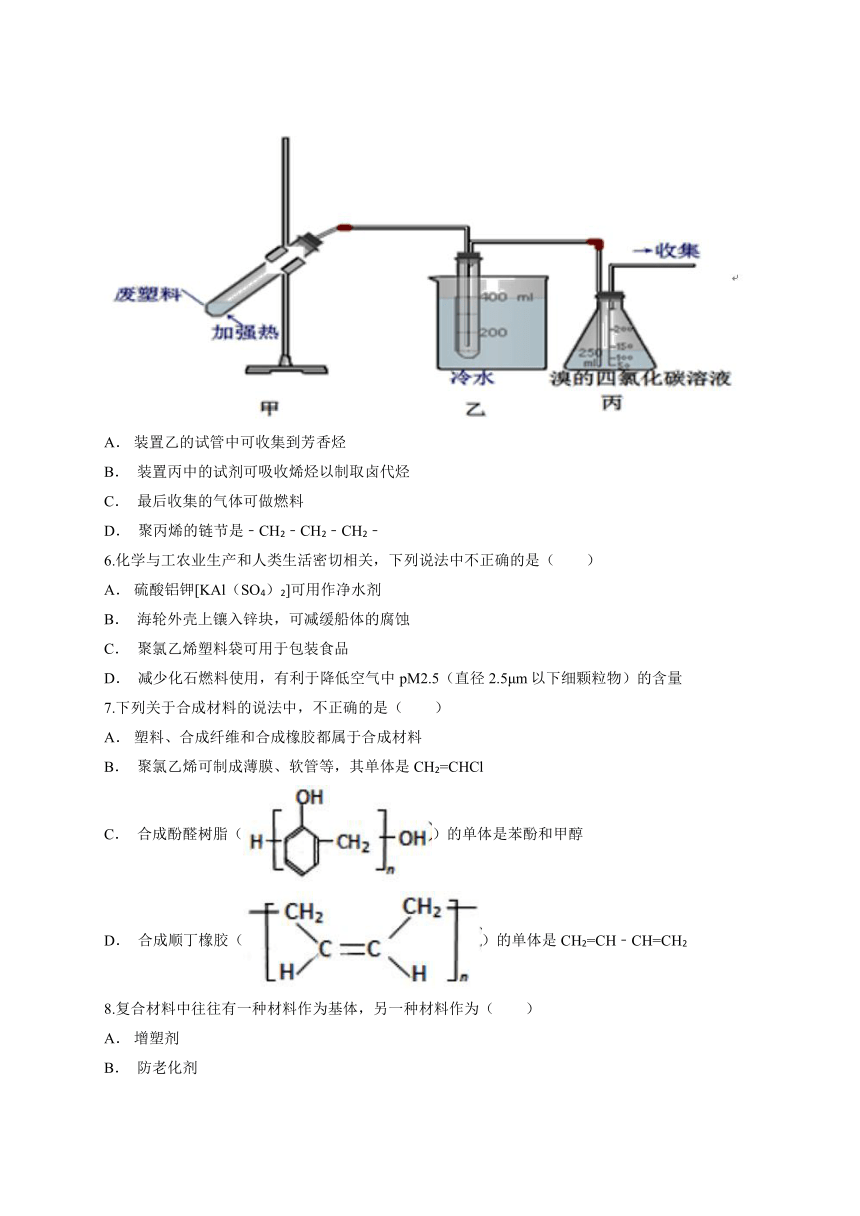
5.加热聚丙烯费塑料可以得到碳、氢气、甲烷、乙烯、苯和甲苯,用图所示装置探究废旧塑料的再利用,下列叙述不正确的是( )
A.
装置乙的试管中可收集到芳香烃
B.
装置丙中的试剂可吸收烯烃以制取卤代烃
C.
最后收集的气体可做燃料
D.
聚丙烯的链节是﹣CH2﹣CH2﹣CH2﹣
6.化学与工农业生产和人类生活密切相关,下列说法中不正确的是( )
A.
硫酸铝钾[KAl(SO4)2]可用作净水剂
B.
海轮外壳上镶入锌块,可减缓船体的腐蚀
C.
聚氯乙烯塑料袋可用于包装食品
D.
减少化石燃料使用,有利于降低空气中pM2.5(直径2.5μm以下细颗粒物)的含量
7.下列关于合成材料的说法中,不正确的是( )
A.
塑料、合成纤维和合成橡胶都属于合成材料
B.
聚氯乙烯可制成薄膜、软管等,其单体是CH2=CHCl
C.
合成酚醛树脂()的单体是苯酚和甲醇
D.
合成顺丁橡胶()的单体是CH2=CH﹣CH=CH2
8.复合材料中往往有一种材料作为基体,另一种材料作为( )
A.
增塑剂
B.
防老化剂
C.
发泡剂
D.
增强剂
9.化学与科技、社会、生活有着密切的联系,下列说法不正确的是( )
A.
橡胶、塑料和光导纤维都是有机高分子化合物
B.
废电池要集中处理,防止其中的重金属盐对土壤和水源造成污染
C.
从海水提取金属镁的过程中涉及氧化还原反应
D.
利用太阳能、风能和氢能替代化石能源能改善空气质量
10.塑化剂的成分主要是邻苯二甲酸二异丁酯等酯类,塑料管道、塑胶容器、瓶盖或其他塑料包装材料都含有塑化剂,塑化剂超标对人体有害,调查发现,最近深受关注的白酒中含有的塑化剂主要是由塑料制品中的塑化剂迁移到酒中所致,此处“迁移”所涉及的主要原理是( )
A.
萃取
B.
蒸馏
C.
溶解
D.
渗析
11.化学与生活、生产、环境等社会实际密切相关.下列叙述正确的是( )
A.
稀的食盐水能杀死H7N9禽流感病毒
B.
涤纶、塑料、光导纤维都是有机高分子材料
C.
用电镀厂的废水直接灌溉农田,可提高水的利用率
D.
外形似海绵、密度小、有磁性的碳与石墨互为同素异形体
12.下列塑料可用作不粘锅的表面材料的是( )
A.
聚氯乙烯
B.
聚四氟乙烯
C.
聚苯乙烯
D.
有机玻璃
13.日常生活中接触到的材料多为合成材料,下列物质中,不属于合成材料的是( )
A.
塑料
B.
棉花
C.
合成纤维
D.
合成橡胶
14.波音787型飞机的机身和机翼大量使用下列哪种材料( )
A.
液晶高分子材料
B.
橡胶
C.
高分子分离膜
D.
碳纤维复合材料
15.橡胶属于重要的工业原料.它是一种有机高分子化合物,具有良好的弹性,但强度较差.为了增加某些橡胶制品的强度,加工时往往需进行硫化处理,即将橡胶原料与硫磺在一定条件下反应;橡胶制品硫化程度越高,强度越大,弹性越差,下列橡胶制品中,加工时硫化程度较高的是( )
A.
橡皮筋
B.
汽车外胎
C.
普通气球
D.
医用乳胶手套
二、实验题(共3小题)
16.废旧塑料回收和利用是减轻“白色污染”、实现资源再利用的有效途径之一,某兴趣小组进行如下探究:
17.某化学课外活动小组探究淀粉水解的条件,进行以下两个实验了:
(1)实验用品:0.5g淀粉、4mL
20%硫酸溶液、氢氧化钠溶液、银氨溶液、碘水;
步骤:在试管1和试管2里各放入0.5g淀粉,在试管1里加入4mL
20%硫酸溶液,在试管2里加入4mL水,都加热3~4min.用过量碱液中和试管1里的硫酸溶液,把一部分液体倒入试管3,在试管2、3里都加入碘水,观察有没有蓝色出现,在试管1里加入银氨溶液,稍加热后,观察试管内壁上有无银镜出现。根据所学知识预测可能的实验现象,实验现象与结论(填入下表):
(2)实验用品:0.5g淀粉、唾液、新制氢氧化铜悬浊液:
步骤:在试管中加入0.5g淀粉,加入少许唾液加热,在水解液中加入新制氢氧化铜悬浊液加热煮沸,观察现象;
现象:_________;
结论:_________;
(3)比较实验(1)(2)可得出的结论:_________。
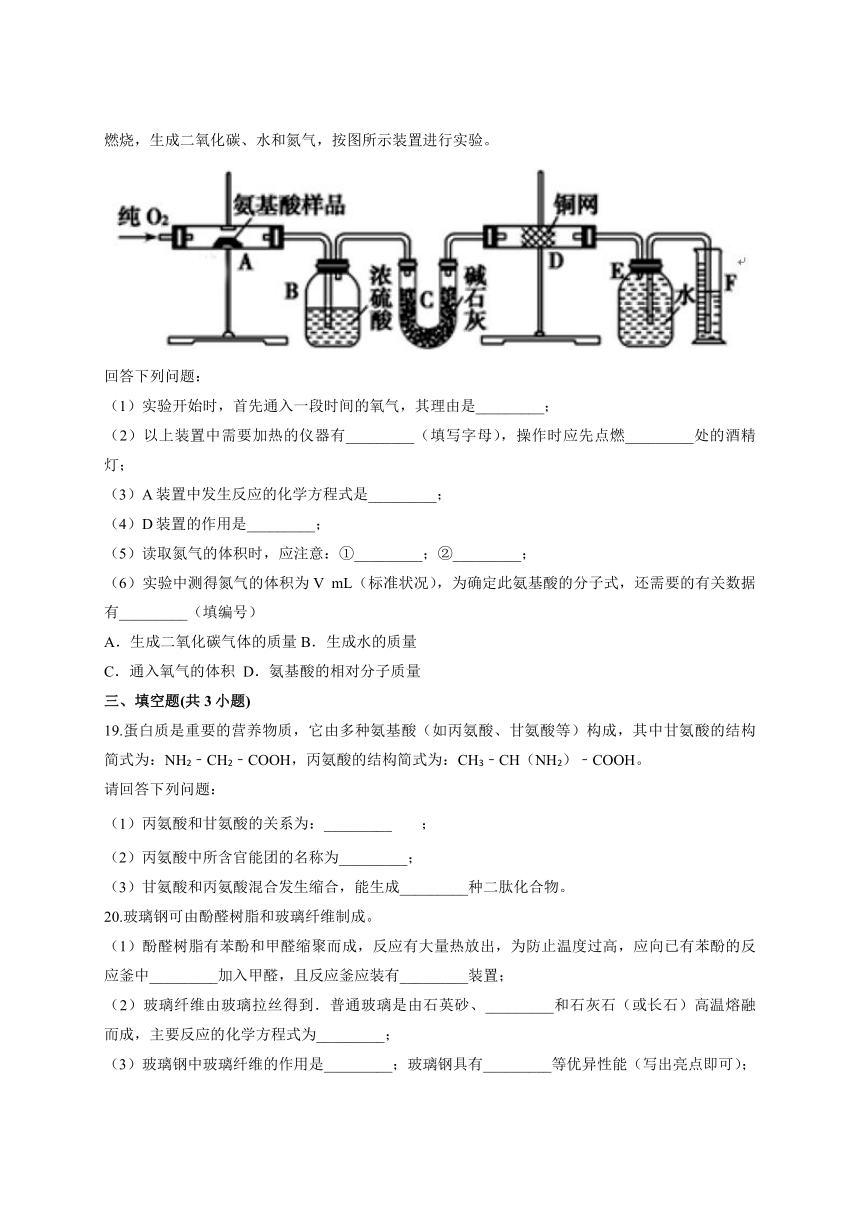
18.实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成,取W
g该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气,按图所示装置进行实验。
回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是_________;
(2)以上装置中需要加热的仪器有_________(填写字母),操作时应先点燃_________处的酒精灯;
(3)A装置中发生反应的化学方程式是_________;
(4)D装置的作用是_________;
(5)读取氮气的体积时,应注意:①_________;②_________;
(6)实验中测得氮气的体积为V
mL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有_________(填编号)
A.生成二氧化碳气体的质量
B.生成水的质量
C.通入氧气的体积
D.氨基酸的相对分子质量
三、填空题(共3小题)
19.蛋白质是重要的营养物质,它由多种氨基酸(如丙氨酸、甘氨酸等)构成,其中甘氨酸的结构简式为:NH2﹣CH2﹣COOH,丙氨酸的结构简式为:CH3﹣CH(NH2)﹣COOH。
请回答下列问题:
(1)丙氨酸和甘氨酸的关系为:_________;
(2)丙氨酸中所含官能团的名称为_________;
(3)甘氨酸和丙氨酸混合发生缩合,能生成_________种二肽化合物。
20.玻璃钢可由酚醛树脂和玻璃纤维制成。
(1)酚醛树脂有苯酚和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向已有苯酚的反应釜中_________加入甲醛,且反应釜应装有_________装置;
(2)玻璃纤维由玻璃拉丝得到.普通玻璃是由石英砂、_________和石灰石(或长石)高温熔融而成,主要反应的化学方程式为_________;
(3)玻璃钢中玻璃纤维的作用是_________;玻璃钢具有_________等优异性能(写出亮点即可);
(4)下列处理废旧热固性酚醛塑料的做法合理的是_________;
a.深埋
b.粉碎后用作树脂填料
c.用作燃料
d.用有机溶剂将其溶解,回收树脂
21.①一种二肽的结构简式为:,合成这种二肽的氨基酸是_________和_________;
②生活中有大量的铝制品.家用铝锅不能用热碱水洗涤去污,原因是(用离子方程式表示)_________;
③大量使用塑料制品产生的污染称之为_________,防治该污染的有效措施之一是进行回收利用,将回收后的塑料进行_________,可以获得乙烯、丙烯等化工原料;
④传统生产水泥的原料中除了石灰石、粘土外,还经常添加_________,以调节水泥的硬化速度。
答案解析
1.【答案】A
【解析】A.在有易燃易爆物的工作场所,严禁穿化纤类衣服,因为化纤类衣服摩擦时容易产生火花,故A正确;
B.淀粉水解的产物可能有麦芽糖、葡萄糖,当水解为葡萄糖后,葡萄糖可能发酵为酒精或者乳酸,才酿成酒,故B错误;
C.食用植物油的主要成分是高级不饱和脂肪酸的甘油酯,故C错误;
D.对十二烷基苯磺酸钠是表面活性剂,发生物理变化,故D错误。
2.【答案】B
【解析】A,贝采里乌斯被称为“有机化学之父”,提出了有机化学概念,法国化学家维勒由氰酸铵合成了尿素,首次打破了有机物和无机物的界限,荷兰化学家范特霍夫提出了有机化合物的三维结构,故A正确;
B,红外光谱法是对各种吸收红外光的化合物的定量和定性分析的一种方法,用于研究化学物质的结构,不能用于研究化学反应历程,故B错误;
C,由利用溶液颜色与反应物(或生成物)浓度的关系,可以确定该化学反应的速率,给出的仪器中只有分光光度计可进行比色分析,故C正确;
D,羰基上的氧可以﹣NH﹣上的氢形成氢键,蛋白质的二级结构主要依靠肽链中﹣NH﹣上的氢原子与羰基上的氧原子形成氢键而实现的,故D正确。
3.【答案】D
【解析】A.高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿造业等,故A正确;
B.复合材料一般是以一种材料作为基体,另一种材料作为增强体,故B正确;
C.导电塑料是将树脂和导电物质混合,用塑料的加工方式进行加工的功能型高分子材料.主要应用于电子、集成电路包装、电磁波屏蔽等领域,故C正确;D.医用高分子材料归属于功能高分子材料,它们都无毒、具有良好的生物相容性和稳定性,有足够的机械强度等特点,故D错误。
4.【答案】C
【解析】A.塑料的熔点很小,所以不能耐高温,故A错误;
B.合成纤维具有强度高、弹性好、耐腐蚀等优点,但合成纤维的熔点较低,所以不能耐高温,故B错误;
C.耐高温新型陶瓷熔点较高,所以能耐高温,故C正确;
D.镁铝合金的熔点较低,故D错误。
5.【答案】D
6.【答案】C
【解析】A.硫酸铝钾可水解生成具有吸附性的氢氧化铝胶体,可用于净水,故A正确;
B.锌比铁活泼,海轮外壳上镶入锌块,为牺牲阳极的阴极保护法,可减缓船体的腐蚀,故B正确;
C.聚氯乙烯塑料中的增塑剂有毒,不能用于包装食品,故C错误;
D.减少化石燃料使用,可减少颗粒物的排放,故D正确。
7.【答案】C
8.【答案】D
【解析】复合材料是将两种或两种以上性质不同的材料经特殊加工而成的材料.其中,一种材料作为基体,另一种材料作增强剂,塑料中一般添加增塑剂和防老化剂,故选D。
9.【答案】A
【解析】A.光导纤维的成分是二氧化硅,不是有机高分子化合物,故A错误;
B.废旧电池进行回收利用,集中处理的主要原因是防治废电池中镉、铅等重金属离子对土壤和水源的污染,故B正确;
C.电解熔融氯化镁,得到金属镁,为氧化还原反应,生成镁和氯气,故C正确;
D.太阳能、风能和氢能等是清洁能源,利用太阳能、风能和氢能等能源替代化石能源可以减少污染物的排放,改善空气质量,故D正确。
10.【答案】C
【解析】A.萃取利用溶质在不同溶剂中溶解度不同,用一种溶剂把溶质从它与另一溶剂所组成的溶液中提取出来;
B.蒸馏把互相溶解但沸点不同的两种液体或将水中难挥发性物质和水分离出来;
C.超过两种以上物质混合而成为一个分子状态的均匀相的过程称为溶解;
D.利用粒子直径大小,可用渗析的方法分离;这里的“迁移”指塑料中的塑化剂溶解在酒精中,故选C。
11.【答案】D
【解析】A.稀的食盐水只能够降低蛋白质的溶解度,不能使蛋白质变性,所以稀的食盐水不能杀死H7N9禽流感病毒,故A错误;
B.光导纤维的主要成分是二氧化硅,属于无机非金属材料,故B错误;
C.用电镀厂的废水直接灌溉农田,会引起环境污染,不利用食品的安全,故C错误;
D.外形似海绵、密度小、有磁性的碳和石墨都是有碳元素组成,二者结构和性质不同,符合同素异形体的概念,属于同素异形体,故D正确。
12.【答案】B
【解析】聚四氟乙烯具有抗酸抗碱、抗各种有机溶剂的特点,不溶于强酸、强碱和有机溶剂,同时具有耐高温的特点,聚氯乙烯、聚苯乙烯、有机玻璃不耐高温,不能做不粘锅的表面材料,
故选B.
13.【答案】B
【解析】塑料、合成纤维、合成橡胶是人工合成材料,棉花、羊毛和真丝等都属于天然材料,故选B。
14.【答案】D
【解析】A.液晶高分子材料是做液晶屏的材料,故A错误;
B.因为橡胶较软不可能做机身,故B错误;
C.高分子分离膜是由聚合物或高分子复合材料制得的具有分离流体混合物功能的薄膜,故C错误;
D.碳纤维复合材料有很大的韧性刚性,而且碳纤维复合材料的密度较小,故D正确。
15.【答案】B
【解析】A.橡皮筋需要较好的弹性,硫化程度不宜过高,故A错误;
B.汽车外胎应具有弹性差、强度很大的特征,硫化程度较高时符合要求,故B正确;
C.气球需要较高的弹性,硫化程度不宜过高,故C错误;
D.医用乳胶手套需要较高的弹性,硫化程度不宜过高,故D错误。
16.【答案】(1)将混合物注入分液漏斗,加入酸性高锰酸钾溶液,振荡,再往混合应液中加入一定量的氢氧化钠溶液振荡、静置、分液
(2)检验并除去气态不饱和烃
(3)无法判定E中是否有水产生
(4)气态烷烃;
【解析】(1)甲苯能够与酸性高锰酸钾溶液反应生成可溶于水中的物质,可以用酸性高锰酸钾溶液除去苯中的甲苯,操作方法为:将混合物注入分液漏斗,加入酸性高锰酸钾溶液,振荡,再往混合应液中加入一定量的氢氧化钠溶液振荡、静置、分液;
(2)装置C中盛有溴水,利用溴水检验并除去废旧粗料分解生成的气态不饱和烃;
(3)装置F用于检验装置E中有水分生成,若没有装置D,用于气体中混有水分,无法证明装置E中有水生成;
(4)从C中出来的气体中,不饱和烃已经除去,另外生成产物有可能为氢气或饱和烃,所以其他成分可能是气体烷烃;CuO能将烃氧化成CO2和H2O,可以通过检验反应产物中有二氧化碳和水生成,就可以证明其它气体为饱和烷烃,所以图2的装置应该使用澄清石灰水,目的是检验产物中有二氧化碳生成,图2装置可以为。
17.【答案】(1)
(2)产生砖红色沉淀;淀粉在唾液作用下水解生成了葡萄糖
(3)淀粉水解需要稀硫酸或唾液中的酶作催化剂
18.【答案】(1)将装置中的N2排净
(2)AD;D
(4):吸收未反应的氧气,保证最终收集的气体为N2;
(5)①量筒内液面与广口瓶中的液面相持平 ②视线与凹液面最低处相切
(6)ABD
19.【答案】(1)互为同系物
(2)氨基、羧基
(3)4
【解析】(1)丙氨酸比甘氨酸多一个CH2原子,二者都是氨基酸,互为同系物;
(2)丙氨酸中含有氨基、羧基2种官能团;
(3)氨基酸生成二肽,就是两个氨基酸分子脱去一个水分子,当同种氨基酸脱水,生成2种二肽;当是异种氨基酸脱水:可以是甘氨酸脱去羟基,丙氨酸脱氢;也可以丙氨酸脱羟基,甘氨酸脱去氢,生成2种二肽,所以共有4种。
20.【答案】(1)间歇性、散热
(2)纯碱;Na2CO3+SiO2Na2SiO3+CO2↑、CaCO3+SiO2CaSiO3+CO2↑
(3)增强体
强度高、质量轻(或耐腐蚀、抗冲击、绝缘性能好等)
(4)bc
【解析】(1)苯酚和甲醛发生缩聚反应,反应有大量热放出,为防止温度过高,应向已有苯酚的反应釜中间歇性的加入甲醛,并装有散热装置;
(2)生产玻璃的原料:石灰石、石英砂、纯碱,反应原理为:Na2CO3+SiO2Na2SiO3+CO2↑、CaCO3+SiO2CaSiO3+CO2↑;
(3)玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料,其中玻璃纤维的作用是增强体,合成材料是基体,它的优点有:强度高、质量轻、耐腐蚀、抗冲击、绝缘性能好等;
(4)废旧合成材料的再生利用主要有三条途径:通过再生和改性,重新做成多种有用的材料和制品;采用热裂解或化学处理方法使其分解,用于制备多种化工原料;将废旧的聚合物作为燃料回收利用热能,塑料深埋很久不会腐烂,会造成白色污染,酚醛塑料不能溶于有机溶剂,故选bc。
21.【答案】①甘氨酸;丙氨酸
②Al2O3+2OHˉ=2AlO2ˉ+H2O
③白色污染;裂解
④石膏
一、单选题(共15小题)
1.下列关于生产、生活中的化学问题的叙述中,正确的是( )
A.
在使用或生产易燃、易爆物的工厂车间,最好不穿化纤类工作服
B.
糯米中的淀粉一经发生水解反应就酿造成酒
C.
食用植物油的主要成分是高级饱和脂肪酸的甘油酯,是人体内不可缺少的重要营养物质
D.
市场销售的洗涤灵的主要成分是对十二烷基苯磺酸钠,它能洗去餐具上的油污,发生的主要是化学变化
2.下列说法不正确的是( )
A.
贝采里乌斯提出了有机化学概念,维勒打破了无机物和有机物的界限,范特霍夫提出了有机化合物的三维结构
B.
同位素示踪法、红外光谱法都是科学家经常使用的研究化学反应历程的手段之一
C.
分光光度计通过测定溶液颜色分析反应物(或生成物)浓度变化,从而确定化学反应速率
D.
科学家将蛋白质的结构层次分为四级进行研究,蛋白质的二级结构主要依靠肽链中﹣NH﹣上的氢原子与羰基上的氧原子形成氢键而实现的
3.下列有关新型高分子材料的说法中不正确的是( )
A.
高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿造业等
B.
复合材料一般是以一种材料作为基体,另一种材料作为增强体
C.
导电塑料是应用于电子工业的一种新型有机高分子材料
D.
合成高分子材料制成的人工器官都受到人体的排斥作用,难以达到生理相容的程度
4.当航天飞机返回地球大气层时,由于空气的剧烈摩擦,飞机尖端的温度可达1000℃以上,为了防止高温将它烧毁,科学家给航天飞机的相应部位安装了可靠的保护层,制作保护层的材料是( )
A.
塑料
B.
合成纤维
C.
新型陶瓷和碳纤维的复合材料
D.
镁铝合金
5.加热聚丙烯费塑料可以得到碳、氢气、甲烷、乙烯、苯和甲苯,用图所示装置探究废旧塑料的再利用,下列叙述不正确的是( )
A.
装置乙的试管中可收集到芳香烃
B.
装置丙中的试剂可吸收烯烃以制取卤代烃
C.
最后收集的气体可做燃料
D.
聚丙烯的链节是﹣CH2﹣CH2﹣CH2﹣
6.化学与工农业生产和人类生活密切相关,下列说法中不正确的是( )
A.
硫酸铝钾[KAl(SO4)2]可用作净水剂
B.
海轮外壳上镶入锌块,可减缓船体的腐蚀
C.
聚氯乙烯塑料袋可用于包装食品
D.
减少化石燃料使用,有利于降低空气中pM2.5(直径2.5μm以下细颗粒物)的含量
7.下列关于合成材料的说法中,不正确的是( )
A.
塑料、合成纤维和合成橡胶都属于合成材料
B.
聚氯乙烯可制成薄膜、软管等,其单体是CH2=CHCl
C.
合成酚醛树脂()的单体是苯酚和甲醇
D.
合成顺丁橡胶()的单体是CH2=CH﹣CH=CH2
8.复合材料中往往有一种材料作为基体,另一种材料作为( )
A.
增塑剂
B.
防老化剂
C.
发泡剂
D.
增强剂
9.化学与科技、社会、生活有着密切的联系,下列说法不正确的是( )
A.
橡胶、塑料和光导纤维都是有机高分子化合物
B.
废电池要集中处理,防止其中的重金属盐对土壤和水源造成污染
C.
从海水提取金属镁的过程中涉及氧化还原反应
D.
利用太阳能、风能和氢能替代化石能源能改善空气质量
10.塑化剂的成分主要是邻苯二甲酸二异丁酯等酯类,塑料管道、塑胶容器、瓶盖或其他塑料包装材料都含有塑化剂,塑化剂超标对人体有害,调查发现,最近深受关注的白酒中含有的塑化剂主要是由塑料制品中的塑化剂迁移到酒中所致,此处“迁移”所涉及的主要原理是( )
A.
萃取
B.
蒸馏
C.
溶解
D.
渗析
11.化学与生活、生产、环境等社会实际密切相关.下列叙述正确的是( )
A.
稀的食盐水能杀死H7N9禽流感病毒
B.
涤纶、塑料、光导纤维都是有机高分子材料
C.
用电镀厂的废水直接灌溉农田,可提高水的利用率
D.
外形似海绵、密度小、有磁性的碳与石墨互为同素异形体
12.下列塑料可用作不粘锅的表面材料的是( )
A.
聚氯乙烯
B.
聚四氟乙烯
C.
聚苯乙烯
D.
有机玻璃
13.日常生活中接触到的材料多为合成材料,下列物质中,不属于合成材料的是( )
A.
塑料
B.
棉花
C.
合成纤维
D.
合成橡胶
14.波音787型飞机的机身和机翼大量使用下列哪种材料( )
A.
液晶高分子材料
B.
橡胶
C.
高分子分离膜
D.
碳纤维复合材料
15.橡胶属于重要的工业原料.它是一种有机高分子化合物,具有良好的弹性,但强度较差.为了增加某些橡胶制品的强度,加工时往往需进行硫化处理,即将橡胶原料与硫磺在一定条件下反应;橡胶制品硫化程度越高,强度越大,弹性越差,下列橡胶制品中,加工时硫化程度较高的是( )
A.
橡皮筋
B.
汽车外胎
C.
普通气球
D.
医用乳胶手套
二、实验题(共3小题)
16.废旧塑料回收和利用是减轻“白色污染”、实现资源再利用的有效途径之一,某兴趣小组进行如下探究:
17.某化学课外活动小组探究淀粉水解的条件,进行以下两个实验了:
(1)实验用品:0.5g淀粉、4mL
20%硫酸溶液、氢氧化钠溶液、银氨溶液、碘水;
步骤:在试管1和试管2里各放入0.5g淀粉,在试管1里加入4mL
20%硫酸溶液,在试管2里加入4mL水,都加热3~4min.用过量碱液中和试管1里的硫酸溶液,把一部分液体倒入试管3,在试管2、3里都加入碘水,观察有没有蓝色出现,在试管1里加入银氨溶液,稍加热后,观察试管内壁上有无银镜出现。根据所学知识预测可能的实验现象,实验现象与结论(填入下表):
(2)实验用品:0.5g淀粉、唾液、新制氢氧化铜悬浊液:
步骤:在试管中加入0.5g淀粉,加入少许唾液加热,在水解液中加入新制氢氧化铜悬浊液加热煮沸,观察现象;
现象:_________;
结论:_________;
(3)比较实验(1)(2)可得出的结论:_________。
18.实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成,取W
g该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气,按图所示装置进行实验。
回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是_________;
(2)以上装置中需要加热的仪器有_________(填写字母),操作时应先点燃_________处的酒精灯;
(3)A装置中发生反应的化学方程式是_________;
(4)D装置的作用是_________;
(5)读取氮气的体积时,应注意:①_________;②_________;
(6)实验中测得氮气的体积为V
mL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有_________(填编号)
A.生成二氧化碳气体的质量
B.生成水的质量
C.通入氧气的体积
D.氨基酸的相对分子质量
三、填空题(共3小题)
19.蛋白质是重要的营养物质,它由多种氨基酸(如丙氨酸、甘氨酸等)构成,其中甘氨酸的结构简式为:NH2﹣CH2﹣COOH,丙氨酸的结构简式为:CH3﹣CH(NH2)﹣COOH。
请回答下列问题:
(1)丙氨酸和甘氨酸的关系为:_________;
(2)丙氨酸中所含官能团的名称为_________;
(3)甘氨酸和丙氨酸混合发生缩合,能生成_________种二肽化合物。
20.玻璃钢可由酚醛树脂和玻璃纤维制成。
(1)酚醛树脂有苯酚和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向已有苯酚的反应釜中_________加入甲醛,且反应釜应装有_________装置;
(2)玻璃纤维由玻璃拉丝得到.普通玻璃是由石英砂、_________和石灰石(或长石)高温熔融而成,主要反应的化学方程式为_________;
(3)玻璃钢中玻璃纤维的作用是_________;玻璃钢具有_________等优异性能(写出亮点即可);
(4)下列处理废旧热固性酚醛塑料的做法合理的是_________;
a.深埋
b.粉碎后用作树脂填料
c.用作燃料
d.用有机溶剂将其溶解,回收树脂
21.①一种二肽的结构简式为:,合成这种二肽的氨基酸是_________和_________;
②生活中有大量的铝制品.家用铝锅不能用热碱水洗涤去污,原因是(用离子方程式表示)_________;
③大量使用塑料制品产生的污染称之为_________,防治该污染的有效措施之一是进行回收利用,将回收后的塑料进行_________,可以获得乙烯、丙烯等化工原料;
④传统生产水泥的原料中除了石灰石、粘土外,还经常添加_________,以调节水泥的硬化速度。
答案解析
1.【答案】A
【解析】A.在有易燃易爆物的工作场所,严禁穿化纤类衣服,因为化纤类衣服摩擦时容易产生火花,故A正确;
B.淀粉水解的产物可能有麦芽糖、葡萄糖,当水解为葡萄糖后,葡萄糖可能发酵为酒精或者乳酸,才酿成酒,故B错误;
C.食用植物油的主要成分是高级不饱和脂肪酸的甘油酯,故C错误;
D.对十二烷基苯磺酸钠是表面活性剂,发生物理变化,故D错误。
2.【答案】B
【解析】A,贝采里乌斯被称为“有机化学之父”,提出了有机化学概念,法国化学家维勒由氰酸铵合成了尿素,首次打破了有机物和无机物的界限,荷兰化学家范特霍夫提出了有机化合物的三维结构,故A正确;
B,红外光谱法是对各种吸收红外光的化合物的定量和定性分析的一种方法,用于研究化学物质的结构,不能用于研究化学反应历程,故B错误;
C,由利用溶液颜色与反应物(或生成物)浓度的关系,可以确定该化学反应的速率,给出的仪器中只有分光光度计可进行比色分析,故C正确;
D,羰基上的氧可以﹣NH﹣上的氢形成氢键,蛋白质的二级结构主要依靠肽链中﹣NH﹣上的氢原子与羰基上的氧原子形成氢键而实现的,故D正确。
3.【答案】D
【解析】A.高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿造业等,故A正确;
B.复合材料一般是以一种材料作为基体,另一种材料作为增强体,故B正确;
C.导电塑料是将树脂和导电物质混合,用塑料的加工方式进行加工的功能型高分子材料.主要应用于电子、集成电路包装、电磁波屏蔽等领域,故C正确;D.医用高分子材料归属于功能高分子材料,它们都无毒、具有良好的生物相容性和稳定性,有足够的机械强度等特点,故D错误。
4.【答案】C
【解析】A.塑料的熔点很小,所以不能耐高温,故A错误;
B.合成纤维具有强度高、弹性好、耐腐蚀等优点,但合成纤维的熔点较低,所以不能耐高温,故B错误;
C.耐高温新型陶瓷熔点较高,所以能耐高温,故C正确;
D.镁铝合金的熔点较低,故D错误。
5.【答案】D
6.【答案】C
【解析】A.硫酸铝钾可水解生成具有吸附性的氢氧化铝胶体,可用于净水,故A正确;
B.锌比铁活泼,海轮外壳上镶入锌块,为牺牲阳极的阴极保护法,可减缓船体的腐蚀,故B正确;
C.聚氯乙烯塑料中的增塑剂有毒,不能用于包装食品,故C错误;
D.减少化石燃料使用,可减少颗粒物的排放,故D正确。
7.【答案】C
8.【答案】D
【解析】复合材料是将两种或两种以上性质不同的材料经特殊加工而成的材料.其中,一种材料作为基体,另一种材料作增强剂,塑料中一般添加增塑剂和防老化剂,故选D。
9.【答案】A
【解析】A.光导纤维的成分是二氧化硅,不是有机高分子化合物,故A错误;
B.废旧电池进行回收利用,集中处理的主要原因是防治废电池中镉、铅等重金属离子对土壤和水源的污染,故B正确;
C.电解熔融氯化镁,得到金属镁,为氧化还原反应,生成镁和氯气,故C正确;
D.太阳能、风能和氢能等是清洁能源,利用太阳能、风能和氢能等能源替代化石能源可以减少污染物的排放,改善空气质量,故D正确。
10.【答案】C
【解析】A.萃取利用溶质在不同溶剂中溶解度不同,用一种溶剂把溶质从它与另一溶剂所组成的溶液中提取出来;
B.蒸馏把互相溶解但沸点不同的两种液体或将水中难挥发性物质和水分离出来;
C.超过两种以上物质混合而成为一个分子状态的均匀相的过程称为溶解;
D.利用粒子直径大小,可用渗析的方法分离;这里的“迁移”指塑料中的塑化剂溶解在酒精中,故选C。
11.【答案】D
【解析】A.稀的食盐水只能够降低蛋白质的溶解度,不能使蛋白质变性,所以稀的食盐水不能杀死H7N9禽流感病毒,故A错误;
B.光导纤维的主要成分是二氧化硅,属于无机非金属材料,故B错误;
C.用电镀厂的废水直接灌溉农田,会引起环境污染,不利用食品的安全,故C错误;
D.外形似海绵、密度小、有磁性的碳和石墨都是有碳元素组成,二者结构和性质不同,符合同素异形体的概念,属于同素异形体,故D正确。
12.【答案】B
【解析】聚四氟乙烯具有抗酸抗碱、抗各种有机溶剂的特点,不溶于强酸、强碱和有机溶剂,同时具有耐高温的特点,聚氯乙烯、聚苯乙烯、有机玻璃不耐高温,不能做不粘锅的表面材料,
故选B.
13.【答案】B
【解析】塑料、合成纤维、合成橡胶是人工合成材料,棉花、羊毛和真丝等都属于天然材料,故选B。
14.【答案】D
【解析】A.液晶高分子材料是做液晶屏的材料,故A错误;
B.因为橡胶较软不可能做机身,故B错误;
C.高分子分离膜是由聚合物或高分子复合材料制得的具有分离流体混合物功能的薄膜,故C错误;
D.碳纤维复合材料有很大的韧性刚性,而且碳纤维复合材料的密度较小,故D正确。
15.【答案】B
【解析】A.橡皮筋需要较好的弹性,硫化程度不宜过高,故A错误;
B.汽车外胎应具有弹性差、强度很大的特征,硫化程度较高时符合要求,故B正确;
C.气球需要较高的弹性,硫化程度不宜过高,故C错误;
D.医用乳胶手套需要较高的弹性,硫化程度不宜过高,故D错误。
16.【答案】(1)将混合物注入分液漏斗,加入酸性高锰酸钾溶液,振荡,再往混合应液中加入一定量的氢氧化钠溶液振荡、静置、分液
(2)检验并除去气态不饱和烃
(3)无法判定E中是否有水产生
(4)气态烷烃;
【解析】(1)甲苯能够与酸性高锰酸钾溶液反应生成可溶于水中的物质,可以用酸性高锰酸钾溶液除去苯中的甲苯,操作方法为:将混合物注入分液漏斗,加入酸性高锰酸钾溶液,振荡,再往混合应液中加入一定量的氢氧化钠溶液振荡、静置、分液;
(2)装置C中盛有溴水,利用溴水检验并除去废旧粗料分解生成的气态不饱和烃;
(3)装置F用于检验装置E中有水分生成,若没有装置D,用于气体中混有水分,无法证明装置E中有水生成;
(4)从C中出来的气体中,不饱和烃已经除去,另外生成产物有可能为氢气或饱和烃,所以其他成分可能是气体烷烃;CuO能将烃氧化成CO2和H2O,可以通过检验反应产物中有二氧化碳和水生成,就可以证明其它气体为饱和烷烃,所以图2的装置应该使用澄清石灰水,目的是检验产物中有二氧化碳生成,图2装置可以为。
17.【答案】(1)
(2)产生砖红色沉淀;淀粉在唾液作用下水解生成了葡萄糖
(3)淀粉水解需要稀硫酸或唾液中的酶作催化剂
18.【答案】(1)将装置中的N2排净
(2)AD;D
(4):吸收未反应的氧气,保证最终收集的气体为N2;
(5)①量筒内液面与广口瓶中的液面相持平 ②视线与凹液面最低处相切
(6)ABD
19.【答案】(1)互为同系物
(2)氨基、羧基
(3)4
【解析】(1)丙氨酸比甘氨酸多一个CH2原子,二者都是氨基酸,互为同系物;
(2)丙氨酸中含有氨基、羧基2种官能团;
(3)氨基酸生成二肽,就是两个氨基酸分子脱去一个水分子,当同种氨基酸脱水,生成2种二肽;当是异种氨基酸脱水:可以是甘氨酸脱去羟基,丙氨酸脱氢;也可以丙氨酸脱羟基,甘氨酸脱去氢,生成2种二肽,所以共有4种。
20.【答案】(1)间歇性、散热
(2)纯碱;Na2CO3+SiO2Na2SiO3+CO2↑、CaCO3+SiO2CaSiO3+CO2↑
(3)增强体
强度高、质量轻(或耐腐蚀、抗冲击、绝缘性能好等)
(4)bc
【解析】(1)苯酚和甲醛发生缩聚反应,反应有大量热放出,为防止温度过高,应向已有苯酚的反应釜中间歇性的加入甲醛,并装有散热装置;
(2)生产玻璃的原料:石灰石、石英砂、纯碱,反应原理为:Na2CO3+SiO2Na2SiO3+CO2↑、CaCO3+SiO2CaSiO3+CO2↑;
(3)玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料,其中玻璃纤维的作用是增强体,合成材料是基体,它的优点有:强度高、质量轻、耐腐蚀、抗冲击、绝缘性能好等;
(4)废旧合成材料的再生利用主要有三条途径:通过再生和改性,重新做成多种有用的材料和制品;采用热裂解或化学处理方法使其分解,用于制备多种化工原料;将废旧的聚合物作为燃料回收利用热能,塑料深埋很久不会腐烂,会造成白色污染,酚醛塑料不能溶于有机溶剂,故选bc。
21.【答案】①甘氨酸;丙氨酸
②Al2O3+2OHˉ=2AlO2ˉ+H2O
③白色污染;裂解
④石膏
