鲁教版五四制八年级化学寒假预习作业质量守恒定律习题(含解析)
文档属性
| 名称 | 鲁教版五四制八年级化学寒假预习作业质量守恒定律习题(含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 153.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-20 00:00:00 | ||
图片预览



文档简介
质量守恒定律
一、单选题
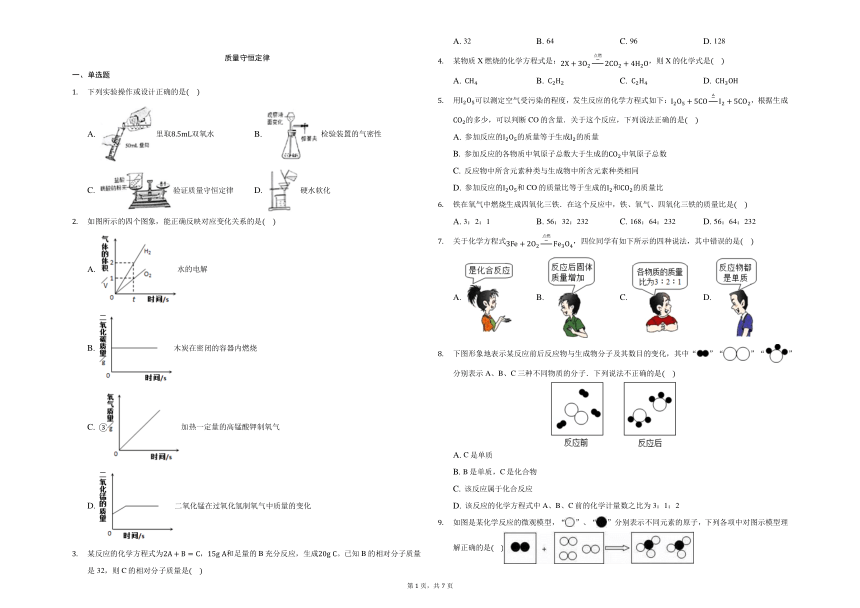
下列实验操作或设计正确的是
A.
里取双氧水
B.
检验装置的气密性
C.
验证质量守恒定律
D.
硬水软化
如图所示的四个图象,能正确反映对应变化关系的是
A.
水的电解
B.
木炭在密闭的容器内燃烧
C.
加热一定量的高锰酸钾制氧气
D.
二氧化锰在过氧化氢制氧气中质量的变化
某反应的化学方程式为,和足量的B充分反应,生成。已知B的相对分子质量是32,则C的相对分子质量是
A.
32
B.
64
C.
96
D.
128
某物质X燃烧的化学方程式是:,则X的化学式是
A.
B.
C.
D.
用可以测定空气受污染的程度,发生反应的化学方程式如下:,根据生成的多少,可以判断CO的含量.关于这个反应,下列说法正确的是
A.
参加反应的的质量等于生成的质量
B.
参加反应的各物质中氧原子总数大于生成的中氧原子总数
C.
反应物中所含元素种类与生成物中所含元素种类相同
D.
参加反应的和CO的质量比等于生成的和的质量比
铁在氧气中燃烧生成四氧化三铁.在这个反应中,铁、氧气、四氧化三铁的质量比是
A.
3:2:1
B.
56:32:232
C.
168:64:232
D.
56:64:232
关于化学方程式,四位同学有如下所示的四种说法,其中错误的是
A.
B.
C.
D.
下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中“”“”“”分别表示A、B、C三种不同物质的分子.下列说法不正确的是
A.
C是单质
B.
B是单质,C是化合物
C.
该反应属于化合反应
D.
该反应的化学方程式中A、B、C前的化学计量数之比为3:1:2
如图是某化学反应的微观模型,“”、“”分别表示不同元素的原子,下列各项中对图示模型理解正确的是?
?
A.
该反应属于分解反应
B.
该反应中,原子的种类变了
C.
反应中共有两种元素参与
D.
参加反应的两种物质分子个数之比为2:3
图是某个化学反应的微观模拟图,下列关于该反应前、后的说法正确的是
A.
该图示不符合质量守恒定律
B.
该反应为化合反应
C.
原子总数减少
D.
分子总数不变
二氧化碳气体转化为“干冰”的过程中发生改变的是
A.
分子种类
B.
原子种类
C.
分子间距
D.
原子大小
在化学反应前后,下列各项中肯定没有发生变化的是
?
?
原子数目????
?分子数目?
?
?
?元素种类?
?
?
物质种类?
?
?
原子种类???
??
物质的总质量?????
化合价
A.
B.
C.
D.
执行探月工程嫦娥三号任务的长征三号乙遥二十三火箭使用的推进剂是与,反应的化学方程式为:,X的化学式为
A.
CO
B.
C.
D.
氯气是有毒的气体,可用氢氧化钠溶液来吸收,其反应原理为:??则X的化学式为
A.
B.
C.
HCl
D.
HClO
下列说法中正确并符合质量守恒定律解释的是
A.
10g酒精和50g水混匀后形成60g酒精溶液
B.
红磷在氧气中燃烧,反应后得到,则参加反应的和磷的总质量一定为30g
C.
2L氢气和1L氧气反应,生成3L水,这符合质量守恒定律
D.
2g氢气和8g氧气恰好完全反应,生成10g水,这符合质量守恒定律
下列叙述符合质量守恒定律的是
A.
5g酒精与5g水混合得到10g酒精溶液
B.
2L氢气与18L?氧气反应生成20L的水
C.
12g碳完全反应时只能消耗32g氧气,则12g碳在64g氧气中充分反应生成76g二氧化碳
D.
镁在空气中燃烧,生成氧化镁的质量等于参加反应的镁的质量和氧气的质量之和
一种可做化肥的化合物在密封加热完全分解后生成氨气、水、和二氧化碳,则该物质中一定含有的元素是
A.
C、H、O
B.
N、H、O
C.
N、C、H
D.
C、H、O、N
在一密闭容器中加入a、b、c、d四种物质,测得反应前后各物质的质量如下表。
物质
a
b
c
d
反应前的质量
40
40
10
32
反应后的质量
12
x
10
0
下列说法正确的是
A.
x等于90
B.
b可能是单质
C.
c一定是催化剂
D.
参加反应的a与d的质量比为7:8
一定条件下,下列物质在密闭容器中反应一段时间,测得反应前后各物质的质量如表所示,下列说法中错误的是
物质
X
Y
Z
W
反应前质量
10
反应后质量
a
A.
X、Z是反应物,Y、W是生成物
B.
C.
Z为化合物
D.
反应中Y、W变化的质量比为22:9
某物质在空气中燃烧时,有二氧化碳、水和二氧化硫生成.则此物质肯定含有的元素是
A.
碳、氢、氧
B.
氧、氢、硫
C.
碳、氧、硫
D.
碳、氢、硫
二、填空题
在反应中,A和B的相时分子质量之比为5:1,已知20g?A与一定量B恰好完全反应,生成5g?D,则在此反应中B和C的质量比为______.
在反应中,______份质量的铁跟______份质量的氧气反应,生成______份质量的四氧化三铁.
“水是生命之源”,饮用水的质量关系到人体健康.
区分硬水和软水,可以选用的物质是______.
新型饮用水消毒剂一氯胺由______种元素组成,其中氮元素与氢元素的质量比是______.
用消毒时,发生反应,其中X的化学式为______.
答案和解析
1.【答案】B
【解析】解:A、里取双氧水应该用10mL量筒量取,故A错。
B、长颈漏斗内液面不再下降,说明气密性良好,故B正确。
C、碳酸钠与稀盐酸反应生成二氧化碳气体,反应后二氧化碳气体逸出,不能用于验证质量守恒定律,故C错。
D、过滤不能将硬水软化,加热煮沸或蒸馏可以将硬水软化;故D错。
故选:B。
A、根据量筒的选取方法。
B、根据装置气密性检查方法进行分析判断。
C、根据碳酸钠与稀盐酸反应生成二氧化碳气体,进行分析判断。
D、根据硬水软化的方法进行分析判断。
本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
2.【答案】A
【解析】解:A、电解水时生成的氢气和氧气的体积比是2:1,故选项正确。
B、木炭在密闭的容器内燃烧时生成二氧化碳的质量应该是从0开始不断增加的一直到反应结束,故选项不正确。
C、加热一定量的高锰酸钾制氧气时氧气的质量是不断增加的,当高锰酸钾完全反应后氧气的质量不再增加,故选项不正确。
D、过氧化氢溶液和二氧化锰混合生成水和氧气,二氧化锰是催化剂质量不变为一定值,故选项不正确。
故选:A。
可以根据图中的信息进行分析、判断,从而得出正确的结论。
解答本题要把图中提供的信息和所学知识有机的结合起来,只有这样才能对问题做出正确的判断。
3.【答案】D
【解析】解:根据质量守恒定律可知15gA和B充分反应生成20gC时,参加反应的B质量应为;
设C的相对分子质量是x,则
?????
????
解得。
故选:D。
依据质量守恒定律可知反应物B的质量,进而确定了B和C的质量关系,然后依据化学反应中物质之间的质量比等于其相对分子质量和的比求解即可。
此题是对化学方程式计算的考查,解题的关键是把质量守恒定律的内容和化学方程式结合起来进行分析、判断。
4.【答案】D
【解析】解:根据质量守恒定律的微观解释可以知道反应前后的原子数目和种类应该相等,分析题给的化学反应方程式可以知道,反应前只出现了6个O,反应后出现了2个C,8个O,8个H,所以在2X中含有的2个O,8个H和2个C,所以X中含有1个C、4个H和1个O,分析题给的四个选项,符合题意的化学式为D。
故选:D。
根据质量守恒定律的微观解释:化学反应前后原子的种类和数目不变.可知在化学反应方程式中,反应物和生成物中所含的原子的种类和数目相同.由此可推断化学反应方程式中反应物或生成物的化学式.
本题考查学生利用化学反应方程式和质量守恒定律来推断物质的化学式,抓住反应前后原子的种类和数目不变来解答.
5.【答案】C
【解析】解:A、参加反应的的质量和CO的质量总和等于生成的质量和的质量总和,故A错误;
B、化学反应前后原子的种类和数目不变,所以参加反应的各物质中氧原子总数等于生成的中氧原子总数,故B错误;
C、化学反应前后元素的种类不变,所以反应物中所含元素种类与生成物中所含元素种类相同,故C正确;
D、参加反应的的质量和CO的质量总和等于生成的质量和的质量总和,而不是和CO的质量比等于生成的和的质量比,故D错误。
故选:C。
根据质量守恒定律的含义进行解答,质量守恒定律是指参加反应的各物质的质量总和等于生成的各物质的质量总和,化学反应前后元素的种类和质量不变.
本题主要考查质量守恒定律的应用,解题的关键是掌握质量守恒定律的含义以及微观解释.
6.【答案】C
【解析】解:铁在氧气中燃烧生成四氧化三铁的化学方程式为:
???????????????????????????????????????::
该反应中铁、氧气、四氧化三铁的质量比:::64:232。
故选:C。
根据铁在氧气中燃烧生成四氧化三铁的化学方程式,结合各物质的质量比为各物质相对分子或原子质量与反应中物质计量数乘积的比,进行分析解答.
本题难度不大,化学方程式中各物质的质量比为各物质相对分子或原子质量与反应中物质计量数乘积的比.
7.【答案】C
【解析】解:A、反应物有两种,生成物是一种,所以化合反应。正确;
B、铁和氧气化合生成四氧化三铁,固体质量增加。正确;
C、根据化学方程式可得各种物质的质量比为::::8:错误;
D、铁和氧气都是由一种元素组成的纯净物,属于单质。正确。
故选:C。
根据反应物和生成物的种类可以判断反应类型、生成物质量方面的情况、反应物和生成物的质量比;根据物质的元素组成可以判断物质的所属类别.
解答本题要充分理解化学方程式表示的含义,只有这样才能对相关方面的问题做出正确的判断.
8.【答案】A
【解析】
【分析】
由反应前后反应物与生成物分子及其数目的变化的微观图,反应由3个A分子与1个B分子发生反应,生成2个C分子,并且A分子、B分子均由同种原子构成的单质分子,而C分子为两种不同原子构成的化合物分子。
【解答】
A.由微粒的构成可知,C分子由不同种的原子构成,不属于单质,故A不正确;
B.B分子由同种原子构成,属于单质,C由两种原子构成,属于化合物,故B正确;
C.该反应为A、B两种物质反应生成C物质,反应符合“多变一”的化合反应的特点,故C正确;
D.该反应由3个A分子与1个B分子发生反应,生成2个C分子,因此反应中A、B、C前的化学计量数之比为3:1:2;故D正确。
故选A。
9.【答案】C
【解析】
【分析】
本题考查反应微观示意图的理解。该题关键是从模型图中看出各物质分子的构成,注意解题是要考虑到模型图中每种分子有几个参加反应,利用反应时的微粒个数关系及结构可轻松判断。
【解答】
A.由图示可知,该反应的反应物是两种、生成物是一种,该反应是化合反应,故A错误;?
B.原子是化学变化中的最小粒子,化学反应前后,原子种类不变,故B错误;?
C.由反应中原子的种类可知,该反应中共有两种元素参与,故C正确;?
D.由反应的图示结合质量守恒定律可知,参加反应的两种物质分子个数之比为1:3,故D错误。??
故选C。
10.【答案】B
【解析】
【分析】
根据微观模拟图,反应前的物质为两种构成不同的分子构成,反应后的物质也是由两种构成不同的分子构成;结合质量守恒定律分析分子的质量、分子的个数及物质质量的变化,然后结合选项进行分析。
【解答】
A.化学反应都遵循质量守恒定律,故A错误;
B.由微观示意图可知,由两种物质反应生成了一种物质,属于化合反应,故B正确;
C.观察微观示意图可知反应前后原子的总数没有发生变化,故C错误;
D.观察微观示意图可知,反应前有6个分子,反应后有5个分子,因此分子数减少,故D错误。
故选B。
11.【答案】C
【解析】
【分析】
首先要判断二氧化碳气体转化为干冰是物理变化还是化学变化;若是物理变化,则分子的大小、种类、性质都是不变的;若是化学变化,则分子的种类、性质是改变的。解答本题的关键是判断改变升华是物理变化还是化学变化;从微观角度讲,物理变化是分子的性质、种类以及大小都不变的变化;化学变化是分子种类、性质以及大小都改变的变化。
【解答】
二氧化碳气体转化为干冰是气态的二氧化碳变成了固体的二氧化碳;故该过程是物理变化。则在变化过程中,分子的大小、性质以及种类都是不变的,只是分子之间的间隔改变了。
故选C。
12.【答案】D
【解析】
【分析】
根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,化学反应的过程,就是参加反应的各物质反应物的原子,重新组合而生成其他物质的过程。在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变;化学反应前后六个不变:原子种类、数目、质量、元素种类、元素质量、物质总质量;两个一定变:分子种类、物质种类;两个可能变:元素化合价、分子数目。
【解答】
分子分成原子所以分子种类一定发生了变化,分子种类变了,物质的种类也就发生了变化,原子进行重新组合,所以原子的种类、数目、质量都没有发生变化,原子的种类不变,元素的种类也不会发生变化,由于分子种类发生了变化,分子的数目可能变了,可能没变,元素的化合价可能变,可能不变。
故选D。
13.【答案】B
【解析】解:由可知,
反应前碳原子是2个,反应后应该是2个,包含在2X中;
反应前氢原子是8个,反应后是8个;
反应前氮原子是6个,反应后是6个;
反应前氧原子是8个,反应后应该是8个,其中4个包含在2X中;
由分析可知,每个X中含有1个碳原子和2个氧原子,是二氧化碳,化学式是。
故选:B。
化学反应前后,元素的种类不变,原子的种类、总个数不变.
化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.
14.【答案】A
【解析】解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前氯、钠、氧、氢原子个数分别为2、2、2、2,反应后的生成物中氯、钠、氧、氢原子个数分别为2、2、1、2,根据反应前后原子种类、数目不变,则每个X分子由2个氢原子和1个氧原子构成,则物质X的化学式为
故选:A.
由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
本题难度不大,掌握利用化学反应前后原子守恒来确定物质的化学式的方法是正确解答此类题的关键.
15.【答案】B
【解析】解:A、10g酒精和50g水混匀后形成60g酒精溶液,没有新物质生成,属于物理变化,不能用质量守恒定律解释,故选项错误。
B、红磷在氧气中燃烧,反应后得到,则参加反应的和磷的总质量一定为30g,故选项说法正确。
C、质量守恒定律是质量守恒,而不是体积守恒,故选项说法错误。
D、氢气和氧气反应的化学方程式为,可知氢气、氧气、水的质量比为4:32::8:9,故1g氢气能与8g氧气完全反应生成9g水;故选项说法错误。
故选:B。
质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用于化学变化,且要注意是质量守恒,而不是体积守恒;物质发生物理变化,则不适用于质量守恒定律来解释;是化学变化时也要对反应前后物质的质量关系进行计算判断,即反应时是否符合固定的质量比,据此分析问题即可.
本题难度不大,掌握质量守恒定律是物质在发生化学变化中表现出来的一种规律、化学变化和物理变化的判别是解题的关键.
16.【答案】D
【解析】解:A、5g酒精与5g水混合得到10g酒精溶液,属于物理变化,不符合质量守恒定律,故选项错误。
B、质量守恒定律的适用范围是化学变化,强调质量守恒,不适用于其他物理量例如体积等,故选项错误。
C、碳在氧气中燃烧生成二氧化碳,反应的化学方程式为:,参加反应的碳和氧气的质量比为12:32:44,12g碳完全反应时只能消耗32g氧气,则12g碳在64g氧气中充分反应,氧气有剩余,生成44g二氧化碳,故选项错误。
D、镁在空气中燃烧,生成的氧化镁的质量等于参加反应的镁的质量和氧气的质量之和,故选项正确。
故选:D。
本题难度不大,掌握质量守恒定律、化学反应中各物质之间的质量比等于相对分子质量和的比等是正确解答本题的关键。
17.【答案】D
【解析】解:某化合物密封加热完全分解后生成氨气、水和二氧化碳,生成物氨气、水和二氧化碳中含有氮、氢、氧、碳四种元素,则反应物中也一定含有这四种元素。某化合物中一定含有氮、氢、氧、碳四种元素。
故选:D。
根据质量守恒定律,反应前后元素种类不变,结合题意进行分析解答.
本题难度不大,掌握质量守恒定律反应前后,元素种类不变并能灵活运用是正确解答本题的关键.
18.【答案】D
【解析】
【分析】
本题主要考查质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和。反应后质量增加的是生成物,减少的是反应物,不变的可能为催化剂,题目难度不大。
【解答】
A.根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,,故A错误;
B.a、d质量减小则为反应物,b质量增加则为生成物,故属于化合反应,因此b一定是化合物,故B错误;
C.c的质量不变,可能为催化剂,故C错误;
D.参加反应的a与d的质量比为::8,故
D正确。
故选D。
19.【答案】A
【解析】解:根据质量守恒定律,由表格中的数字可知:,故克,根据反应物反应后质量减少,生成物质量增加则可推测反应物为Z;生成物为X、Y、W;
A、由以上推测可知,反应物为Z;生成物为X、Y、W,故错误;
B、由分析知,故正确;
C、从以上推测可以看出,该反应为Z物质分解为XYW三种物质,故Z为化合物,故正确;
D、反应中Y、W两种物质变化的质量比为::9,故正确。
故选:A。
在一密闭容器中,X、Y、Z、W四种物质,在一定的条件下反应一段时间后,测得反应前后各物质质量如表可知,根据质量守恒定律,则可求X的待测值;则由物质的增加或减少,可推测反应物与生成物等信息.
本题难度不大,根据质量守恒定律认真分析各物质反应前后的质量变化情况解答此类题的关键.
20.【答案】D
【解析】解:因为生成物二氧化硫、二氧化碳和水中含有C、H、O、S四种元素,所以反应物中也应该有这四种元素,又知某物质在氧气中充分燃烧,故生成物中的氧元素可能来自氧气,故可判断该生成物中一定含有碳元素、硫元素和氢元素,是否含有氧元素无法确定。
故选:D。
根据“化学变化前后元素的种类不变,原子的种类、个数不变”解答.
根据质量守恒定律可以判断物质的元素组成.
21.【答案】2:17
【解析】解:因为A和B的相时分子质量之比为5:1,所以2A::1,
设参与反应的B的质量为x,
::x,
解之得:;
根据质量守恒定律可得生成的C的质量为:;
在此反应中B和C的质量比为:2g::17.
故答案为:2:17.
根据化学方程式和已知条件“A和B的相时分子质量之比为5:1”以及A的质量,列出比例式,即可求出参与反应的B的质量;
根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.则生成的C的质量的质量的质量的质量;然后写出两者的比即可.
本题主要考查学生运用化学方程式和质量守恒定律进行计算的能力.
22.【答案】168
?
64
?
232
【解析】解:物质的质量比等于相对分子质量和的比.
168?64???
232
则三者的质量比是168:64:232
故答案为:168;64;232
根据相对分子质量及化学式前的化学计量数即可得出答案.
本题主要考查学生对元素的相对原子质量和化学方程式意义的认识.
23.【答案】肥皂水;
三;7:1;
【解析】
【分析】
本题主要考查根据质量守恒定律推断物质的化学式和根据物质的化学式计算元素的化合价,难度较小。
【解答】
硬水加入肥皂水,生成的泡沫少,并产生大量的浮渣;软水加入肥皂水,生成的泡沫多,所以区分硬水和软水,可以选用的物质是肥皂水.
故答案为:肥皂水.
含有三种元素,其中氮元素与氢元素的质量比为:14:::1.
故答案为:三;7:1.
根据所给化学方程式可以看出:化学方程式的右边比左边多出了2个氢原子和1个氧原子;根据质量守恒定律中的元素种类不变和原子个数不变的特点,可知多出的原子全部来自1个X分子中,即X的化学式为
故答案为:
第2页,共2页
第1页,共1页
一、单选题
下列实验操作或设计正确的是
A.
里取双氧水
B.
检验装置的气密性
C.
验证质量守恒定律
D.
硬水软化
如图所示的四个图象,能正确反映对应变化关系的是
A.
水的电解
B.
木炭在密闭的容器内燃烧
C.
加热一定量的高锰酸钾制氧气
D.
二氧化锰在过氧化氢制氧气中质量的变化
某反应的化学方程式为,和足量的B充分反应,生成。已知B的相对分子质量是32,则C的相对分子质量是
A.
32
B.
64
C.
96
D.
128
某物质X燃烧的化学方程式是:,则X的化学式是
A.
B.
C.
D.
用可以测定空气受污染的程度,发生反应的化学方程式如下:,根据生成的多少,可以判断CO的含量.关于这个反应,下列说法正确的是
A.
参加反应的的质量等于生成的质量
B.
参加反应的各物质中氧原子总数大于生成的中氧原子总数
C.
反应物中所含元素种类与生成物中所含元素种类相同
D.
参加反应的和CO的质量比等于生成的和的质量比
铁在氧气中燃烧生成四氧化三铁.在这个反应中,铁、氧气、四氧化三铁的质量比是
A.
3:2:1
B.
56:32:232
C.
168:64:232
D.
56:64:232
关于化学方程式,四位同学有如下所示的四种说法,其中错误的是
A.
B.
C.
D.
下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中“”“”“”分别表示A、B、C三种不同物质的分子.下列说法不正确的是
A.
C是单质
B.
B是单质,C是化合物
C.
该反应属于化合反应
D.
该反应的化学方程式中A、B、C前的化学计量数之比为3:1:2
如图是某化学反应的微观模型,“”、“”分别表示不同元素的原子,下列各项中对图示模型理解正确的是?
?
A.
该反应属于分解反应
B.
该反应中,原子的种类变了
C.
反应中共有两种元素参与
D.
参加反应的两种物质分子个数之比为2:3
图是某个化学反应的微观模拟图,下列关于该反应前、后的说法正确的是
A.
该图示不符合质量守恒定律
B.
该反应为化合反应
C.
原子总数减少
D.
分子总数不变
二氧化碳气体转化为“干冰”的过程中发生改变的是
A.
分子种类
B.
原子种类
C.
分子间距
D.
原子大小
在化学反应前后,下列各项中肯定没有发生变化的是
?
?
原子数目????
?分子数目?
?
?
?元素种类?
?
?
物质种类?
?
?
原子种类???
??
物质的总质量?????
化合价
A.
B.
C.
D.
执行探月工程嫦娥三号任务的长征三号乙遥二十三火箭使用的推进剂是与,反应的化学方程式为:,X的化学式为
A.
CO
B.
C.
D.
氯气是有毒的气体,可用氢氧化钠溶液来吸收,其反应原理为:??则X的化学式为
A.
B.
C.
HCl
D.
HClO
下列说法中正确并符合质量守恒定律解释的是
A.
10g酒精和50g水混匀后形成60g酒精溶液
B.
红磷在氧气中燃烧,反应后得到,则参加反应的和磷的总质量一定为30g
C.
2L氢气和1L氧气反应,生成3L水,这符合质量守恒定律
D.
2g氢气和8g氧气恰好完全反应,生成10g水,这符合质量守恒定律
下列叙述符合质量守恒定律的是
A.
5g酒精与5g水混合得到10g酒精溶液
B.
2L氢气与18L?氧气反应生成20L的水
C.
12g碳完全反应时只能消耗32g氧气,则12g碳在64g氧气中充分反应生成76g二氧化碳
D.
镁在空气中燃烧,生成氧化镁的质量等于参加反应的镁的质量和氧气的质量之和
一种可做化肥的化合物在密封加热完全分解后生成氨气、水、和二氧化碳,则该物质中一定含有的元素是
A.
C、H、O
B.
N、H、O
C.
N、C、H
D.
C、H、O、N
在一密闭容器中加入a、b、c、d四种物质,测得反应前后各物质的质量如下表。
物质
a
b
c
d
反应前的质量
40
40
10
32
反应后的质量
12
x
10
0
下列说法正确的是
A.
x等于90
B.
b可能是单质
C.
c一定是催化剂
D.
参加反应的a与d的质量比为7:8
一定条件下,下列物质在密闭容器中反应一段时间,测得反应前后各物质的质量如表所示,下列说法中错误的是
物质
X
Y
Z
W
反应前质量
10
反应后质量
a
A.
X、Z是反应物,Y、W是生成物
B.
C.
Z为化合物
D.
反应中Y、W变化的质量比为22:9
某物质在空气中燃烧时,有二氧化碳、水和二氧化硫生成.则此物质肯定含有的元素是
A.
碳、氢、氧
B.
氧、氢、硫
C.
碳、氧、硫
D.
碳、氢、硫
二、填空题
在反应中,A和B的相时分子质量之比为5:1,已知20g?A与一定量B恰好完全反应,生成5g?D,则在此反应中B和C的质量比为______.
在反应中,______份质量的铁跟______份质量的氧气反应,生成______份质量的四氧化三铁.
“水是生命之源”,饮用水的质量关系到人体健康.
区分硬水和软水,可以选用的物质是______.
新型饮用水消毒剂一氯胺由______种元素组成,其中氮元素与氢元素的质量比是______.
用消毒时,发生反应,其中X的化学式为______.
答案和解析
1.【答案】B
【解析】解:A、里取双氧水应该用10mL量筒量取,故A错。
B、长颈漏斗内液面不再下降,说明气密性良好,故B正确。
C、碳酸钠与稀盐酸反应生成二氧化碳气体,反应后二氧化碳气体逸出,不能用于验证质量守恒定律,故C错。
D、过滤不能将硬水软化,加热煮沸或蒸馏可以将硬水软化;故D错。
故选:B。
A、根据量筒的选取方法。
B、根据装置气密性检查方法进行分析判断。
C、根据碳酸钠与稀盐酸反应生成二氧化碳气体,进行分析判断。
D、根据硬水软化的方法进行分析判断。
本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键。
2.【答案】A
【解析】解:A、电解水时生成的氢气和氧气的体积比是2:1,故选项正确。
B、木炭在密闭的容器内燃烧时生成二氧化碳的质量应该是从0开始不断增加的一直到反应结束,故选项不正确。
C、加热一定量的高锰酸钾制氧气时氧气的质量是不断增加的,当高锰酸钾完全反应后氧气的质量不再增加,故选项不正确。
D、过氧化氢溶液和二氧化锰混合生成水和氧气,二氧化锰是催化剂质量不变为一定值,故选项不正确。
故选:A。
可以根据图中的信息进行分析、判断,从而得出正确的结论。
解答本题要把图中提供的信息和所学知识有机的结合起来,只有这样才能对问题做出正确的判断。
3.【答案】D
【解析】解:根据质量守恒定律可知15gA和B充分反应生成20gC时,参加反应的B质量应为;
设C的相对分子质量是x,则
?????
????
解得。
故选:D。
依据质量守恒定律可知反应物B的质量,进而确定了B和C的质量关系,然后依据化学反应中物质之间的质量比等于其相对分子质量和的比求解即可。
此题是对化学方程式计算的考查,解题的关键是把质量守恒定律的内容和化学方程式结合起来进行分析、判断。
4.【答案】D
【解析】解:根据质量守恒定律的微观解释可以知道反应前后的原子数目和种类应该相等,分析题给的化学反应方程式可以知道,反应前只出现了6个O,反应后出现了2个C,8个O,8个H,所以在2X中含有的2个O,8个H和2个C,所以X中含有1个C、4个H和1个O,分析题给的四个选项,符合题意的化学式为D。
故选:D。
根据质量守恒定律的微观解释:化学反应前后原子的种类和数目不变.可知在化学反应方程式中,反应物和生成物中所含的原子的种类和数目相同.由此可推断化学反应方程式中反应物或生成物的化学式.
本题考查学生利用化学反应方程式和质量守恒定律来推断物质的化学式,抓住反应前后原子的种类和数目不变来解答.
5.【答案】C
【解析】解:A、参加反应的的质量和CO的质量总和等于生成的质量和的质量总和,故A错误;
B、化学反应前后原子的种类和数目不变,所以参加反应的各物质中氧原子总数等于生成的中氧原子总数,故B错误;
C、化学反应前后元素的种类不变,所以反应物中所含元素种类与生成物中所含元素种类相同,故C正确;
D、参加反应的的质量和CO的质量总和等于生成的质量和的质量总和,而不是和CO的质量比等于生成的和的质量比,故D错误。
故选:C。
根据质量守恒定律的含义进行解答,质量守恒定律是指参加反应的各物质的质量总和等于生成的各物质的质量总和,化学反应前后元素的种类和质量不变.
本题主要考查质量守恒定律的应用,解题的关键是掌握质量守恒定律的含义以及微观解释.
6.【答案】C
【解析】解:铁在氧气中燃烧生成四氧化三铁的化学方程式为:
???????????????????????????????????????::
该反应中铁、氧气、四氧化三铁的质量比:::64:232。
故选:C。
根据铁在氧气中燃烧生成四氧化三铁的化学方程式,结合各物质的质量比为各物质相对分子或原子质量与反应中物质计量数乘积的比,进行分析解答.
本题难度不大,化学方程式中各物质的质量比为各物质相对分子或原子质量与反应中物质计量数乘积的比.
7.【答案】C
【解析】解:A、反应物有两种,生成物是一种,所以化合反应。正确;
B、铁和氧气化合生成四氧化三铁,固体质量增加。正确;
C、根据化学方程式可得各种物质的质量比为::::8:错误;
D、铁和氧气都是由一种元素组成的纯净物,属于单质。正确。
故选:C。
根据反应物和生成物的种类可以判断反应类型、生成物质量方面的情况、反应物和生成物的质量比;根据物质的元素组成可以判断物质的所属类别.
解答本题要充分理解化学方程式表示的含义,只有这样才能对相关方面的问题做出正确的判断.
8.【答案】A
【解析】
【分析】
由反应前后反应物与生成物分子及其数目的变化的微观图,反应由3个A分子与1个B分子发生反应,生成2个C分子,并且A分子、B分子均由同种原子构成的单质分子,而C分子为两种不同原子构成的化合物分子。
【解答】
A.由微粒的构成可知,C分子由不同种的原子构成,不属于单质,故A不正确;
B.B分子由同种原子构成,属于单质,C由两种原子构成,属于化合物,故B正确;
C.该反应为A、B两种物质反应生成C物质,反应符合“多变一”的化合反应的特点,故C正确;
D.该反应由3个A分子与1个B分子发生反应,生成2个C分子,因此反应中A、B、C前的化学计量数之比为3:1:2;故D正确。
故选A。
9.【答案】C
【解析】
【分析】
本题考查反应微观示意图的理解。该题关键是从模型图中看出各物质分子的构成,注意解题是要考虑到模型图中每种分子有几个参加反应,利用反应时的微粒个数关系及结构可轻松判断。
【解答】
A.由图示可知,该反应的反应物是两种、生成物是一种,该反应是化合反应,故A错误;?
B.原子是化学变化中的最小粒子,化学反应前后,原子种类不变,故B错误;?
C.由反应中原子的种类可知,该反应中共有两种元素参与,故C正确;?
D.由反应的图示结合质量守恒定律可知,参加反应的两种物质分子个数之比为1:3,故D错误。??
故选C。
10.【答案】B
【解析】
【分析】
根据微观模拟图,反应前的物质为两种构成不同的分子构成,反应后的物质也是由两种构成不同的分子构成;结合质量守恒定律分析分子的质量、分子的个数及物质质量的变化,然后结合选项进行分析。
【解答】
A.化学反应都遵循质量守恒定律,故A错误;
B.由微观示意图可知,由两种物质反应生成了一种物质,属于化合反应,故B正确;
C.观察微观示意图可知反应前后原子的总数没有发生变化,故C错误;
D.观察微观示意图可知,反应前有6个分子,反应后有5个分子,因此分子数减少,故D错误。
故选B。
11.【答案】C
【解析】
【分析】
首先要判断二氧化碳气体转化为干冰是物理变化还是化学变化;若是物理变化,则分子的大小、种类、性质都是不变的;若是化学变化,则分子的种类、性质是改变的。解答本题的关键是判断改变升华是物理变化还是化学变化;从微观角度讲,物理变化是分子的性质、种类以及大小都不变的变化;化学变化是分子种类、性质以及大小都改变的变化。
【解答】
二氧化碳气体转化为干冰是气态的二氧化碳变成了固体的二氧化碳;故该过程是物理变化。则在变化过程中,分子的大小、性质以及种类都是不变的,只是分子之间的间隔改变了。
故选C。
12.【答案】D
【解析】
【分析】
根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,化学反应的过程,就是参加反应的各物质反应物的原子,重新组合而生成其他物质的过程。在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变;化学反应前后六个不变:原子种类、数目、质量、元素种类、元素质量、物质总质量;两个一定变:分子种类、物质种类;两个可能变:元素化合价、分子数目。
【解答】
分子分成原子所以分子种类一定发生了变化,分子种类变了,物质的种类也就发生了变化,原子进行重新组合,所以原子的种类、数目、质量都没有发生变化,原子的种类不变,元素的种类也不会发生变化,由于分子种类发生了变化,分子的数目可能变了,可能没变,元素的化合价可能变,可能不变。
故选D。
13.【答案】B
【解析】解:由可知,
反应前碳原子是2个,反应后应该是2个,包含在2X中;
反应前氢原子是8个,反应后是8个;
反应前氮原子是6个,反应后是6个;
反应前氧原子是8个,反应后应该是8个,其中4个包含在2X中;
由分析可知,每个X中含有1个碳原子和2个氧原子,是二氧化碳,化学式是。
故选:B。
化学反应前后,元素的种类不变,原子的种类、总个数不变.
化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.
14.【答案】A
【解析】解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前氯、钠、氧、氢原子个数分别为2、2、2、2,反应后的生成物中氯、钠、氧、氢原子个数分别为2、2、1、2,根据反应前后原子种类、数目不变,则每个X分子由2个氢原子和1个氧原子构成,则物质X的化学式为
故选:A.
由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
本题难度不大,掌握利用化学反应前后原子守恒来确定物质的化学式的方法是正确解答此类题的关键.
15.【答案】B
【解析】解:A、10g酒精和50g水混匀后形成60g酒精溶液,没有新物质生成,属于物理变化,不能用质量守恒定律解释,故选项错误。
B、红磷在氧气中燃烧,反应后得到,则参加反应的和磷的总质量一定为30g,故选项说法正确。
C、质量守恒定律是质量守恒,而不是体积守恒,故选项说法错误。
D、氢气和氧气反应的化学方程式为,可知氢气、氧气、水的质量比为4:32::8:9,故1g氢气能与8g氧气完全反应生成9g水;故选项说法错误。
故选:B。
质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用于化学变化,且要注意是质量守恒,而不是体积守恒;物质发生物理变化,则不适用于质量守恒定律来解释;是化学变化时也要对反应前后物质的质量关系进行计算判断,即反应时是否符合固定的质量比,据此分析问题即可.
本题难度不大,掌握质量守恒定律是物质在发生化学变化中表现出来的一种规律、化学变化和物理变化的判别是解题的关键.
16.【答案】D
【解析】解:A、5g酒精与5g水混合得到10g酒精溶液,属于物理变化,不符合质量守恒定律,故选项错误。
B、质量守恒定律的适用范围是化学变化,强调质量守恒,不适用于其他物理量例如体积等,故选项错误。
C、碳在氧气中燃烧生成二氧化碳,反应的化学方程式为:,参加反应的碳和氧气的质量比为12:32:44,12g碳完全反应时只能消耗32g氧气,则12g碳在64g氧气中充分反应,氧气有剩余,生成44g二氧化碳,故选项错误。
D、镁在空气中燃烧,生成的氧化镁的质量等于参加反应的镁的质量和氧气的质量之和,故选项正确。
故选:D。
本题难度不大,掌握质量守恒定律、化学反应中各物质之间的质量比等于相对分子质量和的比等是正确解答本题的关键。
17.【答案】D
【解析】解:某化合物密封加热完全分解后生成氨气、水和二氧化碳,生成物氨气、水和二氧化碳中含有氮、氢、氧、碳四种元素,则反应物中也一定含有这四种元素。某化合物中一定含有氮、氢、氧、碳四种元素。
故选:D。
根据质量守恒定律,反应前后元素种类不变,结合题意进行分析解答.
本题难度不大,掌握质量守恒定律反应前后,元素种类不变并能灵活运用是正确解答本题的关键.
18.【答案】D
【解析】
【分析】
本题主要考查质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和。反应后质量增加的是生成物,减少的是反应物,不变的可能为催化剂,题目难度不大。
【解答】
A.根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,,故A错误;
B.a、d质量减小则为反应物,b质量增加则为生成物,故属于化合反应,因此b一定是化合物,故B错误;
C.c的质量不变,可能为催化剂,故C错误;
D.参加反应的a与d的质量比为::8,故
D正确。
故选D。
19.【答案】A
【解析】解:根据质量守恒定律,由表格中的数字可知:,故克,根据反应物反应后质量减少,生成物质量增加则可推测反应物为Z;生成物为X、Y、W;
A、由以上推测可知,反应物为Z;生成物为X、Y、W,故错误;
B、由分析知,故正确;
C、从以上推测可以看出,该反应为Z物质分解为XYW三种物质,故Z为化合物,故正确;
D、反应中Y、W两种物质变化的质量比为::9,故正确。
故选:A。
在一密闭容器中,X、Y、Z、W四种物质,在一定的条件下反应一段时间后,测得反应前后各物质质量如表可知,根据质量守恒定律,则可求X的待测值;则由物质的增加或减少,可推测反应物与生成物等信息.
本题难度不大,根据质量守恒定律认真分析各物质反应前后的质量变化情况解答此类题的关键.
20.【答案】D
【解析】解:因为生成物二氧化硫、二氧化碳和水中含有C、H、O、S四种元素,所以反应物中也应该有这四种元素,又知某物质在氧气中充分燃烧,故生成物中的氧元素可能来自氧气,故可判断该生成物中一定含有碳元素、硫元素和氢元素,是否含有氧元素无法确定。
故选:D。
根据“化学变化前后元素的种类不变,原子的种类、个数不变”解答.
根据质量守恒定律可以判断物质的元素组成.
21.【答案】2:17
【解析】解:因为A和B的相时分子质量之比为5:1,所以2A::1,
设参与反应的B的质量为x,
::x,
解之得:;
根据质量守恒定律可得生成的C的质量为:;
在此反应中B和C的质量比为:2g::17.
故答案为:2:17.
根据化学方程式和已知条件“A和B的相时分子质量之比为5:1”以及A的质量,列出比例式,即可求出参与反应的B的质量;
根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.则生成的C的质量的质量的质量的质量;然后写出两者的比即可.
本题主要考查学生运用化学方程式和质量守恒定律进行计算的能力.
22.【答案】168
?
64
?
232
【解析】解:物质的质量比等于相对分子质量和的比.
168?64???
232
则三者的质量比是168:64:232
故答案为:168;64;232
根据相对分子质量及化学式前的化学计量数即可得出答案.
本题主要考查学生对元素的相对原子质量和化学方程式意义的认识.
23.【答案】肥皂水;
三;7:1;
【解析】
【分析】
本题主要考查根据质量守恒定律推断物质的化学式和根据物质的化学式计算元素的化合价,难度较小。
【解答】
硬水加入肥皂水,生成的泡沫少,并产生大量的浮渣;软水加入肥皂水,生成的泡沫多,所以区分硬水和软水,可以选用的物质是肥皂水.
故答案为:肥皂水.
含有三种元素,其中氮元素与氢元素的质量比为:14:::1.
故答案为:三;7:1.
根据所给化学方程式可以看出:化学方程式的右边比左边多出了2个氢原子和1个氧原子;根据质量守恒定律中的元素种类不变和原子个数不变的特点,可知多出的原子全部来自1个X分子中,即X的化学式为
故答案为:
第2页,共2页
第1页,共1页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
