上海市闵行区2020-2021学年九年级上学期期末(一模)化学试卷(word版有答案)
文档属性
| 名称 | 上海市闵行区2020-2021学年九年级上学期期末(一模)化学试卷(word版有答案) |  | |
| 格式 | zip | ||
| 文件大小 | 164.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-20 17:19:47 | ||
图片预览



文档简介
上海市闵行区2020-2021学年九年级上学期期末(一模)化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.铝元素的符号是
A.Al
B.Cl
C.AI
D.AL
2.属于化学变化的是
A.冰雪融化
B.花香四溢
C.研磨咖啡
D.粮食酿酒
3.加碘食盐含有碘酸钾(KIO3),其中碘元素(I)化合价为
A.+2
B.+3
C.+5
D.-5
4.属于溶液的是
A.奶茶
B.蒸馏水
C.咖啡
D.矿泉水
5.互为同素异形体的是
A.水银与银
B.木炭与石墨
C.氧气与臭氧
D.冰与干冰
6.下列物质在氧气中燃烧,能生成有刺激性气味气体的是
A.木炭
B.铁丝
C.红磷
D.硫粉
7.清洁用品中,呈酸性的是
A.洁厕灵pH=1
B.油烟净pH=13
C.肥皂水pH=10
D.牙膏pH=8
8.影响固体物质溶解度的操作是
A.加热
B.振荡
C.搅拌
D.加压
9.真空包装食品进入高原地区,包装袋往往会鼓起,这是因为包装袋内的气体分子
A.质量增大
B.间隔增大
C.体积增大
D.个数增多
10.属于氧化物的是
A.液氧
B.熟石灰
C.水
D.胆矾
11.下列符号中的“2”与O2中的“2”所表示的含义相似的是
A.H2O
B.2H
C.2CO
D.
12.燃烧前常将汽油(含C8H18等)喷成雾状,可以
A.减少O2消耗量
B.增大汽油与空气的接触面
C.减少CO2生成量
D.使C8H18等分子变得更小
13.物质用途体现其物理性质的是
A.氮气充入薯片包装袋
B.稀有气体制霓虹灯
C.无水硫酸铜检验水
D.氧气供人呼吸
14.利用如图装置验证空气中氧气的含量,叙述错误的是
A.实验前需检查装置气密性
B.白磷熄灭,冷却至室温后打开止水夹
C.最终量筒中液面降至约40mL刻度线
D.参与反应元素的存在形态都发生了改变
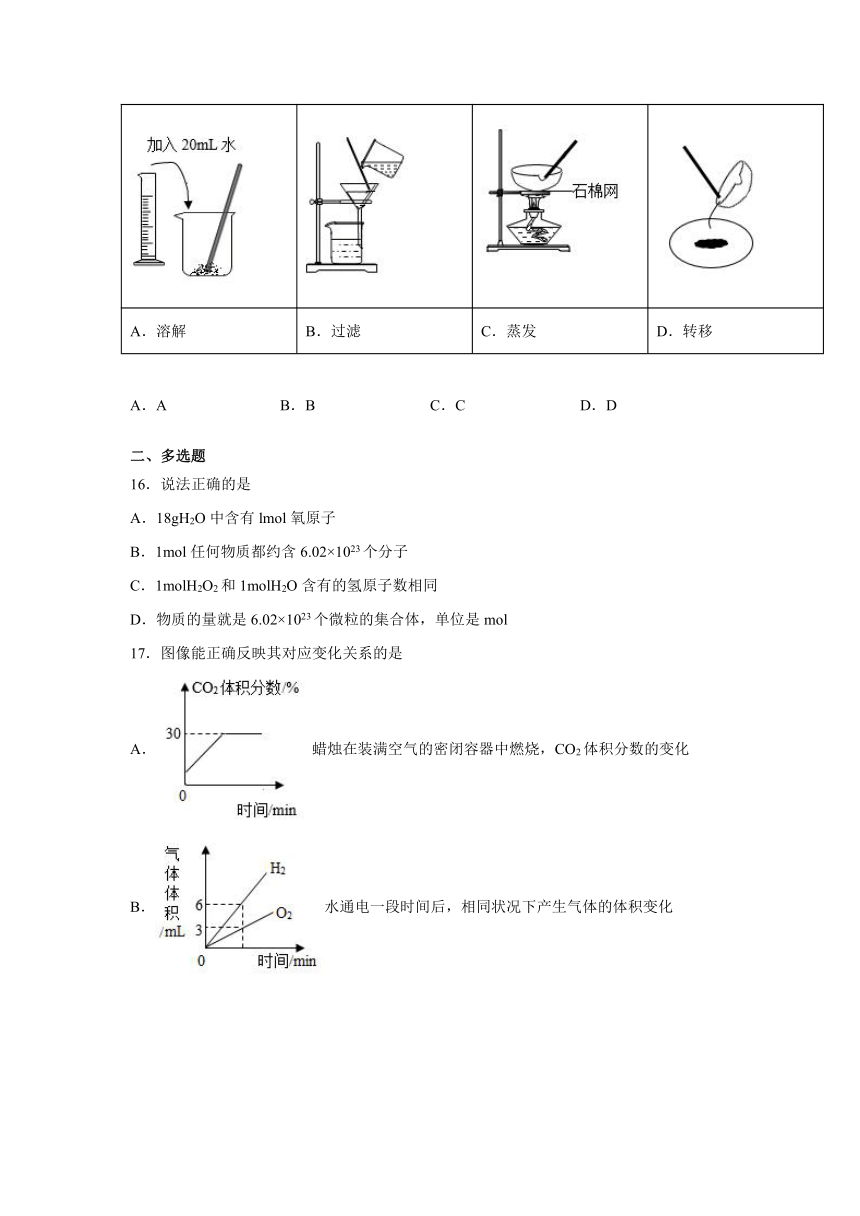
15.已知:20℃时,NaC1的溶解度为36g/100g水,现称取10g粗盐,经过溶解、过滤、蒸发、转移等步骤,除去泥沙得到尽可能多的精盐。下列操作正确且合理的是
A.溶解
B.过滤
C.蒸发
D.转移
A.A
B.B
C.C
D.D
二、多选题
16.说法正确的是
A.18gH2O中含有lmol氧原子
B.1mol任何物质都约含6.02×1023个分子
C.1molH2O2和1molH2O含有的氢原子数相同
D.物质的量就是6.02×1023个微粒的集合体,单位是mol
17.图像能正确反映其对应变化关系的是
A.蜡烛在装满空气的密闭容器中燃烧,CO2体积分数的变化
B.水通电一段时间后,相同状况下产生气体的体积变化
C.向一定质量饱和石灰水中加少量生石灰
D.在二氧化锰中不断加入过氧化氢溶液,水的质量变化
三、填空题
18.学好化学,科学防疫
①活性炭口罩能有效阻隔有害气体,原因是活性炭具有_______性。
②84消毒液和洁厕灵不能混合使用,会发生反应2HCl+NaClO=NaCl+H2O+X↑,X气体有毒,X的化学式为_______。
③过氧乙酸(C2H4O3)也是常见消毒剂,它是由_______种元素组成的,其中氢、氧原子的物质的量之比为_______。7.6g过氧乙酸中约含碳原子______个。
四、实验题
19.下表是硝酸钾和氯化钠的部分溶解度数据,回答下列问题。
温度(℃)
0
20
40
60
80
溶解度(g/100g水)
氯化钠
35.7
36.0
36.6
37.3
38.4
硝酸钾
13.3
31.6
63.9
110.0
169.0
①60℃时,硝酸钾的溶解度是_______。
②20℃,50g水中加入30g硝酸钾,所得溶液的质量是_______g。
③若硝酸钾中混有少量的氯化钠,提纯硝酸钾可采取的方法是_______。
④在20℃时,将等质量的硝酸钾和氯化钠分别加入到各盛有100g水的甲、乙两个烧杯中,充分搅拌后如图,说法错误的是_______(填序号)。
A
烧杯甲中溶液一定是不饱和溶液
B
烧杯乙中溶液的溶质是硝酸钾
C
若使烧杯乙中固体全部溶解,其溶液浓度一定增大
D
将温度升高到50℃,烧杯乙中的固体一定全部溶解
⑤20℃时,在100g水中溶解NaCl和KNO3,进行以下实验:
Ⅰ.溶液c所含溶质为_______,固体a为_______g。
Ⅱ.对整个实验过程分析正确的是_______。
A
固体b是纯净物
B
溶液c、d中NaC1质量分数相等
C
溶液d中硝酸钾的质量小于氯化钠的质量
D
实验过程中硝酸钾溶液始终是不饱和溶液
20.某混合气体中可能含有CO和CO2,兴趣小组同学设计了三套装置探究气体的成分。(A中澄清石灰水,B中足量澄清石灰水。)
①写出实验过程中可能发生反应的任意两个化学方程式_______、_______。
②你认为设计不合理的是_______(填序号),理由是_______。
③你认为设计合理的装置中,能说明原混合气体中含有一氧化碳的现象是____、____。
五、综合应用题
21.根据下图回答有关问题:
①图中仪器a的名称是_______。
②实验室用双氧水和二氧化锰制取氧气时,需产生平稳的气流并收集一瓶较纯净的氧气,可从图中选择的装置组合是_______(填字母),反应的化学方程式为_______,反应类型是_______;若用G装置收集氧气,验满的方法是_______。
③装置D是小组同学组装的实验室制二氧化碳气体的发生装置,该装置的优点是_______;为了解装置具有该优点的原因,他们在装置D中连接压强传感器,从而测定实验中试管内气体压强变化的情况(如下图)。
下列说法正确的是_______(填序号)。
Ⅰ.ab段试管中液面逐渐上升
Ⅱ.bc段石灰石与稀盐酸完全接触
Ⅲ.c点的对应操作是打开弹簣夹
Ⅳ.bc段压强基本不变,说明装置气密性好
④取25g石灰石样品,加入146g稀盐酸,恰好完全反应后测得剩余物质的质量为162.2g,(假定CO2全部从溶液中跑出),已知石灰石中的杂质不与稀盐酸发生反应。
Ⅰ.反应中生成二氧化碳的物质的量为_______mol。
Ⅱ.石灰石样品中碳酸钙的质量分数_______。(根据化学方程式列式计算)
参考答案
1.A
2.D
3.C
4.D
5.C
6.D
7.A
8.A
9.B
10.C
11.A
12.B
13.B
14.C
15.D
16.AC
17.BC
18.吸附
Cl2
3
4:3
1.204×1023
19.110.0g/100g水
65.8
降温结晶法
AC
KNO3、NaCl
114
AD
20.
甲
若气体中含有CO,经过氧化铜后也会生成CO2使B中澄清石灰水变浑浊,因此无法鉴别原气体中是否含有CO2
玻璃管中黑色固体变红色
尾气点燃有蓝色火焰
21.锥形瓶
CE
2H2O22H2O+O2↑
分解反应
将带火星的木条伸到导管n处,若该木条复燃,则证明已收集满氧气
随时控制反应的发生与停止
Ⅲ、Ⅳ
0.2mol
解:根据质量守恒定律可知生成二氧化碳的质量为25g+146g-162.2g=8.8g;设石灰石样品中碳酸钙的质量分数为x
答:石灰石样品中碳酸钙的质量分数80%。
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.铝元素的符号是
A.Al
B.Cl
C.AI
D.AL
2.属于化学变化的是
A.冰雪融化
B.花香四溢
C.研磨咖啡
D.粮食酿酒
3.加碘食盐含有碘酸钾(KIO3),其中碘元素(I)化合价为
A.+2
B.+3
C.+5
D.-5
4.属于溶液的是
A.奶茶
B.蒸馏水
C.咖啡
D.矿泉水
5.互为同素异形体的是
A.水银与银
B.木炭与石墨
C.氧气与臭氧
D.冰与干冰
6.下列物质在氧气中燃烧,能生成有刺激性气味气体的是
A.木炭
B.铁丝
C.红磷
D.硫粉
7.清洁用品中,呈酸性的是
A.洁厕灵pH=1
B.油烟净pH=13
C.肥皂水pH=10
D.牙膏pH=8
8.影响固体物质溶解度的操作是
A.加热
B.振荡
C.搅拌
D.加压
9.真空包装食品进入高原地区,包装袋往往会鼓起,这是因为包装袋内的气体分子
A.质量增大
B.间隔增大
C.体积增大
D.个数增多
10.属于氧化物的是
A.液氧
B.熟石灰
C.水
D.胆矾
11.下列符号中的“2”与O2中的“2”所表示的含义相似的是
A.H2O
B.2H
C.2CO
D.
12.燃烧前常将汽油(含C8H18等)喷成雾状,可以
A.减少O2消耗量
B.增大汽油与空气的接触面
C.减少CO2生成量
D.使C8H18等分子变得更小
13.物质用途体现其物理性质的是
A.氮气充入薯片包装袋
B.稀有气体制霓虹灯
C.无水硫酸铜检验水
D.氧气供人呼吸
14.利用如图装置验证空气中氧气的含量,叙述错误的是
A.实验前需检查装置气密性
B.白磷熄灭,冷却至室温后打开止水夹
C.最终量筒中液面降至约40mL刻度线
D.参与反应元素的存在形态都发生了改变
15.已知:20℃时,NaC1的溶解度为36g/100g水,现称取10g粗盐,经过溶解、过滤、蒸发、转移等步骤,除去泥沙得到尽可能多的精盐。下列操作正确且合理的是
A.溶解
B.过滤
C.蒸发
D.转移
A.A
B.B
C.C
D.D
二、多选题
16.说法正确的是
A.18gH2O中含有lmol氧原子
B.1mol任何物质都约含6.02×1023个分子
C.1molH2O2和1molH2O含有的氢原子数相同
D.物质的量就是6.02×1023个微粒的集合体,单位是mol
17.图像能正确反映其对应变化关系的是
A.蜡烛在装满空气的密闭容器中燃烧,CO2体积分数的变化
B.水通电一段时间后,相同状况下产生气体的体积变化
C.向一定质量饱和石灰水中加少量生石灰
D.在二氧化锰中不断加入过氧化氢溶液,水的质量变化
三、填空题
18.学好化学,科学防疫
①活性炭口罩能有效阻隔有害气体,原因是活性炭具有_______性。
②84消毒液和洁厕灵不能混合使用,会发生反应2HCl+NaClO=NaCl+H2O+X↑,X气体有毒,X的化学式为_______。
③过氧乙酸(C2H4O3)也是常见消毒剂,它是由_______种元素组成的,其中氢、氧原子的物质的量之比为_______。7.6g过氧乙酸中约含碳原子______个。
四、实验题
19.下表是硝酸钾和氯化钠的部分溶解度数据,回答下列问题。
温度(℃)
0
20
40
60
80
溶解度(g/100g水)
氯化钠
35.7
36.0
36.6
37.3
38.4
硝酸钾
13.3
31.6
63.9
110.0
169.0
①60℃时,硝酸钾的溶解度是_______。
②20℃,50g水中加入30g硝酸钾,所得溶液的质量是_______g。
③若硝酸钾中混有少量的氯化钠,提纯硝酸钾可采取的方法是_______。
④在20℃时,将等质量的硝酸钾和氯化钠分别加入到各盛有100g水的甲、乙两个烧杯中,充分搅拌后如图,说法错误的是_______(填序号)。
A
烧杯甲中溶液一定是不饱和溶液
B
烧杯乙中溶液的溶质是硝酸钾
C
若使烧杯乙中固体全部溶解,其溶液浓度一定增大
D
将温度升高到50℃,烧杯乙中的固体一定全部溶解
⑤20℃时,在100g水中溶解NaCl和KNO3,进行以下实验:
Ⅰ.溶液c所含溶质为_______,固体a为_______g。
Ⅱ.对整个实验过程分析正确的是_______。
A
固体b是纯净物
B
溶液c、d中NaC1质量分数相等
C
溶液d中硝酸钾的质量小于氯化钠的质量
D
实验过程中硝酸钾溶液始终是不饱和溶液
20.某混合气体中可能含有CO和CO2,兴趣小组同学设计了三套装置探究气体的成分。(A中澄清石灰水,B中足量澄清石灰水。)
①写出实验过程中可能发生反应的任意两个化学方程式_______、_______。
②你认为设计不合理的是_______(填序号),理由是_______。
③你认为设计合理的装置中,能说明原混合气体中含有一氧化碳的现象是____、____。
五、综合应用题
21.根据下图回答有关问题:
①图中仪器a的名称是_______。
②实验室用双氧水和二氧化锰制取氧气时,需产生平稳的气流并收集一瓶较纯净的氧气,可从图中选择的装置组合是_______(填字母),反应的化学方程式为_______,反应类型是_______;若用G装置收集氧气,验满的方法是_______。
③装置D是小组同学组装的实验室制二氧化碳气体的发生装置,该装置的优点是_______;为了解装置具有该优点的原因,他们在装置D中连接压强传感器,从而测定实验中试管内气体压强变化的情况(如下图)。
下列说法正确的是_______(填序号)。
Ⅰ.ab段试管中液面逐渐上升
Ⅱ.bc段石灰石与稀盐酸完全接触
Ⅲ.c点的对应操作是打开弹簣夹
Ⅳ.bc段压强基本不变,说明装置气密性好
④取25g石灰石样品,加入146g稀盐酸,恰好完全反应后测得剩余物质的质量为162.2g,(假定CO2全部从溶液中跑出),已知石灰石中的杂质不与稀盐酸发生反应。
Ⅰ.反应中生成二氧化碳的物质的量为_______mol。
Ⅱ.石灰石样品中碳酸钙的质量分数_______。(根据化学方程式列式计算)
参考答案
1.A
2.D
3.C
4.D
5.C
6.D
7.A
8.A
9.B
10.C
11.A
12.B
13.B
14.C
15.D
16.AC
17.BC
18.吸附
Cl2
3
4:3
1.204×1023
19.110.0g/100g水
65.8
降温结晶法
AC
KNO3、NaCl
114
AD
20.
甲
若气体中含有CO,经过氧化铜后也会生成CO2使B中澄清石灰水变浑浊,因此无法鉴别原气体中是否含有CO2
玻璃管中黑色固体变红色
尾气点燃有蓝色火焰
21.锥形瓶
CE
2H2O22H2O+O2↑
分解反应
将带火星的木条伸到导管n处,若该木条复燃,则证明已收集满氧气
随时控制反应的发生与停止
Ⅲ、Ⅳ
0.2mol
解:根据质量守恒定律可知生成二氧化碳的质量为25g+146g-162.2g=8.8g;设石灰石样品中碳酸钙的质量分数为x
答:石灰石样品中碳酸钙的质量分数80%。
同课章节目录
