高中化学人教版(2019)必修二 5.3 无机非金属材料
文档属性
| 名称 | 高中化学人教版(2019)必修二 5.3 无机非金属材料 |

|
|
| 格式 | zip | ||
| 文件大小 | 1005.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-27 00:00:00 | ||
图片预览










文档简介
(共30张PPT)
第三节 无机非金属材料
第五章 化工生产中的重要非金属元素
1.了解硅酸盐及其结构特点,了解传统硅酸盐产品(陶瓷、玻璃、水泥)的工
业生产(原料、设备等)。
2.了解硅和二氧化硅的性质,认识碳化硅、氮化硅、纳米材料等新型无机非
金属材料。
3.知道硅及其化合物在材料家族中的应用,增强关注社会的意识和责任感。
核心素养发展目标
二、新型无机非金属材料
内容索引
NEIRONGSUOYIN
一、传统无机非金属材料——硅酸盐材料
传统无机非金属材料——硅酸盐材料
CHUAN
TONG
WU
JI
FEI
JIN
SHU
CAI
LIAO——GUI
SUAN
YAN
CAI
LIAO
01
1.硅酸盐及其结构
(1)硅酸盐的概念
硅酸盐是由硅、氧和金属组成的化合物的总称。它们种类繁多、组成各异、结构复杂,在自然界中广泛存在。
(2)硅酸盐的结构
知识梳理
在硅酸盐中,Si和O构成了硅氧四面体,其结构如图所示。每个Si结合
个O,Si在中心,O在四面体的4个顶角;许多这样的四面体还可以通过顶角的
相互连接,每个
为两个四面体所共有,与
个Si相结合。
4
O
O
2
(3)硅酸盐的特性
硅氧四面体结构的特殊性,决定了硅酸盐材料大多具有硬度高、熔点高、难溶于水、化学性质稳定、耐腐蚀等特点。
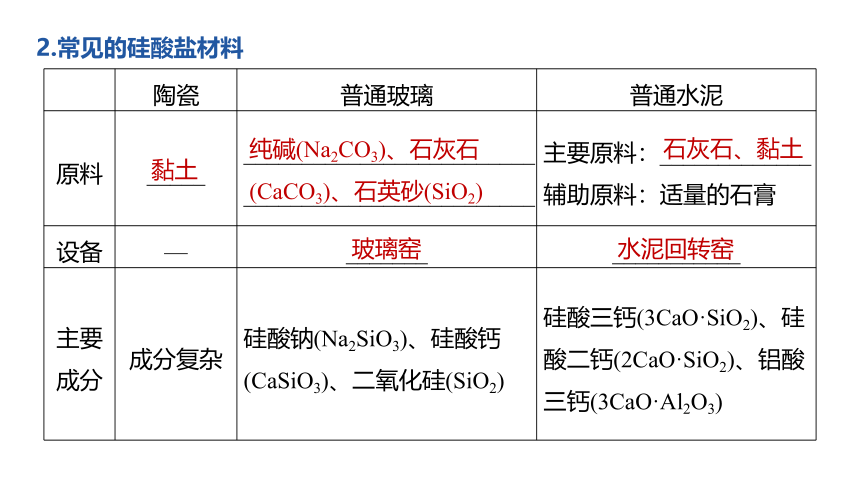
2.常见的硅酸盐材料
?
陶瓷
普通玻璃
普通水泥
原料
_____
__________________________________________________
主要原料:_____________
辅助原料:适量的石膏
设备
—
_______
___________
主要
成分
成分复杂
硅酸钠(Na2SiO3)、硅酸钙(CaSiO3)、二氧化硅(SiO2)
硅酸三钙(3CaO·SiO2)、硅酸二钙(2CaO·SiO2)、铝酸三钙(3CaO·Al2O3)
黏土
纯碱(Na2CO3)、石灰石
(CaCO3)、石英砂(SiO2)
石灰石、黏土
玻璃窑
水泥回转窑
特点
抗氧化、抗酸碱腐蚀、耐高温、绝缘
玻璃是非晶体,称为玻璃态物质,无固定熔点,在某一温度范围内软化可加工成制品
具有水硬性,与水掺和搅拌并静置后,很容易凝固变硬
用途
建筑材料、绝缘材料、日用器皿、卫生洁具
建筑材料、光学仪器、各种器皿、制造玻璃纤维
大量用于建筑和水利工程
(1)硅酸盐是由硅、氧和金属组成的混合物( )
(2)硅酸盐结构较为复杂,大多不溶于水,化学性质很稳定( )
(3)硅氧四面体中,硅原子与氧原子都是以共价键结合( )
(4)水泥与玻璃的共同原料是石灰石,水泥与陶瓷的共同原料是黏土( )
(5)陶瓷、玻璃、水泥的生产都需要在高温下进行( )
(6)玻璃和水泥生产中都发生复杂的物理和化学变化( )
判断正误
×
√
√
√
√
√
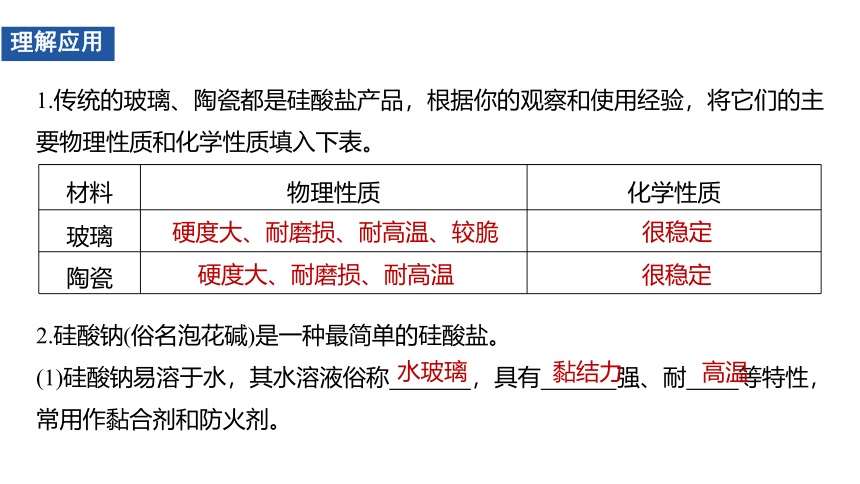
1.传统的玻璃、陶瓷都是硅酸盐产品,根据你的观察和使用经验,将它们的主要物理性质和化学性质填入下表。
理解应用
材料
物理性质
化学性质
玻璃
?
?
陶瓷
?
?
硬度大、耐磨损、耐高温、较脆
很稳定
硬度大、耐磨损、耐高温
很稳定
2.硅酸钠(俗名泡花碱)是一种最简单的硅酸盐。
(1)硅酸钠易溶于水,其水溶液俗称
,具有
强、耐
等特性,常用作黏合剂和防火剂。
水玻璃
黏结力
高温
(2)硅酸钠溶液与盐酸反应生成硅酸(H2SiO3)沉淀,其离子方程式是
。
(3)少量的二氧化碳通入硅酸钠溶液中,反应的离子方程式是
。
2H+===H2SiO3↓
H2O===H2SiO3↓+CO
相关链接
硅酸盐的丰富性和多样性
由于铝与硅在元素周期表中位置相邻、粒子大小相近,+3价的铝常或多或少地置换硅酸盐中+4价的硅而形成铝硅酸盐。为了保持电中性,会伴随引入其他正离子,从而大大增加了硅酸盐品种的多样性和结构的复杂性,同时也为应用硅酸盐材料提供了更广阔的选择。硅酸盐岩石长期在水和大气中二氧化碳的侵蚀下,风化为黏土,并且形成土壤胶体。土壤胶体粒子表面积巨大且带负电,能与NH
、K+等数十种生物所需的营养离子相互作用,使土壤具有保肥能力。这是大自然对人类及地球生物的馈赠,我们应该爱护大地母亲。保持土壤的良好结构和化学成分,就是保证农业、牧业和林业持续发展的基础。
解析 普通玻璃主要成分为Na2SiO3、CaSiO3和SiO2。
1.下列关于硅酸盐材料的说法错误的是
A.生活中常见的硅酸盐材料有玻璃、水泥、陶瓷
B.普通玻璃的主要成分是二氧化硅
C.陶瓷的主要原料是黏土
D.硅酸盐水泥以石灰石和黏土为主要原料
跟踪强化
1
2
3
√
2.下列关于水玻璃的性质和用途的叙述中不正确的是
A.这是一种矿物胶,既不燃烧也不受腐蚀
B.在建筑工业上可以作黏合剂、耐酸水泥掺料
C.木材、织物浸过水玻璃后具有防腐性能且不易燃烧
D.水玻璃的化学性质稳定,在空气中不易变质
解析 水玻璃为硅酸钠溶液,其化学性质稳定,但可与空气中的二氧化碳反应生成硅酸沉淀。
1
2
3
√
3.某博物馆陈列着大量明清砖瓦和精美瓷器(婺州窑),婺州窑瓷器胎体的原料为高岭土[AlnSi2O5(OH)4]。下列说法不正确的是
A.古代的陶瓷、砖瓦都是硅酸盐产品
B.高岭土为含水的铝硅酸盐
C.n=3
D.我国在新石器时代已能烧制陶器
解析 根据化合物中正负化合价代数和为0的规则:n×(+3)+2×(+4)+5×(-2)+4×(-1)=0,解得n=2。
1
2
3
√
返回
02
新型无机非金属材料
XIN
XING
WU
JI
FEI
JIN
SHU
CAI
LIAO
1.硅和二氧化硅
(1)硅的存在与性质
①硅在自然界主要以
和
的形式存在;
②单质硅是应用最为广泛的半导体材料;
③高温下,硅能与氧气反应生成
,与氯气反应生成
。
(2)二氧化硅的性质
①二氧化硅硬度大、熔点高,不溶于水;
②酸性氧化物:SiO2+2NaOH===
;
③具有氧化性:SiO2+2C
;
④特性:SiO2+4HF===
。
知识梳理
硅酸盐
氧化物
SiO2
SiCl4
Na2SiO3+H2O
Si+2CO↑
SiF4↑+2H2O
2.新型陶瓷
(1)新型陶瓷与传统陶瓷相比,在
上有很大的变化,在
等方面具有很多新的特性和功能。
(2)常见新型陶瓷及其用途(连线)
成分
光学、热学、电
学、磁学
(3)高温结构陶瓷——碳化硅(SiC)
碳化硅俗称
,它是由碳原子和硅原子通过
连接而形成,与
的结构类似,具有硬度大和优异的
性能。
金刚砂
共价键
金刚石
高温抗氧化
3.碳纳米材料
(1)富勒烯是由
构成的一系列笼形分子的总称,如C50、C60、C70、C120等,其代表物是
。
(2)碳纳米管是由
卷成的管状物,具有
尺度的直径。比表面积大,具有高强度和优良的电学性能。
(3)石墨烯是只有一个
直径厚度的单层石墨,其独特的结构使其电阻率低、热导率高,具有很高的强度。
碳原子
C60
石墨片层
纳米
碳原子
特别提示
碳纳米材料(富勒烯、石墨烯等)、金刚石、石墨都是碳的同素异形体,它们具有不同的结构(碳原子排列方式不同)和性质。
(1)硅晶片是生产芯片的基础材料( )
(2)生产光导纤维的原料是二氧化硅( )
(3)二氧化硅是酸性氧化物,只能与碱反应,不能与酸反应( )
(4)磨口玻璃塞试剂瓶不能盛放烧碱溶液,但能盛放氢氟酸( )
(5)金刚砂和金刚石结构类似,互为同素异形体( )
(6)富勒烯和石墨烯完全燃烧的产物都是二氧化碳( )
判断正误
√
√
×
×
×
√
1.工业制备高纯硅的原理如图所示:
深度思考
(1)写出工业制备高纯硅反应的化学方程式:
①
;
②
;
③
。
(2)上述反应共同的反应类型是
,反应①中焦炭的作用是
,反应③中氢气的作用是
。
(3)在半导体工业中有这样一句行话:“从沙滩到用户”,你是如何理解的?
氧化还原反应(或置换反应)
还原剂
还原剂
提示 沙子的主要成分是SiO2,作为半导体材料的硅单质是用焦炭还原SiO2制得的。
2.回答下列问题。
(1)碳和硅的原子结构有何异同?从二者在元素周期表中的位置能获得什么信息?
提示 原子的最外层电子数相同,电子层数不同。不在同一周期,位于同一族。从二者在周期表中的位置可知碳的非金属性强于硅。
(2)碳和硅单质的存在形式有何相似之处?其性质有何不同?
提示 单质都有晶体和无定形两种。硅晶体是良好的半导体材料,而石墨是良导体,金刚石、C60不导电。
(3)碳和硅的氧化物有何异同?
提示 硅的氧化物只有SiO2,而碳的氧化物有CO和CO2两种。SiO2、CO2均属于酸性氧化物,CO属于不成盐氧化物。SiO2为固态,存在于地表及地壳中;CO2、CO为气态,存在于大气中;SiO2的性质比CO2更稳定等。
3.氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定,工业上普遍采用高纯硅与纯氮在1
300
℃时反应获得。
(1)根据性质,推测氮化硅陶瓷的用途是________(填字母)。
A.制汽轮机叶片
B.制有色金属
C.制永久性模具
D.制造柴油机
(2)写出氮原子结构示意图________,根据元素周期律知识,请写出氮化硅的化学式______。
ACD
Si3N4
(3)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应,试推测该陶瓷被氢氟酸腐蚀的化学方程式:
______________________________。
(4)现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为____________________________________。
Si3N4+12HF===3SiF4↑+4NH3↑
3SiCl4+2N2+6H2
Si3N4+12HCl
相关链接
近几年,具有特殊功能的特殊的含硅材料得到迅速发展。例如硅与碳的化合物碳化硅(SiC,俗称金刚砂),具有金刚石结构,硬度很大,可用作砂纸、砂轮的磨料;含4%硅的硅钢具有很高的导磁性,主要用作变压器铁芯;人工合成的硅橡胶是目前最好的既耐高温又耐低温的橡胶,在-60~250
℃仍能保持良好的弹性,用于制造火箭、导弹、飞机的零件和绝缘材料等;人工制造的分子筛(一种具有均匀微孔结构的铝硅酸盐),主要用作吸附剂和催化剂;等等。
1.下列物品或设备的成分中含有二氧化硅的是
①门窗玻璃 ②水晶镜片 ③石英钟表 ④玛瑙首饰 ⑤硅太阳能电池
⑥光导纤维 ⑦计算机芯片
A.①②③④⑥
B.全部
C.⑤⑦
D.①②⑥⑦
1
2
3
跟踪强化
解析 玻璃、石英、水晶、玛瑙和光导纤维的成分中都含有二氧化硅,计算机芯片、硅太阳能电池的主要成分是单质硅。
√
2.(2018·三门峡高一期末)高纯度晶硅是典型的无机非金属材料,又称“半导体”材料。它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:
1
2
3
下列说法不正确的是
A.步骤①的化学方程式:SiO2+C
Si+CO2↑
B.步骤①中每生成1
mol
Si,转移4
mol电子
C.步骤③中的反应为氧化还原反应
D.高纯硅是制造太阳能电池的常用材料,二氧化硅是制造光导纤维的基本原料
√
3.下列物质与其对应的用途搭配不正确的是
A.高能燃料——火箭动力
B.石英砂——制造光导纤维
C.半导体硅晶片——制造计算机芯片
D.高强度耐火陶瓷——制造轮船
√
1
2
3
解析 制造轮船材料为钢铁,不能选用高强度耐火陶瓷。
返回
第三节 无机非金属材料
第五章 化工生产中的重要非金属元素
1.了解硅酸盐及其结构特点,了解传统硅酸盐产品(陶瓷、玻璃、水泥)的工
业生产(原料、设备等)。
2.了解硅和二氧化硅的性质,认识碳化硅、氮化硅、纳米材料等新型无机非
金属材料。
3.知道硅及其化合物在材料家族中的应用,增强关注社会的意识和责任感。
核心素养发展目标
二、新型无机非金属材料
内容索引
NEIRONGSUOYIN
一、传统无机非金属材料——硅酸盐材料
传统无机非金属材料——硅酸盐材料
CHUAN
TONG
WU
JI
FEI
JIN
SHU
CAI
LIAO——GUI
SUAN
YAN
CAI
LIAO
01
1.硅酸盐及其结构
(1)硅酸盐的概念
硅酸盐是由硅、氧和金属组成的化合物的总称。它们种类繁多、组成各异、结构复杂,在自然界中广泛存在。
(2)硅酸盐的结构
知识梳理
在硅酸盐中,Si和O构成了硅氧四面体,其结构如图所示。每个Si结合
个O,Si在中心,O在四面体的4个顶角;许多这样的四面体还可以通过顶角的
相互连接,每个
为两个四面体所共有,与
个Si相结合。
4
O
O
2
(3)硅酸盐的特性
硅氧四面体结构的特殊性,决定了硅酸盐材料大多具有硬度高、熔点高、难溶于水、化学性质稳定、耐腐蚀等特点。
2.常见的硅酸盐材料
?
陶瓷
普通玻璃
普通水泥
原料
_____
__________________________________________________
主要原料:_____________
辅助原料:适量的石膏
设备
—
_______
___________
主要
成分
成分复杂
硅酸钠(Na2SiO3)、硅酸钙(CaSiO3)、二氧化硅(SiO2)
硅酸三钙(3CaO·SiO2)、硅酸二钙(2CaO·SiO2)、铝酸三钙(3CaO·Al2O3)
黏土
纯碱(Na2CO3)、石灰石
(CaCO3)、石英砂(SiO2)
石灰石、黏土
玻璃窑
水泥回转窑
特点
抗氧化、抗酸碱腐蚀、耐高温、绝缘
玻璃是非晶体,称为玻璃态物质,无固定熔点,在某一温度范围内软化可加工成制品
具有水硬性,与水掺和搅拌并静置后,很容易凝固变硬
用途
建筑材料、绝缘材料、日用器皿、卫生洁具
建筑材料、光学仪器、各种器皿、制造玻璃纤维
大量用于建筑和水利工程
(1)硅酸盐是由硅、氧和金属组成的混合物( )
(2)硅酸盐结构较为复杂,大多不溶于水,化学性质很稳定( )
(3)硅氧四面体中,硅原子与氧原子都是以共价键结合( )
(4)水泥与玻璃的共同原料是石灰石,水泥与陶瓷的共同原料是黏土( )
(5)陶瓷、玻璃、水泥的生产都需要在高温下进行( )
(6)玻璃和水泥生产中都发生复杂的物理和化学变化( )
判断正误
×
√
√
√
√
√
1.传统的玻璃、陶瓷都是硅酸盐产品,根据你的观察和使用经验,将它们的主要物理性质和化学性质填入下表。
理解应用
材料
物理性质
化学性质
玻璃
?
?
陶瓷
?
?
硬度大、耐磨损、耐高温、较脆
很稳定
硬度大、耐磨损、耐高温
很稳定
2.硅酸钠(俗名泡花碱)是一种最简单的硅酸盐。
(1)硅酸钠易溶于水,其水溶液俗称
,具有
强、耐
等特性,常用作黏合剂和防火剂。
水玻璃
黏结力
高温
(2)硅酸钠溶液与盐酸反应生成硅酸(H2SiO3)沉淀,其离子方程式是
。
(3)少量的二氧化碳通入硅酸钠溶液中,反应的离子方程式是
。
2H+===H2SiO3↓
H2O===H2SiO3↓+CO
相关链接
硅酸盐的丰富性和多样性
由于铝与硅在元素周期表中位置相邻、粒子大小相近,+3价的铝常或多或少地置换硅酸盐中+4价的硅而形成铝硅酸盐。为了保持电中性,会伴随引入其他正离子,从而大大增加了硅酸盐品种的多样性和结构的复杂性,同时也为应用硅酸盐材料提供了更广阔的选择。硅酸盐岩石长期在水和大气中二氧化碳的侵蚀下,风化为黏土,并且形成土壤胶体。土壤胶体粒子表面积巨大且带负电,能与NH
、K+等数十种生物所需的营养离子相互作用,使土壤具有保肥能力。这是大自然对人类及地球生物的馈赠,我们应该爱护大地母亲。保持土壤的良好结构和化学成分,就是保证农业、牧业和林业持续发展的基础。
解析 普通玻璃主要成分为Na2SiO3、CaSiO3和SiO2。
1.下列关于硅酸盐材料的说法错误的是
A.生活中常见的硅酸盐材料有玻璃、水泥、陶瓷
B.普通玻璃的主要成分是二氧化硅
C.陶瓷的主要原料是黏土
D.硅酸盐水泥以石灰石和黏土为主要原料
跟踪强化
1
2
3
√
2.下列关于水玻璃的性质和用途的叙述中不正确的是
A.这是一种矿物胶,既不燃烧也不受腐蚀
B.在建筑工业上可以作黏合剂、耐酸水泥掺料
C.木材、织物浸过水玻璃后具有防腐性能且不易燃烧
D.水玻璃的化学性质稳定,在空气中不易变质
解析 水玻璃为硅酸钠溶液,其化学性质稳定,但可与空气中的二氧化碳反应生成硅酸沉淀。
1
2
3
√
3.某博物馆陈列着大量明清砖瓦和精美瓷器(婺州窑),婺州窑瓷器胎体的原料为高岭土[AlnSi2O5(OH)4]。下列说法不正确的是
A.古代的陶瓷、砖瓦都是硅酸盐产品
B.高岭土为含水的铝硅酸盐
C.n=3
D.我国在新石器时代已能烧制陶器
解析 根据化合物中正负化合价代数和为0的规则:n×(+3)+2×(+4)+5×(-2)+4×(-1)=0,解得n=2。
1
2
3
√
返回
02
新型无机非金属材料
XIN
WU
JI
FEI
JIN
SHU
CAI
LIAO
1.硅和二氧化硅
(1)硅的存在与性质
①硅在自然界主要以
和
的形式存在;
②单质硅是应用最为广泛的半导体材料;
③高温下,硅能与氧气反应生成
,与氯气反应生成
。
(2)二氧化硅的性质
①二氧化硅硬度大、熔点高,不溶于水;
②酸性氧化物:SiO2+2NaOH===
;
③具有氧化性:SiO2+2C
;
④特性:SiO2+4HF===
。
知识梳理
硅酸盐
氧化物
SiO2
SiCl4
Na2SiO3+H2O
Si+2CO↑
SiF4↑+2H2O
2.新型陶瓷
(1)新型陶瓷与传统陶瓷相比,在
上有很大的变化,在
等方面具有很多新的特性和功能。
(2)常见新型陶瓷及其用途(连线)
成分
光学、热学、电
学、磁学
(3)高温结构陶瓷——碳化硅(SiC)
碳化硅俗称
,它是由碳原子和硅原子通过
连接而形成,与
的结构类似,具有硬度大和优异的
性能。
金刚砂
共价键
金刚石
高温抗氧化
3.碳纳米材料
(1)富勒烯是由
构成的一系列笼形分子的总称,如C50、C60、C70、C120等,其代表物是
。
(2)碳纳米管是由
卷成的管状物,具有
尺度的直径。比表面积大,具有高强度和优良的电学性能。
(3)石墨烯是只有一个
直径厚度的单层石墨,其独特的结构使其电阻率低、热导率高,具有很高的强度。
碳原子
C60
石墨片层
纳米
碳原子
特别提示
碳纳米材料(富勒烯、石墨烯等)、金刚石、石墨都是碳的同素异形体,它们具有不同的结构(碳原子排列方式不同)和性质。
(1)硅晶片是生产芯片的基础材料( )
(2)生产光导纤维的原料是二氧化硅( )
(3)二氧化硅是酸性氧化物,只能与碱反应,不能与酸反应( )
(4)磨口玻璃塞试剂瓶不能盛放烧碱溶液,但能盛放氢氟酸( )
(5)金刚砂和金刚石结构类似,互为同素异形体( )
(6)富勒烯和石墨烯完全燃烧的产物都是二氧化碳( )
判断正误
√
√
×
×
×
√
1.工业制备高纯硅的原理如图所示:
深度思考
(1)写出工业制备高纯硅反应的化学方程式:
①
;
②
;
③
。
(2)上述反应共同的反应类型是
,反应①中焦炭的作用是
,反应③中氢气的作用是
。
(3)在半导体工业中有这样一句行话:“从沙滩到用户”,你是如何理解的?
氧化还原反应(或置换反应)
还原剂
还原剂
提示 沙子的主要成分是SiO2,作为半导体材料的硅单质是用焦炭还原SiO2制得的。
2.回答下列问题。
(1)碳和硅的原子结构有何异同?从二者在元素周期表中的位置能获得什么信息?
提示 原子的最外层电子数相同,电子层数不同。不在同一周期,位于同一族。从二者在周期表中的位置可知碳的非金属性强于硅。
(2)碳和硅单质的存在形式有何相似之处?其性质有何不同?
提示 单质都有晶体和无定形两种。硅晶体是良好的半导体材料,而石墨是良导体,金刚石、C60不导电。
(3)碳和硅的氧化物有何异同?
提示 硅的氧化物只有SiO2,而碳的氧化物有CO和CO2两种。SiO2、CO2均属于酸性氧化物,CO属于不成盐氧化物。SiO2为固态,存在于地表及地壳中;CO2、CO为气态,存在于大气中;SiO2的性质比CO2更稳定等。
3.氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定,工业上普遍采用高纯硅与纯氮在1
300
℃时反应获得。
(1)根据性质,推测氮化硅陶瓷的用途是________(填字母)。
A.制汽轮机叶片
B.制有色金属
C.制永久性模具
D.制造柴油机
(2)写出氮原子结构示意图________,根据元素周期律知识,请写出氮化硅的化学式______。
ACD
Si3N4
(3)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应,试推测该陶瓷被氢氟酸腐蚀的化学方程式:
______________________________。
(4)现用四氯化硅和氮气在氢气气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为____________________________________。
Si3N4+12HF===3SiF4↑+4NH3↑
3SiCl4+2N2+6H2
Si3N4+12HCl
相关链接
近几年,具有特殊功能的特殊的含硅材料得到迅速发展。例如硅与碳的化合物碳化硅(SiC,俗称金刚砂),具有金刚石结构,硬度很大,可用作砂纸、砂轮的磨料;含4%硅的硅钢具有很高的导磁性,主要用作变压器铁芯;人工合成的硅橡胶是目前最好的既耐高温又耐低温的橡胶,在-60~250
℃仍能保持良好的弹性,用于制造火箭、导弹、飞机的零件和绝缘材料等;人工制造的分子筛(一种具有均匀微孔结构的铝硅酸盐),主要用作吸附剂和催化剂;等等。
1.下列物品或设备的成分中含有二氧化硅的是
①门窗玻璃 ②水晶镜片 ③石英钟表 ④玛瑙首饰 ⑤硅太阳能电池
⑥光导纤维 ⑦计算机芯片
A.①②③④⑥
B.全部
C.⑤⑦
D.①②⑥⑦
1
2
3
跟踪强化
解析 玻璃、石英、水晶、玛瑙和光导纤维的成分中都含有二氧化硅,计算机芯片、硅太阳能电池的主要成分是单质硅。
√
2.(2018·三门峡高一期末)高纯度晶硅是典型的无机非金属材料,又称“半导体”材料。它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:
1
2
3
下列说法不正确的是
A.步骤①的化学方程式:SiO2+C
Si+CO2↑
B.步骤①中每生成1
mol
Si,转移4
mol电子
C.步骤③中的反应为氧化还原反应
D.高纯硅是制造太阳能电池的常用材料,二氧化硅是制造光导纤维的基本原料
√
3.下列物质与其对应的用途搭配不正确的是
A.高能燃料——火箭动力
B.石英砂——制造光导纤维
C.半导体硅晶片——制造计算机芯片
D.高强度耐火陶瓷——制造轮船
√
1
2
3
解析 制造轮船材料为钢铁,不能选用高强度耐火陶瓷。
返回
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
