初中化学京改版(2013)九年级上册第七章化学反应的定量研究单元 同步试题
文档属性
| 名称 | 初中化学京改版(2013)九年级上册第七章化学反应的定量研究单元 同步试题 |

|
|
| 格式 | docx | ||
| 文件大小 | 120.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-26 00:00:00 | ||
图片预览



文档简介
初中化学京改版(2013)九年级上册第七章化学反应的定量研究单元同步
一、单选题
1.下列化学方程式书写正确的是(?
?
?)
A.
B.
C.
D.
2.下列描述与化学方程式表示一致的是(
)
A.碳在空气中充分燃烧
B.铁丝在纯氧气中燃烧
C.红磷在空气中充分燃烧
D.镁带燃烧
3.在抗击新冠肺炎的阻击战中消毒液一度紧缺,次氯酸钠(白色固体,具有腐蚀性,易分解产生有害气体)就是其中一种,相关企业加紧生产,生产次氯酸钠的一个反应的化学方程式是。以下有关说法不正确的是( )
A.X的化学式是H2O
B.反应中只有氯元素的化合价发生了变化
C.生产中要对排放的废气和尾气进行处理
D.实验室称量次氯酸钠固体配制消毒液时要垫一张纸
4.某化学实验小组在完成实验室制取二氧化碳的实验后,过滤得100g混合溶液,已知其中H+和Ca2+的个数比为1:1,向其中加入20g碳酸钠样品(杂质既不溶于水也不与其他物质反应),恰好完全反应后过滤,得到14.1g滤渣,求所加碳酸钠样品的纯度为(
)
A.26.5%
B.53%
C.79.5%
D.84.8%
5.一定量甲烷(化学式:CH4)在氧气中不完全燃烧,生成一氧化碳、二氧化碳和水的分子个数之比可能为
A.1:1:2
B.2:1:4
C.2:3:6
D.3:1:8
6.烟花爆竹中的发色剂Cu(NO3)2在燃放时产生绿色火焰,发生如下反应:,则X的化学式为
( )
A.NO
B.NO2
C.N2O5
D.N2O
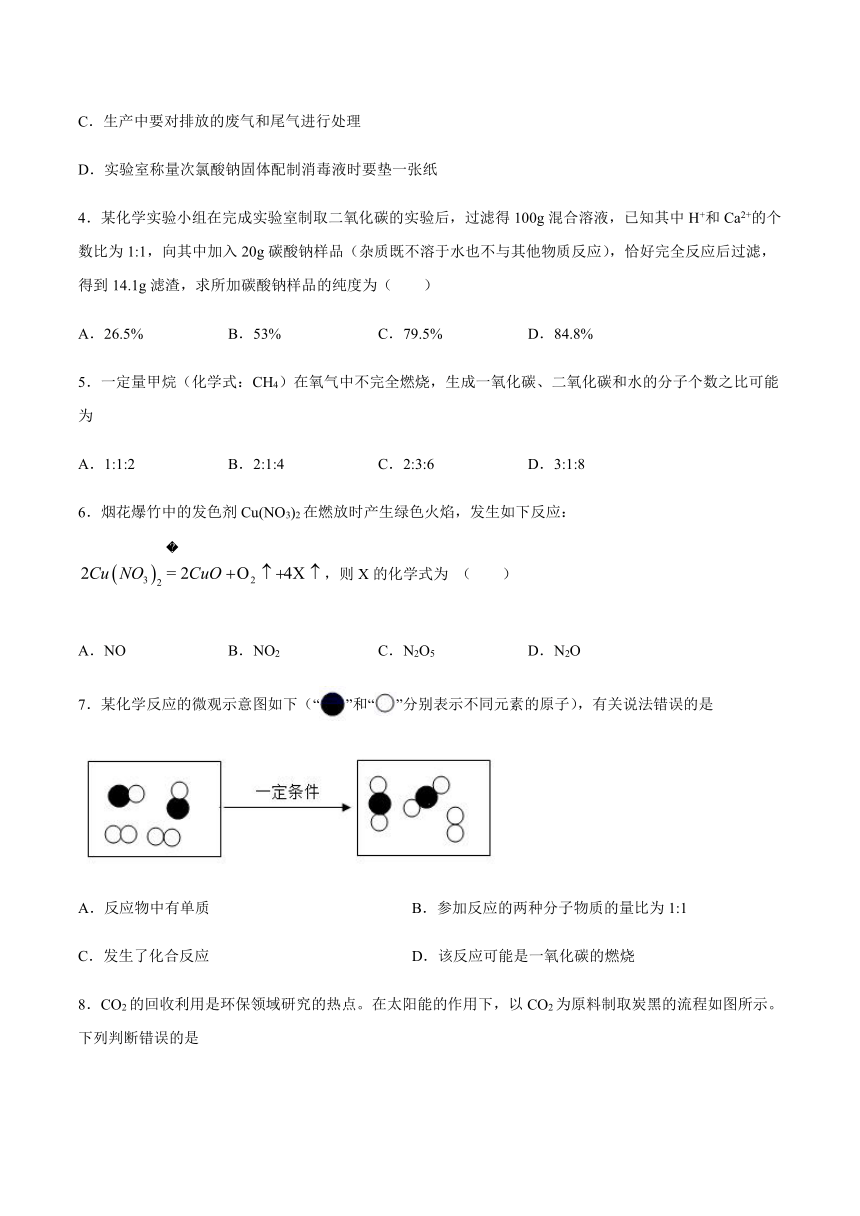
7.某化学反应的微观示意图如下(“”和“”分别表示不同元素的原子),有关说法错误的是
A.反应物中有单质
B.参加反应的两种分子物质的量比为1:1
C.发生了化合反应
D.该反应可能是一氧化碳的燃烧
8.CO2的回收利用是环保领域研究的热点。在太阳能的作用下,以CO2为原料制取炭黑的流程如图所示。下列判断错误的是
A.CO2和FeO在427°
C发生反应生成C和Fe3O4
B.Fe3O4在太阳能等的作用下分解生成FeO和O2
C.FeO在反应过程中可以循环使用
D.该总反应的化学方程式为CO2=C+O2
9.碳酸钙和氧化钙组成的混合物中钙元素的质量分数为50%,将30g该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是( )
A.15g
B.13.2g
C.9g
D.6.6g
10.我国成功发射的“嫦娥三号”使用长三丙运载火箭其中火箭燃料用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,当两者完全反应生成三种新物质,反应的化学方程式为C2H8N2+2N2O43X+2CO2+4H2O,下列有关说法错误的是( )
A.反应前后氮元素的化合价没有发生变化
B.X的化学式为N2
C.N2O4属于氧化物,在反应中做助燃剂
D.该反应属于放热反应
11.下列叙述、对应的化学方程式及基本反应类型都正确的是
A.小苏打用于治疗胃酸过多
复分解反应
B.溶洞的形成
化合反应
C.正常雨水的pH约为5.6的原因
化合反应
D.证明铜的活动性比银强
置换反应
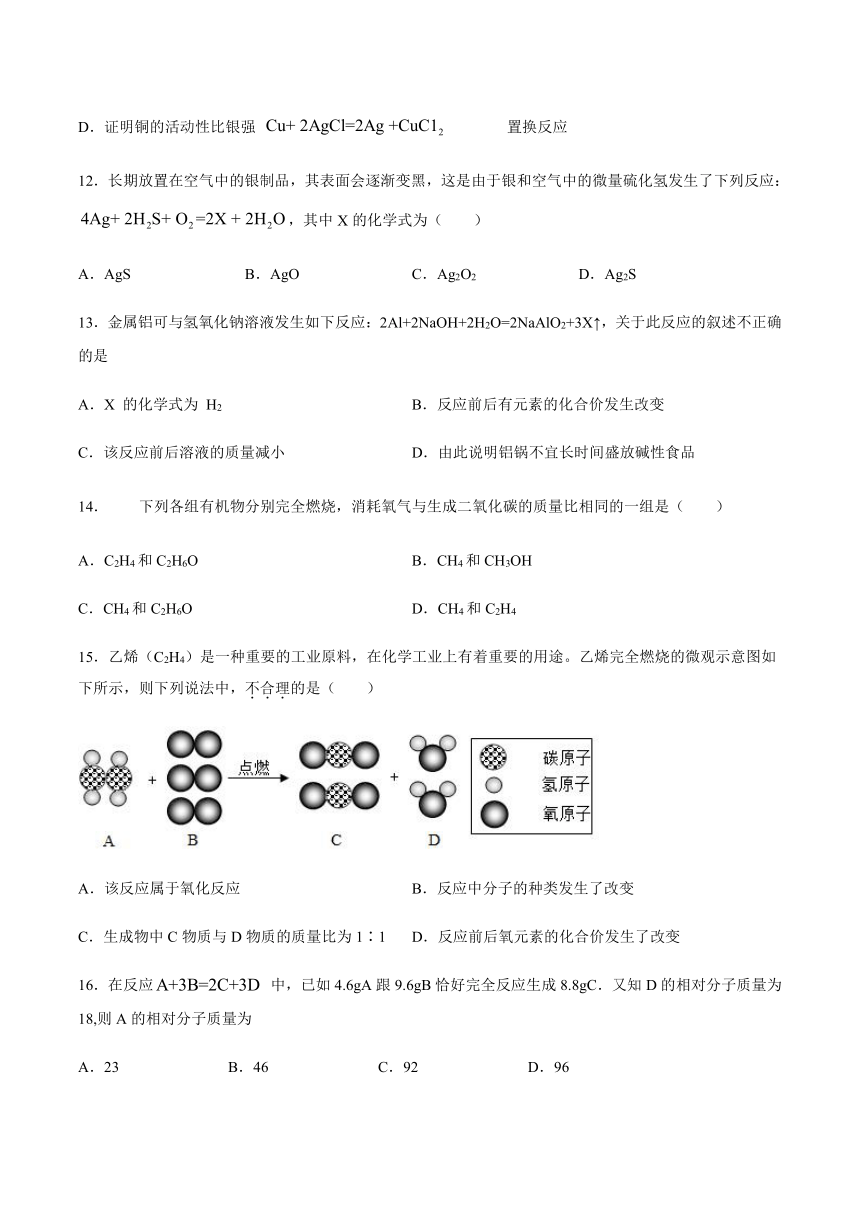
12.长期放置在空气中的银制品,其表面会逐渐变黑,这是由于银和空气中的微量硫化氢发生了下列反应:,其中X的化学式为( )
A.AgS
B.AgO
C.Ag2O2
D.Ag2S
13.金属铝可与氢氧化钠溶液发生如下反应:2Al+2NaOH+2H2O=2NaAlO2+3X↑,关于此反应的叙述不正确的是
A.X
的化学式为
H2
B.反应前后有元素的化合价发生改变
C.该反应前后溶液的质量减小
D.由此说明铝锅不宜长时间盛放碱性食品
14.下列各组有机物分别完全燃烧,消耗氧气与生成二氧化碳的质量比相同的一组是( )
A.C2H4和C2H6O
B.CH4和CH3OH
C.CH4和C2H6O
D.CH4和C2H4
15.乙烯(C2H4)是一种重要的工业原料,在化学工业上有着重要的用途。乙烯完全燃烧的微观示意图如下所示,则下列说法中,不合理的是( )
A.该反应属于氧化反应
B.反应中分子的种类发生了改变
C.生成物中C物质与D物质的质量比为1∶1
D.反应前后氧元素的化合价发生了改变
16.在反应
中,已如4.6gA跟9.6gB恰好完全反应生成8.8gC.又知D的相对分子质量为18,则A的相对分子质量为
A.23
B.46
C.92
D.96
17.某有机物在氧气中燃烧只生成二氧化碳、
一氧化碳和水。据此判断该有机物组成说法正确的是(
)
A.只含有碳、氢元素
B.含有碳、氢、氧三种元素
C.含有碳、氢元素,可能含有氧元素
D.无法确定
18.将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:下列有关说法正确的是( )
物质
a
b
c
d
反应前的质量/g
6.4
14.0
3.2
1.0
反应一段时间后的质量/g
10.0
7.2
x
1.0
A.a和b是反应物
B.x=3.2
C.该反应属于分解反应
D.d一定是催化剂
二、填空题
19.写出下列变化的化学反应方程式。
(1)用氯酸钾制取氧气_______。
(2)铁丝在氧气中燃烧_______。
(3)木炭在空气中燃烧_______。
(4)硫磺在空气中燃烧_______。
(5)镁在空气中燃烧_______。
20.工业上使用一种国产低温催化剂生产氢气的反应过程如图所示。
(1)该微观反应过程中出现了____________种氧化物;
(2)该化学反应前后不发生变化的是_____________(填“离子”、“分子”或“原子”);
(3)参加反应的与分子个数之比为______________;
(4)该反应的化学方程式为_______________________。
三、综合应用题
21.
(一)实验室采用高锰酸钾制取氧气。
(1)写出制取氧气的化学方程式________;
(2)如图所示,发生装置应选用________(填编号,下同),C、D、E三种收集氧气的方法中,不能采用的是_______。
(3)为测定高锰酸钾分解生成氧气的体积,应选用如图装置__________(填编号)。
(4)实验结束后剩余的固体是________(填“纯净物”或“混合物”)。
(二)称取一定质量的铜,放入足量稀硝酸(HNO3)中,反应的化学方程式为:(R表示产生气体的化学式),用排水法收集产生的气体R,生成气体R的质量与反应时间的关系如图所示,请回答下列问题:
(1)气体R的化学式是________,t1时生成气体R的质量是_____g。
(2)称取铜的质量是多少?_______
22.石灰石是主要矿产品之一,某学校研究性学习小组为了测量当地矿石山石灰石中CaCO3的质量分数,取一些矿石样品,并取稀盐酸200g,平均分成4份,分4次进行实验,结果如下:
实验
1
2
3
4
加样品的质量(g)
5
10
15
20
生成CO2的质量(g)
1.76
3.52
4.4
m
问:(1)哪几次实验中矿石有剩余?
(2)表中m的数值是_____。
(3)试计算这种石灰石中CaCO3的质量分数。
(4)试计算这种稀盐酸溶质的质量分数。
参考答案
1.C2.C3.D4.C5.D6.B7.B8.D9.C10.A11.C12.D13.C14.A15.C16.B17.C18.C
19.
20.3
原子
1:1
21.
A
E
丙
混合物
NO
4.8
19.2g
22.(1)第3和第4;(2)4.4;(3)80%;(4)29.2%
一、单选题
1.下列化学方程式书写正确的是(?
?
?)
A.
B.
C.
D.
2.下列描述与化学方程式表示一致的是(
)
A.碳在空气中充分燃烧
B.铁丝在纯氧气中燃烧
C.红磷在空气中充分燃烧
D.镁带燃烧
3.在抗击新冠肺炎的阻击战中消毒液一度紧缺,次氯酸钠(白色固体,具有腐蚀性,易分解产生有害气体)就是其中一种,相关企业加紧生产,生产次氯酸钠的一个反应的化学方程式是。以下有关说法不正确的是( )
A.X的化学式是H2O
B.反应中只有氯元素的化合价发生了变化
C.生产中要对排放的废气和尾气进行处理
D.实验室称量次氯酸钠固体配制消毒液时要垫一张纸
4.某化学实验小组在完成实验室制取二氧化碳的实验后,过滤得100g混合溶液,已知其中H+和Ca2+的个数比为1:1,向其中加入20g碳酸钠样品(杂质既不溶于水也不与其他物质反应),恰好完全反应后过滤,得到14.1g滤渣,求所加碳酸钠样品的纯度为(
)
A.26.5%
B.53%
C.79.5%
D.84.8%
5.一定量甲烷(化学式:CH4)在氧气中不完全燃烧,生成一氧化碳、二氧化碳和水的分子个数之比可能为
A.1:1:2
B.2:1:4
C.2:3:6
D.3:1:8
6.烟花爆竹中的发色剂Cu(NO3)2在燃放时产生绿色火焰,发生如下反应:,则X的化学式为
( )
A.NO
B.NO2
C.N2O5
D.N2O
7.某化学反应的微观示意图如下(“”和“”分别表示不同元素的原子),有关说法错误的是
A.反应物中有单质
B.参加反应的两种分子物质的量比为1:1
C.发生了化合反应
D.该反应可能是一氧化碳的燃烧
8.CO2的回收利用是环保领域研究的热点。在太阳能的作用下,以CO2为原料制取炭黑的流程如图所示。下列判断错误的是
A.CO2和FeO在427°
C发生反应生成C和Fe3O4
B.Fe3O4在太阳能等的作用下分解生成FeO和O2
C.FeO在反应过程中可以循环使用
D.该总反应的化学方程式为CO2=C+O2
9.碳酸钙和氧化钙组成的混合物中钙元素的质量分数为50%,将30g该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是( )
A.15g
B.13.2g
C.9g
D.6.6g
10.我国成功发射的“嫦娥三号”使用长三丙运载火箭其中火箭燃料用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,当两者完全反应生成三种新物质,反应的化学方程式为C2H8N2+2N2O43X+2CO2+4H2O,下列有关说法错误的是( )
A.反应前后氮元素的化合价没有发生变化
B.X的化学式为N2
C.N2O4属于氧化物,在反应中做助燃剂
D.该反应属于放热反应
11.下列叙述、对应的化学方程式及基本反应类型都正确的是
A.小苏打用于治疗胃酸过多
复分解反应
B.溶洞的形成
化合反应
C.正常雨水的pH约为5.6的原因
化合反应
D.证明铜的活动性比银强
置换反应
12.长期放置在空气中的银制品,其表面会逐渐变黑,这是由于银和空气中的微量硫化氢发生了下列反应:,其中X的化学式为( )
A.AgS
B.AgO
C.Ag2O2
D.Ag2S
13.金属铝可与氢氧化钠溶液发生如下反应:2Al+2NaOH+2H2O=2NaAlO2+3X↑,关于此反应的叙述不正确的是
A.X
的化学式为
H2
B.反应前后有元素的化合价发生改变
C.该反应前后溶液的质量减小
D.由此说明铝锅不宜长时间盛放碱性食品
14.下列各组有机物分别完全燃烧,消耗氧气与生成二氧化碳的质量比相同的一组是( )
A.C2H4和C2H6O
B.CH4和CH3OH
C.CH4和C2H6O
D.CH4和C2H4
15.乙烯(C2H4)是一种重要的工业原料,在化学工业上有着重要的用途。乙烯完全燃烧的微观示意图如下所示,则下列说法中,不合理的是( )
A.该反应属于氧化反应
B.反应中分子的种类发生了改变
C.生成物中C物质与D物质的质量比为1∶1
D.反应前后氧元素的化合价发生了改变
16.在反应
中,已如4.6gA跟9.6gB恰好完全反应生成8.8gC.又知D的相对分子质量为18,则A的相对分子质量为
A.23
B.46
C.92
D.96
17.某有机物在氧气中燃烧只生成二氧化碳、
一氧化碳和水。据此判断该有机物组成说法正确的是(
)
A.只含有碳、氢元素
B.含有碳、氢、氧三种元素
C.含有碳、氢元素,可能含有氧元素
D.无法确定
18.将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:下列有关说法正确的是( )
物质
a
b
c
d
反应前的质量/g
6.4
14.0
3.2
1.0
反应一段时间后的质量/g
10.0
7.2
x
1.0
A.a和b是反应物
B.x=3.2
C.该反应属于分解反应
D.d一定是催化剂
二、填空题
19.写出下列变化的化学反应方程式。
(1)用氯酸钾制取氧气_______。
(2)铁丝在氧气中燃烧_______。
(3)木炭在空气中燃烧_______。
(4)硫磺在空气中燃烧_______。
(5)镁在空气中燃烧_______。
20.工业上使用一种国产低温催化剂生产氢气的反应过程如图所示。
(1)该微观反应过程中出现了____________种氧化物;
(2)该化学反应前后不发生变化的是_____________(填“离子”、“分子”或“原子”);
(3)参加反应的与分子个数之比为______________;
(4)该反应的化学方程式为_______________________。
三、综合应用题
21.
(一)实验室采用高锰酸钾制取氧气。
(1)写出制取氧气的化学方程式________;
(2)如图所示,发生装置应选用________(填编号,下同),C、D、E三种收集氧气的方法中,不能采用的是_______。
(3)为测定高锰酸钾分解生成氧气的体积,应选用如图装置__________(填编号)。
(4)实验结束后剩余的固体是________(填“纯净物”或“混合物”)。
(二)称取一定质量的铜,放入足量稀硝酸(HNO3)中,反应的化学方程式为:(R表示产生气体的化学式),用排水法收集产生的气体R,生成气体R的质量与反应时间的关系如图所示,请回答下列问题:
(1)气体R的化学式是________,t1时生成气体R的质量是_____g。
(2)称取铜的质量是多少?_______
22.石灰石是主要矿产品之一,某学校研究性学习小组为了测量当地矿石山石灰石中CaCO3的质量分数,取一些矿石样品,并取稀盐酸200g,平均分成4份,分4次进行实验,结果如下:
实验
1
2
3
4
加样品的质量(g)
5
10
15
20
生成CO2的质量(g)
1.76
3.52
4.4
m
问:(1)哪几次实验中矿石有剩余?
(2)表中m的数值是_____。
(3)试计算这种石灰石中CaCO3的质量分数。
(4)试计算这种稀盐酸溶质的质量分数。
参考答案
1.C2.C3.D4.C5.D6.B7.B8.D9.C10.A11.C12.D13.C14.A15.C16.B17.C18.C
19.
20.3
原子
1:1
21.
A
E
丙
混合物
NO
4.8
19.2g
22.(1)第3和第4;(2)4.4;(3)80%;(4)29.2%
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
