高中化学新教材同步必修第二册 实验活动6 化学能转化成电能
文档属性
| 名称 | 高中化学新教材同步必修第二册 实验活动6 化学能转化成电能 |

|
|
| 格式 | pptx | ||
| 文件大小 | 353.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-01-29 00:00:00 | ||
图片预览




文档简介
实验活动6 化学能转化成电能
第六章 第二节 化学反应的速率与限度
实验目的
1.理解氧化还原反应在化学能转化成电能过程中的作用,体会化学的价值。
2.认识原电池的构成要素及其作用。
实验用品
烧杯、导线、电流表。
锌片、铜片、石墨棒、稀硫酸。
实验步骤
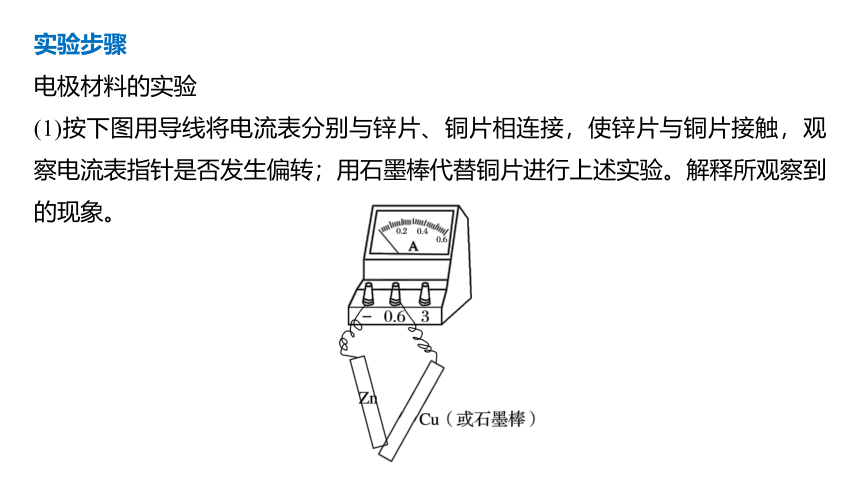
电极材料的实验
(1)按下图用导线将电流表分别与锌片、铜片相连接,使锌片与铜片接触,观察电流表指针是否发生偏转;用石墨棒代替铜片进行上述实验。解释所观察到的现象。
电极材料
电流表指针是
否发生偏转
解释
锌片、铜片
否
没有电解质溶液,不能发生原电池反应
锌片、石墨棒
否
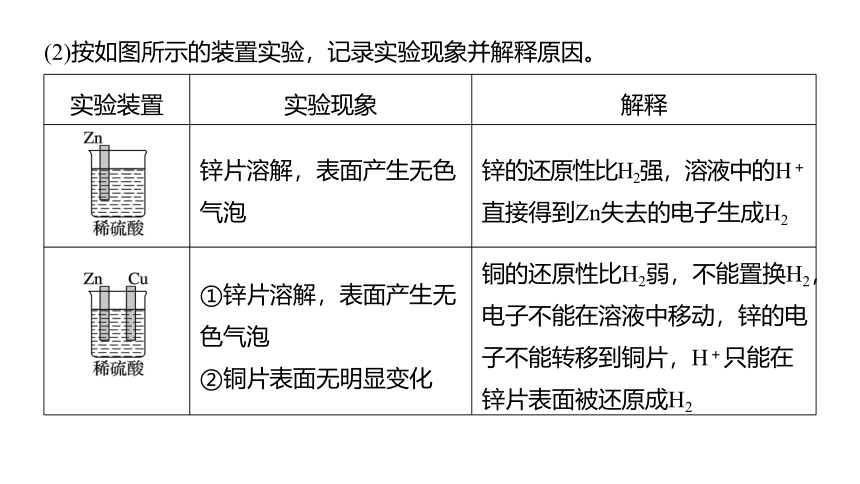
(2)按如图所示的装置实验,记录实验现象并解释原因。
实验装置
实验现象
解释
锌片溶解,表面产生无色气泡
锌的还原性比H2强,溶液中的H+直接得到Zn失去的电子生成H2
①锌片溶解,表面产生无色气泡
②铜片表面无明显变化
铜的还原性比H2弱,不能置换H2,电子不能在溶液中移动,锌的电子不能转移到铜片,H+只能在锌片表面被还原成H2
①锌片溶解,表面产生无色气泡
②石墨棒表面无明显变化
石墨为惰性材料,不能置换H2,电子不能通过溶液转移到石墨棒,H+只能在锌片表面被还原成H2
(3)按如图所示的装置实验,记录实验现象并解释原因。
实验材料
实验现象
解释
Zn、Cu、H2SO4
①锌片溶解
②铜片不溶解,表面产生无色气泡
③电流表指针偏转
锌失去的电子通过导线转移至铜片表面产生电流,溶液中的H+在铜片表面获得Zn失去的电子生成H2
Zn、石墨、H2SO4
①锌片溶解
②石墨棒表面产生无色气泡
③电流表指针偏转
锌失去的电子通过导线转移至石墨棒表面产生电流,溶液中的H+在石墨棒表面获得Zn失去的电子生成H2
Cu、石墨、H2SO4
铜片不溶解,电流表指针不偏转
铜的还原性比H2弱,不能发生氧化还原反应,没有电子转移,因而不能产生电流
问题讨论
(1)发生原电池反应的要素有哪些?
化学反应: 。
装置条件:① ,② ,③ 。
(2)写出实验(2)中Zn置换H2的离子方程式,并标出电子转移的方向和数目:
_______________________________________。
自发进行的氧化还原反应
活动性不同的电极
电解质溶液
形成闭合回路
(3)指出实验(3)锌铜原电池的电极名称,并写出电极反应和电池总反应。
负极: ;
正极: ;
电池反应: 。
(4)实验(3),若锌片、铜片接触,插入硫酸溶液,能否观察到电流? 。
(5)实验(3)中锌、石墨原电池中,锌片换成铁片,能否形成电流?若能产生电流,写出电极反应和电池反应。
提示 能产生电流。
负极:Fe-2e-===Fe2+
正极:2H++2e-===H2↑
电池反应:Fe+2H+===Fe2++H2↑
Zn-2e-===Zn2+,氧化反应
2H++2e-===H2↑,还原反应
Zn+2H+===Zn2++H2↑
不能
1.下列装置能发生原电池反应使电流表指针偏转的是____(填序号)。
跟踪强化
1
2
⑤
2.根据题目1中选出的原电池解答下列问题:
(1)负极是____,发生_____(填“氧化”或“还原”)反应。
该极的现象:_____________。
电极反应式:________________。
(2)正极是_____,电极反应式:______________________________________。
(3)溶液中的Fe3+移向___极。
(4)电池总反应式:_________________________。
1
2
Cu
氧化
铜片逐渐溶解
Cu-2e-===Cu2+
石墨
Fe3++e-===Fe2+(或2Fe3++2e-===2Fe2+)
正
Cu+2Fe3+===Cu2++2Fe2+
第六章 第二节 化学反应的速率与限度
实验目的
1.理解氧化还原反应在化学能转化成电能过程中的作用,体会化学的价值。
2.认识原电池的构成要素及其作用。
实验用品
烧杯、导线、电流表。
锌片、铜片、石墨棒、稀硫酸。
实验步骤
电极材料的实验
(1)按下图用导线将电流表分别与锌片、铜片相连接,使锌片与铜片接触,观察电流表指针是否发生偏转;用石墨棒代替铜片进行上述实验。解释所观察到的现象。
电极材料
电流表指针是
否发生偏转
解释
锌片、铜片
否
没有电解质溶液,不能发生原电池反应
锌片、石墨棒
否
(2)按如图所示的装置实验,记录实验现象并解释原因。
实验装置
实验现象
解释
锌片溶解,表面产生无色气泡
锌的还原性比H2强,溶液中的H+直接得到Zn失去的电子生成H2
①锌片溶解,表面产生无色气泡
②铜片表面无明显变化
铜的还原性比H2弱,不能置换H2,电子不能在溶液中移动,锌的电子不能转移到铜片,H+只能在锌片表面被还原成H2
①锌片溶解,表面产生无色气泡
②石墨棒表面无明显变化
石墨为惰性材料,不能置换H2,电子不能通过溶液转移到石墨棒,H+只能在锌片表面被还原成H2
(3)按如图所示的装置实验,记录实验现象并解释原因。
实验材料
实验现象
解释
Zn、Cu、H2SO4
①锌片溶解
②铜片不溶解,表面产生无色气泡
③电流表指针偏转
锌失去的电子通过导线转移至铜片表面产生电流,溶液中的H+在铜片表面获得Zn失去的电子生成H2
Zn、石墨、H2SO4
①锌片溶解
②石墨棒表面产生无色气泡
③电流表指针偏转
锌失去的电子通过导线转移至石墨棒表面产生电流,溶液中的H+在石墨棒表面获得Zn失去的电子生成H2
Cu、石墨、H2SO4
铜片不溶解,电流表指针不偏转
铜的还原性比H2弱,不能发生氧化还原反应,没有电子转移,因而不能产生电流
问题讨论
(1)发生原电池反应的要素有哪些?
化学反应: 。
装置条件:① ,② ,③ 。
(2)写出实验(2)中Zn置换H2的离子方程式,并标出电子转移的方向和数目:
_______________________________________。
自发进行的氧化还原反应
活动性不同的电极
电解质溶液
形成闭合回路
(3)指出实验(3)锌铜原电池的电极名称,并写出电极反应和电池总反应。
负极: ;
正极: ;
电池反应: 。
(4)实验(3),若锌片、铜片接触,插入硫酸溶液,能否观察到电流? 。
(5)实验(3)中锌、石墨原电池中,锌片换成铁片,能否形成电流?若能产生电流,写出电极反应和电池反应。
提示 能产生电流。
负极:Fe-2e-===Fe2+
正极:2H++2e-===H2↑
电池反应:Fe+2H+===Fe2++H2↑
Zn-2e-===Zn2+,氧化反应
2H++2e-===H2↑,还原反应
Zn+2H+===Zn2++H2↑
不能
1.下列装置能发生原电池反应使电流表指针偏转的是____(填序号)。
跟踪强化
1
2
⑤
2.根据题目1中选出的原电池解答下列问题:
(1)负极是____,发生_____(填“氧化”或“还原”)反应。
该极的现象:_____________。
电极反应式:________________。
(2)正极是_____,电极反应式:______________________________________。
(3)溶液中的Fe3+移向___极。
(4)电池总反应式:_________________________。
1
2
Cu
氧化
铜片逐渐溶解
Cu-2e-===Cu2+
石墨
Fe3++e-===Fe2+(或2Fe3++2e-===2Fe2+)
正
Cu+2Fe3+===Cu2++2Fe2+
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
