高中化学人教版(新课程标准)选修5有机化学基础第一章认识有机化合物章节检测
文档属性
| 名称 | 高中化学人教版(新课程标准)选修5有机化学基础第一章认识有机化合物章节检测 |

|
|
| 格式 | docx | ||
| 文件大小 | 267.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-01 00:00:00 | ||
图片预览



文档简介
高中化学人教版(新课程标准)选修5有机化学基础第一章认识有机化合物章节检测
一、单选题
1.在蒸发皿中加热蒸干下列物质的水溶液并灼烧(低于400℃),可以得到该物质固体的是(???
)
A.?氯化铝??????????????????????????????B.?碳酸氢钾??????????????????????????????C.?碳酸钠??????????????????????????????D.?亚硫酸钠
2.某有机物的结构简式如图所示,下列关于这种有机物的说法错误的有(??
)
①该物质的分子式为
???
②能使溴水、酸性
溶液褪色???
③分别与
、
反应,两个反应中反应物的物质的量之比均是1∶1???
④能发生取代、加成、水解、氧化反应
A.?1种???????????????????????????????????????B.?2种???????????????????????????????????????C.?3种???????????????????????????????????????D.?4种
3.下列物质在给定条件下的同分异构体数目正确的是(???
)。
A.?的一溴代物有5种
B.?分子组成是
属于羧酸的同分异构体有5种
C.?分子组成是
属于醛的同分异构体有3种D.?
属于烷烃的同分异构体有3种
4.用下列实验装置进行有关实验,能达到实验目的是(??
)
A.?实验室用装置制取并收集乙烯气体
B.?用装置从下口放出分液后上层的有机相
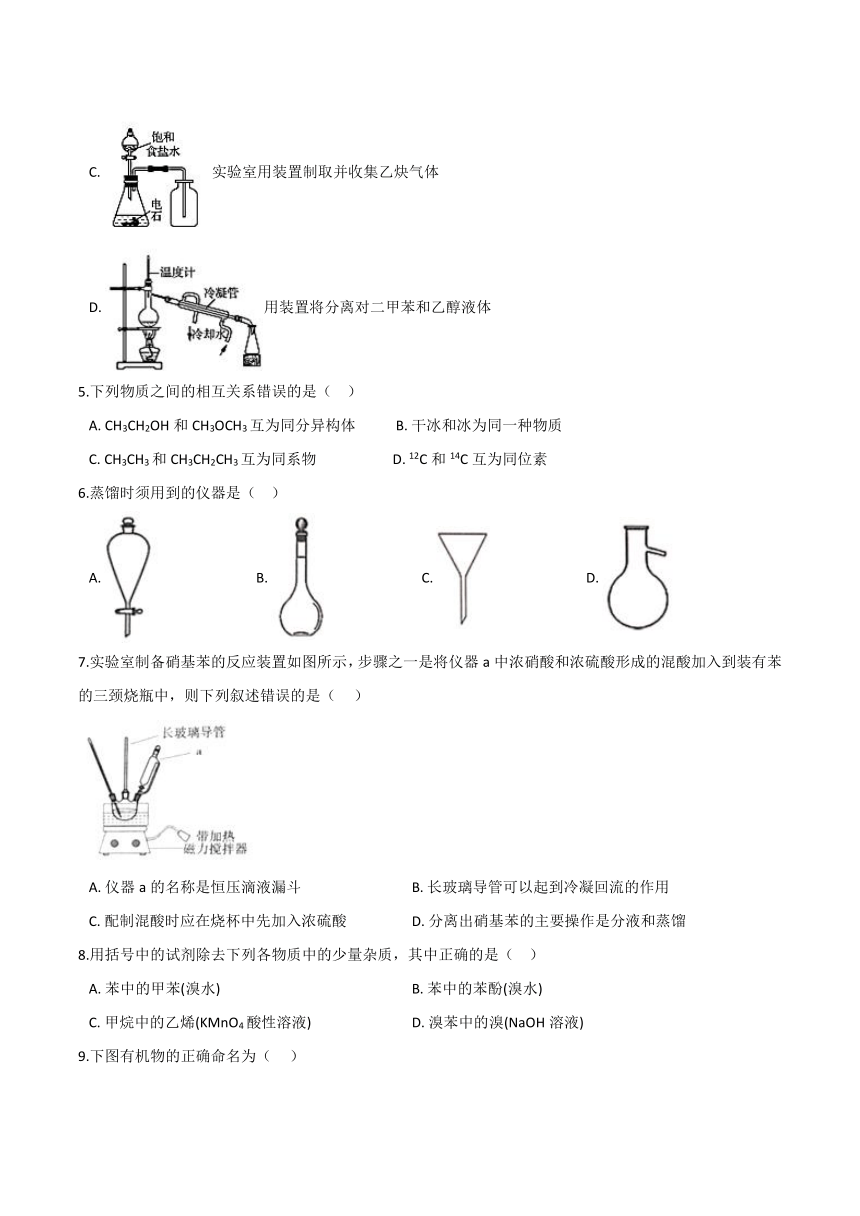
C.?实验室用装置制取并收集乙炔气体
D.?用装置将分离对二甲苯和乙醇液体
5.下列物质之间的相互关系错误的是(??
)
A.?CH3CH2OH和CH3OCH3互为同分异构体???????????B.?干冰和冰为同一种物质
C.?CH3CH3和CH3CH2CH3互为同系物?????????
???????????D.?12C和14C互为同位素
6.蒸馏时须用到的仪器是(
??)
A.????????????????????????????B.????????????????????????????C.????????????????????????????D.?
7.实验室制备硝基苯的反应装置如图所示,步骤之一是将仪器a中浓硝酸和浓硫酸形成的混酸加入到装有苯的三颈烧瓶中,则下列叙述错误的是(???
)
A.?仪器a的名称是恒压滴液漏斗
B.?长玻璃导管可以起到冷凝回流的作用
C.?配制混酸时应在烧杯中先加入浓硫酸
D.?分离出硝基苯的主要操作是分液和蒸馏
8.用括号中的试剂除去下列各物质中的少量杂质,其中正确的是(
??)
A.?苯中的甲苯(溴水)
B.?苯中的苯酚(溴水)
C.?甲烷中的乙烯(KMnO4酸性溶液)
D.?溴苯中的溴(NaOH溶液)
9.下图有机物的正确命名为(
???)
A.?2-乙基-3,3-二甲基戊烷????????????????????????????????????B.?3,3-二甲基-4-乙基戊烷
C.?3,3,4-三甲基己烷??????????????????????????????????????????D.?3,4,4-三甲基己烷
10.下列化合物在核磁共振氢谱中能出现两组峰,且峰面积之比为
1∶1
的是(
??)
A.?CH3COOCH3????????????????????B.?CH3OCH3????????????????????C.?CH3COOH????????????????????D.?HOCH2CH2OH
11.下列各组物质只用一种试剂(可加热)不能全部检验出来的是(???
)
A.?甲苯、氯仿、己烯、乙醇?????????????????????????????????
???B.?乙醇、乙醛、乙酸、甘油
C.?乙醇、环己烷、四氯化碳、苯?????????????????????????????D.?溴乙烷、苯、硝基苯、乙醇
12.实验室有如下仪器:烧杯、漏斗、锥形瓶、分液漏斗、石棉网、酒精灯、玻璃棒、蒸发皿、蒸馏烧瓶、球形冷凝管、牛角管。只用上述仪器(夹持仪器省略)不能完成的实验为(???
)
A.?从
溶液中得到
晶体????????????????????????B.?萃取碘水中的碘单质
C.?分离溴苯(沸点156℃)和苯(沸点80℃)????????D.?分离除过油污的铁屑与
溶液
13.下列物质中,碳碳间成键方式与其他不同的是(??
)
A.?CH3-CH3???????????????????????B.????????????????????????C.????????????????????????D.?
14.下列各对物质中属于同分异构体的是(
??)
A.?12C和14C???????????????????????????????????????????????????????????B.?O2和O3
C.?与
??????????????????????????????D.?与
15.下表为各物质中所含有的少量杂质以及除去这些杂质应选用的试剂或操作方法,正确的一组为(
??)
序号
物质
杂质
选用的试剂或操作方法
A
Al2(SO4)3溶液
MgSO4
加入过量烧碱后过滤,再用硫酸酸化滤液
B
FeCl3
CaCO3
溶解、过滤、蒸发结晶
C
CCl4
Br2
用NaOH溶液洗涤、分液
D
CO2
SO2
通过盛有品红溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶
A.?A??
?????????????????????????????????????????B.?B??
?????????????????????????????????????????C.?C??
?????????????????????????????????????????D.?D
二、填空题
16.有下列几组物质:
A?
H和
H????
B?
甲烷和己烷???
C?
正丁烷和异丁烷
D
和
?????
E.
和
其中,①属于同分异构体的是________;②属于同位素的是________;③属于同一种物质的是________;④属于同系物的是________。
17.下列是八种环状的烃类物质:
(1)互为同分异构体的有________和________、________和________(填写名称)。
(2)正四面体烷的二氯取代产物有________种;金刚烷的一氯取代产物有________种。
(3)化合物A的相对分子质量为86,所含碳的质量分数为55.8%,氢的质量分数为7.0%,其余为氧。
①A的分子式为________。
②A有多种同分异构体,写出五个同时满足下列条件的同分异构体的结构简式:
a.能发生水解反应b。能使溴的四氯化碳溶液褪色
________、________、________、________、________。
18.??????????????
(1)曲酸是一种非常有潜力的食品添加剂,经测定曲酸的分子式为C6H6O4
,
结构简式为
,其所含有的官能团有(写结构简式)________。
(2)多巴用于帕金森综合症的治疗,其结构简式为
。这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果。L多巴分子中所含的官能团的名称是________。
19.0.1
mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6
mol,则该烃的分子式为________。若该烃不能使溴水或高锰酸钾溶液褪色,但在一定条件下,可以和液溴发生取代反应,其一溴取代物只有一种,则此烃属于________烃,结构简式为________,名称是________。
若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2.2—二甲基丁烷,则此烃属于________烃,结构简式为________,名称是________。
20.在最新的家用汽车的调查中发现,新车中气体的质量不符合标准.汽车污染主要来源于汽车配件及材料.它们都会产生大量的有毒有机物气体.其中一种有毒气体的质谱图如下:
则由图可知该分子的相对分子质量是________,若该分子的核磁共振氢谱中有4个吸收峰则有机物的名称为________,其苯环上的一氯代物有________种。
三、实验探究题
21.已知某种治疗胃病药品的主要成分是铝碳酸镁片,化学式为AlaMgb(OH)mCO3·nH2O,假设药品中的其他成分受热不分解,不溶于水且不与稀硫酸反应。某研究性学习小组设计了如下实验探究铝碳酸镁片的组成。
(1)[实验一]
取m
g该药片,研成粉末放入硬质玻璃管中,加热,充分反应后测得装置C增重2.16
g,装置D增重0.44
g。
装置C和D中盛放的药品是C________,D________。
(2)实验开始前先通入一段时间空气,其目的是________,其操作方法是________。
当B处的酒精灯点燃后以及反应结束后一段时间内仍然再通入空气的目的是________。
(3)[实验二]另取mg该药片,加入100mL1mol·L-1的稀硫酸,充分反应后滤去不溶物,向滤液中逐渐加入1mol·L-1的NaOH溶液,产生沉淀的物质的量与加入NaOH溶液体积之间的关系如图所示:
根据以上所给数据求出x=________。
(4)通过计算确定铝碳酸镁的化学式为________。
(5)有医生建议患有严重胃溃疡的患者最好慎用该药,试用你所学的知识解释这样建议的理由是________。
(6)有同学认为不需要做实验一,只需要在实验二的基础上再得知两个数据就可以求出铝碳酸镁的化学式,你认为这两个数据应该是________。
22.亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示装置(夹持装置及尾气吸收装置已省略)和药品探究亚硝酸钠与硫酸反应的气体产物。
已知:气体的沸点
:
℃,
:21℃
(1)写出装置A中发生反应的化学方程式________。
(2)B装置中选择的水浴方式为________(填“冰水浴”或“热水浴”)。
(3)反应前应先打开弹簧夹,先通一段时间
,其目的是________。
(4)能够说明气体产物中有
的实验现象是________。
23.工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理:
①Al4C3与硫酸反应可生成CH4
②AlN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与过量NaOH溶液反应的化学方程式________。
(2)实验装置(如图所示,量气管为碱式滴定管改装)
连好装置后,首先应进行的操作是________。
(3)实验过程:称得装置D的初始质量为yg;称取xgAlN样品置于装置B锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管的初始读数为amL(量气装置左右液面相平)。
①欲首先测量Al4C3质量分数的有关数据,对三个活塞的操作是:
关闭活塞
________,打开活塞________
②若无恒压管,对所测气体体积的影响是________(填“偏大”“偏小”或“无影响”)
③量气管中液面不再发生变化,说明反应已经结束。读取读数之前,应对量气管进行的操作为,首先恢复至室温,然后________;若量气管中的液面高于A右侧干燥管中的液面,所测气体的体积________(填“偏大”“偏小”或“无影响”)。
④记录滴定管的读数为bmL(已知:该实验条件下的气体摩尔体积为VmL·mol-1),则Al4C3的质量分数为________(用含a、b、x、Vm的代数式表示)。
⑤测量AlN质量分数的数据:首先关闭活塞K1
,
打开活塞K3
,
通过分液漏斗加入________,与装置B瓶内物质充分反应;反应完成后,________(填入该步应进行的操作),最后称得装置D的质量为zg。则样品中AlN的质量分数为________(用含x、y、z、的代数式表示)。
参考答案
1
C
2
B
3
A
4
D
5
B
6
D
7
C
8
D
9
C
10
A
11
C
12
C
13
B
14
D
15
C
16
C、E;A;D;B
17
(1)苯;棱晶烷;环辛四烯;立方烷
(2)1;2
(3)C4H6O2;;;;;
18
(1)
(2)酚羟基、氨基、羧基
19C6H12;环烷烃;;环己烷;烯烃;(CH3)3C-CH=CH2;3,3-二甲基-1-丁烯
2092
;甲苯
;3
21
(1)无水CaCl2或P2O5;碱石灰或NaOH固体
(2)排除装置B中的CO2、H2O;关闭弹簧夹b,打开弹簧夹a;赶走固体分解产生的CO2、H2O,使其被充分吸收
(3)200
(4)Al2Mg6(OH)16CO3·4H2O
(5)因为胃酸和该药作用产生的CO2会刺激胃黏膜,导致胃穿孔
(6)产生CO2的物质的量;药片中主要成分的含量
22
(1)
(2)冰水浴
(3)将装置中的空气排出,防止对
的检验产生干扰
(4)通入
后,C装置的圆底烧瓶中出现红棕色气体
23
(1)AlN+NaOH+H2O=NaAlO2+NH3↑
(2)检查装置的气密性
(3)K2、K3;K1;偏大;调整量气管高度,使左右两边液面相平;偏小;;过量NaOH溶液;打开K2
,
通入一段时间空气;
一、单选题
1.在蒸发皿中加热蒸干下列物质的水溶液并灼烧(低于400℃),可以得到该物质固体的是(???
)
A.?氯化铝??????????????????????????????B.?碳酸氢钾??????????????????????????????C.?碳酸钠??????????????????????????????D.?亚硫酸钠
2.某有机物的结构简式如图所示,下列关于这种有机物的说法错误的有(??
)
①该物质的分子式为
???
②能使溴水、酸性
溶液褪色???
③分别与
、
反应,两个反应中反应物的物质的量之比均是1∶1???
④能发生取代、加成、水解、氧化反应
A.?1种???????????????????????????????????????B.?2种???????????????????????????????????????C.?3种???????????????????????????????????????D.?4种
3.下列物质在给定条件下的同分异构体数目正确的是(???
)。
A.?的一溴代物有5种
B.?分子组成是
属于羧酸的同分异构体有5种
C.?分子组成是
属于醛的同分异构体有3种D.?
属于烷烃的同分异构体有3种
4.用下列实验装置进行有关实验,能达到实验目的是(??
)
A.?实验室用装置制取并收集乙烯气体
B.?用装置从下口放出分液后上层的有机相
C.?实验室用装置制取并收集乙炔气体
D.?用装置将分离对二甲苯和乙醇液体
5.下列物质之间的相互关系错误的是(??
)
A.?CH3CH2OH和CH3OCH3互为同分异构体???????????B.?干冰和冰为同一种物质
C.?CH3CH3和CH3CH2CH3互为同系物?????????
???????????D.?12C和14C互为同位素
6.蒸馏时须用到的仪器是(
??)
A.????????????????????????????B.????????????????????????????C.????????????????????????????D.?
7.实验室制备硝基苯的反应装置如图所示,步骤之一是将仪器a中浓硝酸和浓硫酸形成的混酸加入到装有苯的三颈烧瓶中,则下列叙述错误的是(???
)
A.?仪器a的名称是恒压滴液漏斗
B.?长玻璃导管可以起到冷凝回流的作用
C.?配制混酸时应在烧杯中先加入浓硫酸
D.?分离出硝基苯的主要操作是分液和蒸馏
8.用括号中的试剂除去下列各物质中的少量杂质,其中正确的是(
??)
A.?苯中的甲苯(溴水)
B.?苯中的苯酚(溴水)
C.?甲烷中的乙烯(KMnO4酸性溶液)
D.?溴苯中的溴(NaOH溶液)
9.下图有机物的正确命名为(
???)
A.?2-乙基-3,3-二甲基戊烷????????????????????????????????????B.?3,3-二甲基-4-乙基戊烷
C.?3,3,4-三甲基己烷??????????????????????????????????????????D.?3,4,4-三甲基己烷
10.下列化合物在核磁共振氢谱中能出现两组峰,且峰面积之比为
1∶1
的是(
??)
A.?CH3COOCH3????????????????????B.?CH3OCH3????????????????????C.?CH3COOH????????????????????D.?HOCH2CH2OH
11.下列各组物质只用一种试剂(可加热)不能全部检验出来的是(???
)
A.?甲苯、氯仿、己烯、乙醇?????????????????????????????????
???B.?乙醇、乙醛、乙酸、甘油
C.?乙醇、环己烷、四氯化碳、苯?????????????????????????????D.?溴乙烷、苯、硝基苯、乙醇
12.实验室有如下仪器:烧杯、漏斗、锥形瓶、分液漏斗、石棉网、酒精灯、玻璃棒、蒸发皿、蒸馏烧瓶、球形冷凝管、牛角管。只用上述仪器(夹持仪器省略)不能完成的实验为(???
)
A.?从
溶液中得到
晶体????????????????????????B.?萃取碘水中的碘单质
C.?分离溴苯(沸点156℃)和苯(沸点80℃)????????D.?分离除过油污的铁屑与
溶液
13.下列物质中,碳碳间成键方式与其他不同的是(??
)
A.?CH3-CH3???????????????????????B.????????????????????????C.????????????????????????D.?
14.下列各对物质中属于同分异构体的是(
??)
A.?12C和14C???????????????????????????????????????????????????????????B.?O2和O3
C.?与
??????????????????????????????D.?与
15.下表为各物质中所含有的少量杂质以及除去这些杂质应选用的试剂或操作方法,正确的一组为(
??)
序号
物质
杂质
选用的试剂或操作方法
A
Al2(SO4)3溶液
MgSO4
加入过量烧碱后过滤,再用硫酸酸化滤液
B
FeCl3
CaCO3
溶解、过滤、蒸发结晶
C
CCl4
Br2
用NaOH溶液洗涤、分液
D
CO2
SO2
通过盛有品红溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶
A.?A??
?????????????????????????????????????????B.?B??
?????????????????????????????????????????C.?C??
?????????????????????????????????????????D.?D
二、填空题
16.有下列几组物质:
A?
H和
H????
B?
甲烷和己烷???
C?
正丁烷和异丁烷
D
和
?????
E.
和
其中,①属于同分异构体的是________;②属于同位素的是________;③属于同一种物质的是________;④属于同系物的是________。
17.下列是八种环状的烃类物质:
(1)互为同分异构体的有________和________、________和________(填写名称)。
(2)正四面体烷的二氯取代产物有________种;金刚烷的一氯取代产物有________种。
(3)化合物A的相对分子质量为86,所含碳的质量分数为55.8%,氢的质量分数为7.0%,其余为氧。
①A的分子式为________。
②A有多种同分异构体,写出五个同时满足下列条件的同分异构体的结构简式:
a.能发生水解反应b。能使溴的四氯化碳溶液褪色
________、________、________、________、________。
18.??????????????
(1)曲酸是一种非常有潜力的食品添加剂,经测定曲酸的分子式为C6H6O4
,
结构简式为
,其所含有的官能团有(写结构简式)________。
(2)多巴用于帕金森综合症的治疗,其结构简式为
。这种药物的研制是基于获得2000年诺贝尔生理学和医学奖的研究成果。L多巴分子中所含的官能团的名称是________。
19.0.1
mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6
mol,则该烃的分子式为________。若该烃不能使溴水或高锰酸钾溶液褪色,但在一定条件下,可以和液溴发生取代反应,其一溴取代物只有一种,则此烃属于________烃,结构简式为________,名称是________。
若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2.2—二甲基丁烷,则此烃属于________烃,结构简式为________,名称是________。
20.在最新的家用汽车的调查中发现,新车中气体的质量不符合标准.汽车污染主要来源于汽车配件及材料.它们都会产生大量的有毒有机物气体.其中一种有毒气体的质谱图如下:
则由图可知该分子的相对分子质量是________,若该分子的核磁共振氢谱中有4个吸收峰则有机物的名称为________,其苯环上的一氯代物有________种。
三、实验探究题
21.已知某种治疗胃病药品的主要成分是铝碳酸镁片,化学式为AlaMgb(OH)mCO3·nH2O,假设药品中的其他成分受热不分解,不溶于水且不与稀硫酸反应。某研究性学习小组设计了如下实验探究铝碳酸镁片的组成。
(1)[实验一]
取m
g该药片,研成粉末放入硬质玻璃管中,加热,充分反应后测得装置C增重2.16
g,装置D增重0.44
g。
装置C和D中盛放的药品是C________,D________。
(2)实验开始前先通入一段时间空气,其目的是________,其操作方法是________。
当B处的酒精灯点燃后以及反应结束后一段时间内仍然再通入空气的目的是________。
(3)[实验二]另取mg该药片,加入100mL1mol·L-1的稀硫酸,充分反应后滤去不溶物,向滤液中逐渐加入1mol·L-1的NaOH溶液,产生沉淀的物质的量与加入NaOH溶液体积之间的关系如图所示:
根据以上所给数据求出x=________。
(4)通过计算确定铝碳酸镁的化学式为________。
(5)有医生建议患有严重胃溃疡的患者最好慎用该药,试用你所学的知识解释这样建议的理由是________。
(6)有同学认为不需要做实验一,只需要在实验二的基础上再得知两个数据就可以求出铝碳酸镁的化学式,你认为这两个数据应该是________。
22.亚硝酸钠是一种工业盐,在生产、生活中应用广泛。现用下图所示装置(夹持装置及尾气吸收装置已省略)和药品探究亚硝酸钠与硫酸反应的气体产物。
已知:气体的沸点
:
℃,
:21℃
(1)写出装置A中发生反应的化学方程式________。
(2)B装置中选择的水浴方式为________(填“冰水浴”或“热水浴”)。
(3)反应前应先打开弹簧夹,先通一段时间
,其目的是________。
(4)能够说明气体产物中有
的实验现象是________。
23.工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理:
①Al4C3与硫酸反应可生成CH4
②AlN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与过量NaOH溶液反应的化学方程式________。
(2)实验装置(如图所示,量气管为碱式滴定管改装)
连好装置后,首先应进行的操作是________。
(3)实验过程:称得装置D的初始质量为yg;称取xgAlN样品置于装置B锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管的初始读数为amL(量气装置左右液面相平)。
①欲首先测量Al4C3质量分数的有关数据,对三个活塞的操作是:
关闭活塞
________,打开活塞________
②若无恒压管,对所测气体体积的影响是________(填“偏大”“偏小”或“无影响”)
③量气管中液面不再发生变化,说明反应已经结束。读取读数之前,应对量气管进行的操作为,首先恢复至室温,然后________;若量气管中的液面高于A右侧干燥管中的液面,所测气体的体积________(填“偏大”“偏小”或“无影响”)。
④记录滴定管的读数为bmL(已知:该实验条件下的气体摩尔体积为VmL·mol-1),则Al4C3的质量分数为________(用含a、b、x、Vm的代数式表示)。
⑤测量AlN质量分数的数据:首先关闭活塞K1
,
打开活塞K3
,
通过分液漏斗加入________,与装置B瓶内物质充分反应;反应完成后,________(填入该步应进行的操作),最后称得装置D的质量为zg。则样品中AlN的质量分数为________(用含x、y、z、的代数式表示)。
参考答案
1
C
2
B
3
A
4
D
5
B
6
D
7
C
8
D
9
C
10
A
11
C
12
C
13
B
14
D
15
C
16
C、E;A;D;B
17
(1)苯;棱晶烷;环辛四烯;立方烷
(2)1;2
(3)C4H6O2;;;;;
18
(1)
(2)酚羟基、氨基、羧基
19C6H12;环烷烃;;环己烷;烯烃;(CH3)3C-CH=CH2;3,3-二甲基-1-丁烯
2092
;甲苯
;3
21
(1)无水CaCl2或P2O5;碱石灰或NaOH固体
(2)排除装置B中的CO2、H2O;关闭弹簧夹b,打开弹簧夹a;赶走固体分解产生的CO2、H2O,使其被充分吸收
(3)200
(4)Al2Mg6(OH)16CO3·4H2O
(5)因为胃酸和该药作用产生的CO2会刺激胃黏膜,导致胃穿孔
(6)产生CO2的物质的量;药片中主要成分的含量
22
(1)
(2)冰水浴
(3)将装置中的空气排出,防止对
的检验产生干扰
(4)通入
后,C装置的圆底烧瓶中出现红棕色气体
23
(1)AlN+NaOH+H2O=NaAlO2+NH3↑
(2)检查装置的气密性
(3)K2、K3;K1;偏大;调整量气管高度,使左右两边液面相平;偏小;;过量NaOH溶液;打开K2
,
通入一段时间空气;
