第三节性质活泼的氧气—氧气的制取
文档属性
| 名称 | 第三节性质活泼的氧气—氧气的制取 |
|
|
| 格式 | rar | ||
| 文件大小 | 148.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-12-12 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
根据大家对氧气的了解和日常生活经验,你已经知道哪些途径(或方法)可以获得氧气?
探究用过氧化氢溶液制取氧气的条件。
取A、B、C三支试管,完成下列实验。
1.向A试管中加入3~5mL过氧化氢溶液,将带火星的木条伸入试管口,观察到了什么现象?
2.向B试管中加入约1/3药匙二氧化锰粉末,然后加入3~5mL过氧化氢溶液,你看到了什么现象?将带火星的木条伸入试管口,你又观察到了什么现象?
3.向C试管中加入几块瓷片,然后加入3~5mL过氧化氢溶液,看有什么现象?将带火星的木条伸入试管口,观察到了什么现象?
请将你观察到的现象填写到实验报告里。
(1)不同的物质放入过氧化氢溶液中,放出氧气的快慢_____(不同/相同);
(2)比较上述三种方法,你认为最适合于实验室里制取氧气的方法是_______,你的理由是__________________________。
(3)此反应能否顺利进行的关键是_____。
凡能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂。
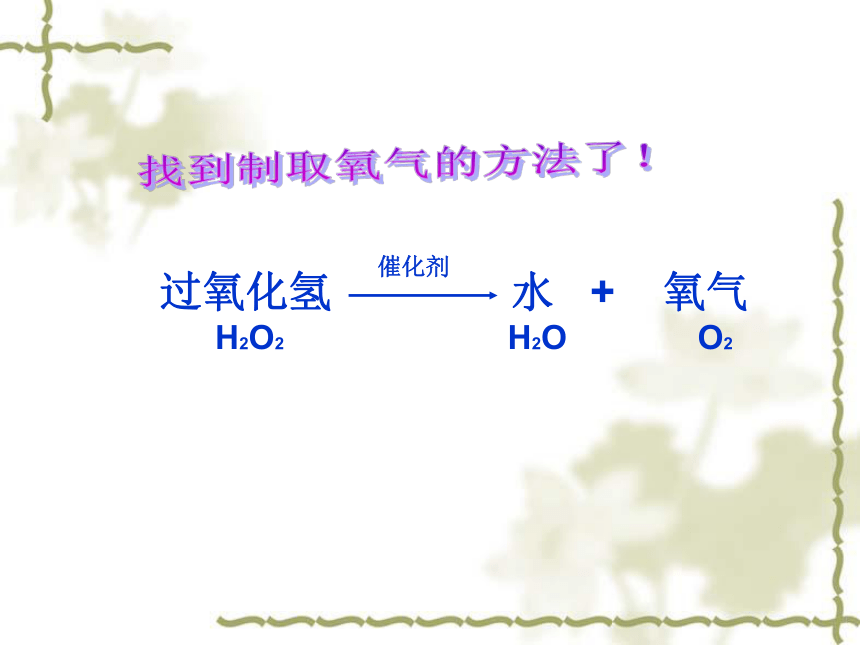
过氧化氢 水 + 氧气
H2O2 H2O O2
催化剂
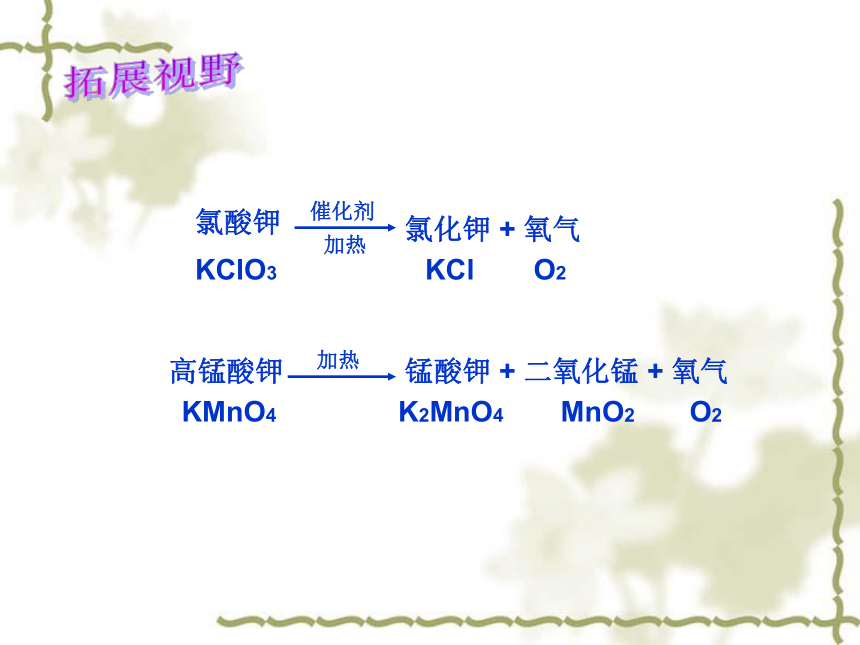
氯酸钾
氯化钾 + 氧气
加热
催化剂
KClO3
KCl
O2
高锰酸钾
锰酸钾 + 二氧化锰 + 氧气
加热
KMnO4
K2MnO4
MnO2
O2
为什么水、过氧化氢、氯酸钾、高锰酸钾等物质在一定条件下能发生化学反应产生氧气?
水 H2O
过氧化氢 H2O2
氯酸钾 KClO3
高锰酸钾 KMnO4
比较分析:
氯酸钾
氯化钾 + 氧气
加热
催化剂
KClO3
KCl
O2
高锰酸钾
锰酸钾 + 二氧化锰 + 氧气
加热
KMnO4
K2MnO4
MnO2
O2
过氧化氢 水 + 氧气 (常温)
H2O2 H2O O2
催化剂
利用化学反应制取少量氧气,反应物中必须含有氧元素,但并不是所有含氧元素的物质都可以用来制取氧气。
理想的选择:
1.反应物廉价易得;
2.生成物不污染环境;
3.反应所需条件在实验室容易实现,最好在常温常压下进行。
用过氧化氢溶液和二氧化锰制取氧气,你认为应该使用下列哪套装置?
固固加热制取气体
固液常温制取气体
可以用排水法收集氧气:
1.灌满水,盖上玻璃片(注意:不要有气泡);
2.倒放在水槽中,在水中将玻璃片移开;
3.当气泡连续均匀的冒出时,将导管伸入瓶口开始收集。
4.当气泡从集气瓶中往外冒时,证明已满。
根据实验报告上的步骤,制取并收集一瓶氧气。
温馨提示:
1.注意节约药品;
2.小组之间注意搞好分工合作;
3.当导管口刚刚有气泡时不要立即收集,等到气泡连续均匀地冒出时开始收集。(想一想,为什么?)
4.收集满后的集气瓶在水面以下盖上玻璃片取出,正放在桌面上。
用如图所示的方法(向上排空气法)再收集一瓶氧气。
温馨提示:1.玻璃片要始终盖在上面;
2.导管要伸到集气瓶底部。
实验过程中你遇到问题了吗?你是怎样解决的?
还有什么问题没有解决?
根据大家对氧气的了解和日常生活经验,你已经知道哪些途径(或方法)可以获得氧气?
探究用过氧化氢溶液制取氧气的条件。
取A、B、C三支试管,完成下列实验。
1.向A试管中加入3~5mL过氧化氢溶液,将带火星的木条伸入试管口,观察到了什么现象?
2.向B试管中加入约1/3药匙二氧化锰粉末,然后加入3~5mL过氧化氢溶液,你看到了什么现象?将带火星的木条伸入试管口,你又观察到了什么现象?
3.向C试管中加入几块瓷片,然后加入3~5mL过氧化氢溶液,看有什么现象?将带火星的木条伸入试管口,观察到了什么现象?
请将你观察到的现象填写到实验报告里。
(1)不同的物质放入过氧化氢溶液中,放出氧气的快慢_____(不同/相同);
(2)比较上述三种方法,你认为最适合于实验室里制取氧气的方法是_______,你的理由是__________________________。
(3)此反应能否顺利进行的关键是_____。
凡能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂。
过氧化氢 水 + 氧气
H2O2 H2O O2
催化剂
氯酸钾
氯化钾 + 氧气
加热
催化剂
KClO3
KCl
O2
高锰酸钾
锰酸钾 + 二氧化锰 + 氧气
加热
KMnO4
K2MnO4
MnO2
O2
为什么水、过氧化氢、氯酸钾、高锰酸钾等物质在一定条件下能发生化学反应产生氧气?
水 H2O
过氧化氢 H2O2
氯酸钾 KClO3
高锰酸钾 KMnO4
比较分析:
氯酸钾
氯化钾 + 氧气
加热
催化剂
KClO3
KCl
O2
高锰酸钾
锰酸钾 + 二氧化锰 + 氧气
加热
KMnO4
K2MnO4
MnO2
O2
过氧化氢 水 + 氧气 (常温)
H2O2 H2O O2
催化剂
利用化学反应制取少量氧气,反应物中必须含有氧元素,但并不是所有含氧元素的物质都可以用来制取氧气。
理想的选择:
1.反应物廉价易得;
2.生成物不污染环境;
3.反应所需条件在实验室容易实现,最好在常温常压下进行。
用过氧化氢溶液和二氧化锰制取氧气,你认为应该使用下列哪套装置?
固固加热制取气体
固液常温制取气体
可以用排水法收集氧气:
1.灌满水,盖上玻璃片(注意:不要有气泡);
2.倒放在水槽中,在水中将玻璃片移开;
3.当气泡连续均匀的冒出时,将导管伸入瓶口开始收集。
4.当气泡从集气瓶中往外冒时,证明已满。
根据实验报告上的步骤,制取并收集一瓶氧气。
温馨提示:
1.注意节约药品;
2.小组之间注意搞好分工合作;
3.当导管口刚刚有气泡时不要立即收集,等到气泡连续均匀地冒出时开始收集。(想一想,为什么?)
4.收集满后的集气瓶在水面以下盖上玻璃片取出,正放在桌面上。
用如图所示的方法(向上排空气法)再收集一瓶氧气。
温馨提示:1.玻璃片要始终盖在上面;
2.导管要伸到集气瓶底部。
实验过程中你遇到问题了吗?你是怎样解决的?
还有什么问题没有解决?
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
