苏教版(2019)必修第二册高中化学专题6化学反应与能量变化第二单元化学反应中的热同步练习
文档属性
| 名称 | 苏教版(2019)必修第二册高中化学专题6化学反应与能量变化第二单元化学反应中的热同步练习 |  | |
| 格式 | docx | ||
| 文件大小 | 310.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-03 07:47:21 | ||
图片预览




文档简介
苏教版(2019)必修第二册高中化学专题6化学反应与能量变化第二单元化学反应中的热同步练习
一、单选题
1.下列关于反应能量的说法正确的是(
)
A.若反应A=B
△H<0,说明A物质比B物质稳定,分子内共价键键能
A比B大
B.Zn(s)+CuSO4
(aq)==ZnSO4
(aq)
+Cu(s)
△H=
-216
kJ·mol-1。则反应物总能量>生成物总能量
C.101kPa时,2H2(g)+O2(g)==2H2O(g)
△H=
-Q
kJ·mol-1,则H2的燃烧热为1/2Q
kJ·mol-l
D.H+(aq)
+OH-
(aq)=H2O(l)
△H=
-57.3
kJ·mol-1,含1mol
NaOH的氢氧化钠溶液与含0.5mol
CH3COOH的醋酸溶液混合后会放出57.3
kJ的热量
2.已知下列两个热化学方程式:2H2(g)
+
O2(g)
=
2H2O(1)
ΔH=
-571.6
kJ?mol-1,C3H8(g)
+
5O2(g)=
3CO2(g)
+
4H2O(l)
ΔH=
-2220
kJ?mol-1,下列说法正确的是(
)
A.相同质量H2和C3H8分别完全燃烧,C3H8放出的热量多
B.C3H8
完全燃烧生成1mol
H2O(l)放出的热量为555
kJ
C.l
mol
H2和2
molC3H8
组成的混合气体完全燃烧放出的热量为5011.6
kJ
D.H2和C3H8的混合气体共4mol,完全燃烧时放出3256
kJ热量,则
n(H2):n(C3H8)=1:1
3.关于化学能与其他能量相互转化的说法正确的是(
)
A.图1所示的装置能将化学能转变为电能
B.图2所示的反应为吸热反应
C.化学反应中能量变化的主要原因是化学键的断裂与形成
D.中和反应中,反应物的总能量比生成物的总能量低
4.NF3是一种温室气体,其存储能量能力是
CO2的
12000~20000
倍,在大气中的寿命可长达
740年,如表所示是几种化学键断裂时所需要吸收的能量,下列说法中正确的是
化学键
N≡N
F—F
N—F
1mol
化学键断裂所需要吸收的能量
946kJ
154.8kJ
283
kJ
A.过程
N2
(g)→2N(g)放出能量
B.过程
N(g)+3F(g)→NF3(g)吸收能量
C.反应
N2(g)+3F2
(g)=2NF3(g)为放热反应
D.NF3中元素的化合价:N
为-3价,F
为+1
价
5.下列属于氧化还原反应且热量变化与如图一致的是
A.NH4NO3
晶体溶于水
B.钠和
H2O
反应
C.NH4Cl
晶体和氢氧化钡晶体的反应
D.CO2
和
C
反应
6.已知在1×105Pa,298
K条件下,1
g
H2燃烧生成液态水放出142.9
kJ的热量,表示该反应的热化学方程式正确的是(
)
A.2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6
kJ·mol-1
B.2H2(g)+O2(g)===2H2O(l)
ΔH=-142.9
kJ·mol-1
C.2H2+O2===2H2O
ΔH=-571.6
kJ·mol-1
D.H2(g)+1/2O2(g)===H2O(g)
ΔH=-285.8
kJ·mol-1
7.已知石墨在一定条件下转化成金刚石是吸热反应,由此可能出的正确结论是
A.石墨比金刚石更稳定
B.金刚石比石墨更稳定
C.石墨转化成金刚石是物理变化
D.石墨和金刚石的结构相同
8.下列变化过程吸收能量的是( )
A.H+H―→H2
B.H+Cl―→HCl
C.H2―→H+H
D.C+O2―→CO2
9.下列有关能量的说法不正确的是
( )
A.化石能源物质内部贮存着大量的能量
B.植物的光合作用使太阳能转化为化学能
C.燃料燃烧时只是将化学能转化为热能
D.由石墨制金刚石是吸热反应,故石墨能量比金刚石能量低
10.已知蒸发1mol
Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
H2(g)
Br2(g)
HBr(g)
1mol分子中的化学键断裂时需要吸收的能量(kJ)
436
a
369
则表中a为
A.404
B.260
C.230
D.200
11.下列反应既属于氧化还原反应,又是吸热反应的是(
)
A.灼热的炭与CO2的反应
B.Ba(OH)2·8H2O
与
NH4Cl
的反应
C.镁条与稀盐酸的反应
D.氢气在氧气中的燃烧反应
12.金刚石和石墨是碳元素的两种结构不同的单质(同素异形体),在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热能,据此,试判断在100kPa下,下列结论正确的是(
)
A.石墨比金刚石稳定
B.金刚石比石墨稳定
C.1mol石墨比1mol金刚石总能量高
D.金刚石转化为石墨是物理变化
13.在下列各说法中,正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1mol
H2SO4与1mol
Ba(OH)2反应放出的热叫做中和热
D.1mol
H2与0.5mol
O2反应放出的热就是H2的标准燃烧热
14.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是
A.1
mol
N2(g)和NA个O2(g)反应放出的能量为180
kJ
B.1
mol
N2(g)和1
mol
O2(g)具有总能量小于2
mol
NO(g)具有的总能量
C.通常情况下,N2(g)和O2(g)混合能直接生成NO(g)
D.吸热反应一定需要加热才能发生
15.一些烷烃的燃烧热(kJ/mol)如下表:
化合物
燃烧热
化合物
燃烧热
甲烷
891.0
正丁烷
2
878.0
乙烷
1
560.8
异丁烷
2
869.6
丙烷
2
221.5
2?甲基丁烷
3
531.3
下列表达正确的是( )
A.热稳定性:正丁烷>异丁烷
B.乙烷燃烧的热化学方程式为
2C2H6(g)+7O2(g)===4CO2(g)+6H2O(g)
ΔH=-1
560.8
kJ/mol
C.正戊烷的燃烧热大于3
531.3
kJ/mol
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
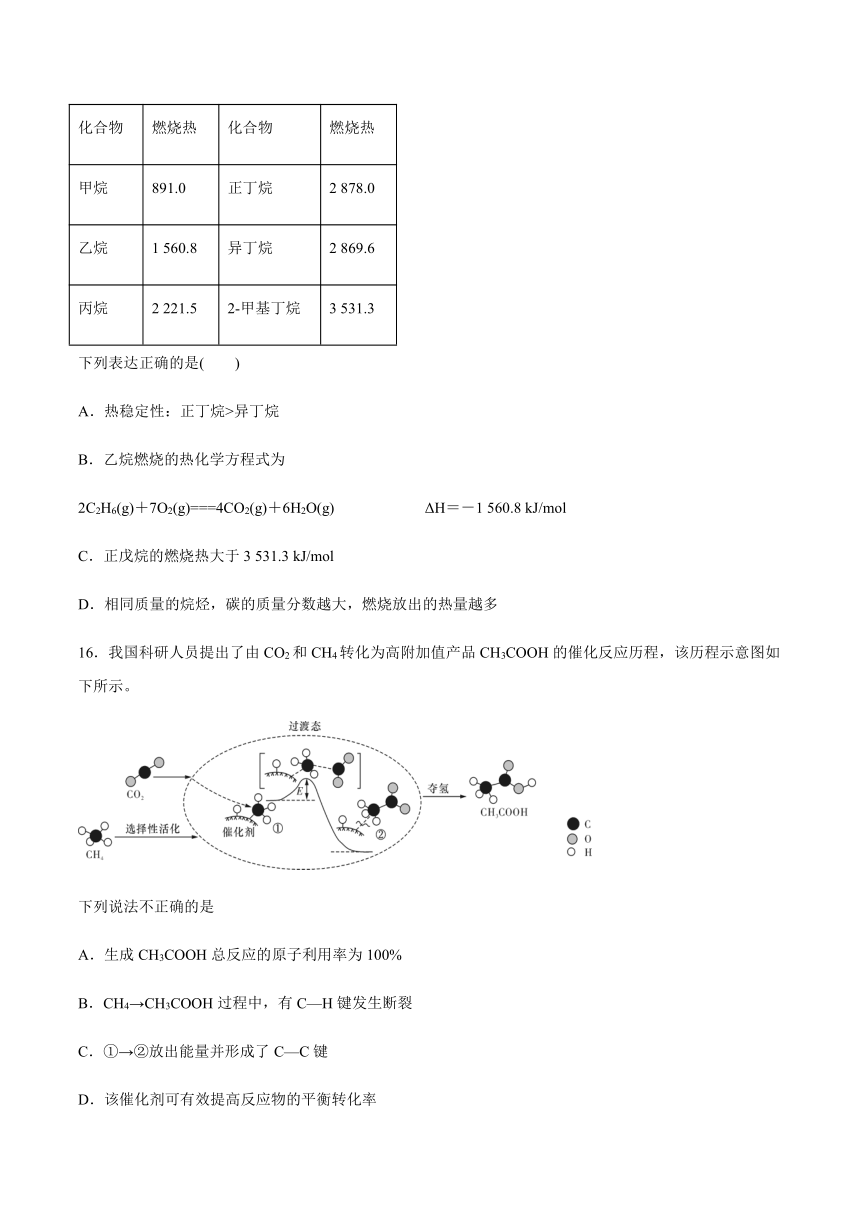
16.我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,该历程示意图如下所示。
下列说法不正确的是
A.生成CH3COOH总反应的原子利用率为100%
B.CH4→CH3COOH过程中,有C—H键发生断裂
C.①→②放出能量并形成了C—C键
D.该催化剂可有效提高反应物的平衡转化率
17.关于放热反应A+B=C+D,以下说法正确的是(EA、EB、EC、ED分别代表A、B、C、D所具有的能量)
A.EA>EB
B.EA>EC+ED
C.EA+EB>EC+ED
D.EA+EB<EC+ED
二、填空题
18.为了研究化学反应A+BC+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
(1)该反应为________(填“放热”或“吸热”)反应。
(2)A和B的总能量比C和D的总能量_______(填“高”或“低”)。
(3)物质中的______能转化成______能释放出来。
(4)反应物化学键断裂吸收的能量__________(填“高”或“低”)于生成物化学键形成放出的能量。
(5)写出一个符合题中条件的化学方程式:______。
19.化学反应一定伴随能量变化。
(1)将20gBa(OH)2·8H2O晶体与10g
NH4Cl晶体一起放入烧杯中,并将烧杯放在滴有几滴水的玻璃片上,用玻璃棒快速搅拌,闻到______气味,用手触摸烧杯底部感觉________,烧杯下面的玻璃片可能与烧杯___。
说明Ba(OH)2·8H2O跟NH4Cl的反应是_____(填“吸热”或“放热”)反应。该反应的化学方程式_________
(2)NaOH稀溶液跟稀盐酸反应的中和热与KOH稀溶液跟稀硫酸反应的中和热_____(填
“相等”或“不等”),原因是(用适当的文字和离子方程式解释)_____
(3)下列措施可以提高燃料的燃烧效率的是________(填序号)
①提高燃料的着火点,②降低燃料的着火点,③将固体燃料粉碎,④将液体燃料雾化,⑤将燃料煤气化处理,⑥通入适量空气
20.已知下列热化学方程式:
??
??
??
??
回答下列问题:
(1).上述反应中属于放热反应的是________。
(2).H2的燃烧热________________;C的燃烧热________________。
(3).燃烧生成液态水,放出的热量为________。
(4).写出CO燃烧的热化学方程式:________________________________。
三、实验题
21.在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20g已研磨成粉末的Ba(OH)2?8H2O,将小烧杯放在事先已滴有3?4滴水的玻璃片上,然后向烧杯中加入约10gNH4Cl晶体,根据实验步骤,填写下表,并回答问题。
实验步骤
实验现象及结论
将晶体混合,立即快速搅拌
有刺激性气味能使湿润的紫色石蕊试纸变蓝的______产生(1)
用手摸烧杯下部
感觉烧杯变凉说明此反应是______反应(2)
用手拿起烧杯
烧杯下面的带有几滴水的玻璃片粘到了烧杯底部
将粘有玻璃片的烧杯放在盛有热水的烧杯上
玻璃片脱离上面烧杯底部
反应后移走多孔塑料片观察反应物
混合物成糊状,证明有______生成(3)
(4)写出实验过程中发生反应的化学方程式:______________________________;
(5)该反应在常温下就可进行,说明:____________________________________。
22.在一个小烧杯里加入约20g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10g氯化铵晶体,并立即用玻璃棒迅速搅拌。试回答下列问题:
(1)写出反应的化学方程式:__。
(2)实验中要立即用玻璃棒迅速搅拌的原因是__。
(3)如果实验中没有看到“结冰”现象,可能的原因是(答出三个或三个以上原因)__。
(4)如果没有看到“结冰”现象,我们还可以采取哪些方式来说明该反应吸热?(答出两种方案)
①第一种方案是_;
②第二种方案是__。
(5)“结冰”现象说明该反应是一个__(填“放出”或“吸收”)能量的反应。即断开旧化学键__(填“吸收”或“放出”)的能量__(填“>”或“<”)形成新化学键__(填“吸收”或“放出”)的能量。
(6)该反应在常温下就可进行,说明__。
参考答案
1.B2.B3.C4.C5.D6.A7.A8.C9.C10.D11.A12.A13.B14.B15.C16.D17.C
18.放热
高
化学
热
低
2Al+6HCl=2AlCl3+3H2↑(或2Na+2H2O=2NaOH+H2↑或NaOH+HCl=NaCl+H2O)
19.刺激性气味
烧杯底部很冷
被冻在一起
吸热
相等
中和反应的实质是:H++OH-=H2O,两个反应参加反应的物质、生成物均相同,反应物、生成物蕴含的化学能相同,所以反应放出的能量也相同
③④⑤⑥
20.
?
21.NH3
吸热
水
BaCl2?8H2O+2NH4Cl═BaCl2+2NH3?H2O+8H2O
吸放热反应与反应是否需要在加热无关
22.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
使反应物充分混合,迅速发生反应
①反应物未进行快速搅拌;②玻璃片上滴加的水太多;③氢氧化钡晶体已部分失水;④环境温度太高;⑤试剂用量太少;⑥氢氧化钡晶体未研成粉末
在烧杯内的反应物中插入温度计,反应后温度计的示数下降,说明该反应是吸热反应
用皮肤感受,感觉烧杯外壁很凉,说明该反应为吸热反应
吸收
吸收
>
放出
有的吸热反应不需要加热也可发生
一、单选题
1.下列关于反应能量的说法正确的是(
)
A.若反应A=B
△H<0,说明A物质比B物质稳定,分子内共价键键能
A比B大
B.Zn(s)+CuSO4
(aq)==ZnSO4
(aq)
+Cu(s)
△H=
-216
kJ·mol-1。则反应物总能量>生成物总能量
C.101kPa时,2H2(g)+O2(g)==2H2O(g)
△H=
-Q
kJ·mol-1,则H2的燃烧热为1/2Q
kJ·mol-l
D.H+(aq)
+OH-
(aq)=H2O(l)
△H=
-57.3
kJ·mol-1,含1mol
NaOH的氢氧化钠溶液与含0.5mol
CH3COOH的醋酸溶液混合后会放出57.3
kJ的热量
2.已知下列两个热化学方程式:2H2(g)
+
O2(g)
=
2H2O(1)
ΔH=
-571.6
kJ?mol-1,C3H8(g)
+
5O2(g)=
3CO2(g)
+
4H2O(l)
ΔH=
-2220
kJ?mol-1,下列说法正确的是(
)
A.相同质量H2和C3H8分别完全燃烧,C3H8放出的热量多
B.C3H8
完全燃烧生成1mol
H2O(l)放出的热量为555
kJ
C.l
mol
H2和2
molC3H8
组成的混合气体完全燃烧放出的热量为5011.6
kJ
D.H2和C3H8的混合气体共4mol,完全燃烧时放出3256
kJ热量,则
n(H2):n(C3H8)=1:1
3.关于化学能与其他能量相互转化的说法正确的是(
)
A.图1所示的装置能将化学能转变为电能
B.图2所示的反应为吸热反应
C.化学反应中能量变化的主要原因是化学键的断裂与形成
D.中和反应中,反应物的总能量比生成物的总能量低
4.NF3是一种温室气体,其存储能量能力是
CO2的
12000~20000
倍,在大气中的寿命可长达
740年,如表所示是几种化学键断裂时所需要吸收的能量,下列说法中正确的是
化学键
N≡N
F—F
N—F
1mol
化学键断裂所需要吸收的能量
946kJ
154.8kJ
283
kJ
A.过程
N2
(g)→2N(g)放出能量
B.过程
N(g)+3F(g)→NF3(g)吸收能量
C.反应
N2(g)+3F2
(g)=2NF3(g)为放热反应
D.NF3中元素的化合价:N
为-3价,F
为+1
价
5.下列属于氧化还原反应且热量变化与如图一致的是
A.NH4NO3
晶体溶于水
B.钠和
H2O
反应
C.NH4Cl
晶体和氢氧化钡晶体的反应
D.CO2
和
C
反应
6.已知在1×105Pa,298
K条件下,1
g
H2燃烧生成液态水放出142.9
kJ的热量,表示该反应的热化学方程式正确的是(
)
A.2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6
kJ·mol-1
B.2H2(g)+O2(g)===2H2O(l)
ΔH=-142.9
kJ·mol-1
C.2H2+O2===2H2O
ΔH=-571.6
kJ·mol-1
D.H2(g)+1/2O2(g)===H2O(g)
ΔH=-285.8
kJ·mol-1
7.已知石墨在一定条件下转化成金刚石是吸热反应,由此可能出的正确结论是
A.石墨比金刚石更稳定
B.金刚石比石墨更稳定
C.石墨转化成金刚石是物理变化
D.石墨和金刚石的结构相同
8.下列变化过程吸收能量的是( )
A.H+H―→H2
B.H+Cl―→HCl
C.H2―→H+H
D.C+O2―→CO2
9.下列有关能量的说法不正确的是
( )
A.化石能源物质内部贮存着大量的能量
B.植物的光合作用使太阳能转化为化学能
C.燃料燃烧时只是将化学能转化为热能
D.由石墨制金刚石是吸热反应,故石墨能量比金刚石能量低
10.已知蒸发1mol
Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
H2(g)
Br2(g)
HBr(g)
1mol分子中的化学键断裂时需要吸收的能量(kJ)
436
a
369
则表中a为
A.404
B.260
C.230
D.200
11.下列反应既属于氧化还原反应,又是吸热反应的是(
)
A.灼热的炭与CO2的反应
B.Ba(OH)2·8H2O
与
NH4Cl
的反应
C.镁条与稀盐酸的反应
D.氢气在氧气中的燃烧反应
12.金刚石和石墨是碳元素的两种结构不同的单质(同素异形体),在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热能,据此,试判断在100kPa下,下列结论正确的是(
)
A.石墨比金刚石稳定
B.金刚石比石墨稳定
C.1mol石墨比1mol金刚石总能量高
D.金刚石转化为石墨是物理变化
13.在下列各说法中,正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1mol
H2SO4与1mol
Ba(OH)2反应放出的热叫做中和热
D.1mol
H2与0.5mol
O2反应放出的热就是H2的标准燃烧热
14.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法正确的是
A.1
mol
N2(g)和NA个O2(g)反应放出的能量为180
kJ
B.1
mol
N2(g)和1
mol
O2(g)具有总能量小于2
mol
NO(g)具有的总能量
C.通常情况下,N2(g)和O2(g)混合能直接生成NO(g)
D.吸热反应一定需要加热才能发生
15.一些烷烃的燃烧热(kJ/mol)如下表:
化合物
燃烧热
化合物
燃烧热
甲烷
891.0
正丁烷
2
878.0
乙烷
1
560.8
异丁烷
2
869.6
丙烷
2
221.5
2?甲基丁烷
3
531.3
下列表达正确的是( )
A.热稳定性:正丁烷>异丁烷
B.乙烷燃烧的热化学方程式为
2C2H6(g)+7O2(g)===4CO2(g)+6H2O(g)
ΔH=-1
560.8
kJ/mol
C.正戊烷的燃烧热大于3
531.3
kJ/mol
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
16.我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,该历程示意图如下所示。
下列说法不正确的是
A.生成CH3COOH总反应的原子利用率为100%
B.CH4→CH3COOH过程中,有C—H键发生断裂
C.①→②放出能量并形成了C—C键
D.该催化剂可有效提高反应物的平衡转化率
17.关于放热反应A+B=C+D,以下说法正确的是(EA、EB、EC、ED分别代表A、B、C、D所具有的能量)
A.EA>EB
B.EA>EC+ED
C.EA+EB>EC+ED
D.EA+EB<EC+ED
二、填空题
18.为了研究化学反应A+BC+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
(1)该反应为________(填“放热”或“吸热”)反应。
(2)A和B的总能量比C和D的总能量_______(填“高”或“低”)。
(3)物质中的______能转化成______能释放出来。
(4)反应物化学键断裂吸收的能量__________(填“高”或“低”)于生成物化学键形成放出的能量。
(5)写出一个符合题中条件的化学方程式:______。
19.化学反应一定伴随能量变化。
(1)将20gBa(OH)2·8H2O晶体与10g
NH4Cl晶体一起放入烧杯中,并将烧杯放在滴有几滴水的玻璃片上,用玻璃棒快速搅拌,闻到______气味,用手触摸烧杯底部感觉________,烧杯下面的玻璃片可能与烧杯___。
说明Ba(OH)2·8H2O跟NH4Cl的反应是_____(填“吸热”或“放热”)反应。该反应的化学方程式_________
(2)NaOH稀溶液跟稀盐酸反应的中和热与KOH稀溶液跟稀硫酸反应的中和热_____(填
“相等”或“不等”),原因是(用适当的文字和离子方程式解释)_____
(3)下列措施可以提高燃料的燃烧效率的是________(填序号)
①提高燃料的着火点,②降低燃料的着火点,③将固体燃料粉碎,④将液体燃料雾化,⑤将燃料煤气化处理,⑥通入适量空气
20.已知下列热化学方程式:
??
??
??
??
回答下列问题:
(1).上述反应中属于放热反应的是________。
(2).H2的燃烧热________________;C的燃烧热________________。
(3).燃烧生成液态水,放出的热量为________。
(4).写出CO燃烧的热化学方程式:________________________________。
三、实验题
21.在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20g已研磨成粉末的Ba(OH)2?8H2O,将小烧杯放在事先已滴有3?4滴水的玻璃片上,然后向烧杯中加入约10gNH4Cl晶体,根据实验步骤,填写下表,并回答问题。
实验步骤
实验现象及结论
将晶体混合,立即快速搅拌
有刺激性气味能使湿润的紫色石蕊试纸变蓝的______产生(1)
用手摸烧杯下部
感觉烧杯变凉说明此反应是______反应(2)
用手拿起烧杯
烧杯下面的带有几滴水的玻璃片粘到了烧杯底部
将粘有玻璃片的烧杯放在盛有热水的烧杯上
玻璃片脱离上面烧杯底部
反应后移走多孔塑料片观察反应物
混合物成糊状,证明有______生成(3)
(4)写出实验过程中发生反应的化学方程式:______________________________;
(5)该反应在常温下就可进行,说明:____________________________________。
22.在一个小烧杯里加入约20g已研磨成粉末的氢氧化钡晶体[Ba(OH)2·8H2O],将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯内加入约10g氯化铵晶体,并立即用玻璃棒迅速搅拌。试回答下列问题:
(1)写出反应的化学方程式:__。
(2)实验中要立即用玻璃棒迅速搅拌的原因是__。
(3)如果实验中没有看到“结冰”现象,可能的原因是(答出三个或三个以上原因)__。
(4)如果没有看到“结冰”现象,我们还可以采取哪些方式来说明该反应吸热?(答出两种方案)
①第一种方案是_;
②第二种方案是__。
(5)“结冰”现象说明该反应是一个__(填“放出”或“吸收”)能量的反应。即断开旧化学键__(填“吸收”或“放出”)的能量__(填“>”或“<”)形成新化学键__(填“吸收”或“放出”)的能量。
(6)该反应在常温下就可进行,说明__。
参考答案
1.B2.B3.C4.C5.D6.A7.A8.C9.C10.D11.A12.A13.B14.B15.C16.D17.C
18.放热
高
化学
热
低
2Al+6HCl=2AlCl3+3H2↑(或2Na+2H2O=2NaOH+H2↑或NaOH+HCl=NaCl+H2O)
19.刺激性气味
烧杯底部很冷
被冻在一起
吸热
相等
中和反应的实质是:H++OH-=H2O,两个反应参加反应的物质、生成物均相同,反应物、生成物蕴含的化学能相同,所以反应放出的能量也相同
③④⑤⑥
20.
?
21.NH3
吸热
水
BaCl2?8H2O+2NH4Cl═BaCl2+2NH3?H2O+8H2O
吸放热反应与反应是否需要在加热无关
22.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
使反应物充分混合,迅速发生反应
①反应物未进行快速搅拌;②玻璃片上滴加的水太多;③氢氧化钡晶体已部分失水;④环境温度太高;⑤试剂用量太少;⑥氢氧化钡晶体未研成粉末
在烧杯内的反应物中插入温度计,反应后温度计的示数下降,说明该反应是吸热反应
用皮肤感受,感觉烧杯外壁很凉,说明该反应为吸热反应
吸收
吸收
>
放出
有的吸热反应不需要加热也可发生
