富集在海水中的元素——氯(第三课时)
文档属性
| 名称 | 富集在海水中的元素——氯(第三课时) |

|
|
| 格式 | zip | ||
| 文件大小 | 241.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-12-13 00:00:00 | ||
图片预览






文档简介
(共16张PPT)
富集在海水中的元素
——氯
第三课时
1、氯气与氢氧化钠、氢氧化钙反应
2、漂白粉日常生活中漂白原理
知识回顾
3、漂白粉日常生活中漂白原理
书写下面反应的化学方程式
设计一套制备干燥纯净氯气的装置
思考交流
提示:选用中学化学常用仪器药品
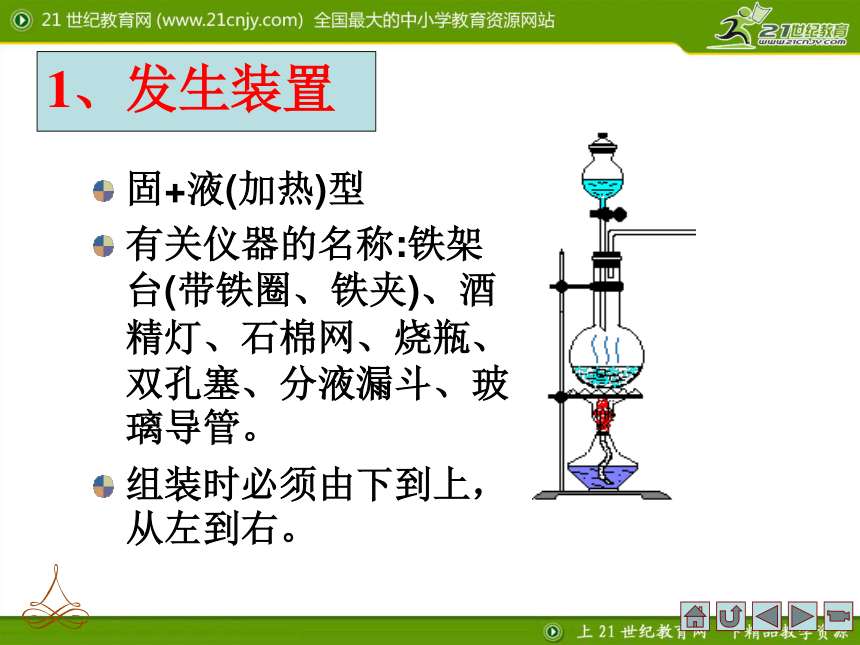
固+液(加热)型
有关仪器的名称:铁架台(带铁圈、铁夹)、酒精灯、石棉网、烧瓶、双孔塞、分液漏斗、玻璃导管。
组装时必须由下到上,从左到右。
1、发生装置
a. 向上排空气法
b. 排饱和食盐水法
2、收集装置
3、尾气吸收
氯气有毒,会污染空气,故用饱和氢氧化钠溶液吸收。
饱和NaOH
Cl2 + 2NaOH == NaCl + NaClO + H2O
HCl气体
水蒸气
饱和食盐水
浓硫酸
浓 H2SO4
饱和食盐水
4、净化装置
氯气实验室制法
小结:一套完整的制气装置,由几部分组成?
气体
发生
装置
气体净化装置
气体收集装置
尾气吸收装置
性质检验装置
实验现象 解释或离子方程式
加AgNO3溶液后 加稀硝酸后
稀盐酸
NaCl溶液
Na2CO3溶液
自来水
蒸馏水
白色沉淀
白色沉淀
白色沉淀
白色沉淀
无现象
沉淀不溶解
沉淀不溶解
沉淀溶解
有气泡
沉淀不溶解
无现象
Cl- + Ag+=AgCl↓
Cl- + Ag+=AgCl↓
CO32- +2Ag+ =Ag2CO3↓
Ag2CO3+2H+=2Ag++CO2↑ + H2O
Cl- + Ag+=AgCl↓
无
检验Cl-时,滴加AgNO3溶液后,再加稀硝酸有何作用?
区分AgCl和Ag2CO3
AgCl不与稀硝酸反应
Ag2CO3可与稀硝酸反应
向某溶液中滴加AgNO3,有白色沉淀生成, 原溶液是否一定含Cl-?
Cl-、CO32-都能与Ag+反应生成白色沉淀
思考交流
氯离子(Cl-)的检验
在被检验的溶液中加入稀硝酸酸化,再滴入AgNO3溶液,若产生白色沉淀,则被检液中含有Cl-。
(2)方法和结论:
(1)试剂:AgNO3溶液、稀硝酸
在被检验的溶液中滴入AgNO3溶液,若产生白色沉淀,再加入稀硝酸,沉淀不溶,则被检液中含有Cl-。
知识归纳
富集在海水中的元素
——氯
第三课时
1、氯气与氢氧化钠、氢氧化钙反应
2、漂白粉日常生活中漂白原理
知识回顾
3、漂白粉日常生活中漂白原理
书写下面反应的化学方程式
设计一套制备干燥纯净氯气的装置
思考交流
提示:选用中学化学常用仪器药品
固+液(加热)型
有关仪器的名称:铁架台(带铁圈、铁夹)、酒精灯、石棉网、烧瓶、双孔塞、分液漏斗、玻璃导管。
组装时必须由下到上,从左到右。
1、发生装置
a. 向上排空气法
b. 排饱和食盐水法
2、收集装置
3、尾气吸收
氯气有毒,会污染空气,故用饱和氢氧化钠溶液吸收。
饱和NaOH
Cl2 + 2NaOH == NaCl + NaClO + H2O
HCl气体
水蒸气
饱和食盐水
浓硫酸
浓 H2SO4
饱和食盐水
4、净化装置
氯气实验室制法
小结:一套完整的制气装置,由几部分组成?
气体
发生
装置
气体净化装置
气体收集装置
尾气吸收装置
性质检验装置
实验现象 解释或离子方程式
加AgNO3溶液后 加稀硝酸后
稀盐酸
NaCl溶液
Na2CO3溶液
自来水
蒸馏水
白色沉淀
白色沉淀
白色沉淀
白色沉淀
无现象
沉淀不溶解
沉淀不溶解
沉淀溶解
有气泡
沉淀不溶解
无现象
Cl- + Ag+=AgCl↓
Cl- + Ag+=AgCl↓
CO32- +2Ag+ =Ag2CO3↓
Ag2CO3+2H+=2Ag++CO2↑ + H2O
Cl- + Ag+=AgCl↓
无
检验Cl-时,滴加AgNO3溶液后,再加稀硝酸有何作用?
区分AgCl和Ag2CO3
AgCl不与稀硝酸反应
Ag2CO3可与稀硝酸反应
向某溶液中滴加AgNO3,有白色沉淀生成, 原溶液是否一定含Cl-?
Cl-、CO32-都能与Ag+反应生成白色沉淀
思考交流
氯离子(Cl-)的检验
在被检验的溶液中加入稀硝酸酸化,再滴入AgNO3溶液,若产生白色沉淀,则被检液中含有Cl-。
(2)方法和结论:
(1)试剂:AgNO3溶液、稀硝酸
在被检验的溶液中滴入AgNO3溶液,若产生白色沉淀,再加入稀硝酸,沉淀不溶,则被检液中含有Cl-。
知识归纳
