2020-2021学年高二化学人教版选修4化学反应原理第四章《电化学基础》测试卷(解析版)
文档属性
| 名称 | 2020-2021学年高二化学人教版选修4化学反应原理第四章《电化学基础》测试卷(解析版) |

|
|
| 格式 | zip | ||
| 文件大小 | 89.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-06 00:00:00 | ||
图片预览




文档简介
第四章《电化学基础》测试卷
一、单选题(共15小题)
1.常温下用石墨作电极,电解100
mL
0.1
mol·L-1的Cu(NO3)2和0.1
mol·L-1的AgNO3组成的混合溶液,当某一电极上生成的气体在标准状况下体积为1.12
L
时,假设溶液体积不变,下列说法正确的是( )
A.
阴极增重1.4
g
B.
所得溶液pH<1
C.
阴极增重0.64
g
D.
所得溶液pH>1
2.化学电池在通讯、交通及日常生活中有着广泛的应用。目前常用的镍镉(Ni-Cd)电池,其电池总反应可以表示:
Cd+2NiO(OH)+2H2O2Ni(OH)2+Cd(OH)2
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是( )
①以上反应是可逆反应 ②以上反应不是可逆反应 ③充电时化学能转变为电能 ④放电时化学能转变为电能
A.
①③
B.
②④
C.
①④
D.
②③
3.由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎。下图是氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是( )
A.
a处通入氧气,b处通入氢气
B.
该装置中只涉及两种形式的能量转化
C.
电池正极电极反应式为O2+2H2O+4e-===4OH-
D.
P-型半导体连接的是电池负极
4.下列有关金属铁的腐蚀与防护,说法正确的是( )
A.
酸雨后易发生析氢腐蚀、炒锅存留盐液时易发生吸氧腐蚀
B.
当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.
铁与电源正极连接可实现电化学保护
D.
将钢管与铜管一起堆放时可保护钢管少受腐蚀
5.钢铁发生吸氧腐蚀时,正极上发生的电极反应是( )
A.
2H++2e-===H2↑
B.
Fe2++2e-===Fe
C.
2H2O+O2+4e-===4OH-
D.
Fe3++e-===Fe2+
6.下列金属的防护方法不正确的是( )
A.
对健身器材涂油漆以防止生锈
B.
对某些工具的“机械转动部位”选用刷油漆的方法来防锈
C.
用牺牲锌块的方法来保护船体
D.
自行车的钢圈上镀上一层Cr防锈
7.图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。下列判断正确的是( )
A.
滤纸上c点附近会变红色
B.
Cu电极质量减小,Pt电极质量增大
C.
Z中溶液的pH先减小,后增大
D.
溶液中的向Cu电极定向移动
8.关于镀铜和电解精炼铜,下列说法中正确的是( )
A.
都用粗铜作阳极、纯铜作阴极
B.
电解液的成分都保持不变
C.
阳极反应都只有Cu-2e-===Cu2+
D.
阴极反应都只有Cu2++2e-===Cu
9.关于钢铁腐蚀与防护的说法不正确的是( )
A.
钢铁的吸氧腐蚀和析氢腐蚀的负极反应式均为Fe-2e-===Fe2+
B.
钢铁发生吸氧腐蚀时,正极反应式为O2+2H2O+4e-===4OH-
C.
地下钢管连接镁块是采用牺牲阳极的阴极保护法
D.
用外加电流的阴极保护法防止钢铁腐蚀时,钢铁接电源的正极
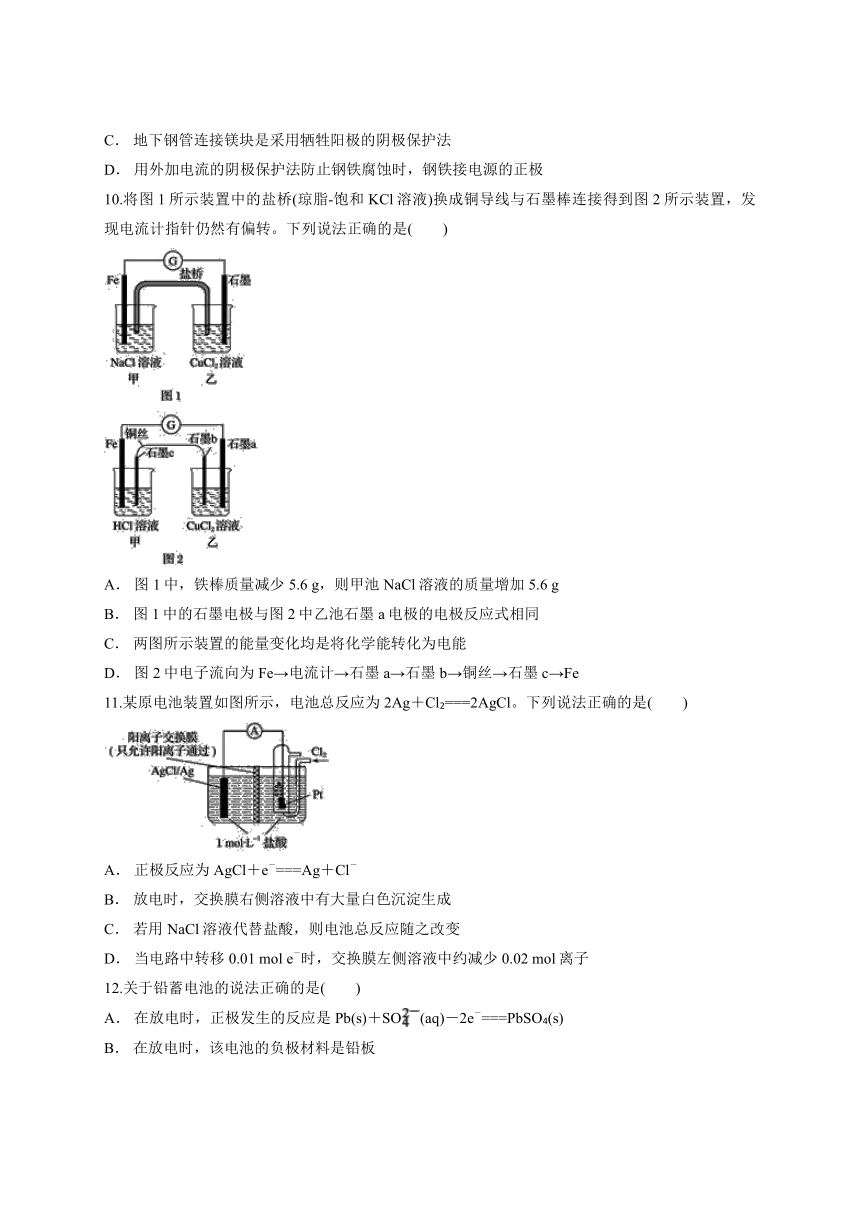
10.将图1所示装置中的盐桥(琼脂?饱和KCl溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是( )
A.
图1中,铁棒质量减少5.6
g,则甲池NaCl溶液的质量增加5.6
g
B.
图1中的石墨电极与图2中乙池石墨a电极的电极反应式相同
C.
两图所示装置的能量变化均是将化学能转化为电能
D.
图2中电子流向为Fe→电流计→石墨a→石墨b→铜丝→石墨c→Fe
11.某原电池装置如图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是( )
A.
正极反应为AgCl+e-===Ag+Cl-
B.
放电时,交换膜右侧溶液中有大量白色沉淀生成
C.
若用NaCl溶液代替盐酸,则电池总反应随之改变
D.
当电路中转移0.01
mol
e-时,交换膜左侧溶液中约减少0.02
mol离子
12.关于铅蓄电池的说法正确的是( )
A.
在放电时,正极发生的反应是Pb(s)+SO(aq)-2e-===PbSO4(s)
B.
在放电时,该电池的负极材料是铅板
C.
在充电时,电池中硫酸的浓度不断变小
D.
在充电时,阳极发生的反应是PbSO4(s)+2e-===Pb(s)+SO(aq)
13.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。下列有关说法正确的是( )
A.
检测时,电解质溶液中的H+向负极移动
B.
若有0.4
mol电子转移,则在标准状况下消耗4.48
L氧气
C.
电池反应的化学方程式为CH3CH2OH+O2===CH3COOH+H2O
D.
正极上发生的反应为O2+4e-+2H2O===4OH-
14.为探究钢铁的吸氧腐蚀原理设计了如图所示的装置,下列有关说法中错误的是( )
A.
正极的电极反应方程式为O2+2H2O+4e-===4OH-
B.
将石墨电极改成Mg电极,难以观察到铁锈生成
C.
若向自来水中加入少量NaCl(s),可较快地看到铁锈
D.
分别向铁、石墨电极附近吹入O2,前者铁锈出现得快
15.下图为铜锌原电池示意图,下列说法正确的是( )
A.
锌片逐渐溶解
B.
烧杯中溶液逐渐呈蓝色
C.
电子由铜片通过导线流向锌片
D.
锌为正极,铜为负极
二、实验题(共3小题)
16.某同学利用生活中或实验室中常用的物品,根据氧化还原反应知识和电化学知识,自己动手设计了一个原电池。请填写下列空白:
(1)实验原理:Fe+2H+===Fe2++H2↑
(2)实验用品:电极(______、______)、稀硫酸、______、________、耳机(或者电流表)(填写所缺的实验用品)。
(3)实验装置如图。
(4)原电池设计及注意的问题:
①按如图所示装置连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一个极是连接在原电池的另一个电极上的),这时可以听见耳机发生“嚓嚓嚓……”的声音。其原因是在原电池中,由化学能转化为____________,在耳机中又由__________转化为声音这种能量;
②如果将装置中的耳机改为电流表,则铁钉应该接电流表的________极,电极反应式为_____________,发生了________反应;
③铜钉应该接电流表的________极,电极反应式为_____________,发生了_________反应。
17.某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下表:
试根据表中的实验现象完成下列问题:
(1)实验①、②中铝所作的电极(指正极或负极)________(填“相同”或“不相同”)。
(2)实验③中铝为________极,电极反应式为________________;石墨为________极,电极反应式为_______________;电池总反应式为_____________________________。
(3)实验④中铝作负极还是正极?_____,理由是___________________________________,铝电极的电极反应式为_______________________________。
(4)根据实验结果总结出影响铝在原电池中作正极或负极的因素为_____________________。
18.已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液、Fe2(SO4)3溶液、硫酸。设计一种以铁和稀硫酸反应为原理的原电池,要求画出装置图(需标明电极材料及电池的正、负极)。
三、填空题(共3小题)
19.如图所示装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL1.0mol·L-1。
(1)A为________池,(填“原电”或“电解”),其中的Ag极为________极,发生________(填“氧化”或“还原”)反应。
(2)B装置中的电极b极为________极,电极反应式为__________________________________,
总反应的化学方程式为____________________________________________________。
经过一段时间后,B装置中溶液的碱性________(填“增强”、“减弱”或“不变”)
(3)若工作一段时间后,当Zn片质量减少3.25
g时,a极逸出的气体在标准状况下的体积为________L。
20.如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。
已知:铅蓄电池在放电时发生下列电极反应:
负极:Pb+-2e-===PbSO4
正极:PbO2+4H+++2e-===PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式____________________________________。
(2)若在电解池中C极一侧滴酚酞溶液,电解一段时间后未呈红色,说明铅蓄电池的A极为________极。
(3)用铅蓄电池电解1
L饱和食盐水(食盐水足量,密度为1.15
g·cm-3)时,
①若收集到11.2
L(标准状况下)氯气,则至少转移电子________mol。
②若铅蓄电池消耗H2SO42
mol,则可收集到H2的体积(标准状况下)为________L。
③若消耗硫酸amol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出)________________(用含a的代数式表示)。
21.某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
根据要求回答相关问题:
(1)通入氢气的电极为________(填“正极”或“负极”),负极的电极反应式为____________________。
(2)石墨电极为________(填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,________(填“铁极”或“石墨极”)区的溶液先变红。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”)。精铜电极上的电极反应式为____________________________
________________________________________________________________________。
答案解析
1.【答案】B
【解析】阴极可以放电的离子依次为0.01
mol
Ag+、0.01
mol
Cu2+,阳极可以放电的阴离子只有OH-;当阳极生成1.12
L
O2时,电路中通过电子:n(e-)=0.05
mol×4=0.2
mol,此时Ag+、Cu2+已全部析出,质量:0.01
mol×108
g·mol-1+0.01
mol×64
g·mol-1=1.72
g;因为当Ag+、Cu2+全部析出以后,相当于电解水,H+不再增加,所以生成的H+所带电荷与0.01
mol
Ag+、0.01
mol
Cu2+所带电荷相等;则溶液中生成:c(H+)=0.3
mol·L-1,pH<1。
2.【答案】B
【解析】Ni-Cd电池的充、放电条件不相同,因此电池的充、放电反应不属于可逆反应。
3.【答案】C
【解析】根据LED中电子移动方向可判断N-型半导体与电池负极相连,
a处为负极,应通入氢气,b处通入氧气,P-型半导体与电池正极相连,
A、D错误;该装置主要涉及化学能、电能、光能三种形式的能量转化,B错误;在KOH溶液中,正极电极反应式为O2+2H2O+4e-===4OH-,C正确。
4.【答案】A
【解析】酸雨后溶液显酸性,容易发生析氢腐蚀,炒锅存留盐液是中性溶液,较易发生吸氧腐蚀,A正确;金属活动性Zn>Fe>Sn,所以镀锡铁镀层破损时,Fe作原电池的负极首先被腐蚀,而镀锌铁镀层破损时,由于Fe作正极,被保护起来,前者更易被腐蚀,B错误;铁与电源负极连接可实现电化学保护,C错误;将钢管与铜管一起堆放形成原电池,钢管作为负极,受腐蚀的程度增加,D错误。
5.【答案】C
【解析】钢铁发生吸氧腐蚀,正极反应为2H2O+O2+4e-===4OH-,C正确。
6.【答案】B
【解析】涂油漆可以起到避免金属和电解质溶液接触形成原电池的目的,A正确;油漆保护层在机械转动部位很容易磨损,起不到保护层的作用,应选用润滑油来达到防锈的目的,B错误;锌、铁与电解液形成原电池时,锌作负极被腐蚀,铁作正极被保护,C正确;钢圈上镀上一层Cr,阻断了铁与氧气的接触,D正确。
7.【答案】A
【解析】紫红色斑即Mn向d端扩散,根据阴离子向阳极移动的原理,可知d端为阳极,b为正极,a为负极,c为阴极。c点NaCl溶液中H+放电,2H2O+2e-===H2↑+2OH-,c点附近会变红色,A正确;Z中Cu电极和a相连,为阴极,Cu2++2e-===Cu,Pt极为阳极,2H2O-4e-===4H++O2↑,pH减小,B、C错误;Z为电解池,池内阴离子向阳极移动,即向Pt极移动,D错误。
8.【答案】D
【解析】A项,电镀时镀件作阴极;B项,电解精炼铜时电解液成分改变;C项,电解精炼铜时,杂质若有比铜活泼的金属(如锌),则还会发生Zn-2e-===Zn2+的反应。
9.【答案】D
【解析】钢铁的吸氧腐蚀和析氢腐蚀都是铁失去电子作负极,电极反应式为Fe-2e-===Fe2+,钢铁发生吸氧腐蚀时O2+2H2O+4e-===4OH-,A、B正确;地下钢管连接镁块,镁比铁活泼,作负极,铁作正极得到保护,C正确;用外加电流的阴极保护法防止钢铁腐蚀时,钢铁连接电源的负极,D错误。
10.【答案】B
【解析】图1为原电池,Fe为负极,电极反应:Fe-2e-===Fe2+,盐桥中的阴离子移向负极,增加质量大于5.6
g,A错误;图1中石墨为正极,电极反应:Cu2++2e-===Cu,图2为电解池,图2乙池中石墨a是阴极,电极反应:Cu2++2e-===Cu,B正确;原电池是将化学能转化为电能,电解池是将电能转化为化学能,C错误;电子不能在溶液中移动,图2中电子流向应为Fe→电流计→石墨a,石墨b→铜丝→石墨c,D错误。
11.【答案】D
【解析】原电池正极发生还原反应,该原电池正极反应式为Cl2+2e-===2Cl-,A项不正确;该原电池放电时,负极材料中的Ag被氧化为Ag+,Ag+与附近的Cl-反应生成AgCl白色沉淀。交换膜右侧溶液中无大量AgCl白色沉淀生成,B项不正确;由原电池负极反应Cl-+Ag-e-===AgCl↓和正极反应Cl2+2e-===2Cl-可知,若用NaCl溶液代替盐酸,电池总反应不变,C项不正确;由原电池的负极反应Cl-+Ag-e-===AgCl↓可知,当电路中转移0.01
mol
e-时,交换膜左侧溶液中减少0.01
mol
Cl-,同时约有0.01
mol
H+通过阳离子交换膜移至右侧,故交换膜左侧溶液中约减少0.02
mol离子,D项正确。
12.【答案】B
【解析】蓄电池反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,正极得电子,发生还原反应,电极反应式为PbO2+4H++SO+2e-===PbSO4+2H2O,A错误;负极失电子,发生氧化反应,电极反应式为Pb-2e-+SO===PbSO4,铅板是负极材料,B正确;充电装置是电解池,阳极失电子,与原电池正极反应相反,为PbSO4+2H2O-2e-===PbO2+4H++SO,阴极得电子,与原电池负极反应相反,为PbSO4+2e-===Pb+SO,硫酸的浓度增大,CD错误。
13.【答案】C
【解析】A项,检测时,电解质溶液中的H+移向正极;B项,若反应中有0.4
mol电子转移,则在标况下消耗的O2体积为2.24
L;D项,电解质溶液呈酸性,正极上发生的反应为O2+4H++4e-===2H2O。
14.【答案】D
【解析】如果铁发生吸氧腐蚀,则铁是负极,失电子被氧化成Fe2+,在正极氧气得电子发生还原反应,电极反应式:2H2O+O2+4e-===4OH-。将氧气吹向石墨电极形成原电池反应,加快腐蚀速率,A正确,D错误;向自来水中加入NaCl(s),可使电解质溶液的导电能力增强,加快腐蚀速率,C正确;若将石墨电极换成Mg电极,Mg比Fe活泼,负极为Mg,Fe被保护,难以看到铁生锈,B正确。
15.【答案】A
【解析】在铜锌原电池中,锌的活动性大于铜,锌为负极、铜为正极。负极锌失去电子不断溶解,在外电路中电子由锌电极流向铜电极;溶液中的氢离子,在正极铜表面得到电子被还原,有氢气产生,铜电极保持不变,溶液中不存在铜离子,不能使溶液成蓝色。
16.【答案】(2)铁钉或铁条;铜钉(其他的惰性电极如铅笔芯、铂等都正确); 烧杯;导线
(4)①电能;电能; ②负;Fe-2e-===Fe2+;氧化
③正;2H++2e-===H2↑;还原
【解析】原电池是将化学能转变为电能的装置,活泼金属作负极,发生氧化反应,不活泼材料作正极,发生还原反应。电流表正极应接原电池正极,电流表负极应接原电池负极。
17.【答案】(1)不相同
(2)负;
2Al-6e-===2Al3+;正;6H++6e-===3H2↑;2Al+6H+==2Al3++3H2↑
(3)负极;铝与氢氧化钠溶液反应,镁与氢氧化钠溶液不反应;
Al-3e-+4OH-==AlO2-+2H2O
(4)另一个电极材料的活泼性和电解质溶液的氧化性
【解析】实验①中镁比铝活泼,镁作原电池的负极,铝作原电池的正极,电流计指针偏向铝;实验②中铝比铜活泼,铝作原电池的负极,铜作原电池的正极,电流计指针偏向铜;实验③中铝失去电子,发生氧化反应,③为负极,石墨为正极,电流计指针偏向石墨。
18.【答案】(答案合理即可)
【解析】因为总反应式为Fe+H2SO4===FeSO4+H2↑,所以负极为Fe,正极可为Cu、Ag或石墨,电解质溶液为稀硫酸,按原电池示意图一般形式画出装置图。
19.【答案】(1)原电池 正 还原
(2)阴 2H++2e-===H2↑ 2NaCl+2H2O2NaOH+H2↑+Cl2↑ 增强 (3)1.12
【解析】B中两电极相同,不能为原电池,A中锌与硫酸铜可以发生自发的氧化还原反应,Zn+Cu2+===Zn2++Cu,锌是负极Zn-2e-===Zn2+;Cu是正极,Cu2++2e-===Cu。因此A装置是原电池。
(2)B装置是电解池,b电极与原电池的负极相连作阴极,氢离子放电,电极反应式为2H++2e-===H2↑(或2H2O+2e-===H2↑+2OH-)。A电极与原电池的正极相连,作阳极,氯离子放电,2Cl--2e-===Cl2↑,合并得到B装置中总反应2NaCl+2H2O2NaOH+H2↑+Cl2↑,有氢氧化钠强碱生成,因此溶液的碱性增强。
(3)若工作一段时间后,当Zn片质量减少3.25
g时,即0.05
mol,根据Zn-2e-===Zn2+可知导线中转移电子0.05
mol×2=0.1
mol。a极电极反应式为2Cl--2e-===Cl2↑,则根据电子转移守恒可知逸出的氯气在标准状况下的体积为0.05
mol×22.4
L·mol-1=1.12
L。
20.【答案】(1)2NaCl+2H2O2NaOH+Cl2↑+H2↑
(2)正
(3)①1 ②22.4 ③×100%
【解析】(1)电解饱和食盐水的化学方程式为2NaCl+2H2O2NaOH+Cl2↑+H2↑。
(2)C极一侧滴酚酞溶液不变红色,该极无OH-生成,C是阳极,A是正极。
(3)①标准状况下11.2
LCl2的物质的量是0.5mol,每生成1
mol
Cl2转移2
mol
e-,至少转移1
mol
e-;
②铅蓄电池放电的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,每消耗2
mol
H2SO4,转移2
mol
e-,可生成1
mol
H2,标准状况时,H2的体积为22.4
L;
③消耗amol
H2SO4,转移amol电子,生成H2、Cl2、NaOH的物质的量分别为mol、mol、amol,w(NaOH)=×100%。
21.【答案】(1)负极 H2-2e-+2OH-===2H2O
(2)阳极 铁极
(3)减小 Cu2++2e-===Cu
【解析】(1)通入氢气的电极为负极,由于电解质溶液是碱性的,所以该电极反应式为H2-2e-+2OH-===2H2O。
(2)由于石墨电极与电源的正极连接,所以石墨电极为阳极,反应一段时间后,在乙装置中滴入酚酞溶液,溶液中的H+在阴极(Fe电极)放电,破坏了附近的水的电离平衡,该区域的溶液显碱性,因此铁极的溶液先变红。
(3)如果粗铜中含有锌、银等杂质,因为粗铜中有活动性比Cu强的金属失去电子,而得到电子的只有Cu2+,所以丙装置中反应一段时间,硫酸铜溶液浓度会减小;精铜电极上的电极反应式为Cu2++2e-===Cu。
一、单选题(共15小题)
1.常温下用石墨作电极,电解100
mL
0.1
mol·L-1的Cu(NO3)2和0.1
mol·L-1的AgNO3组成的混合溶液,当某一电极上生成的气体在标准状况下体积为1.12
L
时,假设溶液体积不变,下列说法正确的是( )
A.
阴极增重1.4
g
B.
所得溶液pH<1
C.
阴极增重0.64
g
D.
所得溶液pH>1
2.化学电池在通讯、交通及日常生活中有着广泛的应用。目前常用的镍镉(Ni-Cd)电池,其电池总反应可以表示:
Cd+2NiO(OH)+2H2O2Ni(OH)2+Cd(OH)2
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是( )
①以上反应是可逆反应 ②以上反应不是可逆反应 ③充电时化学能转变为电能 ④放电时化学能转变为电能
A.
①③
B.
②④
C.
①④
D.
②③
3.由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎。下图是氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是( )
A.
a处通入氧气,b处通入氢气
B.
该装置中只涉及两种形式的能量转化
C.
电池正极电极反应式为O2+2H2O+4e-===4OH-
D.
P-型半导体连接的是电池负极
4.下列有关金属铁的腐蚀与防护,说法正确的是( )
A.
酸雨后易发生析氢腐蚀、炒锅存留盐液时易发生吸氧腐蚀
B.
当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.
铁与电源正极连接可实现电化学保护
D.
将钢管与铜管一起堆放时可保护钢管少受腐蚀
5.钢铁发生吸氧腐蚀时,正极上发生的电极反应是( )
A.
2H++2e-===H2↑
B.
Fe2++2e-===Fe
C.
2H2O+O2+4e-===4OH-
D.
Fe3++e-===Fe2+
6.下列金属的防护方法不正确的是( )
A.
对健身器材涂油漆以防止生锈
B.
对某些工具的“机械转动部位”选用刷油漆的方法来防锈
C.
用牺牲锌块的方法来保护船体
D.
自行车的钢圈上镀上一层Cr防锈
7.图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。下列判断正确的是( )
A.
滤纸上c点附近会变红色
B.
Cu电极质量减小,Pt电极质量增大
C.
Z中溶液的pH先减小,后增大
D.
溶液中的向Cu电极定向移动
8.关于镀铜和电解精炼铜,下列说法中正确的是( )
A.
都用粗铜作阳极、纯铜作阴极
B.
电解液的成分都保持不变
C.
阳极反应都只有Cu-2e-===Cu2+
D.
阴极反应都只有Cu2++2e-===Cu
9.关于钢铁腐蚀与防护的说法不正确的是( )
A.
钢铁的吸氧腐蚀和析氢腐蚀的负极反应式均为Fe-2e-===Fe2+
B.
钢铁发生吸氧腐蚀时,正极反应式为O2+2H2O+4e-===4OH-
C.
地下钢管连接镁块是采用牺牲阳极的阴极保护法
D.
用外加电流的阴极保护法防止钢铁腐蚀时,钢铁接电源的正极
10.将图1所示装置中的盐桥(琼脂?饱和KCl溶液)换成铜导线与石墨棒连接得到图2所示装置,发现电流计指针仍然有偏转。下列说法正确的是( )
A.
图1中,铁棒质量减少5.6
g,则甲池NaCl溶液的质量增加5.6
g
B.
图1中的石墨电极与图2中乙池石墨a电极的电极反应式相同
C.
两图所示装置的能量变化均是将化学能转化为电能
D.
图2中电子流向为Fe→电流计→石墨a→石墨b→铜丝→石墨c→Fe
11.某原电池装置如图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是( )
A.
正极反应为AgCl+e-===Ag+Cl-
B.
放电时,交换膜右侧溶液中有大量白色沉淀生成
C.
若用NaCl溶液代替盐酸,则电池总反应随之改变
D.
当电路中转移0.01
mol
e-时,交换膜左侧溶液中约减少0.02
mol离子
12.关于铅蓄电池的说法正确的是( )
A.
在放电时,正极发生的反应是Pb(s)+SO(aq)-2e-===PbSO4(s)
B.
在放电时,该电池的负极材料是铅板
C.
在充电时,电池中硫酸的浓度不断变小
D.
在充电时,阳极发生的反应是PbSO4(s)+2e-===Pb(s)+SO(aq)
13.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。下列有关说法正确的是( )
A.
检测时,电解质溶液中的H+向负极移动
B.
若有0.4
mol电子转移,则在标准状况下消耗4.48
L氧气
C.
电池反应的化学方程式为CH3CH2OH+O2===CH3COOH+H2O
D.
正极上发生的反应为O2+4e-+2H2O===4OH-
14.为探究钢铁的吸氧腐蚀原理设计了如图所示的装置,下列有关说法中错误的是( )
A.
正极的电极反应方程式为O2+2H2O+4e-===4OH-
B.
将石墨电极改成Mg电极,难以观察到铁锈生成
C.
若向自来水中加入少量NaCl(s),可较快地看到铁锈
D.
分别向铁、石墨电极附近吹入O2,前者铁锈出现得快
15.下图为铜锌原电池示意图,下列说法正确的是( )
A.
锌片逐渐溶解
B.
烧杯中溶液逐渐呈蓝色
C.
电子由铜片通过导线流向锌片
D.
锌为正极,铜为负极
二、实验题(共3小题)
16.某同学利用生活中或实验室中常用的物品,根据氧化还原反应知识和电化学知识,自己动手设计了一个原电池。请填写下列空白:
(1)实验原理:Fe+2H+===Fe2++H2↑
(2)实验用品:电极(______、______)、稀硫酸、______、________、耳机(或者电流表)(填写所缺的实验用品)。
(3)实验装置如图。
(4)原电池设计及注意的问题:
①按如图所示装置连接好实验仪器,注意观察(耳朵听)耳机是否有声音发出,如果没有,可将原电池的两个电极中的一极接触耳机插头上的一极(注意:接触的同时耳机的另一个极是连接在原电池的另一个电极上的),这时可以听见耳机发生“嚓嚓嚓……”的声音。其原因是在原电池中,由化学能转化为____________,在耳机中又由__________转化为声音这种能量;
②如果将装置中的耳机改为电流表,则铁钉应该接电流表的________极,电极反应式为_____________,发生了________反应;
③铜钉应该接电流表的________极,电极反应式为_____________,发生了_________反应。
17.某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下表:
试根据表中的实验现象完成下列问题:
(1)实验①、②中铝所作的电极(指正极或负极)________(填“相同”或“不相同”)。
(2)实验③中铝为________极,电极反应式为________________;石墨为________极,电极反应式为_______________;电池总反应式为_____________________________。
(3)实验④中铝作负极还是正极?_____,理由是___________________________________,铝电极的电极反应式为_______________________________。
(4)根据实验结果总结出影响铝在原电池中作正极或负极的因素为_____________________。
18.已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液、Fe2(SO4)3溶液、硫酸。设计一种以铁和稀硫酸反应为原理的原电池,要求画出装置图(需标明电极材料及电池的正、负极)。
三、填空题(共3小题)
19.如图所示装置中电极a、b均为碳棒,两烧杯中所盛溶液均为500mL1.0mol·L-1。
(1)A为________池,(填“原电”或“电解”),其中的Ag极为________极,发生________(填“氧化”或“还原”)反应。
(2)B装置中的电极b极为________极,电极反应式为__________________________________,
总反应的化学方程式为____________________________________________________。
经过一段时间后,B装置中溶液的碱性________(填“增强”、“减弱”或“不变”)
(3)若工作一段时间后,当Zn片质量减少3.25
g时,a极逸出的气体在标准状况下的体积为________L。
20.如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。
已知:铅蓄电池在放电时发生下列电极反应:
负极:Pb+-2e-===PbSO4
正极:PbO2+4H+++2e-===PbSO4+2H2O
(1)请写出电解饱和食盐水的化学方程式____________________________________。
(2)若在电解池中C极一侧滴酚酞溶液,电解一段时间后未呈红色,说明铅蓄电池的A极为________极。
(3)用铅蓄电池电解1
L饱和食盐水(食盐水足量,密度为1.15
g·cm-3)时,
①若收集到11.2
L(标准状况下)氯气,则至少转移电子________mol。
②若铅蓄电池消耗H2SO42
mol,则可收集到H2的体积(标准状况下)为________L。
③若消耗硫酸amol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出)________________(用含a的代数式表示)。
21.某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
根据要求回答相关问题:
(1)通入氢气的电极为________(填“正极”或“负极”),负极的电极反应式为____________________。
(2)石墨电极为________(填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,________(填“铁极”或“石墨极”)区的溶液先变红。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”)。精铜电极上的电极反应式为____________________________
________________________________________________________________________。
答案解析
1.【答案】B
【解析】阴极可以放电的离子依次为0.01
mol
Ag+、0.01
mol
Cu2+,阳极可以放电的阴离子只有OH-;当阳极生成1.12
L
O2时,电路中通过电子:n(e-)=0.05
mol×4=0.2
mol,此时Ag+、Cu2+已全部析出,质量:0.01
mol×108
g·mol-1+0.01
mol×64
g·mol-1=1.72
g;因为当Ag+、Cu2+全部析出以后,相当于电解水,H+不再增加,所以生成的H+所带电荷与0.01
mol
Ag+、0.01
mol
Cu2+所带电荷相等;则溶液中生成:c(H+)=0.3
mol·L-1,pH<1。
2.【答案】B
【解析】Ni-Cd电池的充、放电条件不相同,因此电池的充、放电反应不属于可逆反应。
3.【答案】C
【解析】根据LED中电子移动方向可判断N-型半导体与电池负极相连,
a处为负极,应通入氢气,b处通入氧气,P-型半导体与电池正极相连,
A、D错误;该装置主要涉及化学能、电能、光能三种形式的能量转化,B错误;在KOH溶液中,正极电极反应式为O2+2H2O+4e-===4OH-,C正确。
4.【答案】A
【解析】酸雨后溶液显酸性,容易发生析氢腐蚀,炒锅存留盐液是中性溶液,较易发生吸氧腐蚀,A正确;金属活动性Zn>Fe>Sn,所以镀锡铁镀层破损时,Fe作原电池的负极首先被腐蚀,而镀锌铁镀层破损时,由于Fe作正极,被保护起来,前者更易被腐蚀,B错误;铁与电源负极连接可实现电化学保护,C错误;将钢管与铜管一起堆放形成原电池,钢管作为负极,受腐蚀的程度增加,D错误。
5.【答案】C
【解析】钢铁发生吸氧腐蚀,正极反应为2H2O+O2+4e-===4OH-,C正确。
6.【答案】B
【解析】涂油漆可以起到避免金属和电解质溶液接触形成原电池的目的,A正确;油漆保护层在机械转动部位很容易磨损,起不到保护层的作用,应选用润滑油来达到防锈的目的,B错误;锌、铁与电解液形成原电池时,锌作负极被腐蚀,铁作正极被保护,C正确;钢圈上镀上一层Cr,阻断了铁与氧气的接触,D正确。
7.【答案】A
【解析】紫红色斑即Mn向d端扩散,根据阴离子向阳极移动的原理,可知d端为阳极,b为正极,a为负极,c为阴极。c点NaCl溶液中H+放电,2H2O+2e-===H2↑+2OH-,c点附近会变红色,A正确;Z中Cu电极和a相连,为阴极,Cu2++2e-===Cu,Pt极为阳极,2H2O-4e-===4H++O2↑,pH减小,B、C错误;Z为电解池,池内阴离子向阳极移动,即向Pt极移动,D错误。
8.【答案】D
【解析】A项,电镀时镀件作阴极;B项,电解精炼铜时电解液成分改变;C项,电解精炼铜时,杂质若有比铜活泼的金属(如锌),则还会发生Zn-2e-===Zn2+的反应。
9.【答案】D
【解析】钢铁的吸氧腐蚀和析氢腐蚀都是铁失去电子作负极,电极反应式为Fe-2e-===Fe2+,钢铁发生吸氧腐蚀时O2+2H2O+4e-===4OH-,A、B正确;地下钢管连接镁块,镁比铁活泼,作负极,铁作正极得到保护,C正确;用外加电流的阴极保护法防止钢铁腐蚀时,钢铁连接电源的负极,D错误。
10.【答案】B
【解析】图1为原电池,Fe为负极,电极反应:Fe-2e-===Fe2+,盐桥中的阴离子移向负极,增加质量大于5.6
g,A错误;图1中石墨为正极,电极反应:Cu2++2e-===Cu,图2为电解池,图2乙池中石墨a是阴极,电极反应:Cu2++2e-===Cu,B正确;原电池是将化学能转化为电能,电解池是将电能转化为化学能,C错误;电子不能在溶液中移动,图2中电子流向应为Fe→电流计→石墨a,石墨b→铜丝→石墨c,D错误。
11.【答案】D
【解析】原电池正极发生还原反应,该原电池正极反应式为Cl2+2e-===2Cl-,A项不正确;该原电池放电时,负极材料中的Ag被氧化为Ag+,Ag+与附近的Cl-反应生成AgCl白色沉淀。交换膜右侧溶液中无大量AgCl白色沉淀生成,B项不正确;由原电池负极反应Cl-+Ag-e-===AgCl↓和正极反应Cl2+2e-===2Cl-可知,若用NaCl溶液代替盐酸,电池总反应不变,C项不正确;由原电池的负极反应Cl-+Ag-e-===AgCl↓可知,当电路中转移0.01
mol
e-时,交换膜左侧溶液中减少0.01
mol
Cl-,同时约有0.01
mol
H+通过阳离子交换膜移至右侧,故交换膜左侧溶液中约减少0.02
mol离子,D项正确。
12.【答案】B
【解析】蓄电池反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,正极得电子,发生还原反应,电极反应式为PbO2+4H++SO+2e-===PbSO4+2H2O,A错误;负极失电子,发生氧化反应,电极反应式为Pb-2e-+SO===PbSO4,铅板是负极材料,B正确;充电装置是电解池,阳极失电子,与原电池正极反应相反,为PbSO4+2H2O-2e-===PbO2+4H++SO,阴极得电子,与原电池负极反应相反,为PbSO4+2e-===Pb+SO,硫酸的浓度增大,CD错误。
13.【答案】C
【解析】A项,检测时,电解质溶液中的H+移向正极;B项,若反应中有0.4
mol电子转移,则在标况下消耗的O2体积为2.24
L;D项,电解质溶液呈酸性,正极上发生的反应为O2+4H++4e-===2H2O。
14.【答案】D
【解析】如果铁发生吸氧腐蚀,则铁是负极,失电子被氧化成Fe2+,在正极氧气得电子发生还原反应,电极反应式:2H2O+O2+4e-===4OH-。将氧气吹向石墨电极形成原电池反应,加快腐蚀速率,A正确,D错误;向自来水中加入NaCl(s),可使电解质溶液的导电能力增强,加快腐蚀速率,C正确;若将石墨电极换成Mg电极,Mg比Fe活泼,负极为Mg,Fe被保护,难以看到铁生锈,B正确。
15.【答案】A
【解析】在铜锌原电池中,锌的活动性大于铜,锌为负极、铜为正极。负极锌失去电子不断溶解,在外电路中电子由锌电极流向铜电极;溶液中的氢离子,在正极铜表面得到电子被还原,有氢气产生,铜电极保持不变,溶液中不存在铜离子,不能使溶液成蓝色。
16.【答案】(2)铁钉或铁条;铜钉(其他的惰性电极如铅笔芯、铂等都正确); 烧杯;导线
(4)①电能;电能; ②负;Fe-2e-===Fe2+;氧化
③正;2H++2e-===H2↑;还原
【解析】原电池是将化学能转变为电能的装置,活泼金属作负极,发生氧化反应,不活泼材料作正极,发生还原反应。电流表正极应接原电池正极,电流表负极应接原电池负极。
17.【答案】(1)不相同
(2)负;
2Al-6e-===2Al3+;正;6H++6e-===3H2↑;2Al+6H+==2Al3++3H2↑
(3)负极;铝与氢氧化钠溶液反应,镁与氢氧化钠溶液不反应;
Al-3e-+4OH-==AlO2-+2H2O
(4)另一个电极材料的活泼性和电解质溶液的氧化性
【解析】实验①中镁比铝活泼,镁作原电池的负极,铝作原电池的正极,电流计指针偏向铝;实验②中铝比铜活泼,铝作原电池的负极,铜作原电池的正极,电流计指针偏向铜;实验③中铝失去电子,发生氧化反应,③为负极,石墨为正极,电流计指针偏向石墨。
18.【答案】(答案合理即可)
【解析】因为总反应式为Fe+H2SO4===FeSO4+H2↑,所以负极为Fe,正极可为Cu、Ag或石墨,电解质溶液为稀硫酸,按原电池示意图一般形式画出装置图。
19.【答案】(1)原电池 正 还原
(2)阴 2H++2e-===H2↑ 2NaCl+2H2O2NaOH+H2↑+Cl2↑ 增强 (3)1.12
【解析】B中两电极相同,不能为原电池,A中锌与硫酸铜可以发生自发的氧化还原反应,Zn+Cu2+===Zn2++Cu,锌是负极Zn-2e-===Zn2+;Cu是正极,Cu2++2e-===Cu。因此A装置是原电池。
(2)B装置是电解池,b电极与原电池的负极相连作阴极,氢离子放电,电极反应式为2H++2e-===H2↑(或2H2O+2e-===H2↑+2OH-)。A电极与原电池的正极相连,作阳极,氯离子放电,2Cl--2e-===Cl2↑,合并得到B装置中总反应2NaCl+2H2O2NaOH+H2↑+Cl2↑,有氢氧化钠强碱生成,因此溶液的碱性增强。
(3)若工作一段时间后,当Zn片质量减少3.25
g时,即0.05
mol,根据Zn-2e-===Zn2+可知导线中转移电子0.05
mol×2=0.1
mol。a极电极反应式为2Cl--2e-===Cl2↑,则根据电子转移守恒可知逸出的氯气在标准状况下的体积为0.05
mol×22.4
L·mol-1=1.12
L。
20.【答案】(1)2NaCl+2H2O2NaOH+Cl2↑+H2↑
(2)正
(3)①1 ②22.4 ③×100%
【解析】(1)电解饱和食盐水的化学方程式为2NaCl+2H2O2NaOH+Cl2↑+H2↑。
(2)C极一侧滴酚酞溶液不变红色,该极无OH-生成,C是阳极,A是正极。
(3)①标准状况下11.2
LCl2的物质的量是0.5mol,每生成1
mol
Cl2转移2
mol
e-,至少转移1
mol
e-;
②铅蓄电池放电的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,每消耗2
mol
H2SO4,转移2
mol
e-,可生成1
mol
H2,标准状况时,H2的体积为22.4
L;
③消耗amol
H2SO4,转移amol电子,生成H2、Cl2、NaOH的物质的量分别为mol、mol、amol,w(NaOH)=×100%。
21.【答案】(1)负极 H2-2e-+2OH-===2H2O
(2)阳极 铁极
(3)减小 Cu2++2e-===Cu
【解析】(1)通入氢气的电极为负极,由于电解质溶液是碱性的,所以该电极反应式为H2-2e-+2OH-===2H2O。
(2)由于石墨电极与电源的正极连接,所以石墨电极为阳极,反应一段时间后,在乙装置中滴入酚酞溶液,溶液中的H+在阴极(Fe电极)放电,破坏了附近的水的电离平衡,该区域的溶液显碱性,因此铁极的溶液先变红。
(3)如果粗铜中含有锌、银等杂质,因为粗铜中有活动性比Cu强的金属失去电子,而得到电子的只有Cu2+,所以丙装置中反应一段时间,硫酸铜溶液浓度会减小;精铜电极上的电极反应式为Cu2++2e-===Cu。
