8.2.1 金属的化学性质 强化训练 人教版九年级化学下册(含答案)
文档属性
| 名称 | 8.2.1 金属的化学性质 强化训练 人教版九年级化学下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 172.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-06 00:00:00 | ||
图片预览



文档简介
8.2.1 金属的化学性质
强化训练
【题组A】金属与氧气反应
1、镁、铝、铁、铜、金五种金属中,常温下易与氧气反应的是 , ;在加热条件下能与氧气反应的是 , ;即使高温也不与氧气反应的是_________;它们金属活动性由强到弱的顺序是__________________
2、我们常说“真金不怕火炼”的原因是( )
A.金的熔点高 B.金的硬度大
C.金的密度大 D.金不活泼,高温时也不与氧气反应
3、下列金属在自然界中能以单质形式存在的是( )
A Fe B Na C Al D Au
4、铝在常温下能与氧气发生反应,那么我们还使用铝制餐具是因为 ,不宜用钢刷来擦洗铝制餐具的原因是 。
【题组B】金属与酸的反应
56038751352551、某同学研究化学反应中的放热现象,分别用等质量的镁和锌与足量的稀盐酸进行实验,
装置如图所示。下列有关现象和结论中不正确的是( )
A.两只试管中都产生大量气泡,手触试管外壁有热感
B.通过气球膨胀的大小能推导镁和铁的金属活动性强弱关系
C.收集到的气体在点燃前一定要检验纯度
D.若将药品换成生石灰和水,则观察到气球先膨胀,冷却至室温后恢复原状
5198110698502、一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,
下列说法不正确的是( )
A、t1时,产生氢气的质量锌比铁大 B、t1时,产生氢气的速率锌比铁大
C、t2时,参加反应锌的质量与铁相同 D、t2时,锌、铁消耗的盐酸质量相同
3、Fe、Mg、Al 三种金属分别跟稀盐酸充分反应,得到相同质量的氢气,其原因有:
① Fe、Mg、Al 的质量相等,盐酸足量;
② Fe、Mg、Al 的质量比为 56:24:27,盐酸足量;
③ Fe、Mg、Al 的质量比为 28:12:9,盐酸足量;
④ Fe、Mg、Al 均为过量。所用盐酸的溶质质量分数和质量都相同。 你认为可能的原因是 ( )
A.③④ B.①② C.①③ D.②③
50863502076454、(已知X、Y在化合物中均为+2价)等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( )
两种金属的相对原子质量:XB.t1时,消耗盐酸的质量:X=Y
C.t2时,消耗金属的质量:X>Y
D.t3时,消耗金属的质量:X=Y
5、现有两种金属单质组成的混合物.向100g稀盐酸中加入该混合物,加入混合物的质量与生成氢气的质量关系如图所示.下列说法正确的是( )
A. 若混合物为Zn和Cu,则m大于0.2?g
B. 若混合物为Zn和Fe,则m可能是0.2?g
C. 若混合物为Fe和Cu,稀盐酸中溶质质量分数为7.3%
D. 若混合物为Fe和Cu,m为0.1?g,则混合物中Fe和Cu的质量比为1:1
42608504572006、甲、乙两烧杯内盛有等质量、等质量分数的盐酸.将镁逐渐加入甲烧杯,铁逐渐加入乙烧杯,测量加入的金属质量m和相应的烧杯内物质质量变化量△m,画出△M﹣m曲线oac和obc的示意图,如图所示.根据图中信息,下列说法错误的是( )
A.m1:m2=3:7
B.m1﹣△M1<m2﹣△M2
C.曲线oac表示的是甲烧杯中△M与m的变化关系
D.当乙烧杯内加入铁的质量为m1时,溶液中溶质不止一种
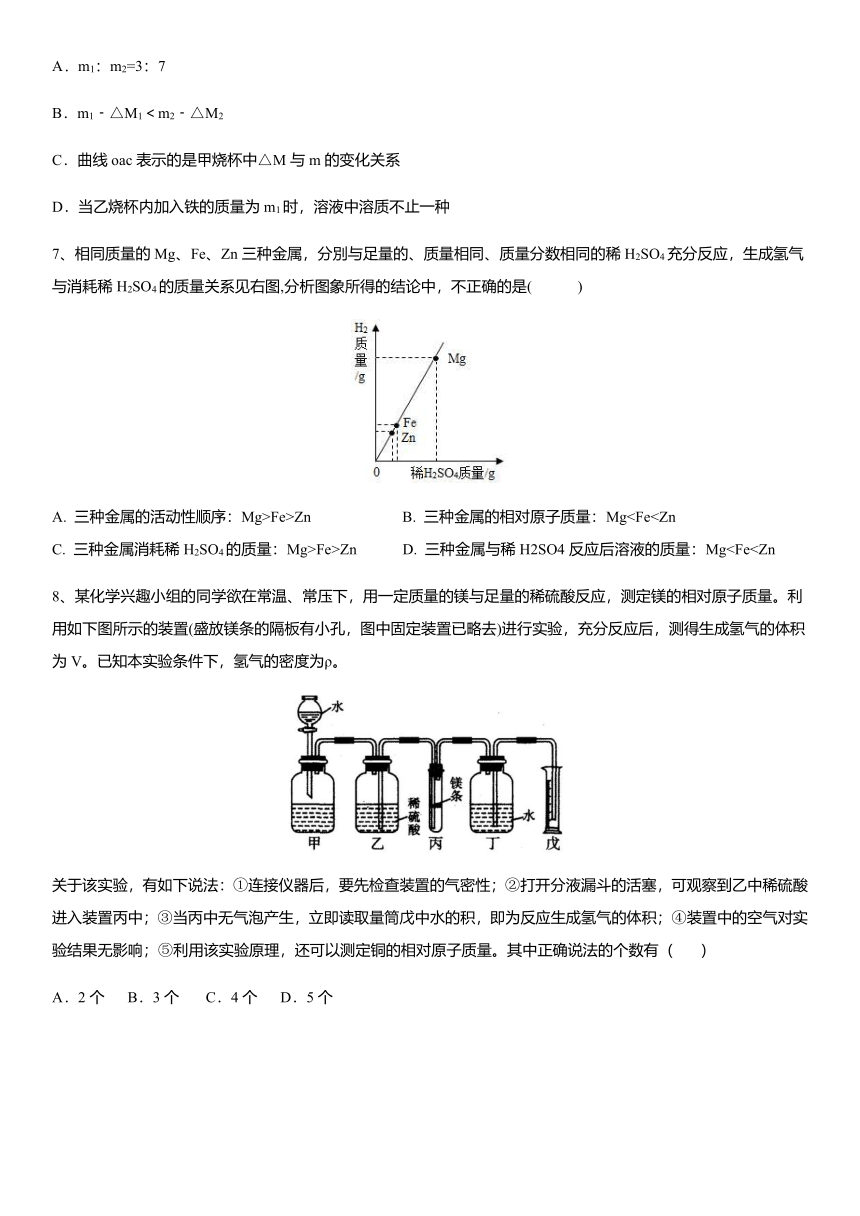
7、相同质量的Mg、Fe、Zn三种金属,分別与足量的、质量相同、质量分数相同的稀H2SO4充分反应,生成氢气与消耗稀H2SO4的质量关系见右图,分析图象所得的结论中,不正确的是( )
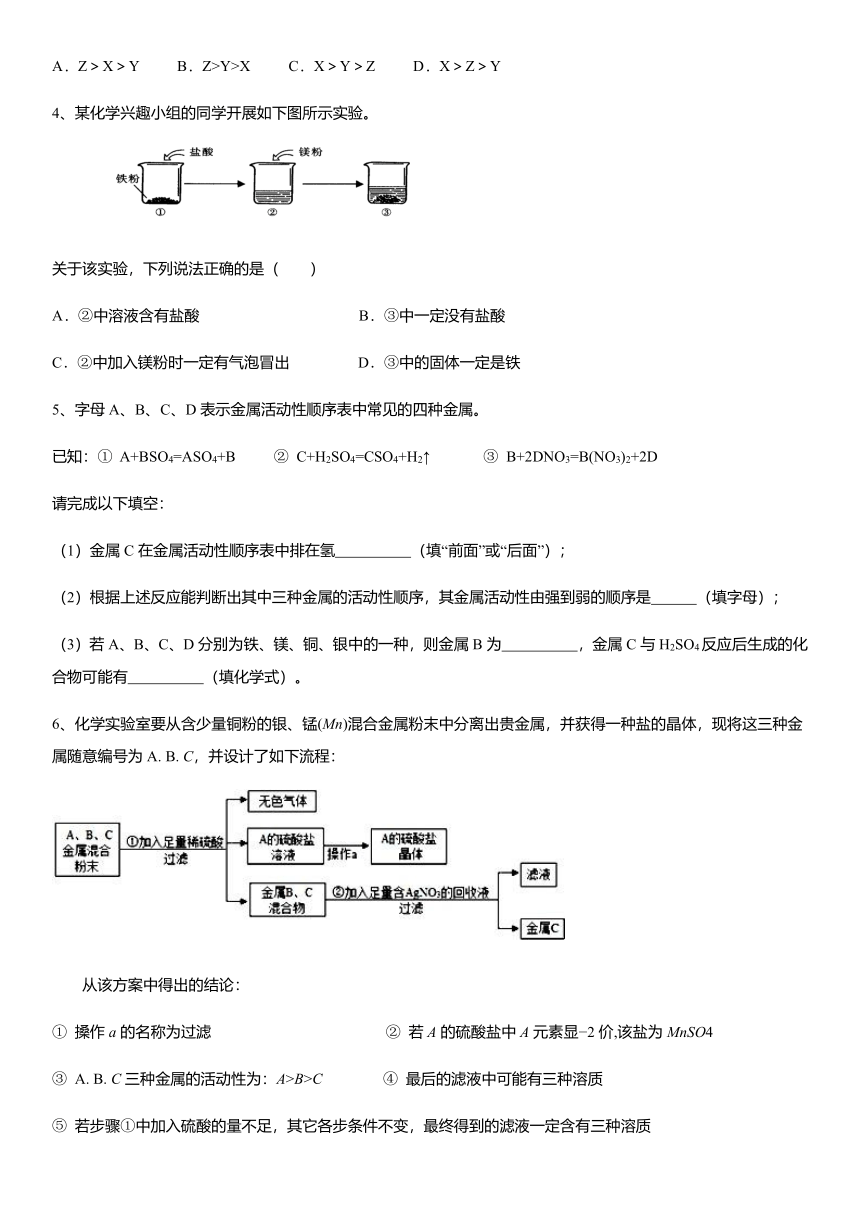
A. 三种金属的活动性顺序:Mg>Fe>Zn B. 三种金属的相对原子质量:MgC. 三种金属消耗稀H2SO4的质量:Mg>Fe>Zn D. 三种金属与稀H2SO4反应后溶液的质量:Mg8、某化学兴趣小组的同学欲在常温、常压下,用一定质量的镁与足量的稀硫酸反应,测定镁的相对原子质量。利用如下图所示的装置(盛放镁条的隔板有小孔,图中固定装置已略去)进行实验,充分反应后,测得生成氢气的体积为V。已知本实验条件下,氢气的密度为ρ。
关于该实验,有如下说法:①连接仪器后,要先检查装置的气密性;②打开分液漏斗的活塞,可观察到乙中稀硫酸进入装置丙中;③当丙中无气泡产生,立即读取量筒戊中水的积,即为反应生成氢气的体积;④装置中的空气对实验结果无影响;⑤利用该实验原理,还可以测定铜的相对原子质量。其中正确说法的个数有(?? ???)?
A.2个??????B.3个???????C.4个??????D.5个
9、 (6分)已知某粗铜粉末中含有少量的铁、锌和金。某化学兴趣小组的同学为测定该粗铜粉末中铜的质量分数,开展如下实验探究:
步骤I:称取质量为m1的粗铜样品;
步骤Ⅱ:向样品中逐滴加入足量的稀盐酸,充分反应;
步骤Ⅲ:过滤,将滤渣洗涤、干燥后称量,质量为m2;
步骤IV:将步骤Ⅲ所得固体在空气中充分灼烧,冷却至室温后称量,质量为m3。
请回答下列问题: (1) 步骤Ⅱ的目的是 ;
(2) 判断步骤Ⅱ中加入的稀盐酸足量的方法是 :
(3) 步骤IV中反应的化学方程式为 ;
(4) 按此方法测得粗铜中铜的质量分数为 (用m1、m2、m3的代数式表示)。
【题组C】金属活动性顺序实验探究
1、小明为探究Cu、Al、Ag的金属活动性顺序,做了如下两个实验。请分析实验,完成填空。
(1) 试管①中观察到的现象是:铝丝表面附着一层 固体,溶液颜色变浅。
(2) 试管②中发生了化学反应,现象明显,该反应的化学方程式是____________。
(3) 通过实验探究,Cu、Al、Ag三种金属活动性由强到弱的顺序是______。
(4) 请你设计再设计一个实验,验证Cu、Al、Ag三种金属活动性顺序?
2、以X、Y、Z三种金属活动性的实验探究过程如下,①取大小相同的三种金属片分别放入CuSO4溶液中一段时间后,X、Z表面出现红色物质,Y没有明显现象;②取大小相等的X、Z两种金属片,分别放入相同的稀盐酸中,X、Z表面都有气泡产生,但X产生气泡速度明显比Z的快,则X、Y、Z三种金属的活动性顺序是( )
A.X>Y>Z B.Z>Y>X C.X>Z>Y D.Z>X>Y
3、X,Y,Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性是( )
①Z + YSO4 == ZSO4 + Y ② X + YSO4 == XSO4 + Y ③ Z + H2SO4 == ZSO4 + H2↑ ④ X + H2SO4 不反应
A.Z>X>Y B.Z>Y>X C.X>Y>Z D.X>Z>Y
4、某化学兴趣小组的同学开展如下图所示实验。
5651508890
关于该实验,下列说法正确的是( )
A.②中溶液含有盐酸 B.③中一定没有盐酸
C.②中加入镁粉时一定有气泡冒出 D.③中的固体一定是铁
5、字母A、B、C、D表示金属活动性顺序表中常见的四种金属。
已知:① A+BSO4=ASO4+B ② C+H2SO4=CSO4+H2↑ ③ B+2DNO3=B(NO3)2+2D
请完成以下填空:
(1)金属C在金属活动性顺序表中排在氢 (填“前面”或“后面”);
(2)根据上述反应能判断出其中三种金属的活动性顺序,其金属活动性由强到弱的顺序是 (填字母);
(3)若A、B、C、D分别为铁、镁、铜、银中的一种,则金属B为 ,金属C与H2SO4反应后生成的化合物可能有 (填化学式)。
6、化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐的晶体,现将这三种金属随意编号为A. B. C,并设计了如下流程:
从该方案中得出的结论:
① 搡作a的名称为过滤 ② 若A的硫酸盐中A元素显?2价,该盐为MnSO4
③ A. B. C三种金属的活动性为:A>B>C ④ 最后的滤液中可能有三种溶质
⑤ 若步骤①中加入硫酸的量不足,其它各步条件不变,最终得到的滤液一定含有三种溶质
上述结论正确的是 ( )
A. ②③④ B. ①②③ C. ②③④⑤ D. ②③⑤
【题组D】金属与盐溶液的反应
类型1. 一种金属加入一种较弱的金属化合物溶液中
1、向Cu(NO3)2溶液中加入一定量的铁粉充分反应,下列情况中可能出现的是( )
①溶液中有Fe2+、Cu2+、不溶物为Cu ②溶液中有Fe2+、Cu2+、不溶物为Fe
③溶液中只有Cu2+、不溶物为Fe ④溶液中只有Fe2+、不溶物为Fe,Cu
A.①③ B.①④ C.②③ D.③④
2、向氯化铜溶液加入一定量的锌粉充分反应,下列情况中可能出现的是 ( )
①溶液中有 Zn2+、Cu2+ ,不溶物为Cu ②溶液中有 Zn2+、Cu2+ ,不溶物为 Zn
③溶液只有 Zn2+ ,不溶物为 Zn ④ 溶液只有 Zn2+ ,不溶物为 Zn 、Cu
A.①③ B.②③ C ①④ D.③④
3、向硫酸铜溶液中加入一定量的铁粉充分反应,下列说法正确的是( )
A.滤渣中一定有铁 B.滤渣中一定有铜 C.滤液中一定有Fe3+ D.滤液中一定有Cu2+
4、将硝酸银与一定量的锌粉充分反应,向滤液中加入少量盐酸,没有沉淀生成,则( )
A.向滤渣中滴加稀盐酸一定有气泡产生 B.滤渣可能有两种金属
C.滤渣中一定有锌 D.滤液中可能有硝酸银和硝酸锌
5、把一定质量的锌粉放入Cu(NO3)2溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气体产生.根据以上现象,下列判断滤渣中的成分正确是( )
A.只有Cu B.只有Zn
C.一定有Cu,可能有Zn D.一定有Zn和Cu
6、向硫酸铜溶液中加入一定量的铁粉充分反应后过滤。下列情况可能出现的是( )
① 滤液中有硫酸亚铁、硫酸铜,滤出的固体为铜 ② 滤液中有硫酸亚铁、硫酸铜,滤出的固体为铁
③ 滤液中只有硫酸亚铁,滤出的固体为铁、铜 ④ 滤液中只有硫酸铜,滤出的固体为铁、铜
A.①④ B.①③ C.②③ D.③④
类型2:一种金属加入到几种金属化合物溶液中
1、某溶液中仅含有AgNO3和Cu(NO3)2两种溶质,将其分成A、B两份,各加入一定质量的锌粉,充分反应后,过滤,洗涤,分别得到滤渣和滤液。
(1)将A得到的滤渣加入到稀盐酸中,有气泡产生,则该滤渣中含有的物质是_________,滤液中含有的溶质
是_________。
(2)往B得到的滤液中滴稀盐酸,有白色沉淀生成,则对应的滤渣中含有_______,滤液中含有的溶质是_____。
2、NaNO3、AgNO3、Cu(NO3)2的混合溶液中加入一定量Fe,充分反应后过滤,
(1)若滤渣中加入盐酸后有气泡产生,则滤渣中一定有_________,此时滤液中所含物质是(不包括水,下同) _________。
(2)若滤液中加入铁片无明显变化,则滤渣中一定有_______,可能有_______,滤液中所含物质是____。
3、向硝酸银、硝酸铜、硝酸锌的混合溶液中,加入一定量的铁粉,充分反应后过滤,得到滤渣和滤液.
(1)若向滤渣中加入稀硫酸,看到有气泡冒出,则滤渣中一定有_________;滤液中一定有的溶质是_____。
(2)若向滤渣中加入稀硫酸,没有气泡冒出,则滤渣中一定有的金属是_________;滤液中一定有的溶质是 ;
4、向AgNO3、Cu(NO3)2的混合溶液中,加入一定量的Zn粉,充分反应后过滤,得到滤液和滤渣,向滤渣中加入稀盐酸。
(1)如果有气泡产生,滤液中含有的溶质是 _________ ;
(2)如果没有气泡产生,滤渣中一定含有的物质是 _________ .
5、在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是( )
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体一定含有铜,一定不含铁和镁
C.滤液中一定含有氯化镁,可能含有氯化铜和氯化亚铁
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
6、向一定质量的硝酸银、硝酸铜的混合溶液中加入锌粉,充分反应后过滤,向滤渣中滴加少量的稀盐酸,无气泡产生。下列相关判断中,正确的是 ( )
A.滤渣中可能含有锌 B.滤渣中一定含有银和铜
C.滤液中可能只有一种溶质 D.滤液中一定有Zn2+ Cu2+ Ag+
7、将一定质量的铁粉加入 Cu(NO3)2 和 AgNO3 的混合溶液中,反应结束后过滤,向滤渣中加入稀盐酸,无明显现象。下列对滤渣和滤液的说法中,不正确的是 ( )
A.滤渣中一定含有银 B.滤液中一定不含Ag+
C.滤渣中可能含有铜 D.滤液中一定含有Fe2+
8、将一定质量的 Zn 加入到 Mg(NO3)2、Fe(NO3)2、AgNO3三种物质的混合溶液中,充分反应 后过滤,滤液仍为浅绿色,下列判断中,正确的是( )
A.滤渣中一定不含单质 Fe B.滤液中一定含有 Ag+
C.滤液中至少含有三种成分 D.反应后固体金属的质量一定变大
9.向CuCl2和FeCl2的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.下列判断正确的是( )
① 滤液中一定含有MgCl2、FeCl2、CuCl2 ② 滤出的固体中一定含有铜,一定不含铁和镁
③ 滤出的固体中一定含有铜,可能含有铁和镁 ④ 滤液中一定含有MgCl2和FeCl2,可能含有CuCl2.
A.①② B.②③ C.③④ D.②④
10.工厂为防止环境污染和回收贵重金属,向含有Cu(NO3)2和AgNO3的废液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣,滤渣中加入稀盐酸,发现有气泡产生,根据上述现象的描述,下列四种判断正确的是( )
A.滤渣中一定有Ag、Cu、Fe
B.滤渣中一定有Ag和Cu,可能含有Fe AgNO3和Cu(NO3)2
C.滤液中一定有含Fe(NO3)2,可能含有AgNO3和Cu(NO3)2
D.滤液中一定含有AgNO3和Cu(NO3)2,可能含有含Fe(NO3)2
11.向AgNO3和Cu(NO3)2混合溶液中加入一定量的铁粉,充分反应后,向滤渣中加入稀盐酸无明显现象。下列说法正确的是( )
A.一定有银生成,一定没有铜生成 B.滤液中一定有Ag+
C.一定有铜生成,可能有银生成 D.滤液阳离子一定有亚铁离子
12.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( )
A.滤渣中一定有银、可能有铜和锌 B.滤滤渣中一定有银和锌、可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银 D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
13.将过量的铁粉加入Cu(NO3)2 和AgNO3 的混合溶液中,充分反应后过滤,下列对滤渣和滤液的说明中,不正确的是( )
A.滤渣中一定含有银 B.向滤渣中滴入稀盐酸,有气泡放出
C.滤液可能为蓝色 D.向滤液中滴入稀盐酸,无明显现象
14.向硝酸铜、硝酸银和硝酸铝的混合溶液中加入一定质量的锌粉,充分反应后,过滤,得到滤渣和滤液。以下判断正确的是( )
A.若滤液为蓝色,则滤渣中一定有银和铜
B.若向滤液中加入稀盐酸无白色沉淀生成,则滤液中一定没有硝酸铜
C.若向滤渣中加入稀盐酸有气体产生,则滤液中只含有硝酸铝和硝酸锌
D.若反应前加入的锌粉质量和反应后滤渣的质量相等,则滤渣中一定不含锌粉和铝粉
15.一定质量的铁粉和锌粉的混合物,加入到硫酸铜溶液中,反应一段时间后,溶液的质量与反应前硫酸铜溶液质量相等。下列说法正确的是( )
A.此时溶液一定呈蓝色 B.此时固体有三种金属
C.锌粉一定反应完了 D.此时溶液中硫酸锌的质量一定小于硫酸亚铁
16.向AgNO3溶液中加入一定质量Fe和Al,充分反应后过滤,得到滤渣和浅绿色滤液。下列说法正确的( )
A.滤液中一定含有Al(NO3)3、Ag NO3 B.滤液中一定含有Fe(NO3)2、Ag NO3
C.滤渣中一定含有Fe D.滤渣中一定含有Ag
8.2.1 金属的化学性质
强化训练
【题组A】金属与氧气反应
1、镁、铝、铁、铜、金五种金属中,常温下易与氧气反应的是 Mg+O2=MgO , 4Al+3O2=2Al2O3 ;在加热条件下能与氧气反应的是 3Fe+2O2Fe3O4 , 2Cu+O2 △ CuO ;即使高温也不与氧气反应的是____金_____;它们金属活动性由强到弱的顺序是______Mg>Al>Fe>Cu>Au_____________
2、我们常说“真金不怕火炼”的原因是( D )
A.金的熔点高 B.金的硬度大
C.金的密度大 D.金不活泼,高温时也不与氧气反应
3、下列金属在自然界中能以单质形式存在的是( D )
A Fe B Na C Al D Au
4、铝在常温下能与氧气发生反应,那么我们还使用铝制餐具是因为 铝与氧气反应生成一层致密的氧化膜,从而阻止铝被进一步氧化 ,不宜用钢刷来擦洗铝制餐具的原因是 容易把其表面的氧化膜除掉,使餐具生锈 。
【题组B】金属与酸的反应
56038751352551、某同学研究化学反应中的放热现象,分别用等质量的镁和锌与足量的稀盐酸进行实验,
装置如图所示。下列有关现象和结论中不正确的是( B )
A.两只试管中都产生大量气泡,手触试管外壁有热感
B.通过气球膨胀的大小能推导镁和铁的金属活动性强弱关系
C.收集到的气体在点燃前一定要检验纯度
D.若将药品换成生石灰和水,则观察到气球先膨胀,冷却至室温后恢复原状
5198110698502、一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,
下列说法不正确的是( C )
A、t1时,产生氢气的质量锌比铁大 B、t1时,产生氢气的速率锌比铁大
C、t2时,参加反应锌的质量与铁相同 D、t2时,锌、铁消耗的盐酸质量相同
3、Fe、Mg、Al 三种金属分别跟稀盐酸充分反应,得到相同质量的氢气,其原因有:
① Fe、Mg、Al 的质量相等,盐酸足量;
② Fe、Mg、Al 的质量比为 56:24:27,盐酸足量;
③ Fe、Mg、Al 的质量比为 28:12:9,盐酸足量;
④ Fe、Mg、Al 均为过量。所用盐酸的溶质质量分数和质量都相同。 你认为可能的原因是 ( A )
A.③④ B.①② C.①③ D.②③
50863502076454、(已知X、Y在化合物中均为+2价)等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( B )
两种金属的相对原子质量:XB.t1时,消耗盐酸的质量:X=Y
C.t2时,消耗金属的质量:X>Y
D.t3时,消耗金属的质量:X=Y
5、现有两种金属单质组成的混合物.向100g稀盐酸中加入该混合物,加入混合物的质量与生成氢气的质量关系如图所示.下列说法正确的是( D )
A. 若混合物为Zn和Cu,则m大于0.2?g
B. 若混合物为Zn和Fe,则m可能是0.2?g
C. 若混合物为Fe和Cu,稀盐酸中溶质质量分数为7.3%
D. 若混合物为Fe和Cu,m为0.1?g,则混合物中Fe和Cu的质量比为1:1
42608504572006、甲、乙两烧杯内盛有等质量、等质量分数的盐酸.将镁逐渐加入甲烧杯,铁逐渐加入乙烧杯,测量加入的金属质量m和相应的烧杯内物质质量变化量△m,画出△M﹣m曲线oac和obc的示意图,如图所示.根据图中信息,下列说法错误的是( B )
A.m1:m2=3:7
B.m1﹣△M1<m2﹣△M2
C.曲线oac表示的是甲烧杯中△M与m的变化关系
D.当乙烧杯内加入铁的质量为m1时,溶液中溶质不止一种
7、相同质量的Mg、Fe、Zn三种金属,分別与足量的、质量相同、质量分数相同的稀H2SO4充分反应,生成氢气与消耗稀H2SO4的质量关系见右图,分析图象所得的结论中,不正确的是( A )
A. 三种金属的活动性顺序:Mg>Fe>Zn B. 三种金属的相对原子质量:MgC. 三种金属消耗稀H2SO4的质量:Mg>Fe>Zn D. 三种金属与稀H2SO4反应后溶液的质量:Mg8、某化学兴趣小组的同学欲在常温、常压下,用一定质量的镁与足量的稀硫酸反应,测定镁的相对原子质量。利用如下图所示的装置(盛放镁条的隔板有小孔,图中固定装置已略去)进行实验,充分反应后,测得生成氢气的体积为V。已知本实验条件下,氢气的密度为ρ。
关于该实验,有如下说法:①连接仪器后,要先检查装置的气密性;②打开分液漏斗的活塞,可观察到乙中稀硫酸进入装置丙中;③当丙中无气泡产生,立即读取量筒戊中水的积,即为反应生成氢气的体积;④装置中的空气对实验结果无影响;⑤利用该实验原理,还可以测定铜的相对原子质量。其中正确说法的个数有(?? B????)?
A.2个??????B.3个???????C.4个??????D.5个
9、 (6分)已知某粗铜粉末中含有少量的铁、锌和金。某化学兴趣小组的同学为测定该粗铜粉末中铜的质量分数,开展如下实验探究:
步骤I:称取质量为m1的粗铜样品;
步骤Ⅱ:向样品中逐滴加入足量的稀盐酸,充分反应;
步骤Ⅲ:过滤,将滤渣洗涤、干燥后称量,质量为m2;
步骤IV:将步骤Ⅲ所得固体在空气中充分灼烧,冷却至室温后称量,质量为m3。
请回答下列问题: (1) 步骤Ⅱ的目的是 ;
(2) 判断步骤Ⅱ中加入的稀盐酸足量的方法是 :
(3) 步骤IV中反应的化学方程式为 ;
(4) 按此方法测得粗铜中铜的质量分数为 (用m1、m2、m3的代数式表示)。
【答案】(1)除去粗铜中的铁、锌 (2)继续或再加入稀盐酸,无气泡冒出
(3)2Cu+O2false2CuO (4)false
【题组C】金属活动性顺序实验探究
1、小明为探究Cu、Al、Ag的金属活动性顺序,做了如下两个实验。请分析实验,完成填空。
(1) 试管①中观察到的现象是:铝丝表面附着一层 固体,溶液颜色变浅。
(2) 试管②中发生了化学反应,现象明显,该反应的化学方程式是____________。
(3) 通过实验探究,Cu、Al、Ag三种金属活动性由强到弱的顺序是______。
(4) 请你设计再设计一个实验,验证Cu、Al、Ag三种金属活动性顺序?
【答案】(1)红色 (2)Cu+2AgNO3= Cu(NO3)2+2Ag (3)Al>Cu>Ag (4)“取中间”合理即可
2、以X、Y、Z三种金属活动性的实验探究过程如下,①取大小相同的三种金属片分别放入CuSO4溶液中一段时间后,X、Z表面出现红色物质,Y没有明显现象;②取大小相等的X、Z两种金属片,分别放入相同的稀盐酸中,X、Z表面都有气泡产生,但X产生气泡速度明显比Z的快,则X、Y、Z三种金属的活动性顺序是( C )
A.X>Y>Z B.Z>Y>X C.X>Z>Y D.Z>X>Y
3、X,Y,Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性是( D )
①Z + YSO4 == ZSO4 + Y ② X + YSO4 == XSO4 + Y ③ Z + H2SO4 == ZSO4 + H2↑ ④ X + H2SO4 不反应
A.Z>X>Y B.Z>Y>X C.X>Y>Z D.X>Z>Y
4、某化学兴趣小组的同学开展如下图所示实验。
5651508890
关于该实验,下列说法正确的是( B )
A.②中溶液含有盐酸 B.③中一定没有盐酸
C.②中加入镁粉时一定有气泡冒出 D.③中的固体一定是铁
5、字母A、B、C、D表示金属活动性顺序表中常见的四种金属。
已知:① A+BSO4=ASO4+B ② C+H2SO4=CSO4+H2↑ ③ B+2DNO3=B(NO3)2+2D
请完成以下填空:
(1)金属C在金属活动性顺序表中排在氢 (填“前面”或“后面”);
(2)根据上述反应能判断出其中三种金属的活动性顺序,其金属活动性由强到弱的顺序是 (填字母);
(3)若A、B、C、D分别为铁、镁、铜、银中的一种,则金属B为 ,金属C与H2SO4反应后生成的化合物可能有 (填化学式)。
【答案】前面 A>B>D Cu MgSO4、FeSO4
6、化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐的晶体,现将这三种金属随意编号为A. B. C,并设计了如下流程:
从该方案中得出的结论:
① 搡作a的名称为过滤 ② 若A的硫酸盐中A元素显?2价,该盐为MnSO4
③ A. B. C三种金属的活动性为:A>B>C ④ 最后的滤液中可能有三种溶质
⑤ 若步骤①中加入硫酸的量不足,其它各步条件不变,最终得到的滤液一定含有三种溶质
上述结论正确的是 ( D )
A. ②③④ B. ①②③ C. ②③④⑤ D. ②③⑤
【题组D】金属与盐溶液的反应
类型1. 一种金属加入一种较弱的金属化合物溶液中
1、向Cu(NO3)2溶液中加入一定量的铁粉充分反应,下列情况中可能出现的是( B )
①溶液中有Fe2+、Cu2+、不溶物为Cu ②溶液中有Fe2+、Cu2+、不溶物为Fe
③溶液中只有Cu2+、不溶物为Fe ④溶液中只有Fe2+、不溶物为Fe,Cu
A.①③ B.①④ C.②③ D.③④
2、向氯化铜溶液加入一定量的锌粉充分反应,下列情况中可能出现的是 ( C )
①溶液中有 Zn2+、Cu2+ ,不溶物为Cu ②溶液中有 Zn2+、Cu2+ ,不溶物为 Zn
③溶液只有 Zn2+ ,不溶物为 Zn ④ 溶液只有 Zn2+ ,不溶物为 Zn 、Cu
A.①③ B.②③ C ①④ D.③④
3、向硫酸铜溶液中加入一定量的铁粉充分反应,下列说法正确的是( C )
A.滤渣中一定有铁 B.滤渣中一定有铜 C.滤液中一定有Fe3+ D.滤液中一定有Cu2+
4、将硝酸银与一定量的锌粉充分反应,向滤液中加入少量盐酸,没有沉淀生成,则( B )
A.向滤渣中滴加稀盐酸一定有气泡产生 B.滤渣可能有两种金属
C.滤渣中一定有锌 D.滤液中可能有硝酸银和硝酸锌
5、把一定质量的锌粉放入Cu(NO3)2溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气体产生.根据以上现象,下列判断滤渣中的成分正确是( D )
A.只有Cu B.只有Zn
C.一定有Cu,可能有Zn D.一定有Zn和Cu
6、向硫酸铜溶液中加入一定量的铁粉充分反应后过滤。下列情况可能出现的是( B )
① 滤液中有硫酸亚铁、硫酸铜,滤出的固体为铜 ② 滤液中有硫酸亚铁、硫酸铜,滤出的固体为铁
③ 滤液中只有硫酸亚铁,滤出的固体为铁、铜 ④ 滤液中只有硫酸铜,滤出的固体为铁、铜
A.①④ B.①③ C.②③ D.③④
类型2:一种金属加入到几种金属化合物溶液中
1、某溶液中仅含有AgNO3和Cu(NO3)2两种溶质,将其分成A、B两份,各加入一定质量的锌粉,充分反应后,过滤,洗涤,分别得到滤渣和滤液。
(1)将A得到的滤渣加入到稀盐酸中,有气泡产生,则该滤渣中含有的物质是_________,滤液中含有的溶质
是_________。
(2)往B得到的滤液中滴稀盐酸,有白色沉淀生成,则对应的滤渣中含有_______,滤液中含有的溶质是_____。
【答案】(1)Zn、Ag、Cu Zn(NO3)2 (2)Ag AgNO3 Cu(NO3)2 Zn(NO3)2
2、NaNO3、AgNO3、Cu(NO3)2的混合溶液中加入一定量Fe,充分反应后过滤,
(1)若滤渣中加入盐酸后有气泡产生,则滤渣中一定有_________,此时滤液中所含物质是(不包括水,下同) _________。
(2)若滤液中加入铁片无明显变化,则滤渣中一定有_______,可能有_______,滤液中所含物质是____。
【答案】(1)Fe、Cu、Ag NaNO3、Fe(NO3)2 (2)Cu、Ag Fe NaNO3、Fe(NO3)2
3、向硝酸银、硝酸铜、硝酸锌的混合溶液中,加入一定量的铁粉,充分反应后过滤,得到滤渣和滤液.
(1)若向滤渣中加入稀硫酸,看到有气泡冒出,则滤渣中一定有_________;滤液中一定有的溶质是_____。
(2)若向滤渣中加入稀硫酸,没有气泡冒出,则滤渣中一定有的金属是_________;滤液中一定有的溶质是 ;
【答案】(1)Ag、Cu、Fe Fe(NO3)2 Zn(NO3)2 (2)Ag Fe(NO3)2 Zn(NO3)2
4、向AgNO3、Cu(NO3)2的混合溶液中,加入一定量的Zn粉,充分反应后过滤,得到滤液和滤渣,向滤渣中加入稀盐酸。
(1)如果有气泡产生,滤液中含有的溶质是 _________ ;
(2)如果没有气泡产生,滤渣中一定含有的物质是 _________ .
【答案】(1)Zn(NO3)2 (2)Ag
5、在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是( B )
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体一定含有铜,一定不含铁和镁
C.滤液中一定含有氯化镁,可能含有氯化铜和氯化亚铁
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
6、向一定质量的硝酸银、硝酸铜的混合溶液中加入锌粉,充分反应后过滤,向滤渣中滴加少量的稀盐酸,无气泡产生。下列相关判断中,正确的是 ( C )
A.滤渣中可能含有锌 B.滤渣中一定含有银和铜
C.滤液中可能只有一种溶质 D.滤液中一定有Zn2+ Cu2+ Ag+
7、将一定质量的铁粉加入 Cu(NO3)2 和 AgNO3 的混合溶液中,反应结束后过滤,向滤渣中加入稀盐酸,无明显现象。下列对滤渣和滤液的说法中,不正确的是 ( B )
A.滤渣中一定含有银 B.滤液中一定不含Ag+
C.滤渣中可能含有铜 D.滤液中一定含有Fe2+
8、将一定质量的 Zn 加入到 Mg(NO3)2、Fe(NO3)2、AgNO3三种物质的混合溶液中,充分反应 后过滤,滤液仍为浅绿色,下列判断中,正确的是( C )
A.滤渣中一定不含单质 Fe B.滤液中一定含有 Ag+
C.滤液中至少含有三种成分 D.反应后固体金属的质量一定变大
9.向CuCl2和FeCl2的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.下列判断正确的是( D )
① 滤液中一定含有MgCl2、FeCl2、CuCl2 ② 滤出的固体中一定含有铜,一定不含铁和镁
③ 滤出的固体中一定含有铜,可能含有铁和镁 ④ 滤液中一定含有MgCl2和FeCl2,可能含有CuCl2.
A.①② B.②③ C.③④ D.②④
10.工厂为防止环境污染和回收贵重金属,向含有Cu(NO3)2和AgNO3的废液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣,滤渣中加入稀盐酸,发现有气泡产生,根据上述现象的描述,下列四种判断正确的是( A )
A.滤渣中一定有Ag、Cu、Fe
B.滤渣中一定有Ag和Cu,可能含有Fe AgNO3和Cu(NO3)2
C.滤液中一定有含Fe(NO3)2,可能含有AgNO3和Cu(NO3)2
D.滤液中一定含有AgNO3和Cu(NO3)2,可能含有含Fe(NO3)2
11.向AgNO3和Cu(NO3)2混合溶液中加入一定量的铁粉,充分反应后,向滤渣中加入稀盐酸无明显现象。下列说法正确的是( D )
A.一定有银生成,一定没有铜生成 B.滤液中一定有Ag+
C.一定有铜生成,可能有银生成 D.滤液阳离子一定有亚铁离子
12.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( D )
A.滤渣中一定有银、可能有铜和锌 B.滤滤渣中一定有银和锌、可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银 D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
13.将过量的铁粉加入Cu(NO3)2 和AgNO3 的混合溶液中,充分反应后过滤,下列对滤渣和滤液的说明中,不正确的是( C )
A.滤渣中一定含有银 B.向滤渣中滴入稀盐酸,有气泡放出
C.滤液可能为蓝色 D.向滤液中滴入稀盐酸,无明显现象
14.向硝酸铜、硝酸银和硝酸铝的混合溶液中加入一定质量的锌粉,充分反应后,过滤,得到滤渣和滤液。以下判断正确的是( C )
A.若滤液为蓝色,则滤渣中一定有银和铜
B.若向滤液中加入稀盐酸无白色沉淀生成,则滤液中一定没有硝酸铜
C.若向滤渣中加入稀盐酸有气体产生,则滤液中只含有硝酸铝和硝酸锌
D.若反应前加入的锌粉质量和反应后滤渣的质量相等,则滤渣中一定不含锌粉和铝粉
15.一定质量的铁粉和锌粉的混合物,加入到硫酸铜溶液中,反应一段时间后,溶液的质量与反应前硫酸铜溶液质量相等。下列说法正确的是( C )
A.此时溶液一定呈蓝色 B.此时固体有三种金属
C.锌粉一定反应完了 D.此时溶液中硫酸锌的质量一定小于硫酸亚铁
16.向AgNO3溶液中加入一定质量Fe和Al,充分反应后过滤,得到滤渣和浅绿色滤液。下列说法正确的( D )
A.滤液中一定含有Al(NO3)3、Ag NO3 B.滤液中一定含有Fe(NO3)2、Ag NO3
C.滤渣中一定含有Fe D.滤渣中一定含有Ag
强化训练
【题组A】金属与氧气反应
1、镁、铝、铁、铜、金五种金属中,常温下易与氧气反应的是 , ;在加热条件下能与氧气反应的是 , ;即使高温也不与氧气反应的是_________;它们金属活动性由强到弱的顺序是__________________
2、我们常说“真金不怕火炼”的原因是( )
A.金的熔点高 B.金的硬度大
C.金的密度大 D.金不活泼,高温时也不与氧气反应
3、下列金属在自然界中能以单质形式存在的是( )
A Fe B Na C Al D Au
4、铝在常温下能与氧气发生反应,那么我们还使用铝制餐具是因为 ,不宜用钢刷来擦洗铝制餐具的原因是 。
【题组B】金属与酸的反应
56038751352551、某同学研究化学反应中的放热现象,分别用等质量的镁和锌与足量的稀盐酸进行实验,
装置如图所示。下列有关现象和结论中不正确的是( )
A.两只试管中都产生大量气泡,手触试管外壁有热感
B.通过气球膨胀的大小能推导镁和铁的金属活动性强弱关系
C.收集到的气体在点燃前一定要检验纯度
D.若将药品换成生石灰和水,则观察到气球先膨胀,冷却至室温后恢复原状
5198110698502、一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,
下列说法不正确的是( )
A、t1时,产生氢气的质量锌比铁大 B、t1时,产生氢气的速率锌比铁大
C、t2时,参加反应锌的质量与铁相同 D、t2时,锌、铁消耗的盐酸质量相同
3、Fe、Mg、Al 三种金属分别跟稀盐酸充分反应,得到相同质量的氢气,其原因有:
① Fe、Mg、Al 的质量相等,盐酸足量;
② Fe、Mg、Al 的质量比为 56:24:27,盐酸足量;
③ Fe、Mg、Al 的质量比为 28:12:9,盐酸足量;
④ Fe、Mg、Al 均为过量。所用盐酸的溶质质量分数和质量都相同。 你认为可能的原因是 ( )
A.③④ B.①② C.①③ D.②③
50863502076454、(已知X、Y在化合物中均为+2价)等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( )
两种金属的相对原子质量:X
C.t2时,消耗金属的质量:X>Y
D.t3时,消耗金属的质量:X=Y
5、现有两种金属单质组成的混合物.向100g稀盐酸中加入该混合物,加入混合物的质量与生成氢气的质量关系如图所示.下列说法正确的是( )
A. 若混合物为Zn和Cu,则m大于0.2?g
B. 若混合物为Zn和Fe,则m可能是0.2?g
C. 若混合物为Fe和Cu,稀盐酸中溶质质量分数为7.3%
D. 若混合物为Fe和Cu,m为0.1?g,则混合物中Fe和Cu的质量比为1:1
42608504572006、甲、乙两烧杯内盛有等质量、等质量分数的盐酸.将镁逐渐加入甲烧杯,铁逐渐加入乙烧杯,测量加入的金属质量m和相应的烧杯内物质质量变化量△m,画出△M﹣m曲线oac和obc的示意图,如图所示.根据图中信息,下列说法错误的是( )
A.m1:m2=3:7
B.m1﹣△M1<m2﹣△M2
C.曲线oac表示的是甲烧杯中△M与m的变化关系
D.当乙烧杯内加入铁的质量为m1时,溶液中溶质不止一种
7、相同质量的Mg、Fe、Zn三种金属,分別与足量的、质量相同、质量分数相同的稀H2SO4充分反应,生成氢气与消耗稀H2SO4的质量关系见右图,分析图象所得的结论中,不正确的是( )
A. 三种金属的活动性顺序:Mg>Fe>Zn B. 三种金属的相对原子质量:Mg
关于该实验,有如下说法:①连接仪器后,要先检查装置的气密性;②打开分液漏斗的活塞,可观察到乙中稀硫酸进入装置丙中;③当丙中无气泡产生,立即读取量筒戊中水的积,即为反应生成氢气的体积;④装置中的空气对实验结果无影响;⑤利用该实验原理,还可以测定铜的相对原子质量。其中正确说法的个数有(?? ???)?
A.2个??????B.3个???????C.4个??????D.5个
9、 (6分)已知某粗铜粉末中含有少量的铁、锌和金。某化学兴趣小组的同学为测定该粗铜粉末中铜的质量分数,开展如下实验探究:
步骤I:称取质量为m1的粗铜样品;
步骤Ⅱ:向样品中逐滴加入足量的稀盐酸,充分反应;
步骤Ⅲ:过滤,将滤渣洗涤、干燥后称量,质量为m2;
步骤IV:将步骤Ⅲ所得固体在空气中充分灼烧,冷却至室温后称量,质量为m3。
请回答下列问题: (1) 步骤Ⅱ的目的是 ;
(2) 判断步骤Ⅱ中加入的稀盐酸足量的方法是 :
(3) 步骤IV中反应的化学方程式为 ;
(4) 按此方法测得粗铜中铜的质量分数为 (用m1、m2、m3的代数式表示)。
【题组C】金属活动性顺序实验探究
1、小明为探究Cu、Al、Ag的金属活动性顺序,做了如下两个实验。请分析实验,完成填空。
(1) 试管①中观察到的现象是:铝丝表面附着一层 固体,溶液颜色变浅。
(2) 试管②中发生了化学反应,现象明显,该反应的化学方程式是____________。
(3) 通过实验探究,Cu、Al、Ag三种金属活动性由强到弱的顺序是______。
(4) 请你设计再设计一个实验,验证Cu、Al、Ag三种金属活动性顺序?
2、以X、Y、Z三种金属活动性的实验探究过程如下,①取大小相同的三种金属片分别放入CuSO4溶液中一段时间后,X、Z表面出现红色物质,Y没有明显现象;②取大小相等的X、Z两种金属片,分别放入相同的稀盐酸中,X、Z表面都有气泡产生,但X产生气泡速度明显比Z的快,则X、Y、Z三种金属的活动性顺序是( )
A.X>Y>Z B.Z>Y>X C.X>Z>Y D.Z>X>Y
3、X,Y,Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性是( )
①Z + YSO4 == ZSO4 + Y ② X + YSO4 == XSO4 + Y ③ Z + H2SO4 == ZSO4 + H2↑ ④ X + H2SO4 不反应
A.Z>X>Y B.Z>Y>X C.X>Y>Z D.X>Z>Y
4、某化学兴趣小组的同学开展如下图所示实验。
5651508890
关于该实验,下列说法正确的是( )
A.②中溶液含有盐酸 B.③中一定没有盐酸
C.②中加入镁粉时一定有气泡冒出 D.③中的固体一定是铁
5、字母A、B、C、D表示金属活动性顺序表中常见的四种金属。
已知:① A+BSO4=ASO4+B ② C+H2SO4=CSO4+H2↑ ③ B+2DNO3=B(NO3)2+2D
请完成以下填空:
(1)金属C在金属活动性顺序表中排在氢 (填“前面”或“后面”);
(2)根据上述反应能判断出其中三种金属的活动性顺序,其金属活动性由强到弱的顺序是 (填字母);
(3)若A、B、C、D分别为铁、镁、铜、银中的一种,则金属B为 ,金属C与H2SO4反应后生成的化合物可能有 (填化学式)。
6、化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐的晶体,现将这三种金属随意编号为A. B. C,并设计了如下流程:
从该方案中得出的结论:
① 搡作a的名称为过滤 ② 若A的硫酸盐中A元素显?2价,该盐为MnSO4
③ A. B. C三种金属的活动性为:A>B>C ④ 最后的滤液中可能有三种溶质
⑤ 若步骤①中加入硫酸的量不足,其它各步条件不变,最终得到的滤液一定含有三种溶质
上述结论正确的是 ( )
A. ②③④ B. ①②③ C. ②③④⑤ D. ②③⑤
【题组D】金属与盐溶液的反应
类型1. 一种金属加入一种较弱的金属化合物溶液中
1、向Cu(NO3)2溶液中加入一定量的铁粉充分反应,下列情况中可能出现的是( )
①溶液中有Fe2+、Cu2+、不溶物为Cu ②溶液中有Fe2+、Cu2+、不溶物为Fe
③溶液中只有Cu2+、不溶物为Fe ④溶液中只有Fe2+、不溶物为Fe,Cu
A.①③ B.①④ C.②③ D.③④
2、向氯化铜溶液加入一定量的锌粉充分反应,下列情况中可能出现的是 ( )
①溶液中有 Zn2+、Cu2+ ,不溶物为Cu ②溶液中有 Zn2+、Cu2+ ,不溶物为 Zn
③溶液只有 Zn2+ ,不溶物为 Zn ④ 溶液只有 Zn2+ ,不溶物为 Zn 、Cu
A.①③ B.②③ C ①④ D.③④
3、向硫酸铜溶液中加入一定量的铁粉充分反应,下列说法正确的是( )
A.滤渣中一定有铁 B.滤渣中一定有铜 C.滤液中一定有Fe3+ D.滤液中一定有Cu2+
4、将硝酸银与一定量的锌粉充分反应,向滤液中加入少量盐酸,没有沉淀生成,则( )
A.向滤渣中滴加稀盐酸一定有气泡产生 B.滤渣可能有两种金属
C.滤渣中一定有锌 D.滤液中可能有硝酸银和硝酸锌
5、把一定质量的锌粉放入Cu(NO3)2溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气体产生.根据以上现象,下列判断滤渣中的成分正确是( )
A.只有Cu B.只有Zn
C.一定有Cu,可能有Zn D.一定有Zn和Cu
6、向硫酸铜溶液中加入一定量的铁粉充分反应后过滤。下列情况可能出现的是( )
① 滤液中有硫酸亚铁、硫酸铜,滤出的固体为铜 ② 滤液中有硫酸亚铁、硫酸铜,滤出的固体为铁
③ 滤液中只有硫酸亚铁,滤出的固体为铁、铜 ④ 滤液中只有硫酸铜,滤出的固体为铁、铜
A.①④ B.①③ C.②③ D.③④
类型2:一种金属加入到几种金属化合物溶液中
1、某溶液中仅含有AgNO3和Cu(NO3)2两种溶质,将其分成A、B两份,各加入一定质量的锌粉,充分反应后,过滤,洗涤,分别得到滤渣和滤液。
(1)将A得到的滤渣加入到稀盐酸中,有气泡产生,则该滤渣中含有的物质是_________,滤液中含有的溶质
是_________。
(2)往B得到的滤液中滴稀盐酸,有白色沉淀生成,则对应的滤渣中含有_______,滤液中含有的溶质是_____。
2、NaNO3、AgNO3、Cu(NO3)2的混合溶液中加入一定量Fe,充分反应后过滤,
(1)若滤渣中加入盐酸后有气泡产生,则滤渣中一定有_________,此时滤液中所含物质是(不包括水,下同) _________。
(2)若滤液中加入铁片无明显变化,则滤渣中一定有_______,可能有_______,滤液中所含物质是____。
3、向硝酸银、硝酸铜、硝酸锌的混合溶液中,加入一定量的铁粉,充分反应后过滤,得到滤渣和滤液.
(1)若向滤渣中加入稀硫酸,看到有气泡冒出,则滤渣中一定有_________;滤液中一定有的溶质是_____。
(2)若向滤渣中加入稀硫酸,没有气泡冒出,则滤渣中一定有的金属是_________;滤液中一定有的溶质是 ;
4、向AgNO3、Cu(NO3)2的混合溶液中,加入一定量的Zn粉,充分反应后过滤,得到滤液和滤渣,向滤渣中加入稀盐酸。
(1)如果有气泡产生,滤液中含有的溶质是 _________ ;
(2)如果没有气泡产生,滤渣中一定含有的物质是 _________ .
5、在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是( )
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体一定含有铜,一定不含铁和镁
C.滤液中一定含有氯化镁,可能含有氯化铜和氯化亚铁
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
6、向一定质量的硝酸银、硝酸铜的混合溶液中加入锌粉,充分反应后过滤,向滤渣中滴加少量的稀盐酸,无气泡产生。下列相关判断中,正确的是 ( )
A.滤渣中可能含有锌 B.滤渣中一定含有银和铜
C.滤液中可能只有一种溶质 D.滤液中一定有Zn2+ Cu2+ Ag+
7、将一定质量的铁粉加入 Cu(NO3)2 和 AgNO3 的混合溶液中,反应结束后过滤,向滤渣中加入稀盐酸,无明显现象。下列对滤渣和滤液的说法中,不正确的是 ( )
A.滤渣中一定含有银 B.滤液中一定不含Ag+
C.滤渣中可能含有铜 D.滤液中一定含有Fe2+
8、将一定质量的 Zn 加入到 Mg(NO3)2、Fe(NO3)2、AgNO3三种物质的混合溶液中,充分反应 后过滤,滤液仍为浅绿色,下列判断中,正确的是( )
A.滤渣中一定不含单质 Fe B.滤液中一定含有 Ag+
C.滤液中至少含有三种成分 D.反应后固体金属的质量一定变大
9.向CuCl2和FeCl2的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.下列判断正确的是( )
① 滤液中一定含有MgCl2、FeCl2、CuCl2 ② 滤出的固体中一定含有铜,一定不含铁和镁
③ 滤出的固体中一定含有铜,可能含有铁和镁 ④ 滤液中一定含有MgCl2和FeCl2,可能含有CuCl2.
A.①② B.②③ C.③④ D.②④
10.工厂为防止环境污染和回收贵重金属,向含有Cu(NO3)2和AgNO3的废液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣,滤渣中加入稀盐酸,发现有气泡产生,根据上述现象的描述,下列四种判断正确的是( )
A.滤渣中一定有Ag、Cu、Fe
B.滤渣中一定有Ag和Cu,可能含有Fe AgNO3和Cu(NO3)2
C.滤液中一定有含Fe(NO3)2,可能含有AgNO3和Cu(NO3)2
D.滤液中一定含有AgNO3和Cu(NO3)2,可能含有含Fe(NO3)2
11.向AgNO3和Cu(NO3)2混合溶液中加入一定量的铁粉,充分反应后,向滤渣中加入稀盐酸无明显现象。下列说法正确的是( )
A.一定有银生成,一定没有铜生成 B.滤液中一定有Ag+
C.一定有铜生成,可能有银生成 D.滤液阳离子一定有亚铁离子
12.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( )
A.滤渣中一定有银、可能有铜和锌 B.滤滤渣中一定有银和锌、可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银 D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
13.将过量的铁粉加入Cu(NO3)2 和AgNO3 的混合溶液中,充分反应后过滤,下列对滤渣和滤液的说明中,不正确的是( )
A.滤渣中一定含有银 B.向滤渣中滴入稀盐酸,有气泡放出
C.滤液可能为蓝色 D.向滤液中滴入稀盐酸,无明显现象
14.向硝酸铜、硝酸银和硝酸铝的混合溶液中加入一定质量的锌粉,充分反应后,过滤,得到滤渣和滤液。以下判断正确的是( )
A.若滤液为蓝色,则滤渣中一定有银和铜
B.若向滤液中加入稀盐酸无白色沉淀生成,则滤液中一定没有硝酸铜
C.若向滤渣中加入稀盐酸有气体产生,则滤液中只含有硝酸铝和硝酸锌
D.若反应前加入的锌粉质量和反应后滤渣的质量相等,则滤渣中一定不含锌粉和铝粉
15.一定质量的铁粉和锌粉的混合物,加入到硫酸铜溶液中,反应一段时间后,溶液的质量与反应前硫酸铜溶液质量相等。下列说法正确的是( )
A.此时溶液一定呈蓝色 B.此时固体有三种金属
C.锌粉一定反应完了 D.此时溶液中硫酸锌的质量一定小于硫酸亚铁
16.向AgNO3溶液中加入一定质量Fe和Al,充分反应后过滤,得到滤渣和浅绿色滤液。下列说法正确的( )
A.滤液中一定含有Al(NO3)3、Ag NO3 B.滤液中一定含有Fe(NO3)2、Ag NO3
C.滤渣中一定含有Fe D.滤渣中一定含有Ag
8.2.1 金属的化学性质
强化训练
【题组A】金属与氧气反应
1、镁、铝、铁、铜、金五种金属中,常温下易与氧气反应的是 Mg+O2=MgO , 4Al+3O2=2Al2O3 ;在加热条件下能与氧气反应的是 3Fe+2O2Fe3O4 , 2Cu+O2 △ CuO ;即使高温也不与氧气反应的是____金_____;它们金属活动性由强到弱的顺序是______Mg>Al>Fe>Cu>Au_____________
2、我们常说“真金不怕火炼”的原因是( D )
A.金的熔点高 B.金的硬度大
C.金的密度大 D.金不活泼,高温时也不与氧气反应
3、下列金属在自然界中能以单质形式存在的是( D )
A Fe B Na C Al D Au
4、铝在常温下能与氧气发生反应,那么我们还使用铝制餐具是因为 铝与氧气反应生成一层致密的氧化膜,从而阻止铝被进一步氧化 ,不宜用钢刷来擦洗铝制餐具的原因是 容易把其表面的氧化膜除掉,使餐具生锈 。
【题组B】金属与酸的反应
56038751352551、某同学研究化学反应中的放热现象,分别用等质量的镁和锌与足量的稀盐酸进行实验,
装置如图所示。下列有关现象和结论中不正确的是( B )
A.两只试管中都产生大量气泡,手触试管外壁有热感
B.通过气球膨胀的大小能推导镁和铁的金属活动性强弱关系
C.收集到的气体在点燃前一定要检验纯度
D.若将药品换成生石灰和水,则观察到气球先膨胀,冷却至室温后恢复原状
5198110698502、一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,
下列说法不正确的是( C )
A、t1时,产生氢气的质量锌比铁大 B、t1时,产生氢气的速率锌比铁大
C、t2时,参加反应锌的质量与铁相同 D、t2时,锌、铁消耗的盐酸质量相同
3、Fe、Mg、Al 三种金属分别跟稀盐酸充分反应,得到相同质量的氢气,其原因有:
① Fe、Mg、Al 的质量相等,盐酸足量;
② Fe、Mg、Al 的质量比为 56:24:27,盐酸足量;
③ Fe、Mg、Al 的质量比为 28:12:9,盐酸足量;
④ Fe、Mg、Al 均为过量。所用盐酸的溶质质量分数和质量都相同。 你认为可能的原因是 ( A )
A.③④ B.①② C.①③ D.②③
50863502076454、(已知X、Y在化合物中均为+2价)等质量的X、Y两种金属分别和足量的同体积、同浓度的盐酸反应,产生气体的质量与时间的关系如图所示.下列说法中不正确的是( B )
两种金属的相对原子质量:X
C.t2时,消耗金属的质量:X>Y
D.t3时,消耗金属的质量:X=Y
5、现有两种金属单质组成的混合物.向100g稀盐酸中加入该混合物,加入混合物的质量与生成氢气的质量关系如图所示.下列说法正确的是( D )
A. 若混合物为Zn和Cu,则m大于0.2?g
B. 若混合物为Zn和Fe,则m可能是0.2?g
C. 若混合物为Fe和Cu,稀盐酸中溶质质量分数为7.3%
D. 若混合物为Fe和Cu,m为0.1?g,则混合物中Fe和Cu的质量比为1:1
42608504572006、甲、乙两烧杯内盛有等质量、等质量分数的盐酸.将镁逐渐加入甲烧杯,铁逐渐加入乙烧杯,测量加入的金属质量m和相应的烧杯内物质质量变化量△m,画出△M﹣m曲线oac和obc的示意图,如图所示.根据图中信息,下列说法错误的是( B )
A.m1:m2=3:7
B.m1﹣△M1<m2﹣△M2
C.曲线oac表示的是甲烧杯中△M与m的变化关系
D.当乙烧杯内加入铁的质量为m1时,溶液中溶质不止一种
7、相同质量的Mg、Fe、Zn三种金属,分別与足量的、质量相同、质量分数相同的稀H2SO4充分反应,生成氢气与消耗稀H2SO4的质量关系见右图,分析图象所得的结论中,不正确的是( A )
A. 三种金属的活动性顺序:Mg>Fe>Zn B. 三种金属的相对原子质量:Mg
关于该实验,有如下说法:①连接仪器后,要先检查装置的气密性;②打开分液漏斗的活塞,可观察到乙中稀硫酸进入装置丙中;③当丙中无气泡产生,立即读取量筒戊中水的积,即为反应生成氢气的体积;④装置中的空气对实验结果无影响;⑤利用该实验原理,还可以测定铜的相对原子质量。其中正确说法的个数有(?? B????)?
A.2个??????B.3个???????C.4个??????D.5个
9、 (6分)已知某粗铜粉末中含有少量的铁、锌和金。某化学兴趣小组的同学为测定该粗铜粉末中铜的质量分数,开展如下实验探究:
步骤I:称取质量为m1的粗铜样品;
步骤Ⅱ:向样品中逐滴加入足量的稀盐酸,充分反应;
步骤Ⅲ:过滤,将滤渣洗涤、干燥后称量,质量为m2;
步骤IV:将步骤Ⅲ所得固体在空气中充分灼烧,冷却至室温后称量,质量为m3。
请回答下列问题: (1) 步骤Ⅱ的目的是 ;
(2) 判断步骤Ⅱ中加入的稀盐酸足量的方法是 :
(3) 步骤IV中反应的化学方程式为 ;
(4) 按此方法测得粗铜中铜的质量分数为 (用m1、m2、m3的代数式表示)。
【答案】(1)除去粗铜中的铁、锌 (2)继续或再加入稀盐酸,无气泡冒出
(3)2Cu+O2false2CuO (4)false
【题组C】金属活动性顺序实验探究
1、小明为探究Cu、Al、Ag的金属活动性顺序,做了如下两个实验。请分析实验,完成填空。
(1) 试管①中观察到的现象是:铝丝表面附着一层 固体,溶液颜色变浅。
(2) 试管②中发生了化学反应,现象明显,该反应的化学方程式是____________。
(3) 通过实验探究,Cu、Al、Ag三种金属活动性由强到弱的顺序是______。
(4) 请你设计再设计一个实验,验证Cu、Al、Ag三种金属活动性顺序?
【答案】(1)红色 (2)Cu+2AgNO3= Cu(NO3)2+2Ag (3)Al>Cu>Ag (4)“取中间”合理即可
2、以X、Y、Z三种金属活动性的实验探究过程如下,①取大小相同的三种金属片分别放入CuSO4溶液中一段时间后,X、Z表面出现红色物质,Y没有明显现象;②取大小相等的X、Z两种金属片,分别放入相同的稀盐酸中,X、Z表面都有气泡产生,但X产生气泡速度明显比Z的快,则X、Y、Z三种金属的活动性顺序是( C )
A.X>Y>Z B.Z>Y>X C.X>Z>Y D.Z>X>Y
3、X,Y,Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性是( D )
①Z + YSO4 == ZSO4 + Y ② X + YSO4 == XSO4 + Y ③ Z + H2SO4 == ZSO4 + H2↑ ④ X + H2SO4 不反应
A.Z>X>Y B.Z>Y>X C.X>Y>Z D.X>Z>Y
4、某化学兴趣小组的同学开展如下图所示实验。
5651508890
关于该实验,下列说法正确的是( B )
A.②中溶液含有盐酸 B.③中一定没有盐酸
C.②中加入镁粉时一定有气泡冒出 D.③中的固体一定是铁
5、字母A、B、C、D表示金属活动性顺序表中常见的四种金属。
已知:① A+BSO4=ASO4+B ② C+H2SO4=CSO4+H2↑ ③ B+2DNO3=B(NO3)2+2D
请完成以下填空:
(1)金属C在金属活动性顺序表中排在氢 (填“前面”或“后面”);
(2)根据上述反应能判断出其中三种金属的活动性顺序,其金属活动性由强到弱的顺序是 (填字母);
(3)若A、B、C、D分别为铁、镁、铜、银中的一种,则金属B为 ,金属C与H2SO4反应后生成的化合物可能有 (填化学式)。
【答案】前面 A>B>D Cu MgSO4、FeSO4
6、化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐的晶体,现将这三种金属随意编号为A. B. C,并设计了如下流程:
从该方案中得出的结论:
① 搡作a的名称为过滤 ② 若A的硫酸盐中A元素显?2价,该盐为MnSO4
③ A. B. C三种金属的活动性为:A>B>C ④ 最后的滤液中可能有三种溶质
⑤ 若步骤①中加入硫酸的量不足,其它各步条件不变,最终得到的滤液一定含有三种溶质
上述结论正确的是 ( D )
A. ②③④ B. ①②③ C. ②③④⑤ D. ②③⑤
【题组D】金属与盐溶液的反应
类型1. 一种金属加入一种较弱的金属化合物溶液中
1、向Cu(NO3)2溶液中加入一定量的铁粉充分反应,下列情况中可能出现的是( B )
①溶液中有Fe2+、Cu2+、不溶物为Cu ②溶液中有Fe2+、Cu2+、不溶物为Fe
③溶液中只有Cu2+、不溶物为Fe ④溶液中只有Fe2+、不溶物为Fe,Cu
A.①③ B.①④ C.②③ D.③④
2、向氯化铜溶液加入一定量的锌粉充分反应,下列情况中可能出现的是 ( C )
①溶液中有 Zn2+、Cu2+ ,不溶物为Cu ②溶液中有 Zn2+、Cu2+ ,不溶物为 Zn
③溶液只有 Zn2+ ,不溶物为 Zn ④ 溶液只有 Zn2+ ,不溶物为 Zn 、Cu
A.①③ B.②③ C ①④ D.③④
3、向硫酸铜溶液中加入一定量的铁粉充分反应,下列说法正确的是( C )
A.滤渣中一定有铁 B.滤渣中一定有铜 C.滤液中一定有Fe3+ D.滤液中一定有Cu2+
4、将硝酸银与一定量的锌粉充分反应,向滤液中加入少量盐酸,没有沉淀生成,则( B )
A.向滤渣中滴加稀盐酸一定有气泡产生 B.滤渣可能有两种金属
C.滤渣中一定有锌 D.滤液中可能有硝酸银和硝酸锌
5、把一定质量的锌粉放入Cu(NO3)2溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气体产生.根据以上现象,下列判断滤渣中的成分正确是( D )
A.只有Cu B.只有Zn
C.一定有Cu,可能有Zn D.一定有Zn和Cu
6、向硫酸铜溶液中加入一定量的铁粉充分反应后过滤。下列情况可能出现的是( B )
① 滤液中有硫酸亚铁、硫酸铜,滤出的固体为铜 ② 滤液中有硫酸亚铁、硫酸铜,滤出的固体为铁
③ 滤液中只有硫酸亚铁,滤出的固体为铁、铜 ④ 滤液中只有硫酸铜,滤出的固体为铁、铜
A.①④ B.①③ C.②③ D.③④
类型2:一种金属加入到几种金属化合物溶液中
1、某溶液中仅含有AgNO3和Cu(NO3)2两种溶质,将其分成A、B两份,各加入一定质量的锌粉,充分反应后,过滤,洗涤,分别得到滤渣和滤液。
(1)将A得到的滤渣加入到稀盐酸中,有气泡产生,则该滤渣中含有的物质是_________,滤液中含有的溶质
是_________。
(2)往B得到的滤液中滴稀盐酸,有白色沉淀生成,则对应的滤渣中含有_______,滤液中含有的溶质是_____。
【答案】(1)Zn、Ag、Cu Zn(NO3)2 (2)Ag AgNO3 Cu(NO3)2 Zn(NO3)2
2、NaNO3、AgNO3、Cu(NO3)2的混合溶液中加入一定量Fe,充分反应后过滤,
(1)若滤渣中加入盐酸后有气泡产生,则滤渣中一定有_________,此时滤液中所含物质是(不包括水,下同) _________。
(2)若滤液中加入铁片无明显变化,则滤渣中一定有_______,可能有_______,滤液中所含物质是____。
【答案】(1)Fe、Cu、Ag NaNO3、Fe(NO3)2 (2)Cu、Ag Fe NaNO3、Fe(NO3)2
3、向硝酸银、硝酸铜、硝酸锌的混合溶液中,加入一定量的铁粉,充分反应后过滤,得到滤渣和滤液.
(1)若向滤渣中加入稀硫酸,看到有气泡冒出,则滤渣中一定有_________;滤液中一定有的溶质是_____。
(2)若向滤渣中加入稀硫酸,没有气泡冒出,则滤渣中一定有的金属是_________;滤液中一定有的溶质是 ;
【答案】(1)Ag、Cu、Fe Fe(NO3)2 Zn(NO3)2 (2)Ag Fe(NO3)2 Zn(NO3)2
4、向AgNO3、Cu(NO3)2的混合溶液中,加入一定量的Zn粉,充分反应后过滤,得到滤液和滤渣,向滤渣中加入稀盐酸。
(1)如果有气泡产生,滤液中含有的溶质是 _________ ;
(2)如果没有气泡产生,滤渣中一定含有的物质是 _________ .
【答案】(1)Zn(NO3)2 (2)Ag
5、在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是( B )
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体一定含有铜,一定不含铁和镁
C.滤液中一定含有氯化镁,可能含有氯化铜和氯化亚铁
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
6、向一定质量的硝酸银、硝酸铜的混合溶液中加入锌粉,充分反应后过滤,向滤渣中滴加少量的稀盐酸,无气泡产生。下列相关判断中,正确的是 ( C )
A.滤渣中可能含有锌 B.滤渣中一定含有银和铜
C.滤液中可能只有一种溶质 D.滤液中一定有Zn2+ Cu2+ Ag+
7、将一定质量的铁粉加入 Cu(NO3)2 和 AgNO3 的混合溶液中,反应结束后过滤,向滤渣中加入稀盐酸,无明显现象。下列对滤渣和滤液的说法中,不正确的是 ( B )
A.滤渣中一定含有银 B.滤液中一定不含Ag+
C.滤渣中可能含有铜 D.滤液中一定含有Fe2+
8、将一定质量的 Zn 加入到 Mg(NO3)2、Fe(NO3)2、AgNO3三种物质的混合溶液中,充分反应 后过滤,滤液仍为浅绿色,下列判断中,正确的是( C )
A.滤渣中一定不含单质 Fe B.滤液中一定含有 Ag+
C.滤液中至少含有三种成分 D.反应后固体金属的质量一定变大
9.向CuCl2和FeCl2的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生.下列判断正确的是( D )
① 滤液中一定含有MgCl2、FeCl2、CuCl2 ② 滤出的固体中一定含有铜,一定不含铁和镁
③ 滤出的固体中一定含有铜,可能含有铁和镁 ④ 滤液中一定含有MgCl2和FeCl2,可能含有CuCl2.
A.①② B.②③ C.③④ D.②④
10.工厂为防止环境污染和回收贵重金属,向含有Cu(NO3)2和AgNO3的废液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣,滤渣中加入稀盐酸,发现有气泡产生,根据上述现象的描述,下列四种判断正确的是( A )
A.滤渣中一定有Ag、Cu、Fe
B.滤渣中一定有Ag和Cu,可能含有Fe AgNO3和Cu(NO3)2
C.滤液中一定有含Fe(NO3)2,可能含有AgNO3和Cu(NO3)2
D.滤液中一定含有AgNO3和Cu(NO3)2,可能含有含Fe(NO3)2
11.向AgNO3和Cu(NO3)2混合溶液中加入一定量的铁粉,充分反应后,向滤渣中加入稀盐酸无明显现象。下列说法正确的是( D )
A.一定有银生成,一定没有铜生成 B.滤液中一定有Ag+
C.一定有铜生成,可能有银生成 D.滤液阳离子一定有亚铁离子
12.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( D )
A.滤渣中一定有银、可能有铜和锌 B.滤滤渣中一定有银和锌、可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银 D.滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
13.将过量的铁粉加入Cu(NO3)2 和AgNO3 的混合溶液中,充分反应后过滤,下列对滤渣和滤液的说明中,不正确的是( C )
A.滤渣中一定含有银 B.向滤渣中滴入稀盐酸,有气泡放出
C.滤液可能为蓝色 D.向滤液中滴入稀盐酸,无明显现象
14.向硝酸铜、硝酸银和硝酸铝的混合溶液中加入一定质量的锌粉,充分反应后,过滤,得到滤渣和滤液。以下判断正确的是( C )
A.若滤液为蓝色,则滤渣中一定有银和铜
B.若向滤液中加入稀盐酸无白色沉淀生成,则滤液中一定没有硝酸铜
C.若向滤渣中加入稀盐酸有气体产生,则滤液中只含有硝酸铝和硝酸锌
D.若反应前加入的锌粉质量和反应后滤渣的质量相等,则滤渣中一定不含锌粉和铝粉
15.一定质量的铁粉和锌粉的混合物,加入到硫酸铜溶液中,反应一段时间后,溶液的质量与反应前硫酸铜溶液质量相等。下列说法正确的是( C )
A.此时溶液一定呈蓝色 B.此时固体有三种金属
C.锌粉一定反应完了 D.此时溶液中硫酸锌的质量一定小于硫酸亚铁
16.向AgNO3溶液中加入一定质量Fe和Al,充分反应后过滤,得到滤渣和浅绿色滤液。下列说法正确的( D )
A.滤液中一定含有Al(NO3)3、Ag NO3 B.滤液中一定含有Fe(NO3)2、Ag NO3
C.滤渣中一定含有Fe D.滤渣中一定含有Ag
同课章节目录
