【新教材】2020-2021学年人教版(2019)高一化学必修二5.2 氮及其化合物 课时1 氮气与氮的固定 一氧化氮和二氧化氮 课件(共45张ppt)
文档属性
| 名称 | 【新教材】2020-2021学年人教版(2019)高一化学必修二5.2 氮及其化合物 课时1 氮气与氮的固定 一氧化氮和二氧化氮 课件(共45张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 778.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-07 00:00:00 | ||
图片预览








文档简介
第五章 化工生产中的重要非金属元素
第二节 氮及其化合物
课时1 氮气与氮的固定 一氧化氮和二氧化氮
学习任务一 氮气与氮的固定
任务探究·深度学习
旧知回顾
自主学习
为了更好地保护文物,部分博物馆启用“真空充氮杀虫灭菌消毒机”来处理
和保护文物,将文物放入该机器内(氮气浓度可高达99.99%),密封三天,好氧菌
和丝状霉菌都会被灭杀。该机器具有此类功能,主要与氮气的性质有关。请
你结合相关化学知识回答,下列关于氮气的哪些说法是正确的?
①氮气的化学性质不活泼 ②氮气不能供给呼吸 ③氮气能抑制菌类的生长
④氮气能吸收部分水分 ⑤氮气不能与任何物质反应
?
答案 ①②③正确。
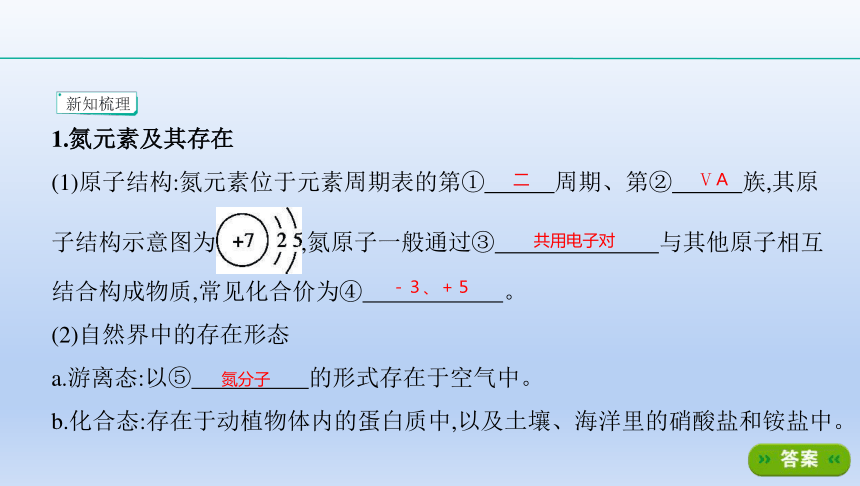
1.氮元素及其存在
(1)原子结构:氮元素位于元素周期表的第① ????周期、第② ????族,其原
子结构示意图为?,氮原子一般通过③ ????与其他原子相互
结合构成物质,常见化合价为④ ????。
(2)自然界中的存在形态
a.游离态:以⑤ ????的形式存在于空气中。
b.化合态:存在于动植物体内的蛋白质中,以及土壤、海洋里的硝酸盐和铵盐中。
新知梳理
二
ⅤA
共用电子对
-3、+5
氮分子
2.氮气的性质
(1)物理性质:无色、无味、难溶于水,密度与空气的相近,约占空气体积的4/5。
(2)化学性质
a.由于氮分子内两个氮原子间以共价三键(?)结合,断开该化学键需要
较多的能量,所以氮气的化学性质很稳定,通常情况下难以与其他物质发生化
学反应,无法被大多数生物体直接吸收。
b.在高温、放电等条件下,氮气能够与镁、氧气、氢气等物质发生化合反应,
化学方程式分别为⑥ 、⑦ ? ? ?
⑧ ????。
、
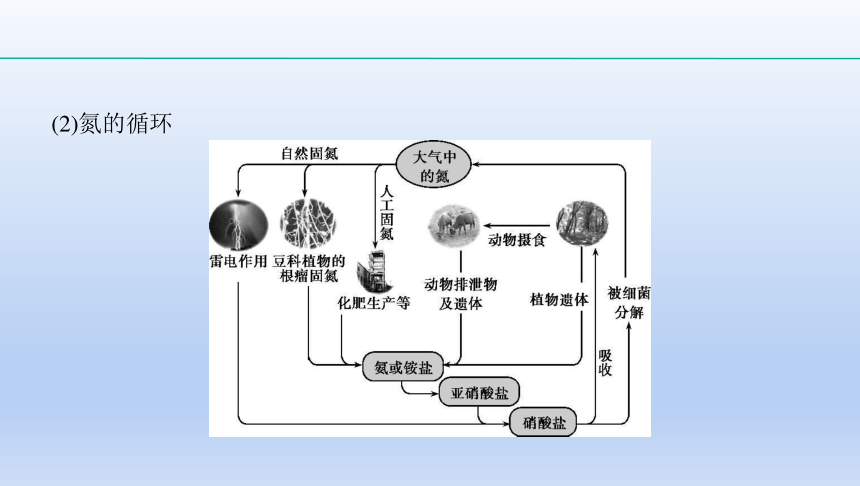
3.氮的固定和循环
(1)氮的固定
1)将大气中⑨ ????的过程叫做氮的固定。
2)固氮形式
a.自然固氮:大自然通过闪电释放的能量将空气中的氮气转化为⑩ ????的
化合物,或者通过豆科植物的根瘤菌将氮气转化成? ????。
b.人工固氮:通过控制条件,将氮气氧化或还原为氮的化合物。最重要的人工
固氮途径就是? ????。
游离态的氮转化为氮的化合物
含氮
氨
工业合成氨
(2)氮的循环
?
判断下列说法的正误(正确的画“√”,错误的画“?”)。
易错辨析
1.氮在自然界中只以游离态形式存在?( )
2.N2在高温条件下与O2发生反应生成NO?( )
3.豆科植物通过根瘤菌吸收空气中的氮属于氮的固定,发生的是化学变化?
( )
4.工业合成氨的过程是固氮的过程?( )
?
√
√
√
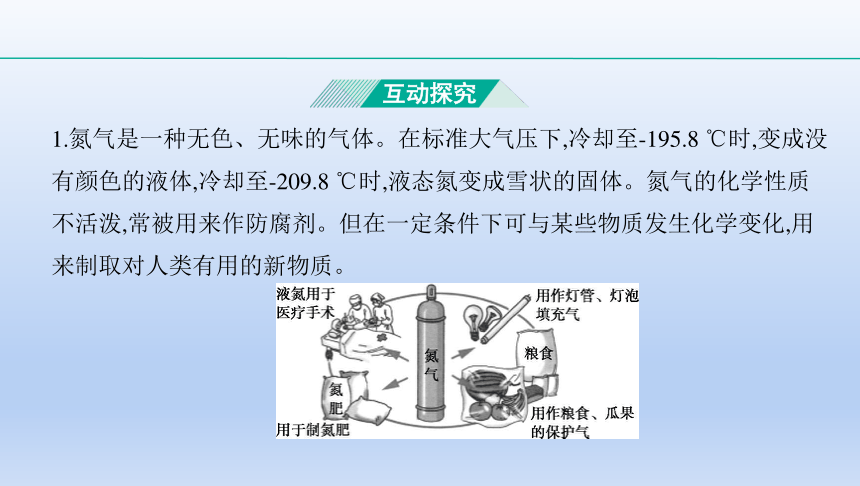
1.氮气是一种无色、无味的气体。在标准大气压下,冷却至-195.8 ℃时,变成没
有颜色的液体,冷却至-209.8 ℃时,液态氮变成雪状的固体。氮气的化学性质
不活泼,常被用来作防腐剂。但在一定条件下可与某些物质发生化学变化,用
来制取对人类有用的新物质。
?
互动探究
(1)请你根据所学知识回答氮气为什么可以用作粮食、瓜果的保护气?
(2)与同学交流或查阅资料分析液氮用于医疗手术的原理是什么?
答案????(1)氮气性质稳定,能够减缓粮食、瓜果被氧气氧化变质的速率。
(2)液氮挥发,吸收热量,使温度迅速下降,通过极度冷冻将病区细菌迅速杀死,
使得病区适宜进行医疗手术。
2.氮气的性质不活泼,但在一定条件下也可以发生化学反应,下列反应中属于
氮的固定的反应是哪几个?在属于氮的固定的反应中,氮气都作氧化剂吗?
①N2+3Mg? Mg3N2
②N2+3H2? 2NH3
③2NO+O2? 2NO2
④N2+O2? 2NO
答案 氮的固定是氮单质转变成氮的化合物的过程,所以反应①②④属于氮
的固定。反应①中氮气作氧化剂,反应②中氮气作氧化剂,反应④中氮气作还
原剂。
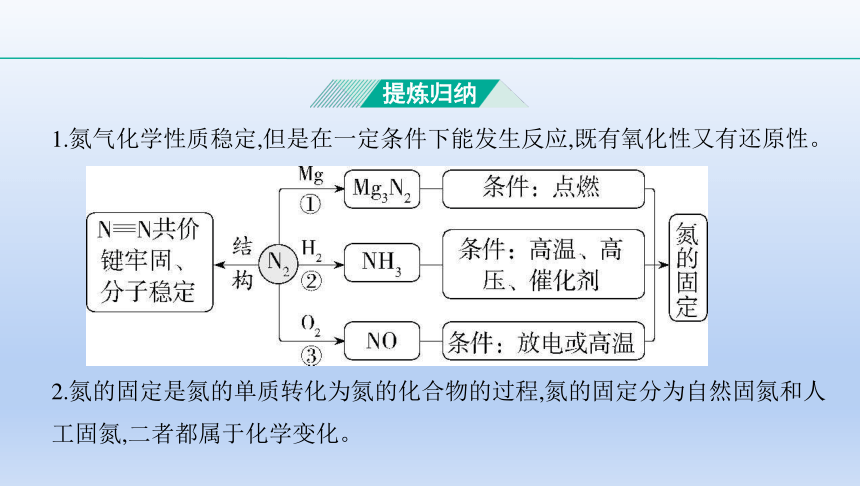
1.氮气化学性质稳定,但是在一定条件下能发生反应,既有氧化性又有还原性。
?
提炼归纳
2.氮的固定是氮的单质转化为氮的化合物的过程,氮的固定分为自然固氮和人
工固氮,二者都属于化学变化。
1.下列关于氮气的性质和用途的叙述中错误的是?( )
A.常温下,氮气是一种很难溶于水的无色、无味气体
B.通常情况下,很难与其他物质发生化学反应
C.从空气中分离出的氮气,可用于填充白炽灯的灯泡
D.从空气中分离出的氮气,不能用于生产氮肥
典题精练
解析???? 常温下,氮气是一种无色、无味的气体,且难溶于水,故A正确;氮气
的化学性质不活泼,通常情况下难与其他物质发生反应,故B正确;氮气的化学
性质不活泼,从空气中分离出的氮气,可用于填充白炽灯的灯泡,故C正确;从空
气中分离出的氮气,能用于生产氮肥,如N2→NH3→氮肥,故D错误。
D
2.下列关于氮气的说法中错误的是?( )
A.通常情况下氮气性质很稳定,所以氮气可作食物保护气
B.N2+O2? 2NO,该反应是汽车尾气造成污染的主要原因之一
C.氮气在空气中约占空气体积的?
D.在反应3Mg+N2? Mg3N2中,氮气作氧化剂
C
解析???? 氮气分子中含有氮氮三键,通常情况下N2性质很稳定,可作食物保护
气,故A正确;氮气与氧气在高温下反应生成一氧化氮,一氧化氮有毒,为空气污
染物,故B正确;N2在空气中约占空气体积的?,故C错误;在反应3Mg+N2?
Mg3N2中,氮气中氮元素化合价降低,所以N2作氧化剂,故D正确。
3.下列叙述中与氮的固定无关的是?( )
A.工业合成氨
B.工业上将氨转化成硝酸和其他氮的氧化物
C.豆科植物的根瘤菌吸收空气中的氮气并将之转化成植物蛋白质
D.电闪雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收
B
解析???? 工业合成氨是将氮气转化为氨气,属于氮的固定,故A不符合题意;
工业上将氨转化成硝酸和其他氮的氧化物,不是氮的固定,故B符合题意;豆科
植物的根瘤菌吸收空气中的氮气并将之转化成植物蛋白是氮的固定,故C不符
合题意;电闪雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收,
属于氮的固定,故D不符合题意。
4.自然界中氮的循环如图所示。下列说法不正确的是( )
A.工业合成氨属于人工固氮
B.在雷电作用下N2与O2可发生化学反应
C.在氮的循环过程中不涉及氧化还原反应
D.含氮无机物与含氮有机物可相互转化
解析???? N2与O2生成NO的反应是氧化还原反应,所以在氮的循环过程中涉
及氧化还原反应,故C错误。
C
学习任务二 一氧化氮和二氧化氮
新知梳理
自主学习
1.NO和NO2的物理性质
NO
① ????色、有毒气体,② ????溶于水
NO2
③ ????色、有刺激性气味的有毒气体,密度比空气的大,易④ ????,易溶于水
2.NO和NO2的化学性质
(1)在常温下,NO很容易与O2反应,化学方程式为⑤ ??????。
(2)NO2溶于水时发生反应的化学方程式为⑥ ??????。
无
不
红棕
液化
3.二氧化氮溶于水的实验
(1)实验过程
实验
装置
?
实验
操作
在如图注射器里充入20 mL NO,然后吸入5 mL水,用乳胶管和弹簧夹封住管口,振荡注射器
打开弹簧夹,快速吸入
10 mL空气后夹上弹簧夹
振荡注射器
实验
现象
无明显现象
无色气体变为红棕色
红棕色气体变浅至消失,有无色气体生成,注射器活塞向内滑动
化学
方程式
⑦ ????、
⑧ ????
(2)对工业生产硝酸的启示
工业上生产硝酸时,向吸收后的废气中再通入适量的氧气或空气,能充分利用
原料,并能减少NO的排放以保护环境。
1.常温下能用排空气法收集一氧化氮吗?为什么?实验室中应该怎样收集一氧
化氮?
互动探究
答案 不能。因为发生反应:2NO+O2? 2NO2。实验室中应该用排水集气
法收集一氧化氮。
2.NO2转化为NO的变化中,NO2只能作氧化剂吗?
答案 NO2与水反应转化为NO的同时生成硝酸,NO2既作氧化剂又作还原剂。
3.把一支充满NO2气体的试管倒置在水槽中充分反应后有什么现象?
答案 由反应3NO2+H2O? 2HNO3+NO可知:当NO2与H2O充分反应后,试管
内气体变为无色,且剩余气体占试管体积的1/3。
4.为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置(夹
持装置已省略),并检查装置的气密性,实验前用排水法收集NO。
?
(1)打开止水夹,推动注射器活塞,使O2进入烧瓶。关上止水夹,首先观察到烧瓶
中的现象是什么?写出产生此现象的化学方程式。
(2)轻轻摇动烧瓶,观察到烧瓶中的现象是什么?利用化学方程式解释产生这种
现象的原因是什么?
(3)假设烧瓶内充有100 mL NO,通入多少O2才能使水充满试管?
答案 (1)首先观察到的现象是烧瓶中的气体由无色变为红棕色,反应的化学
方程式为2NO+O2? 2NO2。
(2)摇动烧瓶,使得NO2与水发生反应:3NO2+H2O? 2HNO3+NO,所以烧瓶中
的红棕色气体又变为无色,且烧瓶内压强减小,烧杯中的水倒吸到烧瓶内,导致
烧瓶中液面上升。
(3)已知:2NO+O2? 2NO2 ①,3NO2+H2O? 2HNO3+NO ②,由反应的化
学方程式①×3+②×2得:4NO+3O2+2H2O? 4HNO3,即当NO和O2的体积比为
4∶3时水可以充满试管,故需通入75 mL O2。
5.农业上有一句俗语“雷雨发庄稼”,其中就涉及氮及其化合物的转化:在一
定条件下,氮气最终转化为硝酸,然后HNO3与土壤中的矿物作用生成硝酸盐,
为庄稼提供氮肥。请你结合本节知识,写出氮气转化为硝酸的化学方程式。
?
答案 氮气转化为硝酸的化学方程式有N2+O2? 2NO、2NO+O2? 2NO2、
3NO2+H2O? 2HNO3+NO。
1.NO和NO2的性质对比
提炼归纳
项目
NO
NO2
色、态、
味、毒性
无色、无味
红棕色、有刺激性气味
有毒气体
水溶性
不溶
易溶且能与水反应
与O2反应
2NO+O2? 2NO2
——
与H2O反应
——
3NO2+H2O? 2HNO3+NO
与O2、H2O共同反应
4NO+3O2+2H2O? 4HNO3
4NO2+O2+2H2O? 4HNO3
氧化性
6NO+4NH3 ? 5N2+6H2O
6NO2+8NH3? 7N2+12HO, NO2+SO2? SO3+NO,NO2
能使湿润的淀粉-KI试纸变蓝
2.氮的氧化物溶于水的计算规律
(1)相关反应原理
3NO2+H2O? 2HNO3+NO a
2NO+O2? 2NO2 b
由化学方程式a×2+b得:
4NO2+O2+2H2O? 4HNO3 c
由化学方程式a×2+b×3得:
4NO+3O2+2H2O? 4HNO3 d
(2)氮的氧化物溶于水的三种类型
①NO2:NO2溶于水时仅涉及反应a,剩余气体为NO;
②NO2和O2的混合气体:NO2和O2的混合气体溶于水时涉及反应c。NO2和O2的
量的关系见下表:
x=?
0x=?
x>?
反应情况
O2过量并剩余
恰好完全反应
NO2过量又发生反应a,
剩余NO
③NO和O2的混合气体:NO和O2的混合气体溶于水时涉及反应d。NO和O2
的量的关系见下表:
x=?
0x=?
x>?
反应情况
O2过量并剩余
恰好完全反应
NO过量并剩余
1.病毒学研究证实,一氧化氮对某些病毒有直接抑制作用。下列关于一氧化氮
的叙述不正确的是?( )
A.一氧化氮是无色气体
B.常温常压下,一氧化氮不能与空气中的氧气直接化合
C.含等质量氧元素的一氧化氮与一氧化碳的物质的量相等
D.一氧化氮不溶于水,能用排水法收集
典题精练
解析???? 一氧化氮很不稳定,极易和空气中的氧气反应生成红棕色的二氧化
氮气体,故B错误。
B
2.下列有关NO2的说法正确的是?( )
A.NO2可由N2与O2在放电条件下直接制备
B.NO2有毒,但因其易溶于水且与水反应,因此不属于大气污染物
C.NO2既有氧化性也有还原性
D.NO2为红棕色气体,因此将NO2通入水中,溶液显红棕色
解析???? N2和O2在放电或高温条件下反应生成NO,故A错误;NO2属于大气污
染物之一,故B错误;NO2与H2O反应生成HNO3和NO,说明NO2既有氧化性又有
还原性,故C正确;NO2通入水中,生成NO和HNO3,溶液呈无色,故D错误。
C
3.将充满二氧化氮的试管倒立于盛有水的水槽中,充分放置后的现象正确的是
?( )
?
解析???? 将充满NO2的试管倒立于盛有水的水槽中,NO2与水反应可生成NO
气体,反应的化学方程式为3NO2+H2O? 2HNO3+NO,一氧化氮不溶于水,所
以试管中仍存在气体,根据化学方程式可知,液体大约会充满试管体积的三分
之二,约三分之一的部分被一氧化氮占有,故选B。
B
4.如图所示,室温下向盛有3.0 mL NO的试管中缓缓通入1.5 mL O2(所有气体的
体积均在标准状况下测定)。
?
试回答下列问题:
(1)写出观察到的现象(可不写满,也可补充):
① ????;
通入O2,试管内气体由无色变为红棕色
② ????;
③ ????。
(2)上述过程中发生反应的化学方程式有 ????????。
(3)最终试管中剩余的气体是 ????,体积为 ????。
试管内液面上升
试管内剩余无色气体
NO
1.0 mL
2NO+O2? 2NO2、3NO2+H2O? 2HNO3+NO
解析 (1)通入的O2与NO恰好完全反应生成NO2:2NO+O2? 2NO2,所以看到
有红棕色气体生成;生成的NO2溶于水:3NO2+H2O? 2HNO3+NO,气体体积减
小,所以会看到试管内液面上升;最终NO有剩余,所以试管内剩余无色气体。
(2)上述过程中发生反应的化学方程式有2NO+O2? 2NO2、3NO2+H2O?
2HNO3+NO。(3)设1.5 mL O2全部参加反应,由总反应4NO+3O2+2H2O?
4HNO3可知,V反应(NO)=V(O2)×?=1.5 mL×?=2.0 mL,而NO的总体积是3.0 mL,故
剩余NO气体的体积是1.0 mL。
1.下列用途中应用了氮气的稳定性的是?( )
A.以氮气为原料制硝酸
B.合成氨气和制氮肥
C.作食物保护气
D.镁可以和氮气反应
评价检测·课堂达标
C
解析???? 利用N2制备硝酸,发生的反应为N2+3H2? 2NH3、4NH3+
5O2? 4NO+6H2O、2NO+O2? 2NO2、3NO2+H2O? 2HNO3+NO,与
N2的稳定性无关,故A错误;根据A选项分析,合成氨气和制氮肥均与N2的稳定性
无关,故B错误;N2的化学性质相对稳定,因此N2常作食物保护气,与N2的稳定性
有关,故C正确;Mg能与N2反应生成Mg3N2,与N2的稳定性无关,故D错误。
2.在水体中部分含氮有机物的循环如图所示。图中属于氮的固定的是?(???? )
?
A.③ B.④ C.⑤ D.⑥
解析???? 将游离态的氮(即氮气)转化为化合态的氮(即氮的化合物)的过程,
叫做氮的固定,分析题图转化关系可知,图中属于氮的固定的是⑤,故选C。
C
3.宇宙飞船的运载火箭的推进器引燃后发生剧烈反应,产生大量高温气体,从
火箭尾部喷出。高温气体的成分有CO2、H2O、N2、NO等,这些气体均无色,
但在卫星发射现场看到火箭喷射出大量的红烟,产生红烟的原因是?( )
A.高温下N2遇空气生成NO2
B.NO与空气中的氧气反应生成NO2
C.CO2遇NO反应生成NO2
D.NO遇H2O反应生成NO2
解析???? 根据原高温气体成分均为无色,卫星发射现场却能看到红烟可推
知,是发生反应:2NO+O2? 2NO2,产生NO2而导致的。
B
4.将盛12 mL一氧化氮和36 mL二氧化氮混合气体的烧瓶倒置于水中,通入一
定量的氧气,完全反应后,剩余气体的体积为4 mL,则充入的氧气的体积可能为
?( )
A.19 mL B.20 mL C.21 mL D.22 mL
解析???? 已知4NO+3O2+2H2O? 4HNO3、4NO2+O2+2H2O? 4HNO3,若
剩余气体为氧气,则充入的氧气总体积为4 mL+12 mL×?+36 mL×?=22 mL;若
剩余气体为NO,则充入的氧气总体积为8 mL×?+36 mL×?=15 mL。
D
5.三效催化剂是最常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图
所示,下列说法正确的是?( )
A.在转化过程中,氮元素均被还原
B.依据图示推出催化剂不参与储存和
还原过程
C.还原过程中生成0.1 mol N2,转移电子
数为0.5NA
D.三效催化剂能有效实现汽车尾气中CO、NOx、CxHy三种成分的净化
D
解析???? 在转化过程中,氮元素的化合价先升高到+5,再降低到0,则应是先被
氧化,再被还原,故A错误;依据题图可知催化剂参与了储存和还原过程,故B错
误;还原过程中生成0.1 mol N2,不能确定N2由几价的N原子得电子生成,则转移
电子数不能确定,故C错误;三效催化剂能有效实现汽车尾气中CO、NOx、CxHy
三种成分的净化,故D正确。
6.某化学学习小组为探究NO2和SO2的反应,进行如下实验(如下图所示)。
?
(1)图1两集气瓶中 ????(填“上”或“下”)瓶颜色深。
(2)图2中反应的现象是 ????。
下
两气体混合后,颜色消失?
(3)图3中“有红棕色气体产生”说明SO2和NO2反应的产物中有 ????,说明
NO2在该反应中显 ????性。
(4)由图2和图3中的现象写出NO2和SO2反应的化学方程式: ??????。
NO
氧化???
NO2+SO2? NO+SO3
解析 题图3中反应生成的气体遇空气显红棕色,说明题图2中NO2和SO2反应
生成了NO,NO2转化为NO,表现氧化性,而SO2表现还原性,被氧化,S元素化合价
升高,只能变成+6价,应转化为SO3。
第二节 氮及其化合物
课时1 氮气与氮的固定 一氧化氮和二氧化氮
学习任务一 氮气与氮的固定
任务探究·深度学习
旧知回顾
自主学习
为了更好地保护文物,部分博物馆启用“真空充氮杀虫灭菌消毒机”来处理
和保护文物,将文物放入该机器内(氮气浓度可高达99.99%),密封三天,好氧菌
和丝状霉菌都会被灭杀。该机器具有此类功能,主要与氮气的性质有关。请
你结合相关化学知识回答,下列关于氮气的哪些说法是正确的?
①氮气的化学性质不活泼 ②氮气不能供给呼吸 ③氮气能抑制菌类的生长
④氮气能吸收部分水分 ⑤氮气不能与任何物质反应
?
答案 ①②③正确。
1.氮元素及其存在
(1)原子结构:氮元素位于元素周期表的第① ????周期、第② ????族,其原
子结构示意图为?,氮原子一般通过③ ????与其他原子相互
结合构成物质,常见化合价为④ ????。
(2)自然界中的存在形态
a.游离态:以⑤ ????的形式存在于空气中。
b.化合态:存在于动植物体内的蛋白质中,以及土壤、海洋里的硝酸盐和铵盐中。
新知梳理
二
ⅤA
共用电子对
-3、+5
氮分子
2.氮气的性质
(1)物理性质:无色、无味、难溶于水,密度与空气的相近,约占空气体积的4/5。
(2)化学性质
a.由于氮分子内两个氮原子间以共价三键(?)结合,断开该化学键需要
较多的能量,所以氮气的化学性质很稳定,通常情况下难以与其他物质发生化
学反应,无法被大多数生物体直接吸收。
b.在高温、放电等条件下,氮气能够与镁、氧气、氢气等物质发生化合反应,
化学方程式分别为⑥ 、⑦ ? ? ?
⑧ ????。
、
3.氮的固定和循环
(1)氮的固定
1)将大气中⑨ ????的过程叫做氮的固定。
2)固氮形式
a.自然固氮:大自然通过闪电释放的能量将空气中的氮气转化为⑩ ????的
化合物,或者通过豆科植物的根瘤菌将氮气转化成? ????。
b.人工固氮:通过控制条件,将氮气氧化或还原为氮的化合物。最重要的人工
固氮途径就是? ????。
游离态的氮转化为氮的化合物
含氮
氨
工业合成氨
(2)氮的循环
?
判断下列说法的正误(正确的画“√”,错误的画“?”)。
易错辨析
1.氮在自然界中只以游离态形式存在?( )
2.N2在高温条件下与O2发生反应生成NO?( )
3.豆科植物通过根瘤菌吸收空气中的氮属于氮的固定,发生的是化学变化?
( )
4.工业合成氨的过程是固氮的过程?( )
?
√
√
√
1.氮气是一种无色、无味的气体。在标准大气压下,冷却至-195.8 ℃时,变成没
有颜色的液体,冷却至-209.8 ℃时,液态氮变成雪状的固体。氮气的化学性质
不活泼,常被用来作防腐剂。但在一定条件下可与某些物质发生化学变化,用
来制取对人类有用的新物质。
?
互动探究
(1)请你根据所学知识回答氮气为什么可以用作粮食、瓜果的保护气?
(2)与同学交流或查阅资料分析液氮用于医疗手术的原理是什么?
答案????(1)氮气性质稳定,能够减缓粮食、瓜果被氧气氧化变质的速率。
(2)液氮挥发,吸收热量,使温度迅速下降,通过极度冷冻将病区细菌迅速杀死,
使得病区适宜进行医疗手术。
2.氮气的性质不活泼,但在一定条件下也可以发生化学反应,下列反应中属于
氮的固定的反应是哪几个?在属于氮的固定的反应中,氮气都作氧化剂吗?
①N2+3Mg? Mg3N2
②N2+3H2? 2NH3
③2NO+O2? 2NO2
④N2+O2? 2NO
答案 氮的固定是氮单质转变成氮的化合物的过程,所以反应①②④属于氮
的固定。反应①中氮气作氧化剂,反应②中氮气作氧化剂,反应④中氮气作还
原剂。
1.氮气化学性质稳定,但是在一定条件下能发生反应,既有氧化性又有还原性。
?
提炼归纳
2.氮的固定是氮的单质转化为氮的化合物的过程,氮的固定分为自然固氮和人
工固氮,二者都属于化学变化。
1.下列关于氮气的性质和用途的叙述中错误的是?( )
A.常温下,氮气是一种很难溶于水的无色、无味气体
B.通常情况下,很难与其他物质发生化学反应
C.从空气中分离出的氮气,可用于填充白炽灯的灯泡
D.从空气中分离出的氮气,不能用于生产氮肥
典题精练
解析???? 常温下,氮气是一种无色、无味的气体,且难溶于水,故A正确;氮气
的化学性质不活泼,通常情况下难与其他物质发生反应,故B正确;氮气的化学
性质不活泼,从空气中分离出的氮气,可用于填充白炽灯的灯泡,故C正确;从空
气中分离出的氮气,能用于生产氮肥,如N2→NH3→氮肥,故D错误。
D
2.下列关于氮气的说法中错误的是?( )
A.通常情况下氮气性质很稳定,所以氮气可作食物保护气
B.N2+O2? 2NO,该反应是汽车尾气造成污染的主要原因之一
C.氮气在空气中约占空气体积的?
D.在反应3Mg+N2? Mg3N2中,氮气作氧化剂
C
解析???? 氮气分子中含有氮氮三键,通常情况下N2性质很稳定,可作食物保护
气,故A正确;氮气与氧气在高温下反应生成一氧化氮,一氧化氮有毒,为空气污
染物,故B正确;N2在空气中约占空气体积的?,故C错误;在反应3Mg+N2?
Mg3N2中,氮气中氮元素化合价降低,所以N2作氧化剂,故D正确。
3.下列叙述中与氮的固定无关的是?( )
A.工业合成氨
B.工业上将氨转化成硝酸和其他氮的氧化物
C.豆科植物的根瘤菌吸收空气中的氮气并将之转化成植物蛋白质
D.电闪雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收
B
解析???? 工业合成氨是将氮气转化为氨气,属于氮的固定,故A不符合题意;
工业上将氨转化成硝酸和其他氮的氧化物,不是氮的固定,故B符合题意;豆科
植物的根瘤菌吸收空气中的氮气并将之转化成植物蛋白是氮的固定,故C不符
合题意;电闪雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收,
属于氮的固定,故D不符合题意。
4.自然界中氮的循环如图所示。下列说法不正确的是( )
A.工业合成氨属于人工固氮
B.在雷电作用下N2与O2可发生化学反应
C.在氮的循环过程中不涉及氧化还原反应
D.含氮无机物与含氮有机物可相互转化
解析???? N2与O2生成NO的反应是氧化还原反应,所以在氮的循环过程中涉
及氧化还原反应,故C错误。
C
学习任务二 一氧化氮和二氧化氮
新知梳理
自主学习
1.NO和NO2的物理性质
NO
① ????色、有毒气体,② ????溶于水
NO2
③ ????色、有刺激性气味的有毒气体,密度比空气的大,易④ ????,易溶于水
2.NO和NO2的化学性质
(1)在常温下,NO很容易与O2反应,化学方程式为⑤ ??????。
(2)NO2溶于水时发生反应的化学方程式为⑥ ??????。
无
不
红棕
液化
3.二氧化氮溶于水的实验
(1)实验过程
实验
装置
?
实验
操作
在如图注射器里充入20 mL NO,然后吸入5 mL水,用乳胶管和弹簧夹封住管口,振荡注射器
打开弹簧夹,快速吸入
10 mL空气后夹上弹簧夹
振荡注射器
实验
现象
无明显现象
无色气体变为红棕色
红棕色气体变浅至消失,有无色气体生成,注射器活塞向内滑动
化学
方程式
⑦ ????、
⑧ ????
(2)对工业生产硝酸的启示
工业上生产硝酸时,向吸收后的废气中再通入适量的氧气或空气,能充分利用
原料,并能减少NO的排放以保护环境。
1.常温下能用排空气法收集一氧化氮吗?为什么?实验室中应该怎样收集一氧
化氮?
互动探究
答案 不能。因为发生反应:2NO+O2? 2NO2。实验室中应该用排水集气
法收集一氧化氮。
2.NO2转化为NO的变化中,NO2只能作氧化剂吗?
答案 NO2与水反应转化为NO的同时生成硝酸,NO2既作氧化剂又作还原剂。
3.把一支充满NO2气体的试管倒置在水槽中充分反应后有什么现象?
答案 由反应3NO2+H2O? 2HNO3+NO可知:当NO2与H2O充分反应后,试管
内气体变为无色,且剩余气体占试管体积的1/3。
4.为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置(夹
持装置已省略),并检查装置的气密性,实验前用排水法收集NO。
?
(1)打开止水夹,推动注射器活塞,使O2进入烧瓶。关上止水夹,首先观察到烧瓶
中的现象是什么?写出产生此现象的化学方程式。
(2)轻轻摇动烧瓶,观察到烧瓶中的现象是什么?利用化学方程式解释产生这种
现象的原因是什么?
(3)假设烧瓶内充有100 mL NO,通入多少O2才能使水充满试管?
答案 (1)首先观察到的现象是烧瓶中的气体由无色变为红棕色,反应的化学
方程式为2NO+O2? 2NO2。
(2)摇动烧瓶,使得NO2与水发生反应:3NO2+H2O? 2HNO3+NO,所以烧瓶中
的红棕色气体又变为无色,且烧瓶内压强减小,烧杯中的水倒吸到烧瓶内,导致
烧瓶中液面上升。
(3)已知:2NO+O2? 2NO2 ①,3NO2+H2O? 2HNO3+NO ②,由反应的化
学方程式①×3+②×2得:4NO+3O2+2H2O? 4HNO3,即当NO和O2的体积比为
4∶3时水可以充满试管,故需通入75 mL O2。
5.农业上有一句俗语“雷雨发庄稼”,其中就涉及氮及其化合物的转化:在一
定条件下,氮气最终转化为硝酸,然后HNO3与土壤中的矿物作用生成硝酸盐,
为庄稼提供氮肥。请你结合本节知识,写出氮气转化为硝酸的化学方程式。
?
答案 氮气转化为硝酸的化学方程式有N2+O2? 2NO、2NO+O2? 2NO2、
3NO2+H2O? 2HNO3+NO。
1.NO和NO2的性质对比
提炼归纳
项目
NO
NO2
色、态、
味、毒性
无色、无味
红棕色、有刺激性气味
有毒气体
水溶性
不溶
易溶且能与水反应
与O2反应
2NO+O2? 2NO2
——
与H2O反应
——
3NO2+H2O? 2HNO3+NO
与O2、H2O共同反应
4NO+3O2+2H2O? 4HNO3
4NO2+O2+2H2O? 4HNO3
氧化性
6NO+4NH3 ? 5N2+6H2O
6NO2+8NH3? 7N2+12HO, NO2+SO2? SO3+NO,NO2
能使湿润的淀粉-KI试纸变蓝
2.氮的氧化物溶于水的计算规律
(1)相关反应原理
3NO2+H2O? 2HNO3+NO a
2NO+O2? 2NO2 b
由化学方程式a×2+b得:
4NO2+O2+2H2O? 4HNO3 c
由化学方程式a×2+b×3得:
4NO+3O2+2H2O? 4HNO3 d
(2)氮的氧化物溶于水的三种类型
①NO2:NO2溶于水时仅涉及反应a,剩余气体为NO;
②NO2和O2的混合气体:NO2和O2的混合气体溶于水时涉及反应c。NO2和O2的
量的关系见下表:
x=?
0
x>?
反应情况
O2过量并剩余
恰好完全反应
NO2过量又发生反应a,
剩余NO
③NO和O2的混合气体:NO和O2的混合气体溶于水时涉及反应d。NO和O2
的量的关系见下表:
x=?
0
x>?
反应情况
O2过量并剩余
恰好完全反应
NO过量并剩余
1.病毒学研究证实,一氧化氮对某些病毒有直接抑制作用。下列关于一氧化氮
的叙述不正确的是?( )
A.一氧化氮是无色气体
B.常温常压下,一氧化氮不能与空气中的氧气直接化合
C.含等质量氧元素的一氧化氮与一氧化碳的物质的量相等
D.一氧化氮不溶于水,能用排水法收集
典题精练
解析???? 一氧化氮很不稳定,极易和空气中的氧气反应生成红棕色的二氧化
氮气体,故B错误。
B
2.下列有关NO2的说法正确的是?( )
A.NO2可由N2与O2在放电条件下直接制备
B.NO2有毒,但因其易溶于水且与水反应,因此不属于大气污染物
C.NO2既有氧化性也有还原性
D.NO2为红棕色气体,因此将NO2通入水中,溶液显红棕色
解析???? N2和O2在放电或高温条件下反应生成NO,故A错误;NO2属于大气污
染物之一,故B错误;NO2与H2O反应生成HNO3和NO,说明NO2既有氧化性又有
还原性,故C正确;NO2通入水中,生成NO和HNO3,溶液呈无色,故D错误。
C
3.将充满二氧化氮的试管倒立于盛有水的水槽中,充分放置后的现象正确的是
?( )
?
解析???? 将充满NO2的试管倒立于盛有水的水槽中,NO2与水反应可生成NO
气体,反应的化学方程式为3NO2+H2O? 2HNO3+NO,一氧化氮不溶于水,所
以试管中仍存在气体,根据化学方程式可知,液体大约会充满试管体积的三分
之二,约三分之一的部分被一氧化氮占有,故选B。
B
4.如图所示,室温下向盛有3.0 mL NO的试管中缓缓通入1.5 mL O2(所有气体的
体积均在标准状况下测定)。
?
试回答下列问题:
(1)写出观察到的现象(可不写满,也可补充):
① ????;
通入O2,试管内气体由无色变为红棕色
② ????;
③ ????。
(2)上述过程中发生反应的化学方程式有 ????????。
(3)最终试管中剩余的气体是 ????,体积为 ????。
试管内液面上升
试管内剩余无色气体
NO
1.0 mL
2NO+O2? 2NO2、3NO2+H2O? 2HNO3+NO
解析 (1)通入的O2与NO恰好完全反应生成NO2:2NO+O2? 2NO2,所以看到
有红棕色气体生成;生成的NO2溶于水:3NO2+H2O? 2HNO3+NO,气体体积减
小,所以会看到试管内液面上升;最终NO有剩余,所以试管内剩余无色气体。
(2)上述过程中发生反应的化学方程式有2NO+O2? 2NO2、3NO2+H2O?
2HNO3+NO。(3)设1.5 mL O2全部参加反应,由总反应4NO+3O2+2H2O?
4HNO3可知,V反应(NO)=V(O2)×?=1.5 mL×?=2.0 mL,而NO的总体积是3.0 mL,故
剩余NO气体的体积是1.0 mL。
1.下列用途中应用了氮气的稳定性的是?( )
A.以氮气为原料制硝酸
B.合成氨气和制氮肥
C.作食物保护气
D.镁可以和氮气反应
评价检测·课堂达标
C
解析???? 利用N2制备硝酸,发生的反应为N2+3H2? 2NH3、4NH3+
5O2? 4NO+6H2O、2NO+O2? 2NO2、3NO2+H2O? 2HNO3+NO,与
N2的稳定性无关,故A错误;根据A选项分析,合成氨气和制氮肥均与N2的稳定性
无关,故B错误;N2的化学性质相对稳定,因此N2常作食物保护气,与N2的稳定性
有关,故C正确;Mg能与N2反应生成Mg3N2,与N2的稳定性无关,故D错误。
2.在水体中部分含氮有机物的循环如图所示。图中属于氮的固定的是?(???? )
?
A.③ B.④ C.⑤ D.⑥
解析???? 将游离态的氮(即氮气)转化为化合态的氮(即氮的化合物)的过程,
叫做氮的固定,分析题图转化关系可知,图中属于氮的固定的是⑤,故选C。
C
3.宇宙飞船的运载火箭的推进器引燃后发生剧烈反应,产生大量高温气体,从
火箭尾部喷出。高温气体的成分有CO2、H2O、N2、NO等,这些气体均无色,
但在卫星发射现场看到火箭喷射出大量的红烟,产生红烟的原因是?( )
A.高温下N2遇空气生成NO2
B.NO与空气中的氧气反应生成NO2
C.CO2遇NO反应生成NO2
D.NO遇H2O反应生成NO2
解析???? 根据原高温气体成分均为无色,卫星发射现场却能看到红烟可推
知,是发生反应:2NO+O2? 2NO2,产生NO2而导致的。
B
4.将盛12 mL一氧化氮和36 mL二氧化氮混合气体的烧瓶倒置于水中,通入一
定量的氧气,完全反应后,剩余气体的体积为4 mL,则充入的氧气的体积可能为
?( )
A.19 mL B.20 mL C.21 mL D.22 mL
解析???? 已知4NO+3O2+2H2O? 4HNO3、4NO2+O2+2H2O? 4HNO3,若
剩余气体为氧气,则充入的氧气总体积为4 mL+12 mL×?+36 mL×?=22 mL;若
剩余气体为NO,则充入的氧气总体积为8 mL×?+36 mL×?=15 mL。
D
5.三效催化剂是最常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图
所示,下列说法正确的是?( )
A.在转化过程中,氮元素均被还原
B.依据图示推出催化剂不参与储存和
还原过程
C.还原过程中生成0.1 mol N2,转移电子
数为0.5NA
D.三效催化剂能有效实现汽车尾气中CO、NOx、CxHy三种成分的净化
D
解析???? 在转化过程中,氮元素的化合价先升高到+5,再降低到0,则应是先被
氧化,再被还原,故A错误;依据题图可知催化剂参与了储存和还原过程,故B错
误;还原过程中生成0.1 mol N2,不能确定N2由几价的N原子得电子生成,则转移
电子数不能确定,故C错误;三效催化剂能有效实现汽车尾气中CO、NOx、CxHy
三种成分的净化,故D正确。
6.某化学学习小组为探究NO2和SO2的反应,进行如下实验(如下图所示)。
?
(1)图1两集气瓶中 ????(填“上”或“下”)瓶颜色深。
(2)图2中反应的现象是 ????。
下
两气体混合后,颜色消失?
(3)图3中“有红棕色气体产生”说明SO2和NO2反应的产物中有 ????,说明
NO2在该反应中显 ????性。
(4)由图2和图3中的现象写出NO2和SO2反应的化学方程式: ??????。
NO
氧化???
NO2+SO2? NO+SO3
解析 题图3中反应生成的气体遇空气显红棕色,说明题图2中NO2和SO2反应
生成了NO,NO2转化为NO,表现氧化性,而SO2表现还原性,被氧化,S元素化合价
升高,只能变成+6价,应转化为SO3。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
