高中化学必修一人教版(2019)第三章 第一节 第一课时 铁的单质 课件(共27张PPT)
文档属性
| 名称 | 高中化学必修一人教版(2019)第三章 第一节 第一课时 铁的单质 课件(共27张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 33.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-08 00:00:00 | ||
图片预览








文档简介
主讲老师:刘老师
第三章 铁 金属材料
3.1.1 铁的单质
第一节 铁及其化合物
学业要求
核心素养对接
1.能列举、描述、辨识铁及其重要化合物的重要物理性质、化学性质及实验现象。
2.能利用氢氧化亚铁的性质,设计其制备方案。
3.能说明Fe2+、Fe3+的检验及其之间的相互转化。
4.能说明铁及其化合物的应用。
1.能利用氢氧化亚铁的性质,设计其制备方案,以培养学生科学探究与创新意识的素养水平。
2.利用Fe2+、Fe3+的检验及其之间的相互转化,培养学生变化观念与平衡思想的素养水平。
图铁冶秋春
秦代铁权
陨石
宝钢夜景
一、铁在自然界的分布
陨铁
赤铁矿
磁铁矿
陨铁是铁的单质,但是铁主要以化合物的形式存在于矿石中
钠在自然界有单质吗?
没有
为什么铁有?
铁的金属活动性弱
战国铁剑
打铁炉
战国铁炉
我国从很早之前就掌握了冶铁技术
1、铁的物理性质
二、单质铁
铁是银白色金属单质
熔点:1535℃
沸点:2750℃
密度:7.86g/cm3
以上数据明显高于金属钠,铁的硬度也比金属钠高得多
方铁
圆铁
颜色、状态
导电、导热性、延展性
特性
地壳含量
_______固体
良好
能被____ 吸引
占第__位
银白色
磁铁
4
1、铁的物理性质
金属单质一般与什么物质反应?
非金属单质,水、酸、盐溶液等
思考与交流 :根据上述推测和之前学习的化学知识,对比金属铁和钠的性质,填写下表
{5940675A-B579-460E-94D1-54222C63F5DA}
铁
钠
非金属单质
酸
盐溶液
水
{5940675A-B579-460E-94D1-54222C63F5DA}
铁
钠
非金属单质
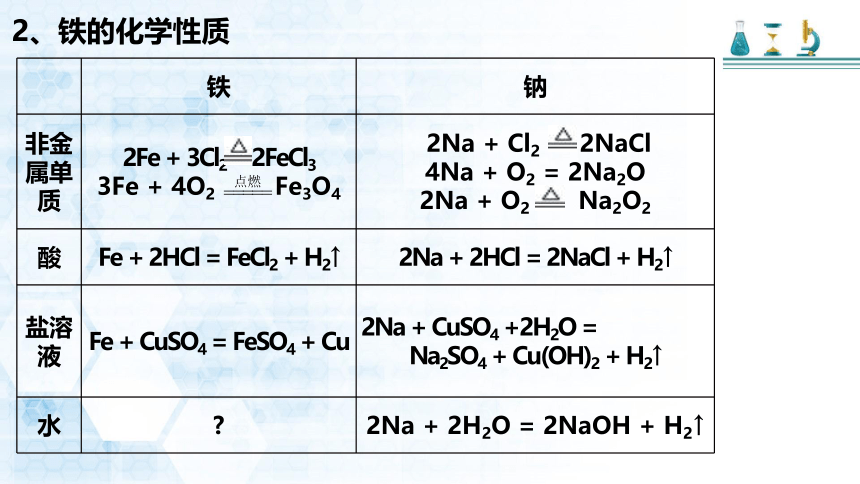
2Fe + 3Cl2 2FeCl3
3Fe + 4O2 Fe3O4
2Na + Cl2 2NaCl
4Na + O2 = 2Na2O
2Na + O2 Na2O2
酸
Fe + 2HCl = FeCl2 + H2↑
2Na + 2HCl = 2NaCl + H2↑
盐溶液
Fe + CuSO4 = FeSO4 + Cu
2Na + CuSO4 +2H2O =
Na2SO4 + Cu(OH)2 + H2↑
水
?
2Na + 2H2O = 2NaOH + H2↑
2、铁的化学性质
铁与钠的化学性质的区别:
1、铁有+2和+3的变价,所以在反应中要注意得到的物质 中铁元素的化合价
铁有变价,那么是什么在决定生成物中铁元素的化合价呢?
氧化剂的氧化性
上面的反应中氧化性较强的是什么物质?
氯气
2、铁的反应现象远没有钠的反应剧烈
铁比钠的活动性弱
{5940675A-B579-460E-94D1-54222C63F5DA}
铁
钠
非金属单质
2Fe + 3Cl2 2FeCl3
3Fe + 4O2 Fe3O4
2Na + Cl2 2NaCl
4Na + O2 = 2Na2O
2Na + O2 Na2O2
酸
Fe + 2HCl = FeCl2 + H2↑
2Na + 2HCl = 2NaCl + H2↑
盐溶液
Fe + CuSO4 = FeSO4 + Cu
2Na + CuSO4 +2H2O =
Na2SO4 + Cu(OH)2 + H2↑
水
?
2Na + 2H2O = 2NaOH + H2↑
铁与水能反应吗?
从生活常识可以知道,铁与冷水,甚至是沸腾的水都不反应在更高的温度下两者能不能反应呢?
【探究】设计一个简单的实验装置,使还原铁粉与水蒸气反应。要求装置中含有以下三个部分:
(1)水蒸气的发生装置
(2)水蒸气与铁粉反应装置
(3)产物的检验(收集)装置
水蒸气的发生装置
水蒸气与铁粉反应装置
产物收集装置
(1)条件:给你3支试管、水槽、蒸发皿、胶塞、导管、酒精喷灯及其他必要的仪器和物品,画出你设计的装置简图。
【实验探究】
思考:
(1)水蒸气怎样制取?
(2)该反应在什么条件下进行?
(3)反应的产物是什么?如何验证?
(2)有人设计了下图装置,用一支大试管代替3支试管就能完成实验,想想其中的原理。
铁与水蒸气的反应:
3Fe + 4H2O(g)
Fe3O4 + 4H2
△
【思考与交流】
实验过程中应注意哪些问题?
肥皂水不能太稀,否则吹起的气泡太小,点燃时难有较大的爆鸣声;
实验结束时应先从肥皂水中撤出导管,再移去燃着的酒精灯。
【现象和结论】
红热的铁与水蒸气反应放出气体,蒸发皿中产生大量肥皂泡,点燃时能燃烧或发出爆鸣声----氢气,反应后试管内固体仍为黑色---四氧化三铁。
红热的铁可以与水蒸气反应,反应方程式为:
3Fe + 4H2O(g) Fe3O4 + 4H2
在钢铁厂的生产中,炽热的铁水或者是钢水注入模具之前,模具必须进行充分的干燥,这样操作的原因是什么?
避免高温下铁与水反应,生成四氧化三铁
1.下列关于铁的叙述中错误的是
A.纯净的铁是光亮的银白色金属
B.铁能被磁体吸引
C.铁是地壳中含量最多的金属元素
D.铁具有延展性和导热性,可制作炊具
√
解析 铁元素在地壳中含量是金属元素的第二位。
练习
2.下列反应中,铁只能生成+3价化合物的是
A.少量铁与稀硫酸反应
B.铁丝在氧气中燃烧
C.过量铁粉在氯气中燃烧
D.Fe投入到CuSO4溶液中
√
解析 C项,虽然铁粉过量,但因为不是在溶液中进行的反应,只能生成FeCl3。
3.a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知(1)a、c均能与稀硫酸反应放出气体;(2)b与d的硝酸盐反应,置换出单质d;(3)c与强碱反应放出气体,e的一种氧化物具有磁性。由此判断a、b、c、d、e依次为( )
A.Fe、Cu、Al、Ag、Mg
B.Mg、Cu、Al、Ag、Fe
C.Al、Cu、Mg、Ag、Fe
D.Mg、Ag、Al、Cu、Fe
B
4.铁与水蒸气反应的实验装置如图,下列说法正确的是
A.实验时,试管口应高于试管底
B.加热时试管内生成黑色物质,点燃肥皂泡可听到爆鸣声
C.反应的化学方程式为2Fe+3H2O(g) Fe2O3+3H2
D.试管中发生化合反应
√
解析 铁与水蒸气反应生成Fe3O4和H2,属于置换反应,实验时应使试管口低于试管底。
资料卡片:人体中的铁元素
微量元素——铁
铁是我们人体所的重要微量元素之一,人体内铁含量4~5g,其中60%~75%的铁存在于血红蛋白,3%存在于肌红蛋白,1%在含铁酶类(如细胞色素化酶,过氧化物酶等),辅助因子及运铁载体中,其余25%~30%的铁及铁蛋白和含铁血黄素的形式存在于肝脏,脾脏和骨髓里。人体没有游离铁离子,铁元素都以与蛋白质的结合形式存在。
铁的生理功能
①参与氧气和二氧化碳运输:铁是血红蛋白的重要组成部分,血红蛋白的功能是向细胞输送氧气,并将二氧化碳带出细胞。
②维持正常的造血功能:红细胞中约含机体总铁量的2/3。铁与红细胞的形成和成熟有密切关系,缺铁会导致新生红细胞中血红蛋白量不足。
③参与氧转运和存储:铁是肌红蛋白的原料,肌红蛋白是由一个血红素和一个球蛋白组成,仅存在于肌肉组织内,其基本功能实在肌肉组织中转运和储存氧。
④增强机体免疫力:铁可以增强机体的免疫力,增加中性粒细胞和吞噬细胞的吞噬功能,同时也增强机体的抗感染能力。
缺铁性贫血已成为仅次于结核病的全球患病率最高、耗资最大的公共卫生问题。那铁元素在人体中又是以什么形式存在呢?
二价铁为人体的主要存在形式
1、铁的物理性质:
小结:
2、铁的化学性质:
银白色金属,良好的导电、导热性、延展性。
Fe+2H+===Fe2++H2↑
Fe+Cu2+===Fe2++Cu
Fe+2Fe3+===3Fe2+
化学课堂欢迎你
其他内容 且听下回分解
第三章 铁 金属材料
3.1.1 铁的单质
第一节 铁及其化合物
学业要求
核心素养对接
1.能列举、描述、辨识铁及其重要化合物的重要物理性质、化学性质及实验现象。
2.能利用氢氧化亚铁的性质,设计其制备方案。
3.能说明Fe2+、Fe3+的检验及其之间的相互转化。
4.能说明铁及其化合物的应用。
1.能利用氢氧化亚铁的性质,设计其制备方案,以培养学生科学探究与创新意识的素养水平。
2.利用Fe2+、Fe3+的检验及其之间的相互转化,培养学生变化观念与平衡思想的素养水平。
图铁冶秋春
秦代铁权
陨石
宝钢夜景
一、铁在自然界的分布
陨铁
赤铁矿
磁铁矿
陨铁是铁的单质,但是铁主要以化合物的形式存在于矿石中
钠在自然界有单质吗?
没有
为什么铁有?
铁的金属活动性弱
战国铁剑
打铁炉
战国铁炉
我国从很早之前就掌握了冶铁技术
1、铁的物理性质
二、单质铁
铁是银白色金属单质
熔点:1535℃
沸点:2750℃
密度:7.86g/cm3
以上数据明显高于金属钠,铁的硬度也比金属钠高得多
方铁
圆铁
颜色、状态
导电、导热性、延展性
特性
地壳含量
_______固体
良好
能被____ 吸引
占第__位
银白色
磁铁
4
1、铁的物理性质
金属单质一般与什么物质反应?
非金属单质,水、酸、盐溶液等
思考与交流 :根据上述推测和之前学习的化学知识,对比金属铁和钠的性质,填写下表
{5940675A-B579-460E-94D1-54222C63F5DA}
铁
钠
非金属单质
酸
盐溶液
水
{5940675A-B579-460E-94D1-54222C63F5DA}
铁
钠
非金属单质
2Fe + 3Cl2 2FeCl3
3Fe + 4O2 Fe3O4
2Na + Cl2 2NaCl
4Na + O2 = 2Na2O
2Na + O2 Na2O2
酸
Fe + 2HCl = FeCl2 + H2↑
2Na + 2HCl = 2NaCl + H2↑
盐溶液
Fe + CuSO4 = FeSO4 + Cu
2Na + CuSO4 +2H2O =
Na2SO4 + Cu(OH)2 + H2↑
水
?
2Na + 2H2O = 2NaOH + H2↑
2、铁的化学性质
铁与钠的化学性质的区别:
1、铁有+2和+3的变价,所以在反应中要注意得到的物质 中铁元素的化合价
铁有变价,那么是什么在决定生成物中铁元素的化合价呢?
氧化剂的氧化性
上面的反应中氧化性较强的是什么物质?
氯气
2、铁的反应现象远没有钠的反应剧烈
铁比钠的活动性弱
{5940675A-B579-460E-94D1-54222C63F5DA}
铁
钠
非金属单质
2Fe + 3Cl2 2FeCl3
3Fe + 4O2 Fe3O4
2Na + Cl2 2NaCl
4Na + O2 = 2Na2O
2Na + O2 Na2O2
酸
Fe + 2HCl = FeCl2 + H2↑
2Na + 2HCl = 2NaCl + H2↑
盐溶液
Fe + CuSO4 = FeSO4 + Cu
2Na + CuSO4 +2H2O =
Na2SO4 + Cu(OH)2 + H2↑
水
?
2Na + 2H2O = 2NaOH + H2↑
铁与水能反应吗?
从生活常识可以知道,铁与冷水,甚至是沸腾的水都不反应在更高的温度下两者能不能反应呢?
【探究】设计一个简单的实验装置,使还原铁粉与水蒸气反应。要求装置中含有以下三个部分:
(1)水蒸气的发生装置
(2)水蒸气与铁粉反应装置
(3)产物的检验(收集)装置
水蒸气的发生装置
水蒸气与铁粉反应装置
产物收集装置
(1)条件:给你3支试管、水槽、蒸发皿、胶塞、导管、酒精喷灯及其他必要的仪器和物品,画出你设计的装置简图。
【实验探究】
思考:
(1)水蒸气怎样制取?
(2)该反应在什么条件下进行?
(3)反应的产物是什么?如何验证?
(2)有人设计了下图装置,用一支大试管代替3支试管就能完成实验,想想其中的原理。
铁与水蒸气的反应:
3Fe + 4H2O(g)
Fe3O4 + 4H2
△
【思考与交流】
实验过程中应注意哪些问题?
肥皂水不能太稀,否则吹起的气泡太小,点燃时难有较大的爆鸣声;
实验结束时应先从肥皂水中撤出导管,再移去燃着的酒精灯。
【现象和结论】
红热的铁与水蒸气反应放出气体,蒸发皿中产生大量肥皂泡,点燃时能燃烧或发出爆鸣声----氢气,反应后试管内固体仍为黑色---四氧化三铁。
红热的铁可以与水蒸气反应,反应方程式为:
3Fe + 4H2O(g) Fe3O4 + 4H2
在钢铁厂的生产中,炽热的铁水或者是钢水注入模具之前,模具必须进行充分的干燥,这样操作的原因是什么?
避免高温下铁与水反应,生成四氧化三铁
1.下列关于铁的叙述中错误的是
A.纯净的铁是光亮的银白色金属
B.铁能被磁体吸引
C.铁是地壳中含量最多的金属元素
D.铁具有延展性和导热性,可制作炊具
√
解析 铁元素在地壳中含量是金属元素的第二位。
练习
2.下列反应中,铁只能生成+3价化合物的是
A.少量铁与稀硫酸反应
B.铁丝在氧气中燃烧
C.过量铁粉在氯气中燃烧
D.Fe投入到CuSO4溶液中
√
解析 C项,虽然铁粉过量,但因为不是在溶液中进行的反应,只能生成FeCl3。
3.a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知(1)a、c均能与稀硫酸反应放出气体;(2)b与d的硝酸盐反应,置换出单质d;(3)c与强碱反应放出气体,e的一种氧化物具有磁性。由此判断a、b、c、d、e依次为( )
A.Fe、Cu、Al、Ag、Mg
B.Mg、Cu、Al、Ag、Fe
C.Al、Cu、Mg、Ag、Fe
D.Mg、Ag、Al、Cu、Fe
B
4.铁与水蒸气反应的实验装置如图,下列说法正确的是
A.实验时,试管口应高于试管底
B.加热时试管内生成黑色物质,点燃肥皂泡可听到爆鸣声
C.反应的化学方程式为2Fe+3H2O(g) Fe2O3+3H2
D.试管中发生化合反应
√
解析 铁与水蒸气反应生成Fe3O4和H2,属于置换反应,实验时应使试管口低于试管底。
资料卡片:人体中的铁元素
微量元素——铁
铁是我们人体所的重要微量元素之一,人体内铁含量4~5g,其中60%~75%的铁存在于血红蛋白,3%存在于肌红蛋白,1%在含铁酶类(如细胞色素化酶,过氧化物酶等),辅助因子及运铁载体中,其余25%~30%的铁及铁蛋白和含铁血黄素的形式存在于肝脏,脾脏和骨髓里。人体没有游离铁离子,铁元素都以与蛋白质的结合形式存在。
铁的生理功能
①参与氧气和二氧化碳运输:铁是血红蛋白的重要组成部分,血红蛋白的功能是向细胞输送氧气,并将二氧化碳带出细胞。
②维持正常的造血功能:红细胞中约含机体总铁量的2/3。铁与红细胞的形成和成熟有密切关系,缺铁会导致新生红细胞中血红蛋白量不足。
③参与氧转运和存储:铁是肌红蛋白的原料,肌红蛋白是由一个血红素和一个球蛋白组成,仅存在于肌肉组织内,其基本功能实在肌肉组织中转运和储存氧。
④增强机体免疫力:铁可以增强机体的免疫力,增加中性粒细胞和吞噬细胞的吞噬功能,同时也增强机体的抗感染能力。
缺铁性贫血已成为仅次于结核病的全球患病率最高、耗资最大的公共卫生问题。那铁元素在人体中又是以什么形式存在呢?
二价铁为人体的主要存在形式
1、铁的物理性质:
小结:
2、铁的化学性质:
银白色金属,良好的导电、导热性、延展性。
Fe+2H+===Fe2++H2↑
Fe+Cu2+===Fe2++Cu
Fe+2Fe3+===3Fe2+
化学课堂欢迎你
其他内容 且听下回分解
