2020-2021学年九年级化学人教版下册 第九单元 溶液单元测试题(有解析答案)
文档属性
| 名称 | 2020-2021学年九年级化学人教版下册 第九单元 溶液单元测试题(有解析答案) |  | |
| 格式 | docx | ||
| 文件大小 | 96.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-08 21:24:27 | ||
图片预览




文档简介
1049020010693400123190000第9单元 溶液 单元测试题
(满分100分;时间:90分钟)
一、 选择题 (本题共计 14 小题 ,每题 2 分 ,共计28分 , ) ?
1. 下列说法正确的是( )
A.修车工用汽油洗掉手上的油污属乳化现象
B.均一稳定的液体都是溶液
C.为加快路面冰雪融化,可向积雪上撒些食盐
D.煮沸的水温度比煮沸的咸汤温度高
?
2. 无土栽培的某种营养液中,含硝酸钾的质量分数为7.1%,某蔬菜生产基地欲配制该营养液200kg,需要硝酸钾的质量为( )
A.7.1kg B.14.2kg C.71kg D.142kg
?
3. 在什么条件下,糖溶解速度最快( )
A.80??C的水加入冰糖块
B.20??C的水加入白糖(颗粒状)
C.80??C的水加入白糖(颗粒状)
D.20??C的水加入冰糖块
?
4. 如图是甲、乙两种固体的溶解度曲线,下列叙述正确的是( )
A.20??C时,甲的溶解度大于乙的溶解度
B.40??C时,甲、乙溶液中溶质的质量分数相等
C.采用降温的方法可将乙的不饱和溶液转化为饱和溶液
D.60??C时,甲的饱和溶液中溶质与溶液的质量比为3:8
?
5. 下列溶液中,溶剂不是水的是( )
A.食盐水 B.雪碧 C.食醋 D.碘酒
?
6. 实验室用氯化钠固体配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是(????????)
A.实验的步骤为计算、称量、量取、溶解
B.量取水时,用到的仪器是量筒和胶头滴管
C.若用量筒量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8%
D.溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解
?
7. 将下列物质分别加入水中,能形成溶液的是( )
A.酒精 B.面粉 C.花生油 D.冰块
?
8. 鱼类腥味产生的原因是由于鱼身上存在有机化学物质甲胺.甲胺易溶于乙醇,因此,煮鱼时加些酒,能使甲胺溶于乙醇并随加热后挥发逸去,经过这样烹饪的鱼就不再有腥味了.下列过程与上面所述原理不相似的是( )
A.用汽油除去衣服上的油污 B.用水除去衣服上的汗渍
C.用洗洁精洗碗 D.用酒精将试管壁上的碘洗掉
?9. 将一定质量的食盐溶解在?10mL?水中,下列等式一定成立的是( )
A.食盐质量+水的质量=溶液的质量
B.食盐体积+水的体积=溶液的体积
C.溶质质量+水的质量=溶液的质量
D.食盐密度+水的密度=溶液的密度
?
10. 下列说法正确的是( )
A.凡是均一、稳定的液体都是溶液
B.配制溶液时只能用水作溶剂
C.用酒精作溶剂的溶液,叫做酒精溶液
D.植物油、水、洗洁精混合振动后形成稳定的液体,该液体是溶液
?
11. 向澄清的石灰水中连续通入CO2,直至过量的全过程中,下列转变关系正确的是( )
A.溶液→乳浊液→溶液 B.溶液→悬浊液→乳浊液
C.悬浊液→乳浊液→溶液 D.溶液→悬浊液→溶液
?12. 下列物质依次为悬浊液、乳浊液、溶液的一组是( )
A.牛奶、汽水、石灰浆
B.矿泉水、自来水、汽油和水的混合物
C.江水、乳白鱼肝油、碘酒
D.盐酸、泥浆、“健力宝”饮料
?
13. 在一定温度下,向盛有200g某氯化钠溶液中再加入10g氯化钠,充分搅拌后,肯定不会改变的是( )
A.氯化钠的溶解度 B.溶液的质量
C.溶液中溶质的质量分数 D.溶液中溶质的质量
?
14. 溶解度为S克的某物质的饱和溶液,跟水以1:4的质量比混合后,溶液的质量百分比浓度为( )
A.80S100+S×100% B.20S100+S×100%
C.80S100+S% D.20S100+S%
二、 多选题 (本题共计 5 小题 ,每题 3 分 ,共计15分 , ) ?
15. 小英的妈妈在洗碗筷时,经常在水中加入一种物质,很快就能将“油乎乎”的菜盘洗得干干净净.小英的妈妈在水中加入的物质可能是( )
A.烧碱 B.洗洁精 C.纯碱 D.汽油
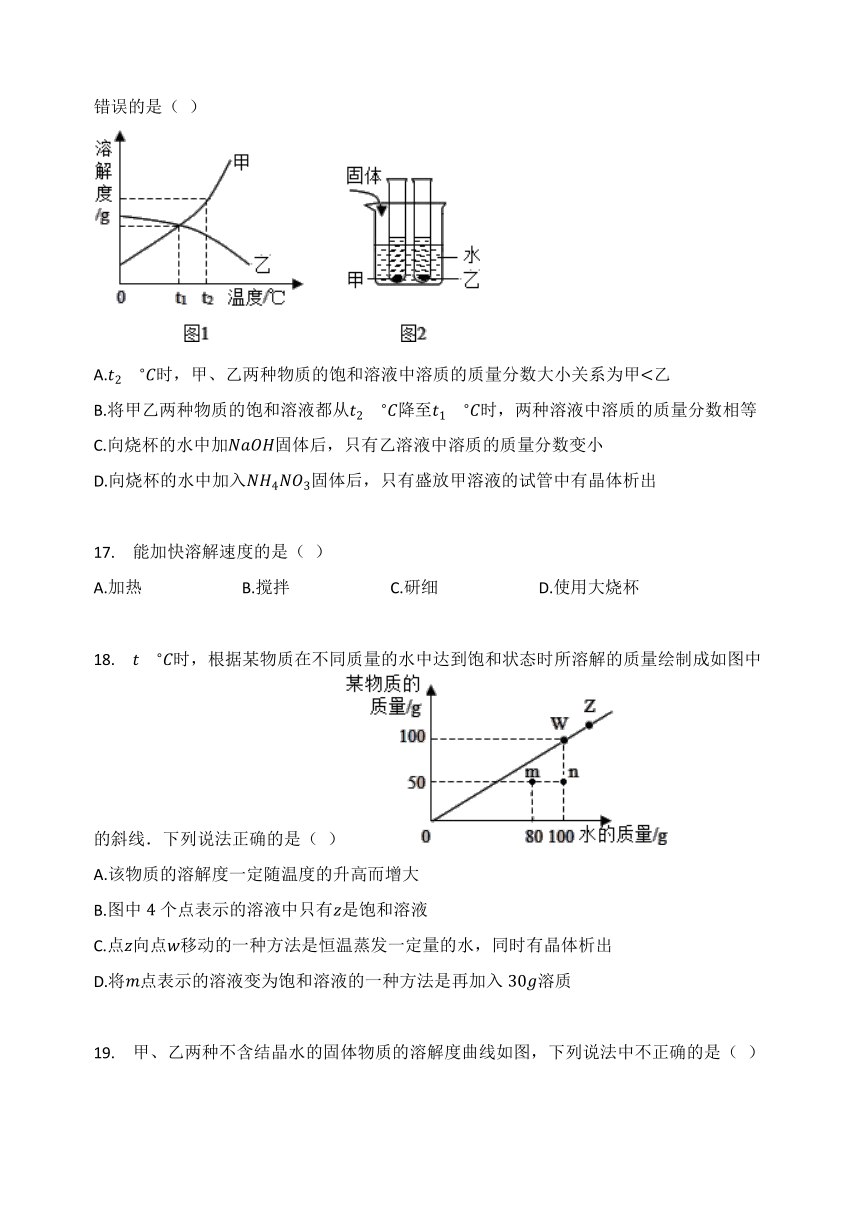
?16. 图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2??C下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发).根据图象和有关信息判断,下列说法中错误的是( )
A.t2??C时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲<乙
B.将甲乙两种物质的饱和溶液都从t2??C降至t1??C时,两种溶液中溶质的质量分数相等
C.向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小
D.向烧杯的水中加入NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出
?
17. 能加快溶解速度的是( )
A.加热 B.搅拌 C.研细 D.使用大烧杯
?
18. t??C时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成如图中的斜线.下列说法正确的是( )
A.该物质的溶解度一定随温度的升高而增大
B.图中4个点表示的溶液中只有z是饱和溶液
C.点z向点w移动的一种方法是恒温蒸发一定量的水,同时有晶体析出
D.将m点表示的溶液变为饱和溶液的一种方法是再加入30g溶质
?
19. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是( )
A.t1??C时,50g甲的饱和溶液中溶解了10g的甲
B.将t2??C甲、乙两种物质的饱和溶液升温至t3??C(溶剂的量不变),两种溶液中溶质的质量分数相等
C.t2??C时,要使接近饱和的乙溶液达到饱和状态,可采升高温度的方法
D.分别将t2??C甲、乙两种物质的溶液降温至t1??C,一定都有晶体析出
三、 填空题 (本题共计 3 小题 ,每题 3 分 ,共计9分 , ) ?
20. 一杯20??C的某物质的不饱和溶液,蒸发20克水或加3克该物质,都可以使溶液达到饱和,则20??C该物质的溶解度为________.
?
21. 大部分固体物质的溶解度随着温度的升高而________,例如________;少数固体物质的溶解度受温度的变化,影响不大,例如________;极少数固体物质的溶解度随温度的升高而减小,例如________.
?
22. K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下.
温度/??C
20
30
50
60
80
溶解度/g
K2CO3
110
114
121
126
139
KNO3
31.6
45.8
85.5
110
169
30??C时,向124g?K2CO3固体中加入100g水,充分溶解后升温至40??C,该溶液中溶质的质量分数________(填“变大”、“变小”或“不变”).
②曲线上M点的含义是________.
四、 解答题 (本题共计 2 小题 ,每题 9 分 ,共计18分 , ) ?
23. 某同学在四个烧杯中分别做有关溶液实验,依据表格回答问题。
烧杯序号??
温度/??C
水的质量/g??
硝酸钾质量/g??
溶液质量/g??
①
20
50
10
60
②
20
100
30
a
③
20
100
36
131.6
④
30
100
45
145
(1)20?时硝酸钾的溶解度是________g,a为________。
(2)将烧杯①所得溶液稀释成溶质的质量分数为10%的溶液,需要加水________g。
(3)若使烧杯③溶液中溶质的质量分数增大,可继续________(填字母序号)。
A.加入少量硝酸钾? ? ? ? B.再加10g水? ? ? ? ? ?C.恒温蒸发部分溶剂? ? ? ? ? D.升到30?C
?
24. 甲、乙两种固体物质的溶解度曲线图如图1所示。请回答下列问题:
(1)M点表示的含义是________。
(2)t2??C时,甲物质的溶解度________乙物质的溶解度(填“大于”、“等于”或“小于”。
(3)t2??C时,将一定质量的甲物质加入到100g水中完全溶解,再降温到t1??C,析出甲物质15g,则t2??C时,加入甲物质的质量为________g。
(4)将等质量t2??C的甲、乙两种物质的饱和溶液分别降温到t1??C,有关所得溶液的说法正确的是________(填字母序号)。
A?甲溶液仍为饱和溶液
B?溶液的质量:甲<乙
C?溶剂的质量:甲=乙
D?溶质质量分数:甲>乙
(5)t1??C时,将甲、乙两种物质各80g分别加入到盛有100g水的两个烧杯中,充分溶解后,恢复到t2??C,现象如图2.则烧杯②中加入的是________(填“甲”或“乙”)物质。
五、 实验探究题 (本题共计 3 小题 ,每题 10 分 ,共计30分 , ) ?
25. 控制变量法是实验探究的重要方法,如图1,下面是实验小组的同学为探究铁生锈的条件设计的实验方案,请回答有关问题.
(1)实验中,植物油的作用是________,加入试管③的蒸馏水若不是新制取的,则需将其加热至沸腾,使其中可能溶解的气体逸出,这是因为气体的溶解度随温度升高而________.
(2)约一周后,同学们观察到只有②试管中的铁钉生锈.对比①②,说明铁生锈是与________发生了反应.
(3)从实验的严密性考虑,有同学认为该实验不足以说明铁生锈是与空气中的氧气发生了反应,应将试管②的实验作优化改进,请将改进方案在图2的方框中的图上补充完整.
?
26. 完成下列实验,你会从中感受到许多乐趣。
①把粉末状硫酸铜晶体加入到盛有100mL热水的烧杯中,直至不能继续溶解为止
②如图所示,将一小块形状不规则的硫酸铜晶体浸入上述硫酸铜溶液中
③在温度没有明显变化的条件下静置一段时间,观察晶体形状和大小的变化
根据以上实验,思考并与同学讨论:
(1)硫酸铜晶体的大小和形状发生变化了吗?
(2)溶液中的硫酸铜发生了怎样的变化?
(3)该实验涉及到本单元所学的哪些内容?
?
27. 为了研究物质的溶解现象,设计并进行了如下实验。
实验
现象
固体溶解,形成紫色溶液
固体几乎不溶解
固体溶解,形成紫红色溶液
(1)对比实验①②的现象,可得出的结论是________。
(2)设计实验②③的目的是________。
(3)用洗涤剂去除油污,是利用洗涤剂的________作用。打开汽水时,汽水会自动喷出来,说明气体在水中的溶解度随________而减小。
(4)往适量的水中加入下列物质,溶液温度明显降低的是(????)。
A.浓硫酸 B.氢氧化钠 C.氯化钠 D.硝酸铵
参考答案与试题解析
一、 选择题 (本题共计 14 小题 ,每题 2 分 ,共计28分 )
1.
【答案】
C
【解答】
解:A、汽油洗去手上的油污,是利用汽油能溶解污染而除去油污,A说法不正确;
B、稳定的液体不一定是溶液,例如水是均一稳定的液体,它不是溶液,B说法不正确;
C、在冰雪上撒食盐.可以使水的凝固点降低,使雪融化,C正确;
D、少量的固体物质溶于水,使溶液的熔点降低,沸点升高,咸汤中含有食盐沸点比水高,D说法不正确.
故答案:C.
2.
【答案】
B
【解答】
需要硝酸钾的质量为
200kg×7.1%=14.2kg
3.
【答案】
C
【解答】
解:水的温度越高、糖的颗粒越小、进行搅拌,则糖溶解的速率越快,相同条件下80??C的水中糖的溶解速率要大于20??C的水中糖的溶解速率,白糖的颗粒要小于冰糖的颗粒,相同条件下白糖的溶解速率要大于冰糖的溶解速率,比较可以发现,80??C的水中白糖的溶解速率最大,观察选项,故选C.
4.
【答案】
D
【解答】
A、溶解度曲线可知,20??C时,甲的溶解度小于乙的溶解度,故错误;
B、不知溶液状态,无法确定溶质质量分数大小,40??C时,甲、乙物质的溶液如是饱和溶液,则溶质质量分数相等,故错误;
C、乙的溶解度随温度的升高而减小,降温的方法只能将乙的饱和溶液转化为不饱和溶液,故错误;
D、60??C时,甲的溶解度为60g,饱和溶液中溶质与溶液的质量比为60g:160g=3:8,正确;
5.
【答案】
D
【解答】
解:A、食盐水中食盐为溶质,而水为溶剂,故A错误;
B、雪碧中含有多种溶质,如二氧化碳,但其溶剂只有水,故B错误;
C、食醋中溶质有多种如醋酸,水为溶剂,故C错误;
D、在碘酒中碘为溶质,酒精是液体为溶剂,故D正确;
故选D.
6.
【答案】
C
【解答】
A.配制100g溶质质量分数为的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠的质量和量取水的体积,最后进行溶解,故A正确;
B.量取水时,用到的仪器是量筒和胶头滴管,故B正确;
C.用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,故C错误;
D.溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解速率,故D正确;
故选C。
7.
【答案】
A
【解答】
A、酒精易溶于水,形成均一稳定的混合物,属于溶液,故A正确;
B、面粉不溶于水,与水混合形成悬浊液,故B错;
C、花生油不溶于水,与水混合形成乳浊液,故C错;
D、冰块与水混合形成纯净物,不属于溶液,故D错。
8.
【答案】
C
【解答】
解:根据“甲胺易溶于乙醇”可判定是利用“溶解”而除去.
A、汽油是优良的有机溶剂,油污易溶于汽油,与上述原理相似;
B、汗渍能溶于水,与上述原理相似;
C、洗涤剂不能使油污溶解但能起到乳化作用从而去污与上述原理不相似;
D、碘能溶于酒精,与上述原理相似;
故选C.
9.
【答案】
C
【解答】
解:A、若食盐水不是饱和溶液的话,食盐质量+水的质量≠溶液的质量;故本选项错误;
B、密度不同的两种物质混合后,体积不能相加,所以,食盐体积+水的体积≠溶液的体积,故本选项错误;
C、溶液是由溶质和溶剂组成的,所以溶质质量+水的质量=溶液的质量,故本选项正确;
D、溶液中溶质和溶剂的质量可以相加,但密度不可以相加;故本选项错误;
故选C.
10.
【答案】
C
【解答】
解:A、水也是均一、稳定的,但不是溶液,故A错误;
B、配制溶液时用水、酒精可以作溶剂,故B错误;
C、用酒精作溶剂的溶液,叫做酒精溶液,故C正确;
D、植物油、水、洗洁精混合振动后形成稳定的液体,该液体是乳浊液,故D错误.
故选:C.
11.
【答案】
D
【解答】
解:
澄清的石灰水属于溶液是均一稳定的混合物,通入二氧化碳后,二氧化碳与氢氧化钙反应生成碳酸钙沉淀,碳酸钙是不溶于水的固体,所以就形成了悬浊液,如果再通入过量二氧化碳时,二氧化碳与碳酸钙、水结合又生成了碳酸氢钙,又能溶于水了.又形成了溶液.
故选D.
12.
【答案】
C
【解答】
解:A、牛奶属于乳浊液;汽水是溶液;石灰浆属于悬浊液,故A错;
B、矿泉水属于溶液;自来水中含有悬浮的物质,属于悬浊液;汽油不溶于水,形成的是乳浊液,故B错;
C、江水中含有不溶性的固体悬浮物,所以是悬浊液;乳白鱼肝油是乳浊液;碘酒是碘溶于酒精形成的,是溶液.故C正确;
D、盐酸、“健力宝”饮料是溶液;泥浆属于悬浊液.故D错.
故选C.
13.
【答案】
A
【解答】
解:由于温度一定所以食盐的溶解度一定不会改变,故A正确.但由于原溶液是否饱和未知,所以200g氯化钠溶液中再加入10g氯化钠是否溶解无法判断,也就是溶质的质量、溶质的质量分数及溶液的质量是否会发生变化不能确定,故BCD均错误.
故选A
14.
【答案】
D
【解答】
解:可设该饱和溶液的质量为ag,则水的质量为4ag,则ag饱和溶液中溶质的质量为S100+S×ag,加水稀释后溶液中溶质的质量分数为:S100+S×aa+4a×100%=20S100+S%,故选D.
二、 多选题 (本题共计 5 小题 ,每题 3 分 ,共计15分 )
15.
【答案】
B,C
【解答】
解:A、烧碱是氢氧化钠的俗称,具有强烈的腐蚀性,不能用于洗碗筷,故选项错误.
B、洗洁精是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,故选项正确.
C、纯碱是碳酸钠的俗称,溶于水显碱性,能与油污发生反应,可以去除油污,故选项正确.
D、汽油能溶解油污,但不适合洗碗筷,故选项错误.
故选BC.
16.
【答案】
A,B
【解答】
解:A、t2??C时甲的溶解度大于乙的溶解度,饱和溶液中溶质的质量分数=溶解度溶解度+100g×100%,则此时两物质的饱和溶液溶解度大的其饱和溶液的溶质质量分数大,则甲的溶质质量分数大于乙的溶质质量分数,描述错误;
B、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而增大,将甲、乙两种物质的饱和溶液都从t2??C将至t1??C时,甲析出晶体,乙的溶解度变大则继续溶解试管内的固体,但溶解固体后是否饱和无法确定,若恰好饱和,则二者的溶质质量分数相等,若溶解后不饱和,则降温后甲的溶质质量分数大于乙的溶质质量分数,故降温后二者的溶质质量分数不相等,故描述错误;
C、氢氧化钠固体溶于水放出大量的热使溶液温度升高,甲物质逐步溶解,溶质的质量分数变大,乙的溶解度减小,析出晶体,溶质质量减小,溶剂不变,所以溶质的质量分数减小,描述正确;
D、NH4NO3固体溶于水吸收热量使溶液温度降低,甲的溶解度随温度的降低而减小,析出晶体,乙的溶解度随温度的升高而增大,变为不饱和溶液,不会析出晶体,描述正确;
故选:AB.
17.
【答案】
A,B,C
【解答】
解:搅拌、升温都能加快水分子运动速度,也就能加快食盐与水的接触机会,从而加快了食盐的溶解速率,固体颗粒大小决定了固体与水的接触面积的大小,也能改变溶解速率,将固体研碎增加了固体与水的接触面积,也就加快了固体的溶解速率.
故选ABC
18.
【答案】
C,D
【解答】
解:A、在图中的信息中并不能知道该物质的溶解度与温度变化的关系,故选项错误;
B、在斜线上的点都是饱和溶液,所以饱和溶液有两个,w和z,故选项错误;
C、恒温蒸发一定量的水,有晶体析出,水量减少,仍旧是饱和溶液,点z向点w移动,故选项正确;
D、由图可知该物质在t??C时的溶解度为100g,所以在80g水中要达到饱和溶液需要80g的该溶质,m点已有50g,故再加入30g溶质可将m点表示的溶液变为饱和溶液,故选项正确;
故选C、D
19.
【答案】
A,D
【解答】
解:A、由甲的溶解度曲线可知,在t1??C时,甲的溶解度是20g,由溶解度的意义可知,在60g甲的饱和溶液中溶解了10g的甲.故A说法不正确;
B、由甲、乙两种物质溶解度曲线可知,在t2??C时甲、乙两种物质的溶解度相等,溶液的溶质的质量分数相等.在升高温度时,甲、乙的溶解度都随温度的升高而增大,溶液都由饱和溶液变为不饱和溶液,溶液中溶质、溶剂质量不变,两种溶液中溶质的质量分数相等.故B说法正确;
C、t2??C时,要使接近饱和的乙溶液达到饱和状态,升高温度,乙的溶解度虽变化不大但也增大,所以不能变成饱和溶液,故C说法正确;
D、由于在t2??C时,甲、乙两种物质的溶液不一定是饱和溶液,所以,在降温至t1??C时,不一定都有晶体析出.故D说法不正确.
故选AD.
三、 填空题 (本题共计 3 小题 ,每题 3 分 ,共计9分 )
20.
【答案】
15g
【解答】
解:从题中的数据可以看出,蒸发20克水或加3克的溶质都会变成饱和,也就是说20克水和3克的溶质刚好可以形成饱和溶液,所以100g水中最多溶解15g溶质,所以20??C该物质的溶解度为15g.
故答案为:15g.
21.
【答案】
增大,硝酸钾,氯化钠,熟石灰
【解答】
解:大部分固体物质的溶解度温度的升高而增大,如KNO3;只有少数固体物质的溶解度受温度的影响不大,如NaCl;极少数固体物质的溶解度随温度升高而减小,如Ca(OH)2.气体的溶解度都随温度的升高而减小,随压强的增大而增大.
故答案为:增大;硝酸钾;氯化钠;熟石灰.
22.
【答案】
变大,t1??C时,甲和乙溶解度相等
【解答】
解:
①30??C时碳酸钾的溶解度是114g,因此向124g?K2CO3固体中加入100g水,充分溶解后,所得溶液是过饱和;升温至40??C,碳酸钾的溶解度增大,但小于124g,仍为饱和溶液,溶质增多,所以溶质的质量分数变大;
②M点表示t1??C时,甲和乙溶解度相等;
答案:
①变大
②t1??C时,甲和乙溶解度相等
四、 解答题 (本题共计 2 小题 ,每题 9 分 ,共计18分 )
23.
【答案】
【解答】
此题暂无解答
24.
【答案】
在t1??C时,甲、乙的溶解度相等
大于
80
AB
甲
【解答】
M点表示的含义是:在t1??C时,甲、乙的溶解度相等;故答案为:在t1??C时,甲、乙的溶解度相等;
t2??C时,甲物质的溶解度大于乙物质的溶解度;故答案为:大于;
t2??C时,将一定质量的甲物质加入到100g水中完全溶解,再降温到t1??C,析出甲物质15g,则t2??C时,加入甲物质的质量=65g+15g=80g;故答案为:80;
将等质量t2??C的甲、乙两种物质的饱和溶液分别降温到t1??C,有关所得溶液的说法正确的是:甲溶液仍为饱和溶液、溶液的质量:甲<乙,因为甲溶液由晶体析出;故答案为:AB;
t1??C时,将甲、乙两种物质各80g分别加入到盛有100g水的两个烧杯中,充分溶解后,恢复到t2??C,现象如图2.则烧杯②中加入的是甲,因为甲固体物质的溶解度,是随温度升高而增大,而乙的溶解度随温度的升高而减少;故答案为:甲;
五、 实验探究题 (本题共计 3 小题 ,每题 10 分 ,共计30分 )
25.
【答案】
防止铁与氧气接触,减小
水
(3)要证明是与氧气反应,则可以在试管中通入氧气,故填:
【解答】
解:(1)植物油能阻止铁与氧气接触,气体的溶解度随温度的升高而减小,故加热时氧气会逸出,
(2)①中铁只与氧气接触不生锈,②中铁与水和氧气同时接触生锈,对比①②,说明铁生锈是与水发生了反应,
(3)要证明是与氧气反应,则可以在试管中通入氧气,
26.
【答案】
硫酸铜晶体的大小不变,形状发生变化,变为规则形状;
硫酸铜晶体的质量不发生变化。
涉及到饱和溶液、溶解度、结晶等知识。
【解答】
饱和溶液加入该种溶质的晶体后会处于动态平衡,溶解进去的溶质和析出的溶质相等,所以晶体的质量不变,但是形状会发生改变,变为规则形状,溶解了多少溶质,就会析出多少溶质。实验涉及到饱和溶液、溶解度、结晶等知识。
27.
【答案】
同种溶质在不同的溶剂中溶解性不同
探究不同溶质在同一种溶剂中的溶解性
乳化,压强的减小
D
【解答】
实验①、②是高锰酸钾溶解在等体积的水、汽油中,现象分别是固体溶解,形成紫色溶液,固体几乎不溶解,所以对比实验①、②可得出的结论是高锰酸钾在水中的溶解性比汽油中的好,也就是同种溶质在不同的溶剂中溶解性不同;故填:同种溶质在不同的溶剂中溶解性不同;
实验②、③分别是高锰酸钾、碘溶解在等体积的汽油里,现象分别是固体几乎不溶解,固体溶解,形成紫红色溶液,目的是比较高锰酸钾和碘在汽油中溶解情况,即探究不同溶质在同一种溶剂中的溶解性;故填:探究不同溶质在同一种溶剂中的溶解性;
用洗涤剂去除油污,是利用洗涤剂的乳化作用。气体的溶解度随着压强的减小而减小,所以打开汽水时,汽水会自动喷出来,故填:乳化;压强的减小;
浓硫酸和氢氧化钠固体溶于水放出热量,溶液温度升高,氯化钠溶于水温度几乎不变;硝酸铵溶于水吸收热量,温度降低;故填:D。
(满分100分;时间:90分钟)
一、 选择题 (本题共计 14 小题 ,每题 2 分 ,共计28分 , ) ?
1. 下列说法正确的是( )
A.修车工用汽油洗掉手上的油污属乳化现象
B.均一稳定的液体都是溶液
C.为加快路面冰雪融化,可向积雪上撒些食盐
D.煮沸的水温度比煮沸的咸汤温度高
?
2. 无土栽培的某种营养液中,含硝酸钾的质量分数为7.1%,某蔬菜生产基地欲配制该营养液200kg,需要硝酸钾的质量为( )
A.7.1kg B.14.2kg C.71kg D.142kg
?
3. 在什么条件下,糖溶解速度最快( )
A.80??C的水加入冰糖块
B.20??C的水加入白糖(颗粒状)
C.80??C的水加入白糖(颗粒状)
D.20??C的水加入冰糖块
?
4. 如图是甲、乙两种固体的溶解度曲线,下列叙述正确的是( )
A.20??C时,甲的溶解度大于乙的溶解度
B.40??C时,甲、乙溶液中溶质的质量分数相等
C.采用降温的方法可将乙的不饱和溶液转化为饱和溶液
D.60??C时,甲的饱和溶液中溶质与溶液的质量比为3:8
?
5. 下列溶液中,溶剂不是水的是( )
A.食盐水 B.雪碧 C.食醋 D.碘酒
?
6. 实验室用氯化钠固体配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是(????????)
A.实验的步骤为计算、称量、量取、溶解
B.量取水时,用到的仪器是量筒和胶头滴管
C.若用量筒量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8%
D.溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解
?
7. 将下列物质分别加入水中,能形成溶液的是( )
A.酒精 B.面粉 C.花生油 D.冰块
?
8. 鱼类腥味产生的原因是由于鱼身上存在有机化学物质甲胺.甲胺易溶于乙醇,因此,煮鱼时加些酒,能使甲胺溶于乙醇并随加热后挥发逸去,经过这样烹饪的鱼就不再有腥味了.下列过程与上面所述原理不相似的是( )
A.用汽油除去衣服上的油污 B.用水除去衣服上的汗渍
C.用洗洁精洗碗 D.用酒精将试管壁上的碘洗掉
?9. 将一定质量的食盐溶解在?10mL?水中,下列等式一定成立的是( )
A.食盐质量+水的质量=溶液的质量
B.食盐体积+水的体积=溶液的体积
C.溶质质量+水的质量=溶液的质量
D.食盐密度+水的密度=溶液的密度
?
10. 下列说法正确的是( )
A.凡是均一、稳定的液体都是溶液
B.配制溶液时只能用水作溶剂
C.用酒精作溶剂的溶液,叫做酒精溶液
D.植物油、水、洗洁精混合振动后形成稳定的液体,该液体是溶液
?
11. 向澄清的石灰水中连续通入CO2,直至过量的全过程中,下列转变关系正确的是( )
A.溶液→乳浊液→溶液 B.溶液→悬浊液→乳浊液
C.悬浊液→乳浊液→溶液 D.溶液→悬浊液→溶液
?12. 下列物质依次为悬浊液、乳浊液、溶液的一组是( )
A.牛奶、汽水、石灰浆
B.矿泉水、自来水、汽油和水的混合物
C.江水、乳白鱼肝油、碘酒
D.盐酸、泥浆、“健力宝”饮料
?
13. 在一定温度下,向盛有200g某氯化钠溶液中再加入10g氯化钠,充分搅拌后,肯定不会改变的是( )
A.氯化钠的溶解度 B.溶液的质量
C.溶液中溶质的质量分数 D.溶液中溶质的质量
?
14. 溶解度为S克的某物质的饱和溶液,跟水以1:4的质量比混合后,溶液的质量百分比浓度为( )
A.80S100+S×100% B.20S100+S×100%
C.80S100+S% D.20S100+S%
二、 多选题 (本题共计 5 小题 ,每题 3 分 ,共计15分 , ) ?
15. 小英的妈妈在洗碗筷时,经常在水中加入一种物质,很快就能将“油乎乎”的菜盘洗得干干净净.小英的妈妈在水中加入的物质可能是( )
A.烧碱 B.洗洁精 C.纯碱 D.汽油
?16. 图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2??C下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发).根据图象和有关信息判断,下列说法中错误的是( )
A.t2??C时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲<乙
B.将甲乙两种物质的饱和溶液都从t2??C降至t1??C时,两种溶液中溶质的质量分数相等
C.向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小
D.向烧杯的水中加入NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出
?
17. 能加快溶解速度的是( )
A.加热 B.搅拌 C.研细 D.使用大烧杯
?
18. t??C时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成如图中的斜线.下列说法正确的是( )
A.该物质的溶解度一定随温度的升高而增大
B.图中4个点表示的溶液中只有z是饱和溶液
C.点z向点w移动的一种方法是恒温蒸发一定量的水,同时有晶体析出
D.将m点表示的溶液变为饱和溶液的一种方法是再加入30g溶质
?
19. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是( )
A.t1??C时,50g甲的饱和溶液中溶解了10g的甲
B.将t2??C甲、乙两种物质的饱和溶液升温至t3??C(溶剂的量不变),两种溶液中溶质的质量分数相等
C.t2??C时,要使接近饱和的乙溶液达到饱和状态,可采升高温度的方法
D.分别将t2??C甲、乙两种物质的溶液降温至t1??C,一定都有晶体析出
三、 填空题 (本题共计 3 小题 ,每题 3 分 ,共计9分 , ) ?
20. 一杯20??C的某物质的不饱和溶液,蒸发20克水或加3克该物质,都可以使溶液达到饱和,则20??C该物质的溶解度为________.
?
21. 大部分固体物质的溶解度随着温度的升高而________,例如________;少数固体物质的溶解度受温度的变化,影响不大,例如________;极少数固体物质的溶解度随温度的升高而减小,例如________.
?
22. K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下.
温度/??C
20
30
50
60
80
溶解度/g
K2CO3
110
114
121
126
139
KNO3
31.6
45.8
85.5
110
169
30??C时,向124g?K2CO3固体中加入100g水,充分溶解后升温至40??C,该溶液中溶质的质量分数________(填“变大”、“变小”或“不变”).
②曲线上M点的含义是________.
四、 解答题 (本题共计 2 小题 ,每题 9 分 ,共计18分 , ) ?
23. 某同学在四个烧杯中分别做有关溶液实验,依据表格回答问题。
烧杯序号??
温度/??C
水的质量/g??
硝酸钾质量/g??
溶液质量/g??
①
20
50
10
60
②
20
100
30
a
③
20
100
36
131.6
④
30
100
45
145
(1)20?时硝酸钾的溶解度是________g,a为________。
(2)将烧杯①所得溶液稀释成溶质的质量分数为10%的溶液,需要加水________g。
(3)若使烧杯③溶液中溶质的质量分数增大,可继续________(填字母序号)。
A.加入少量硝酸钾? ? ? ? B.再加10g水? ? ? ? ? ?C.恒温蒸发部分溶剂? ? ? ? ? D.升到30?C
?
24. 甲、乙两种固体物质的溶解度曲线图如图1所示。请回答下列问题:
(1)M点表示的含义是________。
(2)t2??C时,甲物质的溶解度________乙物质的溶解度(填“大于”、“等于”或“小于”。
(3)t2??C时,将一定质量的甲物质加入到100g水中完全溶解,再降温到t1??C,析出甲物质15g,则t2??C时,加入甲物质的质量为________g。
(4)将等质量t2??C的甲、乙两种物质的饱和溶液分别降温到t1??C,有关所得溶液的说法正确的是________(填字母序号)。
A?甲溶液仍为饱和溶液
B?溶液的质量:甲<乙
C?溶剂的质量:甲=乙
D?溶质质量分数:甲>乙
(5)t1??C时,将甲、乙两种物质各80g分别加入到盛有100g水的两个烧杯中,充分溶解后,恢复到t2??C,现象如图2.则烧杯②中加入的是________(填“甲”或“乙”)物质。
五、 实验探究题 (本题共计 3 小题 ,每题 10 分 ,共计30分 , ) ?
25. 控制变量法是实验探究的重要方法,如图1,下面是实验小组的同学为探究铁生锈的条件设计的实验方案,请回答有关问题.
(1)实验中,植物油的作用是________,加入试管③的蒸馏水若不是新制取的,则需将其加热至沸腾,使其中可能溶解的气体逸出,这是因为气体的溶解度随温度升高而________.
(2)约一周后,同学们观察到只有②试管中的铁钉生锈.对比①②,说明铁生锈是与________发生了反应.
(3)从实验的严密性考虑,有同学认为该实验不足以说明铁生锈是与空气中的氧气发生了反应,应将试管②的实验作优化改进,请将改进方案在图2的方框中的图上补充完整.
?
26. 完成下列实验,你会从中感受到许多乐趣。
①把粉末状硫酸铜晶体加入到盛有100mL热水的烧杯中,直至不能继续溶解为止
②如图所示,将一小块形状不规则的硫酸铜晶体浸入上述硫酸铜溶液中
③在温度没有明显变化的条件下静置一段时间,观察晶体形状和大小的变化
根据以上实验,思考并与同学讨论:
(1)硫酸铜晶体的大小和形状发生变化了吗?
(2)溶液中的硫酸铜发生了怎样的变化?
(3)该实验涉及到本单元所学的哪些内容?
?
27. 为了研究物质的溶解现象,设计并进行了如下实验。
实验
现象
固体溶解,形成紫色溶液
固体几乎不溶解
固体溶解,形成紫红色溶液
(1)对比实验①②的现象,可得出的结论是________。
(2)设计实验②③的目的是________。
(3)用洗涤剂去除油污,是利用洗涤剂的________作用。打开汽水时,汽水会自动喷出来,说明气体在水中的溶解度随________而减小。
(4)往适量的水中加入下列物质,溶液温度明显降低的是(????)。
A.浓硫酸 B.氢氧化钠 C.氯化钠 D.硝酸铵
参考答案与试题解析
一、 选择题 (本题共计 14 小题 ,每题 2 分 ,共计28分 )
1.
【答案】
C
【解答】
解:A、汽油洗去手上的油污,是利用汽油能溶解污染而除去油污,A说法不正确;
B、稳定的液体不一定是溶液,例如水是均一稳定的液体,它不是溶液,B说法不正确;
C、在冰雪上撒食盐.可以使水的凝固点降低,使雪融化,C正确;
D、少量的固体物质溶于水,使溶液的熔点降低,沸点升高,咸汤中含有食盐沸点比水高,D说法不正确.
故答案:C.
2.
【答案】
B
【解答】
需要硝酸钾的质量为
200kg×7.1%=14.2kg
3.
【答案】
C
【解答】
解:水的温度越高、糖的颗粒越小、进行搅拌,则糖溶解的速率越快,相同条件下80??C的水中糖的溶解速率要大于20??C的水中糖的溶解速率,白糖的颗粒要小于冰糖的颗粒,相同条件下白糖的溶解速率要大于冰糖的溶解速率,比较可以发现,80??C的水中白糖的溶解速率最大,观察选项,故选C.
4.
【答案】
D
【解答】
A、溶解度曲线可知,20??C时,甲的溶解度小于乙的溶解度,故错误;
B、不知溶液状态,无法确定溶质质量分数大小,40??C时,甲、乙物质的溶液如是饱和溶液,则溶质质量分数相等,故错误;
C、乙的溶解度随温度的升高而减小,降温的方法只能将乙的饱和溶液转化为不饱和溶液,故错误;
D、60??C时,甲的溶解度为60g,饱和溶液中溶质与溶液的质量比为60g:160g=3:8,正确;
5.
【答案】
D
【解答】
解:A、食盐水中食盐为溶质,而水为溶剂,故A错误;
B、雪碧中含有多种溶质,如二氧化碳,但其溶剂只有水,故B错误;
C、食醋中溶质有多种如醋酸,水为溶剂,故C错误;
D、在碘酒中碘为溶质,酒精是液体为溶剂,故D正确;
故选D.
6.
【答案】
C
【解答】
A.配制100g溶质质量分数为的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠的质量和量取水的体积,最后进行溶解,故A正确;
B.量取水时,用到的仪器是量筒和胶头滴管,故B正确;
C.用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大,故C错误;
D.溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解速率,故D正确;
故选C。
7.
【答案】
A
【解答】
A、酒精易溶于水,形成均一稳定的混合物,属于溶液,故A正确;
B、面粉不溶于水,与水混合形成悬浊液,故B错;
C、花生油不溶于水,与水混合形成乳浊液,故C错;
D、冰块与水混合形成纯净物,不属于溶液,故D错。
8.
【答案】
C
【解答】
解:根据“甲胺易溶于乙醇”可判定是利用“溶解”而除去.
A、汽油是优良的有机溶剂,油污易溶于汽油,与上述原理相似;
B、汗渍能溶于水,与上述原理相似;
C、洗涤剂不能使油污溶解但能起到乳化作用从而去污与上述原理不相似;
D、碘能溶于酒精,与上述原理相似;
故选C.
9.
【答案】
C
【解答】
解:A、若食盐水不是饱和溶液的话,食盐质量+水的质量≠溶液的质量;故本选项错误;
B、密度不同的两种物质混合后,体积不能相加,所以,食盐体积+水的体积≠溶液的体积,故本选项错误;
C、溶液是由溶质和溶剂组成的,所以溶质质量+水的质量=溶液的质量,故本选项正确;
D、溶液中溶质和溶剂的质量可以相加,但密度不可以相加;故本选项错误;
故选C.
10.
【答案】
C
【解答】
解:A、水也是均一、稳定的,但不是溶液,故A错误;
B、配制溶液时用水、酒精可以作溶剂,故B错误;
C、用酒精作溶剂的溶液,叫做酒精溶液,故C正确;
D、植物油、水、洗洁精混合振动后形成稳定的液体,该液体是乳浊液,故D错误.
故选:C.
11.
【答案】
D
【解答】
解:
澄清的石灰水属于溶液是均一稳定的混合物,通入二氧化碳后,二氧化碳与氢氧化钙反应生成碳酸钙沉淀,碳酸钙是不溶于水的固体,所以就形成了悬浊液,如果再通入过量二氧化碳时,二氧化碳与碳酸钙、水结合又生成了碳酸氢钙,又能溶于水了.又形成了溶液.
故选D.
12.
【答案】
C
【解答】
解:A、牛奶属于乳浊液;汽水是溶液;石灰浆属于悬浊液,故A错;
B、矿泉水属于溶液;自来水中含有悬浮的物质,属于悬浊液;汽油不溶于水,形成的是乳浊液,故B错;
C、江水中含有不溶性的固体悬浮物,所以是悬浊液;乳白鱼肝油是乳浊液;碘酒是碘溶于酒精形成的,是溶液.故C正确;
D、盐酸、“健力宝”饮料是溶液;泥浆属于悬浊液.故D错.
故选C.
13.
【答案】
A
【解答】
解:由于温度一定所以食盐的溶解度一定不会改变,故A正确.但由于原溶液是否饱和未知,所以200g氯化钠溶液中再加入10g氯化钠是否溶解无法判断,也就是溶质的质量、溶质的质量分数及溶液的质量是否会发生变化不能确定,故BCD均错误.
故选A
14.
【答案】
D
【解答】
解:可设该饱和溶液的质量为ag,则水的质量为4ag,则ag饱和溶液中溶质的质量为S100+S×ag,加水稀释后溶液中溶质的质量分数为:S100+S×aa+4a×100%=20S100+S%,故选D.
二、 多选题 (本题共计 5 小题 ,每题 3 分 ,共计15分 )
15.
【答案】
B,C
【解答】
解:A、烧碱是氢氧化钠的俗称,具有强烈的腐蚀性,不能用于洗碗筷,故选项错误.
B、洗洁精是洗涤剂,有乳化作用,能将大的油滴分散成细小的油滴随水冲走,故选项正确.
C、纯碱是碳酸钠的俗称,溶于水显碱性,能与油污发生反应,可以去除油污,故选项正确.
D、汽油能溶解油污,但不适合洗碗筷,故选项错误.
故选BC.
16.
【答案】
A,B
【解答】
解:A、t2??C时甲的溶解度大于乙的溶解度,饱和溶液中溶质的质量分数=溶解度溶解度+100g×100%,则此时两物质的饱和溶液溶解度大的其饱和溶液的溶质质量分数大,则甲的溶质质量分数大于乙的溶质质量分数,描述错误;
B、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而增大,将甲、乙两种物质的饱和溶液都从t2??C将至t1??C时,甲析出晶体,乙的溶解度变大则继续溶解试管内的固体,但溶解固体后是否饱和无法确定,若恰好饱和,则二者的溶质质量分数相等,若溶解后不饱和,则降温后甲的溶质质量分数大于乙的溶质质量分数,故降温后二者的溶质质量分数不相等,故描述错误;
C、氢氧化钠固体溶于水放出大量的热使溶液温度升高,甲物质逐步溶解,溶质的质量分数变大,乙的溶解度减小,析出晶体,溶质质量减小,溶剂不变,所以溶质的质量分数减小,描述正确;
D、NH4NO3固体溶于水吸收热量使溶液温度降低,甲的溶解度随温度的降低而减小,析出晶体,乙的溶解度随温度的升高而增大,变为不饱和溶液,不会析出晶体,描述正确;
故选:AB.
17.
【答案】
A,B,C
【解答】
解:搅拌、升温都能加快水分子运动速度,也就能加快食盐与水的接触机会,从而加快了食盐的溶解速率,固体颗粒大小决定了固体与水的接触面积的大小,也能改变溶解速率,将固体研碎增加了固体与水的接触面积,也就加快了固体的溶解速率.
故选ABC
18.
【答案】
C,D
【解答】
解:A、在图中的信息中并不能知道该物质的溶解度与温度变化的关系,故选项错误;
B、在斜线上的点都是饱和溶液,所以饱和溶液有两个,w和z,故选项错误;
C、恒温蒸发一定量的水,有晶体析出,水量减少,仍旧是饱和溶液,点z向点w移动,故选项正确;
D、由图可知该物质在t??C时的溶解度为100g,所以在80g水中要达到饱和溶液需要80g的该溶质,m点已有50g,故再加入30g溶质可将m点表示的溶液变为饱和溶液,故选项正确;
故选C、D
19.
【答案】
A,D
【解答】
解:A、由甲的溶解度曲线可知,在t1??C时,甲的溶解度是20g,由溶解度的意义可知,在60g甲的饱和溶液中溶解了10g的甲.故A说法不正确;
B、由甲、乙两种物质溶解度曲线可知,在t2??C时甲、乙两种物质的溶解度相等,溶液的溶质的质量分数相等.在升高温度时,甲、乙的溶解度都随温度的升高而增大,溶液都由饱和溶液变为不饱和溶液,溶液中溶质、溶剂质量不变,两种溶液中溶质的质量分数相等.故B说法正确;
C、t2??C时,要使接近饱和的乙溶液达到饱和状态,升高温度,乙的溶解度虽变化不大但也增大,所以不能变成饱和溶液,故C说法正确;
D、由于在t2??C时,甲、乙两种物质的溶液不一定是饱和溶液,所以,在降温至t1??C时,不一定都有晶体析出.故D说法不正确.
故选AD.
三、 填空题 (本题共计 3 小题 ,每题 3 分 ,共计9分 )
20.
【答案】
15g
【解答】
解:从题中的数据可以看出,蒸发20克水或加3克的溶质都会变成饱和,也就是说20克水和3克的溶质刚好可以形成饱和溶液,所以100g水中最多溶解15g溶质,所以20??C该物质的溶解度为15g.
故答案为:15g.
21.
【答案】
增大,硝酸钾,氯化钠,熟石灰
【解答】
解:大部分固体物质的溶解度温度的升高而增大,如KNO3;只有少数固体物质的溶解度受温度的影响不大,如NaCl;极少数固体物质的溶解度随温度升高而减小,如Ca(OH)2.气体的溶解度都随温度的升高而减小,随压强的增大而增大.
故答案为:增大;硝酸钾;氯化钠;熟石灰.
22.
【答案】
变大,t1??C时,甲和乙溶解度相等
【解答】
解:
①30??C时碳酸钾的溶解度是114g,因此向124g?K2CO3固体中加入100g水,充分溶解后,所得溶液是过饱和;升温至40??C,碳酸钾的溶解度增大,但小于124g,仍为饱和溶液,溶质增多,所以溶质的质量分数变大;
②M点表示t1??C时,甲和乙溶解度相等;
答案:
①变大
②t1??C时,甲和乙溶解度相等
四、 解答题 (本题共计 2 小题 ,每题 9 分 ,共计18分 )
23.
【答案】
【解答】
此题暂无解答
24.
【答案】
在t1??C时,甲、乙的溶解度相等
大于
80
AB
甲
【解答】
M点表示的含义是:在t1??C时,甲、乙的溶解度相等;故答案为:在t1??C时,甲、乙的溶解度相等;
t2??C时,甲物质的溶解度大于乙物质的溶解度;故答案为:大于;
t2??C时,将一定质量的甲物质加入到100g水中完全溶解,再降温到t1??C,析出甲物质15g,则t2??C时,加入甲物质的质量=65g+15g=80g;故答案为:80;
将等质量t2??C的甲、乙两种物质的饱和溶液分别降温到t1??C,有关所得溶液的说法正确的是:甲溶液仍为饱和溶液、溶液的质量:甲<乙,因为甲溶液由晶体析出;故答案为:AB;
t1??C时,将甲、乙两种物质各80g分别加入到盛有100g水的两个烧杯中,充分溶解后,恢复到t2??C,现象如图2.则烧杯②中加入的是甲,因为甲固体物质的溶解度,是随温度升高而增大,而乙的溶解度随温度的升高而减少;故答案为:甲;
五、 实验探究题 (本题共计 3 小题 ,每题 10 分 ,共计30分 )
25.
【答案】
防止铁与氧气接触,减小
水
(3)要证明是与氧气反应,则可以在试管中通入氧气,故填:
【解答】
解:(1)植物油能阻止铁与氧气接触,气体的溶解度随温度的升高而减小,故加热时氧气会逸出,
(2)①中铁只与氧气接触不生锈,②中铁与水和氧气同时接触生锈,对比①②,说明铁生锈是与水发生了反应,
(3)要证明是与氧气反应,则可以在试管中通入氧气,
26.
【答案】
硫酸铜晶体的大小不变,形状发生变化,变为规则形状;
硫酸铜晶体的质量不发生变化。
涉及到饱和溶液、溶解度、结晶等知识。
【解答】
饱和溶液加入该种溶质的晶体后会处于动态平衡,溶解进去的溶质和析出的溶质相等,所以晶体的质量不变,但是形状会发生改变,变为规则形状,溶解了多少溶质,就会析出多少溶质。实验涉及到饱和溶液、溶解度、结晶等知识。
27.
【答案】
同种溶质在不同的溶剂中溶解性不同
探究不同溶质在同一种溶剂中的溶解性
乳化,压强的减小
D
【解答】
实验①、②是高锰酸钾溶解在等体积的水、汽油中,现象分别是固体溶解,形成紫色溶液,固体几乎不溶解,所以对比实验①、②可得出的结论是高锰酸钾在水中的溶解性比汽油中的好,也就是同种溶质在不同的溶剂中溶解性不同;故填:同种溶质在不同的溶剂中溶解性不同;
实验②、③分别是高锰酸钾、碘溶解在等体积的汽油里,现象分别是固体几乎不溶解,固体溶解,形成紫红色溶液,目的是比较高锰酸钾和碘在汽油中溶解情况,即探究不同溶质在同一种溶剂中的溶解性;故填:探究不同溶质在同一种溶剂中的溶解性;
用洗涤剂去除油污,是利用洗涤剂的乳化作用。气体的溶解度随着压强的减小而减小,所以打开汽水时,汽水会自动喷出来,故填:乳化;压强的减小;
浓硫酸和氢氧化钠固体溶于水放出热量,溶液温度升高,氯化钠溶于水温度几乎不变;硝酸铵溶于水吸收热量,温度降低;故填:D。
同课章节目录
