高中化学人教版(2019)选择性必修二第三章第三节分子晶体与共价晶体 课件(共67张ppt)
文档属性
| 名称 | 高中化学人教版(2019)选择性必修二第三章第三节分子晶体与共价晶体 课件(共67张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 13.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-09 00:00:00 | ||
图片预览







文档简介
选择性必修 2 物质结构与性质 第三章 晶体结构与性质
高二年级 化学
分子晶体与共价晶体
学习目标
1. 能从微粒组成及微粒间的相互作用,理解分子晶体、共价
晶体的结构特点。
2. 能基于分子晶体、共价晶体的结构特点分析二者某些物理
性质的差异性原因。
3. 能应用分子晶体,共价晶体的相关知识解释一些实验现象
或某些化学事实及其研究的应用价值。
为什么冰比水轻?
冰、干冰、可燃冰的结构有什么不同?
为什么干冰可以用作制冷剂?
金刚石为什么是最硬的物质?
这些常识,你知道吗?
引入新课
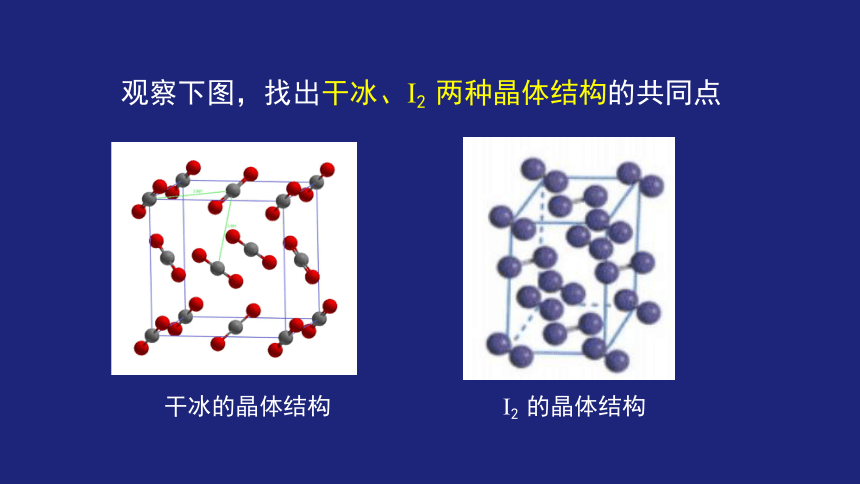
观察下图,找出干冰、I2 两种晶体结构的共同点
干冰的晶体结构 I2 的晶体结构
干冰的晶体结构 I2 的晶体结构
构成微粒:分子
微粒内作用:共价键
观察下图,找出干冰、I2 两种晶体结构的共同点
干冰的晶体结构 I2 的晶体结构
构成微粒:分子
微粒内作用:共价键
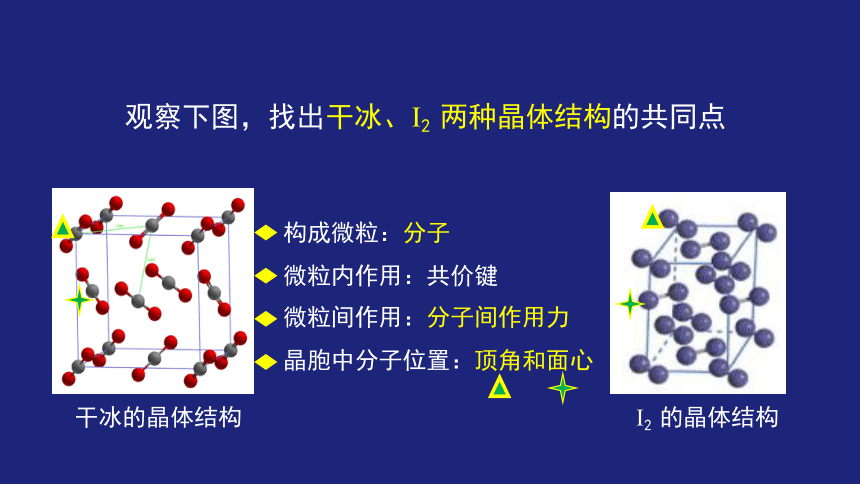
观察下图,找出干冰、I2 两种晶体结构的共同点
微粒间作用:分子间作用力
晶胞中分子位置:顶角和面心
一、分子晶体
1. 概念:
直接由分子构成的晶体
分子间作用力
分子
3. 微粒间作用力:
2. 构成微粒:
冰
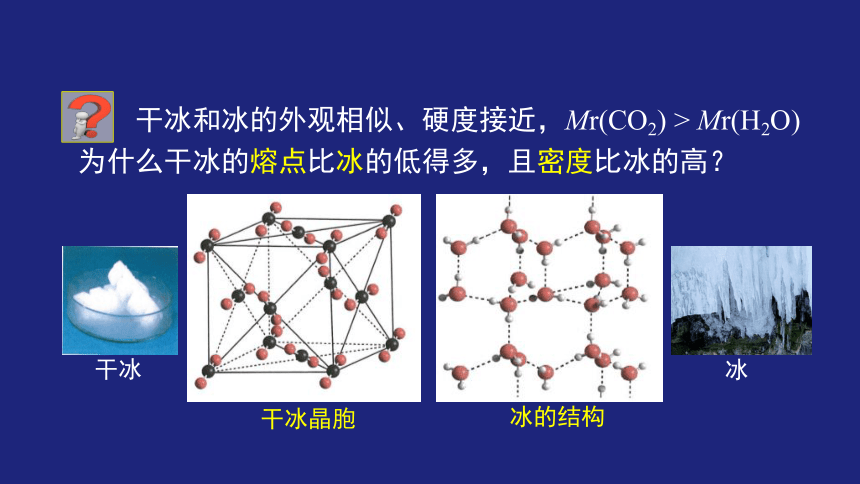
干冰晶胞
冰的结构
干冰
冰
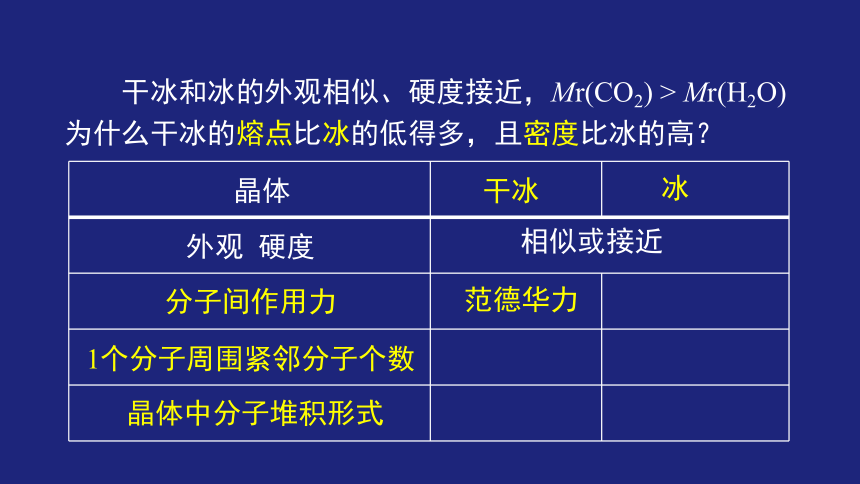
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
干冰
冰
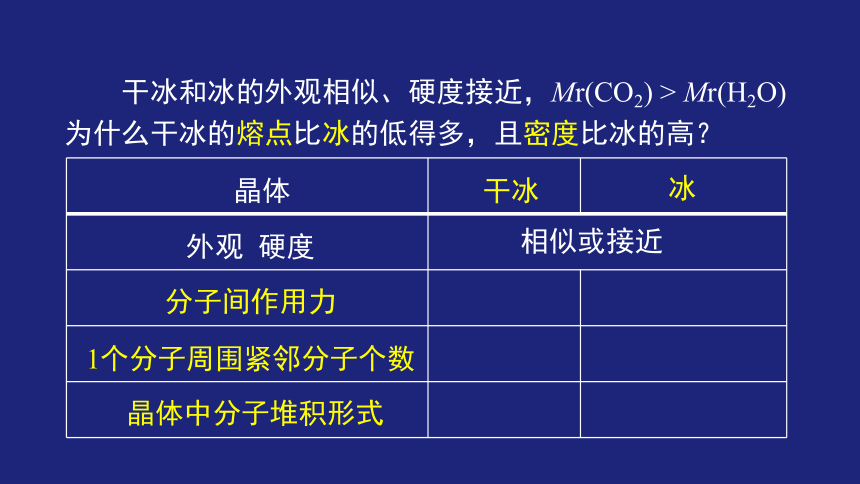
外观 硬度
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
相似或接近
晶体中分子堆积形式
分子间作用力
1个分子周围紧邻分子个数
晶体
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
干冰
冰
外观 硬度
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
相似或接近
晶体中分子堆积形式
分子间作用力
1个分子周围紧邻分子个数
晶体
范德华力
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
与一个 CO2 分子紧邻的 CO2 分子共有____个
与一个 CO2 分子紧邻的 CO2 分子共有____个
12
干冰
冰
外观 硬度
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
相似或接近
晶体中分子堆积形式
分子间作用力
1个分子周围紧邻分子个数
晶体
范德华力
密堆积
12 个
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
碳 60 的晶胞
O2 的晶胞
分子密堆积
怎样理解水的密度在 4 ℃ 时最大?
水的这一特殊性对生命的存在有什么重要意义?
资料
氢键具有方向性
分子非密堆积
冰中一个水分子
周围有 4 个水分子
冰的结构
周期性有序排列
水约 4 ℃
水超过 4 ℃
冰
大量氢键
非密堆积
空隙大
密度小
氢键减少
部分解体
空隙减小
密度增大
热运动加剧
分子间距加大
密度减小
水结冰时体积增大,密度减小,从而浮在水面
冰浮在水面,成为一隔热层,使下面的水的温度保持
在 4 ℃ 左右。
结冰时散热,冰融时吸热,这一过程有缓冲水温变化
的作用,也有利于生物的生存。
怎样理解水的密度在 4 ℃ 时最大?
水的这一特殊性对生命的存在有什么重要意义?
干冰
冰
外观 硬度
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
相似或接近
晶体中分子堆积形式
分子间作用力
1个分子周围紧邻分子个数
晶体
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
范德华力
密堆积
12 个
4 个
非密堆积
氢键
若分子间作用力主要为范德华力时, 以 1 个分子为中心,周围有 12 个紧邻分子,即分子密堆积结构。 如:干冰。
若分子间作用力主要为氢键时,氢键具有方向性,使晶体中的空间利用率不高,留有相当大的空隙,为分子非密堆积结构。如:冰。
4. 分子晶体的结构特征
一、分子晶体
干冰能让镁持续燃烧吗?
干冰能让镁持续燃烧吗?
干冰能让镁持续燃烧
镁可以跟二氧化碳反应
干冰有易升华的特性
实验结论:
5. 分子晶体的性质
一、分子晶体
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}分子晶体
氧气
氮气
白磷
水
熔点 /℃
-218.3
-210.1
44.2
0
分子晶体
硫化氢
甲烷
乙酸
尿素
熔点 /℃
-85.6
-182
16.6
132.7
表 3-2 某些分子晶体的熔点
大多数分子晶体的熔点是相对比较低的
思考
H2S
H2O
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
熔点 /℃
-85.6
0
Mr
34
18
晶体
这是为什么?
>
<
冰中水分子间除了范德华力,大部分是氢键,破坏时需要吸收更多的能量。
5. 分子晶体的性质
一、分子晶体
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}微观结构
宏观性质
分子
无离子、自由电子
纯净物不导电
电解质的水溶液导电
分子间作用力
(比化学键弱)
硬度小
熔点低
分子的极性
相似相溶
(1)所有非金属氢化物:
如 H2O、H2S、NH3、HCl、CH4 等;
(2)部分非金属单质:
如卤素 (X2)、O2、S8、N2、P4、C60、稀有气体等;
6.常见的分子晶体
一、分子晶体
(3)部分非金属氧化物:
如 CO2、P4O6、P4O10、SO2 等;
(4)几乎所有的酸;
(5)绝大多数有机物的晶体:如乙醇、冰醋酸、蔗糖。
6.常见的分子晶体
一、分子晶体
了解可燃冰
20 世纪末,科学家发现海底和大陆冰川或永久冻土底部存在大量天然气水合物晶体,这种晶体的主要成分是甲烷,因而又称甲烷水合物,它的外形像冰,而且在常温常压下会迅速分解释放出可燃的甲烷,因而又称“可燃冰”。
科学·技术·社会
了解可燃冰
天然气在水合物晶体中,装在以氢键相连的几个水分子构成的笼中,因而又称笼状化合物。天然气水合物晶体中的水分子笼也是多种多样的,它们是一类笼状的分子晶体。
科学·技术·社会
全球的海底和冰川底部藏在天然气水合物中的天然气,总量超过煤、石油和天然气等化石燃料的总和的两倍,是巨大的潜在能源。2017 年,我国南海神狐海域试采实现连续超过七天的稳定采气。
蓝鲸一号
科学·技术·社会
分子晶体小结
只含分子的晶体
低熔点、硬度小
含有氢键的分子晶体具有更为特殊的物理性质
(熔沸点偏高、水溶性高、水的密度反常等)
分子密堆积 如:干冰
只有范德华力
含有氢键
分子之间
分子非密堆积 如:冰
构成
结构
性质
金刚石——
钻石的原身
天然的金刚石经常呈现规则多面体的外形,这是金刚石微观原子有序排列的宏观表现
金刚石的微观结构是怎样的?请观看动画
资料
金刚石晶体的结构特点
金刚石晶体中,每个碳原子以四个共价键对称地与相邻的 4 个碳原子相结合,键角为 109? 28?,即金刚石中的碳采取 sp3 杂化轨道形成共价键三维骨架结构。
二、共价晶体
1.定义:
2.构成粒子:
原子
3.粒子间作用:
共价键
4.空间结构:
三维骨架结构
相邻原子间以共价键结合而形成的三维骨架结构的晶体
109? 28?,三维骨架
键能:
347.7 kJ/mol
(很大)
键长:154 pm(很短)
熔点很高:
大于 3500 0C
硬度最大:
摩氏 10 度
结构决定性质
金刚石的用途
除了金刚石,还有哪些物质属于共价晶体呢?让我们沿着元素周期表一起寻找。
5. 常见共价晶体
(1)某些单质:以碳为中心,
同主族向下:
硅(Si)锗(Ge)和灰锡(Sn)等
同周期向左、向右:
硼(B)高聚氮
二、共价晶体
与金刚石极其相似,只是将碳原子换成了硅原子
硅晶体的结构
资料
硅晶体的结构
思考:
请推测晶体硅中 Si-Si 键的键参数与金刚石中 C-C 键的键参数相比,有什么变化?
原子半径:Si > C
键长变长,键能变小
(2)某些非金属化合物:
碳化硅(SiC) 氮化硅(Si3N4)
氮化硼(BN)等
以 Si3N4 为基础,用 Al 取代部分 Si,
用 O 取代部分 N 而获得结构多样化的
陶瓷,用于制作 LED 发光材料。
5. 常见共价晶体
二、共价晶体
6. 共价晶体的性质
资料卡片 P 82
二、共价晶体
硬度是衡量固体软硬程度的指标。硬度有不同的标度,最普通的硬度标度是画痕硬度,即摩氏硬度。以固体互相刻画时出现刻痕的固体的硬度较低。金刚石不能被任何天然矿物刻划出刻痕,因而是最硬的。以金刚石的硬度为 10,以另 9 种天然矿物为代表。可将摩氏硬度分为十度,即:
某些共价晶体的熔点和硬度
共价晶体
金刚石
氮化硼
碳化硅
石英
硅
锗
熔点 /0C
>3500
3000
2700
1710
1410
1211
硬 度
10
9.5
9.5
7
6.5
6.0
资料卡片 P 82
共价键
三维骨架结构
熔点高
硬度大
一般不导电
难溶于一些常见的溶剂
二、共价晶体
6. 共价晶体的性质
(1)怎样从原子结构的角度理解金刚石、硅和锗的熔点和
硬度依次降低?
金刚石、硅和锗中原子半径依次增大,键长变长,键能变小,共价键稳定性下降,熔点和硬度依次下降。
思考 P 82
SiO2 自然界含量最高的固态二元氧化物
有多种结构,最常见的是低温石英(α-SiO2)
黄沙、石英矿脉、花岗石中的白色晶体以及
透明的水晶都是低温石英。
二氧化硅的存在
石英的左、右型晶体
压电材料:
制作石英手表
低温石英的结构中有顶角相连的硅氧四面体形成螺旋上升的长链,而没有封闭的环状结构
二氧化硅的结构
二氧化硅的用途
以 SiO2 为原料制造的高科技产品:
单晶硅 硅芯片 硅太阳能电池 二氧化硅光导纤维
俗名“金刚砂”,它具有类似金刚石的结构和性质,其空间结构中碳原子和硅原子相间排列,化学式为 SiC。
SiC 的球棍模型
功能陶瓷
高级耐火材料
磨料
用途
碳化硅
(2)“具有共价键的晶体叫做共价晶体”,这种说法对吗?
为什么?
不对,共价晶体中都有共价键,但含有共价键的不一定是共价晶体。如分子晶体 CO2、H2O 的分子中也含有共价键。
思考 P 82
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}晶体类型
分子晶体
共价晶体
直接构成晶体的粒子
分子
原子
粒子间相互作用
分子间作用力
共价键
熔点
较低
很高
硬度
较小
很大
代表物
冰、干冰
金刚石
课堂小结
下列说法中,错误的是( )
A. 只含分子的晶体一定是分子晶体
B. 碘晶体升华时破坏了共价键
C. 几乎所有的酸都属于分子晶体
D. 稀有气体分子中只含原子,但稀有气体的晶体属于
分子晶体
课堂反馈
B
P 84-1
√
√
√
×
下列说法中,正确的是( )
A. 冰融化时,分子中 H-O 键发生断裂
B. 共价晶体中,共价键越强,熔点越高
C. 分子晶体中,共价键键能越大,该分子晶体的熔沸点
一定越高
D. 分子晶体中,分子间作用力越大,对应的物质越稳定
课堂反馈
B
分子晶体:影响熔、沸点的是分子间作用力,决定分子
稳定性的是分子内的共价键
P 84-2
下列说法中,正确的是( )
A. 分子晶体一定存在分子间作用力和共价键
B. 分子晶体的熔点一般比共价晶体的熔点高
C. 稀有气体形成的晶体属于分子晶体
D. CO2 晶体是分子晶体,可推测 SiO2 晶体也是分子晶体
课堂反馈
C
稀有气体
P 85-4
SiO2 晶体是共价晶体
低
请将下列晶体分类,并填入下表:
金刚石 干冰 冰 可燃冰 硫黄
C60 碘 石英 白磷(P4) 苯甲酸 金刚砂(SiC) 稀有气体的晶体
氧气的晶体 氮气的晶体
课堂反馈
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}分子晶体
共价晶体
P 85-7
请将下列晶体分类,并填入下表:
课堂反馈
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}分子晶体
干冰、冰、可燃冰、硫黄、C60、碘 白磷(P4)、苯甲酸 、稀有气体的晶体
氧气的晶体、氮气的晶体
共价晶体
金刚石、石英、金刚砂(SiC)
下列事实能说明刚玉(Al2O3)是共价晶体的是( )
①Al2O3 是两性氧化物;
②硬度很大;
③它的熔点是 2045 ℃;
④自然界中的刚玉有红宝石和蓝宝石
A. ①② B. ②③ C. ①④ D. ③④
课堂反馈
B
P 85-3
1. 整理笔记、落实知识
2. 完成 P 84 课后习题 5、6、8、9
3. 阅读 P 83 “科学·技术·社会”,了解金刚石的“前世今生”,
写一篇小论文。
课后作业
金刚石再硬、智慧能使它变软;
拥有智慧,平凡的石墨也能变成璀璨的钻石。
同 学 们 再 见 !
高二年级 化学
分子晶体与共价晶体
学习目标
1. 能从微粒组成及微粒间的相互作用,理解分子晶体、共价
晶体的结构特点。
2. 能基于分子晶体、共价晶体的结构特点分析二者某些物理
性质的差异性原因。
3. 能应用分子晶体,共价晶体的相关知识解释一些实验现象
或某些化学事实及其研究的应用价值。
为什么冰比水轻?
冰、干冰、可燃冰的结构有什么不同?
为什么干冰可以用作制冷剂?
金刚石为什么是最硬的物质?
这些常识,你知道吗?
引入新课
观察下图,找出干冰、I2 两种晶体结构的共同点
干冰的晶体结构 I2 的晶体结构
干冰的晶体结构 I2 的晶体结构
构成微粒:分子
微粒内作用:共价键
观察下图,找出干冰、I2 两种晶体结构的共同点
干冰的晶体结构 I2 的晶体结构
构成微粒:分子
微粒内作用:共价键
观察下图,找出干冰、I2 两种晶体结构的共同点
微粒间作用:分子间作用力
晶胞中分子位置:顶角和面心
一、分子晶体
1. 概念:
直接由分子构成的晶体
分子间作用力
分子
3. 微粒间作用力:
2. 构成微粒:
冰
干冰晶胞
冰的结构
干冰
冰
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
干冰
冰
外观 硬度
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
相似或接近
晶体中分子堆积形式
分子间作用力
1个分子周围紧邻分子个数
晶体
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
干冰
冰
外观 硬度
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
相似或接近
晶体中分子堆积形式
分子间作用力
1个分子周围紧邻分子个数
晶体
范德华力
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
与一个 CO2 分子紧邻的 CO2 分子共有____个
与一个 CO2 分子紧邻的 CO2 分子共有____个
12
干冰
冰
外观 硬度
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
相似或接近
晶体中分子堆积形式
分子间作用力
1个分子周围紧邻分子个数
晶体
范德华力
密堆积
12 个
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
碳 60 的晶胞
O2 的晶胞
分子密堆积
怎样理解水的密度在 4 ℃ 时最大?
水的这一特殊性对生命的存在有什么重要意义?
资料
氢键具有方向性
分子非密堆积
冰中一个水分子
周围有 4 个水分子
冰的结构
周期性有序排列
水约 4 ℃
水超过 4 ℃
冰
大量氢键
非密堆积
空隙大
密度小
氢键减少
部分解体
空隙减小
密度增大
热运动加剧
分子间距加大
密度减小
水结冰时体积增大,密度减小,从而浮在水面
冰浮在水面,成为一隔热层,使下面的水的温度保持
在 4 ℃ 左右。
结冰时散热,冰融时吸热,这一过程有缓冲水温变化
的作用,也有利于生物的生存。
怎样理解水的密度在 4 ℃ 时最大?
水的这一特殊性对生命的存在有什么重要意义?
干冰
冰
外观 硬度
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
相似或接近
晶体中分子堆积形式
分子间作用力
1个分子周围紧邻分子个数
晶体
干冰和冰的外观相似、硬度接近,Mr(CO2) > Mr(H2O)
为什么干冰的熔点比冰的低得多,且密度比冰的高?
范德华力
密堆积
12 个
4 个
非密堆积
氢键
若分子间作用力主要为范德华力时, 以 1 个分子为中心,周围有 12 个紧邻分子,即分子密堆积结构。 如:干冰。
若分子间作用力主要为氢键时,氢键具有方向性,使晶体中的空间利用率不高,留有相当大的空隙,为分子非密堆积结构。如:冰。
4. 分子晶体的结构特征
一、分子晶体
干冰能让镁持续燃烧吗?
干冰能让镁持续燃烧吗?
干冰能让镁持续燃烧
镁可以跟二氧化碳反应
干冰有易升华的特性
实验结论:
5. 分子晶体的性质
一、分子晶体
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}分子晶体
氧气
氮气
白磷
水
熔点 /℃
-218.3
-210.1
44.2
0
分子晶体
硫化氢
甲烷
乙酸
尿素
熔点 /℃
-85.6
-182
16.6
132.7
表 3-2 某些分子晶体的熔点
大多数分子晶体的熔点是相对比较低的
思考
H2S
H2O
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
熔点 /℃
-85.6
0
Mr
34
18
晶体
这是为什么?
>
<
冰中水分子间除了范德华力,大部分是氢键,破坏时需要吸收更多的能量。
5. 分子晶体的性质
一、分子晶体
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}微观结构
宏观性质
分子
无离子、自由电子
纯净物不导电
电解质的水溶液导电
分子间作用力
(比化学键弱)
硬度小
熔点低
分子的极性
相似相溶
(1)所有非金属氢化物:
如 H2O、H2S、NH3、HCl、CH4 等;
(2)部分非金属单质:
如卤素 (X2)、O2、S8、N2、P4、C60、稀有气体等;
6.常见的分子晶体
一、分子晶体
(3)部分非金属氧化物:
如 CO2、P4O6、P4O10、SO2 等;
(4)几乎所有的酸;
(5)绝大多数有机物的晶体:如乙醇、冰醋酸、蔗糖。
6.常见的分子晶体
一、分子晶体
了解可燃冰
20 世纪末,科学家发现海底和大陆冰川或永久冻土底部存在大量天然气水合物晶体,这种晶体的主要成分是甲烷,因而又称甲烷水合物,它的外形像冰,而且在常温常压下会迅速分解释放出可燃的甲烷,因而又称“可燃冰”。
科学·技术·社会
了解可燃冰
天然气在水合物晶体中,装在以氢键相连的几个水分子构成的笼中,因而又称笼状化合物。天然气水合物晶体中的水分子笼也是多种多样的,它们是一类笼状的分子晶体。
科学·技术·社会
全球的海底和冰川底部藏在天然气水合物中的天然气,总量超过煤、石油和天然气等化石燃料的总和的两倍,是巨大的潜在能源。2017 年,我国南海神狐海域试采实现连续超过七天的稳定采气。
蓝鲸一号
科学·技术·社会
分子晶体小结
只含分子的晶体
低熔点、硬度小
含有氢键的分子晶体具有更为特殊的物理性质
(熔沸点偏高、水溶性高、水的密度反常等)
分子密堆积 如:干冰
只有范德华力
含有氢键
分子之间
分子非密堆积 如:冰
构成
结构
性质
金刚石——
钻石的原身
天然的金刚石经常呈现规则多面体的外形,这是金刚石微观原子有序排列的宏观表现
金刚石的微观结构是怎样的?请观看动画
资料
金刚石晶体的结构特点
金刚石晶体中,每个碳原子以四个共价键对称地与相邻的 4 个碳原子相结合,键角为 109? 28?,即金刚石中的碳采取 sp3 杂化轨道形成共价键三维骨架结构。
二、共价晶体
1.定义:
2.构成粒子:
原子
3.粒子间作用:
共价键
4.空间结构:
三维骨架结构
相邻原子间以共价键结合而形成的三维骨架结构的晶体
109? 28?,三维骨架
键能:
347.7 kJ/mol
(很大)
键长:154 pm(很短)
熔点很高:
大于 3500 0C
硬度最大:
摩氏 10 度
结构决定性质
金刚石的用途
除了金刚石,还有哪些物质属于共价晶体呢?让我们沿着元素周期表一起寻找。
5. 常见共价晶体
(1)某些单质:以碳为中心,
同主族向下:
硅(Si)锗(Ge)和灰锡(Sn)等
同周期向左、向右:
硼(B)高聚氮
二、共价晶体
与金刚石极其相似,只是将碳原子换成了硅原子
硅晶体的结构
资料
硅晶体的结构
思考:
请推测晶体硅中 Si-Si 键的键参数与金刚石中 C-C 键的键参数相比,有什么变化?
原子半径:Si > C
键长变长,键能变小
(2)某些非金属化合物:
碳化硅(SiC) 氮化硅(Si3N4)
氮化硼(BN)等
以 Si3N4 为基础,用 Al 取代部分 Si,
用 O 取代部分 N 而获得结构多样化的
陶瓷,用于制作 LED 发光材料。
5. 常见共价晶体
二、共价晶体
6. 共价晶体的性质
资料卡片 P 82
二、共价晶体
硬度是衡量固体软硬程度的指标。硬度有不同的标度,最普通的硬度标度是画痕硬度,即摩氏硬度。以固体互相刻画时出现刻痕的固体的硬度较低。金刚石不能被任何天然矿物刻划出刻痕,因而是最硬的。以金刚石的硬度为 10,以另 9 种天然矿物为代表。可将摩氏硬度分为十度,即:
某些共价晶体的熔点和硬度
共价晶体
金刚石
氮化硼
碳化硅
石英
硅
锗
熔点 /0C
>3500
3000
2700
1710
1410
1211
硬 度
10
9.5
9.5
7
6.5
6.0
资料卡片 P 82
共价键
三维骨架结构
熔点高
硬度大
一般不导电
难溶于一些常见的溶剂
二、共价晶体
6. 共价晶体的性质
(1)怎样从原子结构的角度理解金刚石、硅和锗的熔点和
硬度依次降低?
金刚石、硅和锗中原子半径依次增大,键长变长,键能变小,共价键稳定性下降,熔点和硬度依次下降。
思考 P 82
SiO2 自然界含量最高的固态二元氧化物
有多种结构,最常见的是低温石英(α-SiO2)
黄沙、石英矿脉、花岗石中的白色晶体以及
透明的水晶都是低温石英。
二氧化硅的存在
石英的左、右型晶体
压电材料:
制作石英手表
低温石英的结构中有顶角相连的硅氧四面体形成螺旋上升的长链,而没有封闭的环状结构
二氧化硅的结构
二氧化硅的用途
以 SiO2 为原料制造的高科技产品:
单晶硅 硅芯片 硅太阳能电池 二氧化硅光导纤维
俗名“金刚砂”,它具有类似金刚石的结构和性质,其空间结构中碳原子和硅原子相间排列,化学式为 SiC。
SiC 的球棍模型
功能陶瓷
高级耐火材料
磨料
用途
碳化硅
(2)“具有共价键的晶体叫做共价晶体”,这种说法对吗?
为什么?
不对,共价晶体中都有共价键,但含有共价键的不一定是共价晶体。如分子晶体 CO2、H2O 的分子中也含有共价键。
思考 P 82
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}晶体类型
分子晶体
共价晶体
直接构成晶体的粒子
分子
原子
粒子间相互作用
分子间作用力
共价键
熔点
较低
很高
硬度
较小
很大
代表物
冰、干冰
金刚石
课堂小结
下列说法中,错误的是( )
A. 只含分子的晶体一定是分子晶体
B. 碘晶体升华时破坏了共价键
C. 几乎所有的酸都属于分子晶体
D. 稀有气体分子中只含原子,但稀有气体的晶体属于
分子晶体
课堂反馈
B
P 84-1
√
√
√
×
下列说法中,正确的是( )
A. 冰融化时,分子中 H-O 键发生断裂
B. 共价晶体中,共价键越强,熔点越高
C. 分子晶体中,共价键键能越大,该分子晶体的熔沸点
一定越高
D. 分子晶体中,分子间作用力越大,对应的物质越稳定
课堂反馈
B
分子晶体:影响熔、沸点的是分子间作用力,决定分子
稳定性的是分子内的共价键
P 84-2
下列说法中,正确的是( )
A. 分子晶体一定存在分子间作用力和共价键
B. 分子晶体的熔点一般比共价晶体的熔点高
C. 稀有气体形成的晶体属于分子晶体
D. CO2 晶体是分子晶体,可推测 SiO2 晶体也是分子晶体
课堂反馈
C
稀有气体
P 85-4
SiO2 晶体是共价晶体
低
请将下列晶体分类,并填入下表:
金刚石 干冰 冰 可燃冰 硫黄
C60 碘 石英 白磷(P4) 苯甲酸 金刚砂(SiC) 稀有气体的晶体
氧气的晶体 氮气的晶体
课堂反馈
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}分子晶体
共价晶体
P 85-7
请将下列晶体分类,并填入下表:
课堂反馈
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}分子晶体
干冰、冰、可燃冰、硫黄、C60、碘 白磷(P4)、苯甲酸 、稀有气体的晶体
氧气的晶体、氮气的晶体
共价晶体
金刚石、石英、金刚砂(SiC)
下列事实能说明刚玉(Al2O3)是共价晶体的是( )
①Al2O3 是两性氧化物;
②硬度很大;
③它的熔点是 2045 ℃;
④自然界中的刚玉有红宝石和蓝宝石
A. ①② B. ②③ C. ①④ D. ③④
课堂反馈
B
P 85-3
1. 整理笔记、落实知识
2. 完成 P 84 课后习题 5、6、8、9
3. 阅读 P 83 “科学·技术·社会”,了解金刚石的“前世今生”,
写一篇小论文。
课后作业
金刚石再硬、智慧能使它变软;
拥有智慧,平凡的石墨也能变成璀璨的钻石。
同 学 们 再 见 !
