第二章 空气、物质的构成 单元复习课件(55张ppt)-九年级化学上册同步精品课堂(科粤版)
文档属性
| 名称 | 第二章 空气、物质的构成 单元复习课件(55张ppt)-九年级化学上册同步精品课堂(科粤版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-17 00:00:00 | ||
图片预览








文档简介
化学(科粤版)
九年级 上册
第二章 空气、物质的构成
单元复习(课件)
知识框架
考点讲练
01
难点突破
趁热打铁
02
03
04
01
知识框架
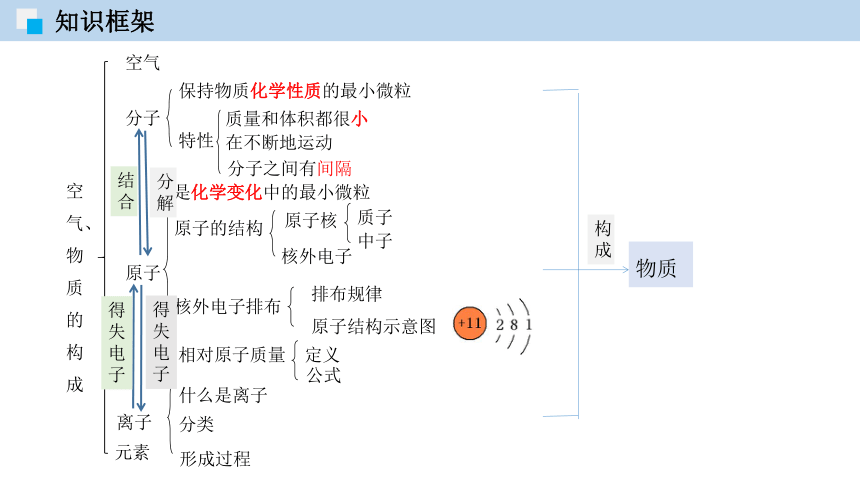
知识框架
空气、物质的构成
空气
分子
原子
空气的成分
空气中氧气含量的测定
空气的组成(体积分数)
原理
装置图
现象
结论
空气的污染和保护
氮气78%
氧气21%
其它气体1%
混合物和纯净物的区分
氮气的性质与用途
氮气和稀有气体的性质与用途
稀有气体的性质与用途
空气中的主要污染物
空气污染的主要危害
空气污染的主要来源
空气污染的防治
元素
离子
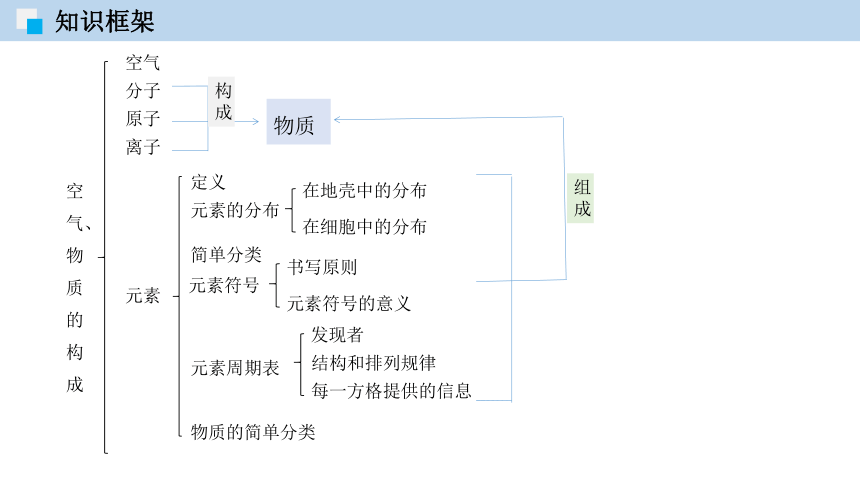
知识框架
空气、物质的构成
空气
分子
元素
分子之间有间隔
保持物质化学性质的最小微粒
特性
质量和体积都很小
在不断地运动
原子
离子
是化学变化中的最小微粒
原子的结构
原子核
核外电子
核外电子排布
质子
中子
排布规律
原子结构示意图
相对原子质量
定义
公式
什么是离子
分类
形成过程
结合
得失电子
分解
得失电子
物质
构成
知识框架
空气、物质的构成
空气
分子
元素
原子
离子
物质
构成
定义
元素的分布
在地壳中的分布
在细胞中的分布
简单分类
元素符号
书写原则
元素符号的意义
元素周期表
发现者
结构和排列规律
每一方格提供的信息
物质的简单分类
组成
02
考点讲练
考点一:空气中氧含量的测定
考点讲练
1.实验原理: ;
过量的红磷燃烧时耗尽集气瓶内的 ,使瓶内气体减少,压强 。打开弹簧夹后,烧杯里的水倒流入集气瓶中。进入集气瓶中水的体积就是集气瓶内被消耗的 的体积。
降低
氧气
氧气
①红磷燃烧,发出 火焰,有 生成,放出热量;
②冷却后,打开弹簧夹,水沿导管进入集气瓶,进入集气瓶
内水的体积约占集气瓶内空气总体积的 。
2.实验现象:
黄色
大量白烟
1/5
3.实验结论:
①___________________________。
②有关氮气的性质:_____________、________________________等
氧气约占空气总体积的1/5
难溶于水
不能燃烧也不支持燃烧
考点讲练
4.注意事项:
(1)不能用以下这些物质的原因:
①碳、硫、蜡烛 : 。
②铁: 。
与氧气反应生产气体,不能造成压强差,水不会倒流
铁与空气中的氧气不能迅速发生反应
(3)要在集气瓶里放少量的水。
?装置漏气;?红磷的量不足;?未完全冷却就打开止水夹。
(4)导致测定结果小于1/5的原因:
(2)点燃的红磷要立即伸入集气瓶中(防止 )。
白烟污染空气
考点讲练
【巩固训练】
1.[邵阳?中考]如图是“实验室测定空气中氧气含量”的实验装置图,下列有关说法错误的是( )
A.可用木炭代替红磷进行实验
B.做该实验前,应检查装置的气密性
C.待装置冷却至室温后才能打开止水夹
D.若红磷不足,将导致测得氧气的含量小于五分之一
A
考点讲练
【巩固训练】
2.如图甲是某同学测定空气中氧气含量的实验,该同学的操作正确,装置的气密性良好请回答下列问题:
(1)该实验中红磷要稍过量,目的是
(2)红磷燃烧产生大量的白烟,白烟产生的原因是:
;
完全消耗装置中的氧气
生成的五氧化二磷固体分散到空气中形成的
(3)瓶中液面最终上升至 处,能说明 。
氧气约占空气体积的1/5
1
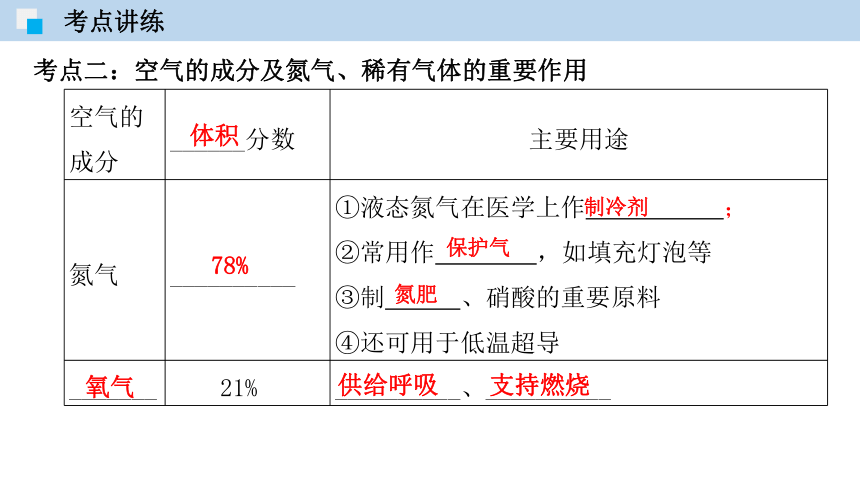
考点二:空气的成分及氮气、稀有气体的重要作用
考点讲练
空气的成分
______分数
主要用途
氮气
__________
①液态氮气在医学上作 ;
②常用作 ,如填充灯泡等
③制 、硝酸的重要原料
④还可用于低温超导
_______
21%
__________、__________
体积
78%
保护气
氮肥
氧气
供给呼吸
支持燃烧
制冷剂
考点讲练
稀有气体
__________
①化学性质稳定,用作________
②通电发出不同颜色的光,可制作多种________
③氦气化学性质很稳定、密度很小,可用来填充____________
二氧化碳
__________
植物______________的原料
其他气体和杂质
0.03%
0.94%
保护气
电光源
探空气球
0.03%
光合作用
考点讲练
1.下列有关空气组成的说法正确的是( )
A.氧气约占空气体积的
B.空气是一种重要的资源
C.氮气的化学性质不活泼,不能与任何物质发生反应
D.化石燃料的大量使用不会引起空气质量的改变
【巩固训练】
B
考点讲练
2.如图所示是空气成分示意图,请回答下列问题。
(1)仔细观察图,填写空白:① ;② 。
(2)“其他成分”中除了含有二氧化碳、水蒸气外,还含有
(填一种)。
(3)洁净的空气对人类非常重要。下列做法有利于净化空气的是 。
A.使用清洁能源
B.工业废气处理达标后再排放
C.积极植树造林
氮气
21%
稀有气体
ABC
考点三:空气污染的危害 保护大气环境
考点讲练
{5940675A-B579-460E-94D1-54222C63F5DA}空气中的主要污染物
①可吸入颗粒物;②有害气体( 、 、二氧化氮等)
污染物的主要来源
①工厂的废气;②汽车排放的尾气;③煤、石油等矿物燃烧
空气污染的危害
①损害人体的健康;②影响作物生长;③破坏生态平衡;④导致全球气候变暖;⑤破坏臭氧层;⑥形成酸雨(主要是 、 等引起)
空气污染的防治
①使用清洁能源;②工厂的废气经过处理后再排放;③使燃料充分燃烧;④对化石燃料进行脱硫处理;⑤积极植树、造林、种草等
二氧化硫
一氧化碳
二氧化硫
二氧化氮
考点讲练
1.[广东?中考]下列物质属于空气污染物的是( )
A.氧气 B.氮气 C.水蒸气 D.二氧化硫
D
2.[宁夏?中考]下列做法不能体现环境友好发展理念的是( )A.分类回收生活垃圾 B.禁止使用化石燃料
C.合理施用农药化肥 D.城市道路使用太阳能景观灯
【巩固训练】
B
考点四:构成物质的微粒
考点讲练
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
分 子
原 子
离 子
构成的物质
共同性质
根本区别
联系
绝大数气体(如氧气、氢气、二氧化碳等)、水等
①金属(如铁、铜等);②稀有气体(如氦气等);③固态非金属(如红磷等)
氯化钠等
体积和质量都很小;都在不断运动;微粒之间有间隔
保持物质化学性质的最小微粒,化学变化中可再分
化学变化中的最小微粒,在化学变化中不可再分
带电的微粒
分子 原子 离子
构成
得失
电子
分解
考点讲练
1.[西宁?中考]下列说法错误的是( )
A.远处就能闻到花的香味,说明分子在不断运动
B.1滴水中大约有1.67×1021个水分子,说明分子很小
C.用水银温度计测量体温时水银柱升高,说明分子间间隔增大
D.由分子构成的物质,分子是保持其化学性质的最小粒子
【巩固训练】
C
2.物质都是由微观粒子构成的,下列粒子不能直接构成物质的是( )
A.电子 B.原子 C.分子 D.离子
A
考点讲练
3.用下列序号进行填空:①分子之间有间隔;②分子体积很小;③温度越高,分子运动越快;④同种分子化学性质相同;⑤分子间隔变小;⑥化学变化中分子可分而原子不可分;⑦分子质量很小;⑧不同种分子化学性质不同;⑨分子在不断运动;⑩分子间隔变大。
(1)氧化汞受热分解: ; (2)液氧和氧气都具有助燃性: ;
(3)酒香不怕巷子深: ; (4)夏天晾晒衣服要比冬天干的更快 ;
(5)CO有毒,CO2无毒: ; (6)1 滴水中大约有1.67×1021 个水分子
(7)水结成冰后体积变大: ;(8)二氧化碳气体制成干冰体积变小 ;
(9)1个氢气分子质量为3.34×10﹣27kg ;
(10)5L水与5L酒精混合后总体积小10L 。
⑥
⑨
⑧
④
③
②
⑩
⑤
⑦
①
考点五:原子的结构
考点讲练
原子
原子核
核外电子
中子
质子
1个质子带1个单位的正电荷
(不带电)
(1个电子带1个单位负电荷)
2.在同一个原子中,质子数_____________中子数;
1.在同一个原子中,核电荷数=_______=__________;
质子数
核外电子数
不一定等于
3.原子中不一定含有 ,如氢原子;
中子
考点讲练
1.科学理论在传承中不断发展,科学家们传承前人的正确观点,纠正错误观点,形成科学理论,关于原子结构的观点有:①在球体内正电荷均匀分布,电子镶嵌其中;②原子是可分的;③原子中有带负电的电子;④原子中有带正电的原子核;⑤原子核很小,但集中了原子的大部分质量。其中经过卢瑟福传承和发展后的观点是( )A.④⑤ B.③④⑤ C.①②③④ D.②③④⑤
【巩固训练】
A
考点讲练
2.下列有关原子的说法正确的是( )
A.原子都是由质子、中子和电子构成的
B.在原子中质子数等于核外电子数
C.原子的质量主要是由质子和电子质量决定的
D.保持氮气化学性质的微粒是氮原子
3.考古学家通过C﹣14测定法将我省宁波地区的文明发展史推到距今8000多年前。C﹣14原子的核电荷数为6.相对原子质量为14,则该原子核外电子数为( )
A.6 B.8 C.14 D.20
A
B
考点六:核外电子的排布规律
考点讲练
排布特点1:电子在核外是 的
电子从离核 (能量最低)的一层开始排,这层为第一层,排满第一层再排第二层,依次类推为三、四、五、六、七层,离核最远的也叫 。
排布特点2:各电子层上最多排2n2个电子:
其中第一层最多排 个电子,最外层最多排 个电子。
2
8
最近
最外层
分层排布
考点讲练
2.原子结构示意图
原子核
电子层
该电子层上的电子数
质子数(核电荷数)
最外层电子数
①决定元素种类的是 ;
②决定元素化学性质的是 ;
判断化学性质是否相似的方法:
a.稳定结构的化学性质相似。
如 和 化学性质相似
b.非稳定结构的, 的化学性质相似。
③决定原子的质量的是 。
原子的最外层电子数
原子核(或质子和中子)
质子数(核电荷数)
最外层电子数相同
考点讲练
【巩固训练】
1.如图是四种粒子的结构示意图,下列有关说法正确的是( )
A.②表示相对稳定结构的粒子
B.①表示的粒子在化学反应中易失电子 C.①②③④表示四种不同元素
D.②④所表示的粒子化学性质相似
A
考点讲练
2.[兴安盟?中考]如图为某粒子结构示意图,下列说法错误的是( )
A.该粒子属于非金属元素
B.该粒子核外电子数为17
C.该粒子具有3个电子层
D.在化学反应中,该元素原子易得电子形成Cl﹣
B
考点七:离子
考点讲练
(1)定义: 叫做离子。
带电的原子
(2)形成:元素的原子在发生化学反应时都有一个趋势:通过得失电子使自己的最外层达到相对稳定的结构。具体过程如下图所示:
考点讲练
(3)分类
·阳离子:多数金属原子 最外层电子形成的,带 电荷;
·阴离子:许多非金属原子 最外层电子形成的,带 电荷;
失去
得到
正
负
(4)符号书写 在元素符号的右上角标上数字和正负号,用来表明离子所带电荷的数量和正负。书写的基本规则是数字在前,符号在后。例如:Mg2+。【注意】当离子所带电荷为1时,1可以省略不写,直接用正负号表示离子带一个单位的正电荷或负电荷,如Na+、OH-等。
考点讲练
【巩固训练】
1.[常德?中考]如图是五种微粒的结构示意图,下列说法正确的是( )
A.①④属于金属元素
B.②的微粒符号是Al3+
C.②③⑤属于阳离子
D.②⑤位于元素周期表的同一周期
B
考点讲练
2.[衡阳?中考]如图是几种微粒结构示意图,请用相应微粒代号填空。
(1)属于金属元素原子的是 ;(2)具有相对稳定结构的是 ;(3)属于同种元素的是 ;(4)表示离子的是 。
①
④和⑤
③和⑤
⑤
考点八:相对原子质量
考点讲练
(4)相对原子质量=质子数+中子数
1.定义:以碳-12原子的质量的1/12为标准,其它原子的质量跟它的比值。
2.公式:
相对原子质量=
原子的实际质量
碳12原子质量的1/12
3.注意:
(1)相对原子质量不是原子的真实质量;
(2)相对原子质量是个比值,单位为 1 ,一般不写;
(3)相对原子质量与原子的真实质量成正比。
考点讲练
【巩固训练】
1.济阳“仁风”西瓜富含硒元素而闻名,硒元素被誉为“抗癌大王”.已知硒原子的核电荷数为34,相对原子质量为79,下列关于该原子的说法正确的是( )
A.质子数为45 B.核外电子数为34
C.中子数为34 D.原子序数为79
B
2.[常州?中考]已知某氧原子的实际质量为mg,其相对原子质量为
16。有一种铕(Eu)原子的相对原子质量为152,铕(Eu)原子的
质量为( )
A
考点九:元素
考点讲练
1.什么是元素:
2.元素的分布:①地壳中含量前五位的元素: ;②细胞中含量最高的元素: ;
O、Si、Al、Fe、Ca
O
具有相同质子数(或核电荷数)的一类原子的总称。
3.元素的简单分类:
元素分为 、 和 。
金属元素
非金属元素
稀有气体元素
金属元素:该类元素原子的最外层电子数一般 4,在化学反应中容易 电子变成稳定结构。
非金属元素:该类元素原子的最外层电子数一般 4(氢元素只有1个电子),在化学反应中容易 电子变成稳定结构。
稀有气体元素:最外层为8个电子(氦元素原子最外层为2),不易得失电子,均为稳定结构。
小于
失去
大于
得到
考点讲练
(2)元素符号表示的意义:
①表示 ;
②表示 。
③有些元素符号还可表示 ,如Fe、He 、C 、Si等(由原子直接构成的物质)
4.元素符号(1)书写原则:
第一个字母大写,第二个字母小写,若该元素符号中只有一个字母,则大写。
某种元素
某种元素的一个原子
一种单质
考点讲练
【巩固训练】
1.如图为原子变化的示意图,其中①②③表示三种原子,“●”、“〇”、“。”表示原子中的不同微粒,①②③中属于同种元素的原子是( )
A.①②③ B.①② C.②③ D.①③
B
考点讲练
2.[柳州?中考]奶制品、豆类、虾皮等食物中含钙丰富,是日常饮食中钙的较好来源,这里的“钙”指( )A.钙离子 B.钙原子 C.钙元素 D.钙单质
C
3.如图为地壳中的元素含量示意图(质量分数)。其中Y表示的元素为( )
A.氧 B.硅 C.铝 D.铁
B
4.下列元素符号书写正确的是( )A.钡﹣BA B.钠﹣Na C.镁﹣mg D.锌﹣zN
B
考点讲练
考点十:元素周期表
(1)发现者:
(2)结构:
(3)排列规律: 同周期: 相同,最外层电子数随着核电荷数的增大逐渐 ;
同族:原子 相同(He例外), 自上而下逐渐增加(化学性质相似)
俄国科学家门捷列夫
7个周期16个族(7个横行18个纵行)
原子电子层数
增加
电子层数
最电外层电子数
考点讲练
(4)元素周期表中每一方格提供的信息:
硫
原子序数
相对原子质量
元素符号
元素名称
S
16
32.07
【注意】
1.原子序数=核电荷数= = ;
2.相对原子质量≈ + ,单位为1,通常不写。
质子数
中子数
核外电子数
质子数
考点讲练
【巩固训练】
镝灯具有亮度大、体积小、电弧稳定等优点,现已广泛用于电影、印刷等照明光源的制造。镝元素的相关信息如图所示,下列有关说法正确的是( )
A.镝属于非金属元素 B.镝原子的核电荷数为66 C.镝的相对原子质量为162.5g D.镝原子的中子数为66
B
考点十一:物质的分类
考点讲练
物质
混合物
纯净物
化合物
单质
金属单质 (如铁、镁等)
非金属单质(如碳、氧气等)
氧化物
其它化合物(酸、碱、盐等)
由两种或多种物质混合而成的物质(如:空气、溶液等)
根据物质的组成是否单一
由一种物质组成的物质。(例如氧气、二氧化碳、高锰酸钾等)
根据元素的组成是否单一
同种元素组成的纯净物
不同种元素组成的纯净物
由两种元素组成,其中
一种是氧元素的化合物
考点讲练
【巩固训练】
1.各图中〇和●分别表示不同元素的原子,则其中表示化合物的是( )
{5940675A-B579-460E-94D1-54222C63F5DA}
A
B
C
D
A
2.属于非金属单质的是( )
A.Al B.Hg C.Si D.Mn
C
03
难点突破
难点突破
难点一 结构示意图和元素周期表的结合考察
【难点梳理】
1.由结构示意图我们可以得知以下信息:
:能判断是哪种元素以及原子序数
:可判断该结构是原子结构还是离子结构;易得到还是易失去电子;与哪种元素化学性质相似;在元素周期表中的哪一族。
:在元素周期表中的哪一周期
难点突破
2.由结构示意图我们可以得知以下信息:
元素名称
元素符号
原子序数
相对原子质量
同周期:原子 相同,从左到右最外层电子数逐渐增加。
周期数= 。
同族:原子 相同(He例外),从上到下电子层数逐渐增加(化学性质相似)
电子层数
原子的电子层数
最电外层电子数
原子序数= = = ;
≈质子数+中子数
质子数
核电荷数
原子的最外层电子数
难点突破
1.在宏观、微观和符号之间建立联系是化学学科特点。
(1)原子序数为20的元素位于元素周期表中第 周期,决定该元素的化学性质的是 。
(2)如图①是某原子结构示意图,其中y= 。
(3)从图②③④所示的三种微粒结构示意图中,所获取信息正确的是 。A.它们表示两种元素 B.④表示的元素是金属元素
C.③④化学性质相同 D.②④表示的是原子,③表示的是阳离子
四
最外层电子数
17
ABD
【典例剖析】
难点突破
2.[日照?中考]几种元素在元素周期表中的部分信息如图所示。请回答下列问题:
(2)图2所示粒子共表示 种元素。X元素的化学性质与图2中 的化学性质相似(填写字母标号)。
(1)下列说法不正确的是 (填写字母标号)。 A.氯原子的质子数为17,最外层电子数为7 B.磷的相对原子质量为30.97g
C.X元素的原子序数为16,元素名称为硫,元素符号为SD.X元素与磷、氯元素位于同周期,与氧元素位于同一族
3
A
B
04
趁热打铁
趁热打铁
1.[聊城?中考]下列关于空气的说法错误的是( )
A.氮气和氧气约占空气体积的78%和21%
B.目前计入空气污染指数的有害气体包括SO2、CO2、NO2等
C.工业上利用分离液态空气制取氧气,这一过程属于物理变化D.为改善空气质量,提倡“绿色出行”,以公共交通工具为主
B
2.[营口?中考]实验室用燃烧法测定空气中氧气的含量,最适宜选用的可燃物是( )
A.红磷 B.木炭 C.细铁丝 D.蜡烛
A
趁热打铁
3.[淄博?中考]世界万物都是由极其微小的粒子构成的,下列说法正确的是( )
A.海水是由海水分子构成的
B.分子、原子、离子都能直接构成物质
C.二氧化碳是由碳原子和氧原子构成的
D.自然界中的物质都是由质子、中子、电子等粒子构成的
B
4.国际纯粹与应用化学联合会(IUPAC)将周期表第116号元素Lv命名为“鉝”(lì)。鉝原子的原子核里有177个中子,该原子的核外电子数为( )
A.193 B.177 C.61 D.116
D
趁热打铁
5.根据如图的信息判断,下列说法错误的是( )
A.氯原子的质子数是17
B.氯元素是非金属元素
C.当x=8时,该微粒是阳离子
D.在化学变化中,氯原子易得电子
C
6.(2020?株洲)下列微观示意图中,黑球代表H原子,白球代表Cl原子,其中代表混合物的是( )
D
趁热打铁
7.[邵阳?中考]如图是四种粒子的结构示意图,下列分析错误的是( )
A.①③化学性质相似
B.②为阴离子
C.③④属于同一种元素
D.③为第三周期元素的原子
8.用如图所示装置进行实验。下列现象能证明空气中O2含量的是( )
A.水槽中液面下降
B.瓶中液面最终上升至1处
C.红磷燃烧,产生白烟
D.瓶中液面先下降,后上升
B
B
趁热打铁
9.中国将建设世界上最大的雾霾实验室“烟雾箱”,用于人工模拟颗粒物的形成、光化学烟雾和灰霾的产生原因等。则:(1)京津冀地区将预警联防联控大气污染组织一场“呼吸保卫战”,合作改善该地区的空气质量,解困十面“霾”伏的环境难题。下列不属于影响空气质量的大气污染物的是 。
A.可吸入颗粒物(PM2.5) B.CO2 C.NO2 D.SO2
(2)近年来,我国多地出现雾霾天气增多现象,工业污染物和汽车尾气等是形成雾霾天气的主要元凶,从采取节能减排措施考虑,如何治理PM2.5细颗粒物的合理做法有
。
B
工业废气经过处理后再排放;上班做公交车,少开私家车等
趁热打铁
10.人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝。结合图中信息回答下列问题:
(1)碘原子在化学反应中容易 (填“失去”或“得到”)电子;(2)碘元素属于 元素(选填“金属”或“非金属”);
(3)已知原子核外的电子层数与元素所在周期表中的周期数相同,则碘元素在元素周期表中应该排在第 周期。
得到
非金属
5
九年级 上册
第二章 空气、物质的构成
单元复习(课件)
知识框架
考点讲练
01
难点突破
趁热打铁
02
03
04
01
知识框架
知识框架
空气、物质的构成
空气
分子
原子
空气的成分
空气中氧气含量的测定
空气的组成(体积分数)
原理
装置图
现象
结论
空气的污染和保护
氮气78%
氧气21%
其它气体1%
混合物和纯净物的区分
氮气的性质与用途
氮气和稀有气体的性质与用途
稀有气体的性质与用途
空气中的主要污染物
空气污染的主要危害
空气污染的主要来源
空气污染的防治
元素
离子
知识框架
空气、物质的构成
空气
分子
元素
分子之间有间隔
保持物质化学性质的最小微粒
特性
质量和体积都很小
在不断地运动
原子
离子
是化学变化中的最小微粒
原子的结构
原子核
核外电子
核外电子排布
质子
中子
排布规律
原子结构示意图
相对原子质量
定义
公式
什么是离子
分类
形成过程
结合
得失电子
分解
得失电子
物质
构成
知识框架
空气、物质的构成
空气
分子
元素
原子
离子
物质
构成
定义
元素的分布
在地壳中的分布
在细胞中的分布
简单分类
元素符号
书写原则
元素符号的意义
元素周期表
发现者
结构和排列规律
每一方格提供的信息
物质的简单分类
组成
02
考点讲练
考点一:空气中氧含量的测定
考点讲练
1.实验原理: ;
过量的红磷燃烧时耗尽集气瓶内的 ,使瓶内气体减少,压强 。打开弹簧夹后,烧杯里的水倒流入集气瓶中。进入集气瓶中水的体积就是集气瓶内被消耗的 的体积。
降低
氧气
氧气
①红磷燃烧,发出 火焰,有 生成,放出热量;
②冷却后,打开弹簧夹,水沿导管进入集气瓶,进入集气瓶
内水的体积约占集气瓶内空气总体积的 。
2.实验现象:
黄色
大量白烟
1/5
3.实验结论:
①___________________________。
②有关氮气的性质:_____________、________________________等
氧气约占空气总体积的1/5
难溶于水
不能燃烧也不支持燃烧
考点讲练
4.注意事项:
(1)不能用以下这些物质的原因:
①碳、硫、蜡烛 : 。
②铁: 。
与氧气反应生产气体,不能造成压强差,水不会倒流
铁与空气中的氧气不能迅速发生反应
(3)要在集气瓶里放少量的水。
?装置漏气;?红磷的量不足;?未完全冷却就打开止水夹。
(4)导致测定结果小于1/5的原因:
(2)点燃的红磷要立即伸入集气瓶中(防止 )。
白烟污染空气
考点讲练
【巩固训练】
1.[邵阳?中考]如图是“实验室测定空气中氧气含量”的实验装置图,下列有关说法错误的是( )
A.可用木炭代替红磷进行实验
B.做该实验前,应检查装置的气密性
C.待装置冷却至室温后才能打开止水夹
D.若红磷不足,将导致测得氧气的含量小于五分之一
A
考点讲练
【巩固训练】
2.如图甲是某同学测定空气中氧气含量的实验,该同学的操作正确,装置的气密性良好请回答下列问题:
(1)该实验中红磷要稍过量,目的是
(2)红磷燃烧产生大量的白烟,白烟产生的原因是:
;
完全消耗装置中的氧气
生成的五氧化二磷固体分散到空气中形成的
(3)瓶中液面最终上升至 处,能说明 。
氧气约占空气体积的1/5
1
考点二:空气的成分及氮气、稀有气体的重要作用
考点讲练
空气的成分
______分数
主要用途
氮气
__________
①液态氮气在医学上作 ;
②常用作 ,如填充灯泡等
③制 、硝酸的重要原料
④还可用于低温超导
_______
21%
__________、__________
体积
78%
保护气
氮肥
氧气
供给呼吸
支持燃烧
制冷剂
考点讲练
稀有气体
__________
①化学性质稳定,用作________
②通电发出不同颜色的光,可制作多种________
③氦气化学性质很稳定、密度很小,可用来填充____________
二氧化碳
__________
植物______________的原料
其他气体和杂质
0.03%
0.94%
保护气
电光源
探空气球
0.03%
光合作用
考点讲练
1.下列有关空气组成的说法正确的是( )
A.氧气约占空气体积的
B.空气是一种重要的资源
C.氮气的化学性质不活泼,不能与任何物质发生反应
D.化石燃料的大量使用不会引起空气质量的改变
【巩固训练】
B
考点讲练
2.如图所示是空气成分示意图,请回答下列问题。
(1)仔细观察图,填写空白:① ;② 。
(2)“其他成分”中除了含有二氧化碳、水蒸气外,还含有
(填一种)。
(3)洁净的空气对人类非常重要。下列做法有利于净化空气的是 。
A.使用清洁能源
B.工业废气处理达标后再排放
C.积极植树造林
氮气
21%
稀有气体
ABC
考点三:空气污染的危害 保护大气环境
考点讲练
{5940675A-B579-460E-94D1-54222C63F5DA}空气中的主要污染物
①可吸入颗粒物;②有害气体( 、 、二氧化氮等)
污染物的主要来源
①工厂的废气;②汽车排放的尾气;③煤、石油等矿物燃烧
空气污染的危害
①损害人体的健康;②影响作物生长;③破坏生态平衡;④导致全球气候变暖;⑤破坏臭氧层;⑥形成酸雨(主要是 、 等引起)
空气污染的防治
①使用清洁能源;②工厂的废气经过处理后再排放;③使燃料充分燃烧;④对化石燃料进行脱硫处理;⑤积极植树、造林、种草等
二氧化硫
一氧化碳
二氧化硫
二氧化氮
考点讲练
1.[广东?中考]下列物质属于空气污染物的是( )
A.氧气 B.氮气 C.水蒸气 D.二氧化硫
D
2.[宁夏?中考]下列做法不能体现环境友好发展理念的是( )A.分类回收生活垃圾 B.禁止使用化石燃料
C.合理施用农药化肥 D.城市道路使用太阳能景观灯
【巩固训练】
B
考点四:构成物质的微粒
考点讲练
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
分 子
原 子
离 子
构成的物质
共同性质
根本区别
联系
绝大数气体(如氧气、氢气、二氧化碳等)、水等
①金属(如铁、铜等);②稀有气体(如氦气等);③固态非金属(如红磷等)
氯化钠等
体积和质量都很小;都在不断运动;微粒之间有间隔
保持物质化学性质的最小微粒,化学变化中可再分
化学变化中的最小微粒,在化学变化中不可再分
带电的微粒
分子 原子 离子
构成
得失
电子
分解
考点讲练
1.[西宁?中考]下列说法错误的是( )
A.远处就能闻到花的香味,说明分子在不断运动
B.1滴水中大约有1.67×1021个水分子,说明分子很小
C.用水银温度计测量体温时水银柱升高,说明分子间间隔增大
D.由分子构成的物质,分子是保持其化学性质的最小粒子
【巩固训练】
C
2.物质都是由微观粒子构成的,下列粒子不能直接构成物质的是( )
A.电子 B.原子 C.分子 D.离子
A
考点讲练
3.用下列序号进行填空:①分子之间有间隔;②分子体积很小;③温度越高,分子运动越快;④同种分子化学性质相同;⑤分子间隔变小;⑥化学变化中分子可分而原子不可分;⑦分子质量很小;⑧不同种分子化学性质不同;⑨分子在不断运动;⑩分子间隔变大。
(1)氧化汞受热分解: ; (2)液氧和氧气都具有助燃性: ;
(3)酒香不怕巷子深: ; (4)夏天晾晒衣服要比冬天干的更快 ;
(5)CO有毒,CO2无毒: ; (6)1 滴水中大约有1.67×1021 个水分子
(7)水结成冰后体积变大: ;(8)二氧化碳气体制成干冰体积变小 ;
(9)1个氢气分子质量为3.34×10﹣27kg ;
(10)5L水与5L酒精混合后总体积小10L 。
⑥
⑨
⑧
④
③
②
⑩
⑤
⑦
①
考点五:原子的结构
考点讲练
原子
原子核
核外电子
中子
质子
1个质子带1个单位的正电荷
(不带电)
(1个电子带1个单位负电荷)
2.在同一个原子中,质子数_____________中子数;
1.在同一个原子中,核电荷数=_______=__________;
质子数
核外电子数
不一定等于
3.原子中不一定含有 ,如氢原子;
中子
考点讲练
1.科学理论在传承中不断发展,科学家们传承前人的正确观点,纠正错误观点,形成科学理论,关于原子结构的观点有:①在球体内正电荷均匀分布,电子镶嵌其中;②原子是可分的;③原子中有带负电的电子;④原子中有带正电的原子核;⑤原子核很小,但集中了原子的大部分质量。其中经过卢瑟福传承和发展后的观点是( )A.④⑤ B.③④⑤ C.①②③④ D.②③④⑤
【巩固训练】
A
考点讲练
2.下列有关原子的说法正确的是( )
A.原子都是由质子、中子和电子构成的
B.在原子中质子数等于核外电子数
C.原子的质量主要是由质子和电子质量决定的
D.保持氮气化学性质的微粒是氮原子
3.考古学家通过C﹣14测定法将我省宁波地区的文明发展史推到距今8000多年前。C﹣14原子的核电荷数为6.相对原子质量为14,则该原子核外电子数为( )
A.6 B.8 C.14 D.20
A
B
考点六:核外电子的排布规律
考点讲练
排布特点1:电子在核外是 的
电子从离核 (能量最低)的一层开始排,这层为第一层,排满第一层再排第二层,依次类推为三、四、五、六、七层,离核最远的也叫 。
排布特点2:各电子层上最多排2n2个电子:
其中第一层最多排 个电子,最外层最多排 个电子。
2
8
最近
最外层
分层排布
考点讲练
2.原子结构示意图
原子核
电子层
该电子层上的电子数
质子数(核电荷数)
最外层电子数
①决定元素种类的是 ;
②决定元素化学性质的是 ;
判断化学性质是否相似的方法:
a.稳定结构的化学性质相似。
如 和 化学性质相似
b.非稳定结构的, 的化学性质相似。
③决定原子的质量的是 。
原子的最外层电子数
原子核(或质子和中子)
质子数(核电荷数)
最外层电子数相同
考点讲练
【巩固训练】
1.如图是四种粒子的结构示意图,下列有关说法正确的是( )
A.②表示相对稳定结构的粒子
B.①表示的粒子在化学反应中易失电子 C.①②③④表示四种不同元素
D.②④所表示的粒子化学性质相似
A
考点讲练
2.[兴安盟?中考]如图为某粒子结构示意图,下列说法错误的是( )
A.该粒子属于非金属元素
B.该粒子核外电子数为17
C.该粒子具有3个电子层
D.在化学反应中,该元素原子易得电子形成Cl﹣
B
考点七:离子
考点讲练
(1)定义: 叫做离子。
带电的原子
(2)形成:元素的原子在发生化学反应时都有一个趋势:通过得失电子使自己的最外层达到相对稳定的结构。具体过程如下图所示:
考点讲练
(3)分类
·阳离子:多数金属原子 最外层电子形成的,带 电荷;
·阴离子:许多非金属原子 最外层电子形成的,带 电荷;
失去
得到
正
负
(4)符号书写 在元素符号的右上角标上数字和正负号,用来表明离子所带电荷的数量和正负。书写的基本规则是数字在前,符号在后。例如:Mg2+。【注意】当离子所带电荷为1时,1可以省略不写,直接用正负号表示离子带一个单位的正电荷或负电荷,如Na+、OH-等。
考点讲练
【巩固训练】
1.[常德?中考]如图是五种微粒的结构示意图,下列说法正确的是( )
A.①④属于金属元素
B.②的微粒符号是Al3+
C.②③⑤属于阳离子
D.②⑤位于元素周期表的同一周期
B
考点讲练
2.[衡阳?中考]如图是几种微粒结构示意图,请用相应微粒代号填空。
(1)属于金属元素原子的是 ;(2)具有相对稳定结构的是 ;(3)属于同种元素的是 ;(4)表示离子的是 。
①
④和⑤
③和⑤
⑤
考点八:相对原子质量
考点讲练
(4)相对原子质量=质子数+中子数
1.定义:以碳-12原子的质量的1/12为标准,其它原子的质量跟它的比值。
2.公式:
相对原子质量=
原子的实际质量
碳12原子质量的1/12
3.注意:
(1)相对原子质量不是原子的真实质量;
(2)相对原子质量是个比值,单位为 1 ,一般不写;
(3)相对原子质量与原子的真实质量成正比。
考点讲练
【巩固训练】
1.济阳“仁风”西瓜富含硒元素而闻名,硒元素被誉为“抗癌大王”.已知硒原子的核电荷数为34,相对原子质量为79,下列关于该原子的说法正确的是( )
A.质子数为45 B.核外电子数为34
C.中子数为34 D.原子序数为79
B
2.[常州?中考]已知某氧原子的实际质量为mg,其相对原子质量为
16。有一种铕(Eu)原子的相对原子质量为152,铕(Eu)原子的
质量为( )
A
考点九:元素
考点讲练
1.什么是元素:
2.元素的分布:①地壳中含量前五位的元素: ;②细胞中含量最高的元素: ;
O、Si、Al、Fe、Ca
O
具有相同质子数(或核电荷数)的一类原子的总称。
3.元素的简单分类:
元素分为 、 和 。
金属元素
非金属元素
稀有气体元素
金属元素:该类元素原子的最外层电子数一般 4,在化学反应中容易 电子变成稳定结构。
非金属元素:该类元素原子的最外层电子数一般 4(氢元素只有1个电子),在化学反应中容易 电子变成稳定结构。
稀有气体元素:最外层为8个电子(氦元素原子最外层为2),不易得失电子,均为稳定结构。
小于
失去
大于
得到
考点讲练
(2)元素符号表示的意义:
①表示 ;
②表示 。
③有些元素符号还可表示 ,如Fe、He 、C 、Si等(由原子直接构成的物质)
4.元素符号(1)书写原则:
第一个字母大写,第二个字母小写,若该元素符号中只有一个字母,则大写。
某种元素
某种元素的一个原子
一种单质
考点讲练
【巩固训练】
1.如图为原子变化的示意图,其中①②③表示三种原子,“●”、“〇”、“。”表示原子中的不同微粒,①②③中属于同种元素的原子是( )
A.①②③ B.①② C.②③ D.①③
B
考点讲练
2.[柳州?中考]奶制品、豆类、虾皮等食物中含钙丰富,是日常饮食中钙的较好来源,这里的“钙”指( )A.钙离子 B.钙原子 C.钙元素 D.钙单质
C
3.如图为地壳中的元素含量示意图(质量分数)。其中Y表示的元素为( )
A.氧 B.硅 C.铝 D.铁
B
4.下列元素符号书写正确的是( )A.钡﹣BA B.钠﹣Na C.镁﹣mg D.锌﹣zN
B
考点讲练
考点十:元素周期表
(1)发现者:
(2)结构:
(3)排列规律: 同周期: 相同,最外层电子数随着核电荷数的增大逐渐 ;
同族:原子 相同(He例外), 自上而下逐渐增加(化学性质相似)
俄国科学家门捷列夫
7个周期16个族(7个横行18个纵行)
原子电子层数
增加
电子层数
最电外层电子数
考点讲练
(4)元素周期表中每一方格提供的信息:
硫
原子序数
相对原子质量
元素符号
元素名称
S
16
32.07
【注意】
1.原子序数=核电荷数= = ;
2.相对原子质量≈ + ,单位为1,通常不写。
质子数
中子数
核外电子数
质子数
考点讲练
【巩固训练】
镝灯具有亮度大、体积小、电弧稳定等优点,现已广泛用于电影、印刷等照明光源的制造。镝元素的相关信息如图所示,下列有关说法正确的是( )
A.镝属于非金属元素 B.镝原子的核电荷数为66 C.镝的相对原子质量为162.5g D.镝原子的中子数为66
B
考点十一:物质的分类
考点讲练
物质
混合物
纯净物
化合物
单质
金属单质 (如铁、镁等)
非金属单质(如碳、氧气等)
氧化物
其它化合物(酸、碱、盐等)
由两种或多种物质混合而成的物质(如:空气、溶液等)
根据物质的组成是否单一
由一种物质组成的物质。(例如氧气、二氧化碳、高锰酸钾等)
根据元素的组成是否单一
同种元素组成的纯净物
不同种元素组成的纯净物
由两种元素组成,其中
一种是氧元素的化合物
考点讲练
【巩固训练】
1.各图中〇和●分别表示不同元素的原子,则其中表示化合物的是( )
{5940675A-B579-460E-94D1-54222C63F5DA}
A
B
C
D
A
2.属于非金属单质的是( )
A.Al B.Hg C.Si D.Mn
C
03
难点突破
难点突破
难点一 结构示意图和元素周期表的结合考察
【难点梳理】
1.由结构示意图我们可以得知以下信息:
:能判断是哪种元素以及原子序数
:可判断该结构是原子结构还是离子结构;易得到还是易失去电子;与哪种元素化学性质相似;在元素周期表中的哪一族。
:在元素周期表中的哪一周期
难点突破
2.由结构示意图我们可以得知以下信息:
元素名称
元素符号
原子序数
相对原子质量
同周期:原子 相同,从左到右最外层电子数逐渐增加。
周期数= 。
同族:原子 相同(He例外),从上到下电子层数逐渐增加(化学性质相似)
电子层数
原子的电子层数
最电外层电子数
原子序数= = = ;
≈质子数+中子数
质子数
核电荷数
原子的最外层电子数
难点突破
1.在宏观、微观和符号之间建立联系是化学学科特点。
(1)原子序数为20的元素位于元素周期表中第 周期,决定该元素的化学性质的是 。
(2)如图①是某原子结构示意图,其中y= 。
(3)从图②③④所示的三种微粒结构示意图中,所获取信息正确的是 。A.它们表示两种元素 B.④表示的元素是金属元素
C.③④化学性质相同 D.②④表示的是原子,③表示的是阳离子
四
最外层电子数
17
ABD
【典例剖析】
难点突破
2.[日照?中考]几种元素在元素周期表中的部分信息如图所示。请回答下列问题:
(2)图2所示粒子共表示 种元素。X元素的化学性质与图2中 的化学性质相似(填写字母标号)。
(1)下列说法不正确的是 (填写字母标号)。 A.氯原子的质子数为17,最外层电子数为7 B.磷的相对原子质量为30.97g
C.X元素的原子序数为16,元素名称为硫,元素符号为SD.X元素与磷、氯元素位于同周期,与氧元素位于同一族
3
A
B
04
趁热打铁
趁热打铁
1.[聊城?中考]下列关于空气的说法错误的是( )
A.氮气和氧气约占空气体积的78%和21%
B.目前计入空气污染指数的有害气体包括SO2、CO2、NO2等
C.工业上利用分离液态空气制取氧气,这一过程属于物理变化D.为改善空气质量,提倡“绿色出行”,以公共交通工具为主
B
2.[营口?中考]实验室用燃烧法测定空气中氧气的含量,最适宜选用的可燃物是( )
A.红磷 B.木炭 C.细铁丝 D.蜡烛
A
趁热打铁
3.[淄博?中考]世界万物都是由极其微小的粒子构成的,下列说法正确的是( )
A.海水是由海水分子构成的
B.分子、原子、离子都能直接构成物质
C.二氧化碳是由碳原子和氧原子构成的
D.自然界中的物质都是由质子、中子、电子等粒子构成的
B
4.国际纯粹与应用化学联合会(IUPAC)将周期表第116号元素Lv命名为“鉝”(lì)。鉝原子的原子核里有177个中子,该原子的核外电子数为( )
A.193 B.177 C.61 D.116
D
趁热打铁
5.根据如图的信息判断,下列说法错误的是( )
A.氯原子的质子数是17
B.氯元素是非金属元素
C.当x=8时,该微粒是阳离子
D.在化学变化中,氯原子易得电子
C
6.(2020?株洲)下列微观示意图中,黑球代表H原子,白球代表Cl原子,其中代表混合物的是( )
D
趁热打铁
7.[邵阳?中考]如图是四种粒子的结构示意图,下列分析错误的是( )
A.①③化学性质相似
B.②为阴离子
C.③④属于同一种元素
D.③为第三周期元素的原子
8.用如图所示装置进行实验。下列现象能证明空气中O2含量的是( )
A.水槽中液面下降
B.瓶中液面最终上升至1处
C.红磷燃烧,产生白烟
D.瓶中液面先下降,后上升
B
B
趁热打铁
9.中国将建设世界上最大的雾霾实验室“烟雾箱”,用于人工模拟颗粒物的形成、光化学烟雾和灰霾的产生原因等。则:(1)京津冀地区将预警联防联控大气污染组织一场“呼吸保卫战”,合作改善该地区的空气质量,解困十面“霾”伏的环境难题。下列不属于影响空气质量的大气污染物的是 。
A.可吸入颗粒物(PM2.5) B.CO2 C.NO2 D.SO2
(2)近年来,我国多地出现雾霾天气增多现象,工业污染物和汽车尾气等是形成雾霾天气的主要元凶,从采取节能减排措施考虑,如何治理PM2.5细颗粒物的合理做法有
。
B
工业废气经过处理后再排放;上班做公交车,少开私家车等
趁热打铁
10.人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝。结合图中信息回答下列问题:
(1)碘原子在化学反应中容易 (填“失去”或“得到”)电子;(2)碘元素属于 元素(选填“金属”或“非金属”);
(3)已知原子核外的电子层数与元素所在周期表中的周期数相同,则碘元素在元素周期表中应该排在第 周期。
得到
非金属
5
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
