2020-2021学年鲁教版化学九年级下册 7.2 碱及其性质 同步练习含解析答案
文档属性
| 名称 | 2020-2021学年鲁教版化学九年级下册 7.2 碱及其性质 同步练习含解析答案 |

|
|
| 格式 | doc | ||
| 文件大小 | 237.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-17 00:00:00 | ||
图片预览




文档简介
7.2 碱及其性质
一.选择题
1.我们已经学习和掌握了很多物质,并进行了分类.下列各组内物质表示同种物质的是( )
A.氢氧化钠、烧碱、火碱
B.氢氧化钙、消石灰、生石灰
C.盐酸、氯化氢、食盐
D.冰、干冰、可燃冰
2.下列叙述完全正确的是( )
A.可用肥皂水区别硬水与软水
B.用托盘天平称量8.10g氯化钠固体
C.在化学反应中只有燃烧才能放出热量
D.用氢氧化钠改良酸性土壤
3.物质的性质决定其用途,下列关于物质的用途不正确的是( )
A.干冰﹣人工降雨 B.铜丝﹣作导线
C.烧碱﹣治疗胃酸过多 D.熟石灰﹣改良酸性土壤
4.氢氧化钙的俗称是( )
A.烧碱 B.消石灰 C.纯碱 D.生石灰
5.冬春季节,园林工人会给许多树的树干刷一段石灰浆,下列有关说法正确的是( )
A.石灰浆属于溶液
B.石灰浆的主要成分是CaO
C.石灰浆可以防止树木上的害虫生卵
D.一段时间后树干上的白色物质是Ca(OH)2
6.农业生产中常用于改良酸性土壤的物质是( )
A.烧碱 B.熟石灰 C.氯化钾 D.硝酸铵
7.下列物质及其用途对应正确提( )
A.熟石灰﹣﹣改良碱性土壤
B.二氧化碳﹣﹣炼铁
C.钛合金﹣﹣航天航海器材
D.氢氧化钠溶液﹣﹣干燥二氧化硫
8.下列有关氢氧化钠的说法不正确的是( )
A.氢氧化钠有腐蚀性
B.固体氢氧化钠有挥发性
C.固体氢氧化钠能吸收水蒸气而潮解
D.氢氧化钠常用于造纸、炼油和橡胶工业
9.氢氧化钠是重要的化工原料,下列不是其俗称的是( )
A.纯碱 B.烧碱 C.苛性钠 D.火碱
10.氢氧化钠、氢氧化钙等是常见的碱,它们在水中都能解离出共同的( )
A.Ca2+ B.H+ C.Na+ D.OH﹣
11.氢氧化钙在农业上可用于改良酸性土壤。氢氧化钙的俗称是( )
A.小苏打 B.熟石灰 C.烧碱 D.纯碱
12.下列对实验现象的描述,不正确的是( )
A.向装有硫酸铜溶液的试管里滴加氢氧化钠溶液,产生蓝色絮状沉淀
B.硫在空气中燃烧产生淡蓝色的火焰,生成刺激性气味的二氧化硫气体
C.细铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体
D.镁条在空气中燃烧,发出耀眼白光,生成一种白色固体
13.对反应X+3NaOH═3Y+Fe(OH)3↓的分析,错误的是( )
A.Y中一定含有Na元素 B.X可以是单质
C.Y可能是NaCl D.X可能是FeCl3
14.向含有HCl和FeCl3的混合溶液中,逐滴加入NaOH溶液至过量。下列图象正确的是( )
A.
B.
C.
D.
15.某一溶液由盐酸、稀硫酸、碳酸钾、氯化铁中的两种混合而成。现向该混合溶液中滴入氢氧化钡溶液,产生的沉淀质量与加入氢氧化钡溶液体积如图所示,则下列判断正确的是( )
A.该溶液中含有硫酸和盐酸
B.该溶液中含有碳酸钾和硫酸
C.该溶液中含有盐酸和氯化铁
D.该溶液中含有稀硫酸和氯化铁
16.下列物质中能与澄清石灰水反应,但反应若不加指示剂则无明显现象的是( )
A.氯化铜溶液 B.碳酸钠溶液 C.氯化镁溶液 D.稀盐酸
17.物质的性质不仅决定了它的用途,还决定了它的保存方法。固体氢氧化钠具有以下性质,实验室中固体氢氧化钠必须密封保存的主要原因是( )
①有腐蚀性;
②易吸收水蒸汽而潮解;
③易溶于水,溶解时放出热量;
④能与空气中的二氧化碳反应。
A.①② B.①③ C.②④ D.③④
二.填空题
18.小明通过图示装置验证CO2能与NaOH发生化学反应。推注射器活塞向充满CO2的集气瓶中注入过量20%的NaOH溶液,振荡集气瓶后打开止水夹。
(1)打开止水夹后观察到的现象是氯化钙溶液流入左边集气瓶中,并且 。
(2)反应后将集气瓶中混合物过滤,所得溶液中除CaCl2、NaOH外,还存在的溶质有 。
19.回答下列问题:
(1)澄清石灰水若敞口久置,观察到现象是 。该反应的化学方程式为 。
(2)氢氧化钠露置在空气中不但能吸收 发生潮解,而且还能与空气中的 反应而变质,因此氢氧化钠必须密封保存。写出氢氧化钠露置空气中变质的化学方程式为: 。
20.如图为酸碱的化学性质知识网络,A、B、C、D是四种常见的不同类别的化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请你据图回答。
(1)A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质是 (填字母);
(2)要使反应①和②的现象不同,物质D可以是 (填化学式);
(3)稀硫酸在工业中还可以用于除锈,当铁锈除完后,还要用水把多余的硫酸冲洗掉,请问要除去多余的硫酸的原因是(请用化学方程式表示) 。
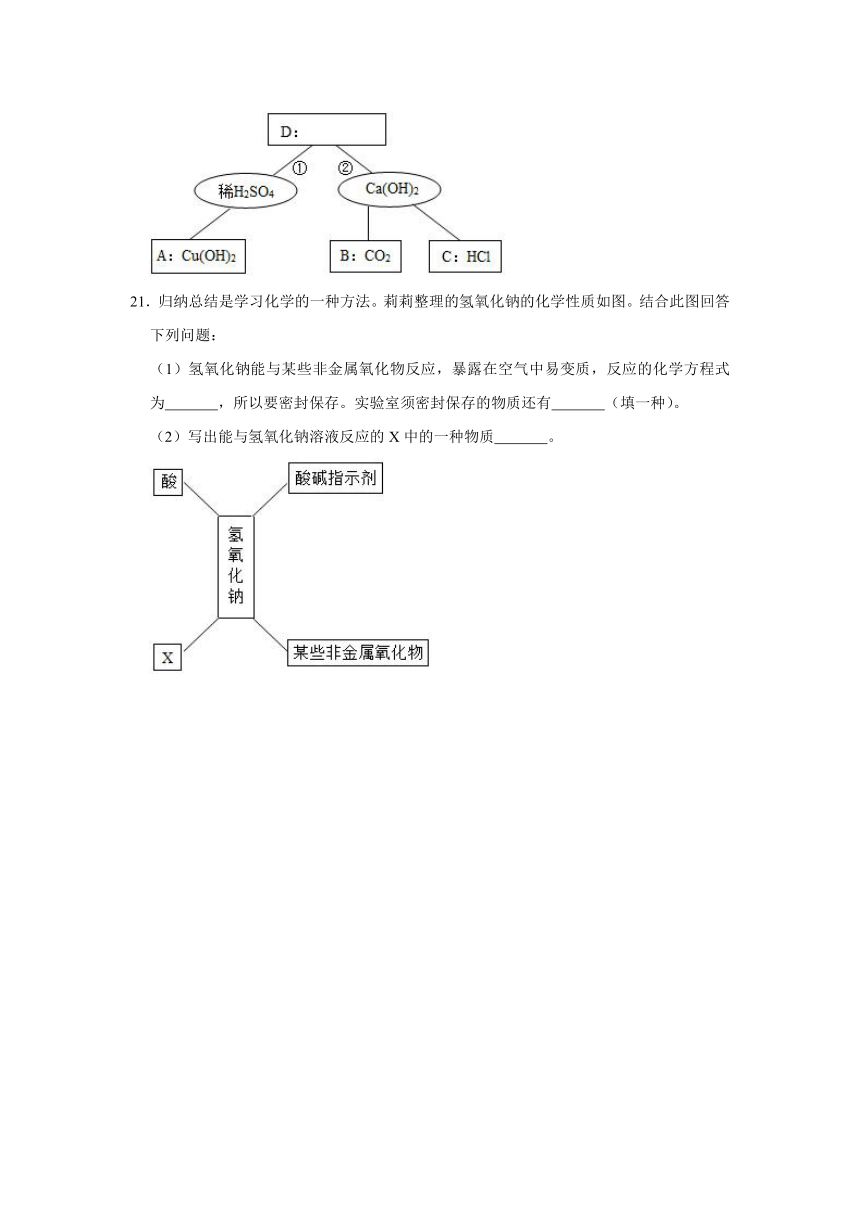
21.归纳总结是学习化学的一种方法。莉莉整理的氢氧化钠的化学性质如图。结合此图回答下列问题:
(1)氢氧化钠能与某些非金属氧化物反应,暴露在空气中易变质,反应的化学方程式为 ,所以要密封保存。实验室须密封保存的物质还有 (填一种)。
(2)写出能与氢氧化钠溶液反应的X中的一种物质 。
参考答案
一.选择题
1.解:A、氢氧化钠俗称火碱、烧碱、苛性钠,该选项组内物质表示的是同种物质,故选项正确。
B、氢氧化钙的俗称是熟石灰或消石灰,生石灰是氧化钙的俗称,该选项组内物质表示的不是同种物质,故选项错误。
C、盐酸是氯化氢气体的水溶液,食盐是氯化钠的俗称,该选项组内物质表示的不是同种物质,故选项错误。
D、冰是固态的水,干冰是固态的二氧化碳,可燃冰是甲烷的水合物,该选项组内物质表示的不是同种物质,故选项错误。
故选:A。
2.解:A.鉴别硬水与软水可用肥皂水,泡沫多浮渣少的是软水,泡沫少浮渣多的是硬水,故说法正确;
B.托盘天平只能精确到0.1g,所以不能称量出8.10g氯化钠固体,故说法错误;
C.在化学反应中不是只有燃烧才能放出热量,如氧化钙与水反应也会放出热量,故说法错误;
D.氢氧化钠具有强烈的腐蚀性,不能用于改良酸性土壤,故说法错误。
故选:A。
3.解:A、干冰升华吸热,使温度降低,可用于人工降雨,故选项说法正确。
B、铜具有优良的导电性,可用作导线,故选项说法正确。
C、烧碱具有强烈的腐蚀性,不能用于治疗胃酸过多,故选项说法错误。
D、熟石灰能与酸发生中和反应,可用于改良酸性土壤,故选项说法正确。
故选:C。
4.解:A、火碱是氢氧化钠的俗称,故选项错误。
B、氢氧化钙俗称熟石灰或消石灰,故选项正确。
C、纯碱是碳酸钠的俗称,故选项错误。
D、生石灰是氧化钙的俗称,故选项错误。
故选:B。
5.解:A.石灰浆是氢氧化钙的悬浊液,故错误;
B.石灰浆的主要成分是氢氧化钙,其化学式为Ca(OH)2,故错误;
C.石灰浆可以防止树木上的害虫生卵,故正确;
D.氢氧化钙能吸收空气中的二氧化碳生成碳酸钙白色沉淀,所以一段时间后树干上的白色物质是CaCO3,故错误。
故选:C。
6.解:A.烧碱是一种碱,显碱性,能与酸性物质反应,但是腐蚀性太强,价格较高,不能用于改良酸性土壤,故错误;
B.氢氧化钙具有碱性,农业生产中可用于改良酸性土壤,故正确;
C.氯化钾是一种盐,显中性,不能用于改良酸性土壤,故错误;
D.硝酸铵是一种盐,显酸性,不能用于改良酸性土壤,故错误。
故选:B。
7.解:
A、熟石灰呈碱性,用于改良酸性土壤,故错误;
B、二氧化碳没有还原性,不能用于炼铁,故错误;
C、钛合金具有密度小、耐高温、耐腐蚀性、强度高、机械性能好等优良性能,被广泛应用于航空、航天、航海、医疗器械等领域,故正确;
D、氢氧化钠溶液与二氧化硫反应,不能干燥二氧化硫,故错误;
故选:C。
8.解:A.氢氧化钠就有强烈的腐蚀性,故正确;
B.氢氧化钠固体没有挥发性,故错误;
C.氢氧化钠具有吸水性,氢氧化钠固体暴露在空气中吸收水分而溶解,故正确;
D.氢氧化钠常用于造纸、炼油和橡胶工业,故正确。
故选:B。
9.解:氢氧化钠俗称烧碱、火碱、苛性钠;纯碱是碳酸钠的俗称。
故选:A。
10.解:A、氢氧化钠在水中电离出钠离子和氢氧根离子,氢氧化钙在水中电离出钙离子和氢氧根离子,故错误;
B、酸在水中都能电离出离子的是氢离子,故错误;
C、氢氧化钠在水中电离出钠离子和氢氧根离子,氢氧化钙在水中电离出钙离子和氢氧根离子,故错误。
D、碱在水中都能电离出离子的是氢氧根离子,故正确;
故选:D。
11.解:氢氧化钙俗称熟石灰或消石灰,可用作建筑材料。
A、小苏打是碳酸氢钠的俗称,故A错误;
B、熟石灰是氢氧化钙的俗称,故B正确;
C、生石灰是氧化钙的俗称,故C错误;
D、纯碱是碳酸钠的俗称,故D错误。
故选:B。
12.解:A、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,氢氧化钠溶液加入硫酸铜溶液中产生蓝色絮状沉淀,故选项说法正确。
B、硫在空气中燃烧,发出淡蓝色火焰,生成刺激性气味的二氧化硫气体是实验结论而不是实验现象,故选项说法错误。
C、细铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故选项说法正确。
D、镁条在空气中燃烧,发出耀眼白光,生成一种白色固体,故选项说法正确。
故选:B。
13.解:A、由X+3NaOH═3Y+Fe(OH)3↓,由质量守恒定律,Y中一定含有Na元素,故选项说法正确。
B、X中含有铁元素,铁不能与氢氧化钠溶液反应,X不可能是单质,故选项说法错误。
C、Y可能是NaCl,则X是氯化铁,氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,故选项说法正确。
D、X可能是FeCl3,氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,故选项说法正确。
故选:B。
14.解:A、盐酸呈酸性,开始时溶液的pH小于7,氢氧化钠先与盐酸反应,溶液pH值变大,恰好中和时等于7,然后氢氧化钠与氯化铁反应生成氢氧化铁沉淀和氯化钠,pH不变,当氢氧化钠过量时,pH大于7,A错误;
B、向含有HCl和FeCl3的混合溶液中,逐滴加入NaOH溶液时,氢离子与氢氧根离子结合成水,铁离子与氢氧根离子结合成氢氧化铁沉淀,离子数目减小,导电性减弱,B错误;
C、向含有HCl和FeCl3的混合溶液中,逐滴加入NaOH溶液时,氢氧化钠溶液中有水,水的质量一直增加,C错误;
D、向含有HCl和FeCl3的混合溶液中,逐滴加入NaOH溶液至过量,氢氧化钠先与盐酸发生中和反应生成氯化钠和水,再与氯化铁反应生成氢氧化铁沉淀,随着反应的进行,氯化铁不断减少,直至反应停止,此时就不会有沉淀生成,D正确;
故选:D。
15.解:某一溶液由盐酸、稀硫酸、碳酸钾、氯化铁中的两种混合而成。现向该混合溶液中滴入氢氧化钡溶液,沉淀的质量先是零,再不断上升,最后形成一条水平直线,说明溶液中一定不含硫酸,因为硫酸与氢氧化钡溶液反应生成不溶于酸的硫酸钡沉淀,一开始就产生沉淀。观察选项C符合变化过程,稀盐酸先与氢氧化钡溶液反应生成
氯化钡溶液,稀盐酸消耗完,氯化铁与氢氧化钡溶液反应生成氢氧化铁沉淀和氯化钡,沉淀的质量先是零,再不断上升,最后形成一条水平直线。
故选:C。
16.解:A、铜离子和氢氧根离子会生成蓝色的氢氧化铁沉淀,有明显的现象,故A不符合题意;
B、碳酸根离子会和钙离子生成白色的碳酸钙沉淀,混合后溶液中出现浑浊,有明显的现象,故B不符合题意;
C、镁离子和氢氧根离子会生成白色氢氧化镁沉淀,有明显的现象,故C不符合题意;
D、稀盐酸和氢氧化钙发生中和反应生成了水,而没现象,需要借助指示剂,故D符合题意。
故选:D。
17.解:由于固体氢氧化钠在空气中易吸收水蒸气而潮解,且能与空气中的二氧化碳反应生成碳酸钠,所以固体氢氧化钠必须密封保存,以防止其变质,因此相关的性质主要是潮解及能与二氧化碳反应。
故选:C。
二.填空题
18.解:(1)推注射器活塞向充满CO2的集气瓶中注入过量20%的NaOH溶液,二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,使瓶内压强减小;打开止水夹后观察到的现象是氯化钙溶液流入左边集气瓶中;碳酸钠与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,还会观察到溶液变浑浊。
(2)根据题意,反应后将集气瓶中混合物过滤,所得溶液中含有CaCl2、NaOH外,碳酸钠与氯化钙不能共存,则一定不含碳酸钠。碳酸钠与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,则还存在的溶质有氯化钠,其化学式为NaCl。
故答案为:
(1)溶液变浑浊;
(2)NaCl。
19.解:(1)澄清石灰水若敞口久置,能与空气中的二氧化碳反应生成碳酸钙沉淀和水,观察到现象是石灰水表面生成一层白膜,该反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O。
(2)氢氧化钠露置在空气中不但能吸收水分发生潮解,而且还能与空气中的二氧化碳反应而变质,因此氢氧化钠必须密封保存。二氧化碳与氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O。
故答案为:
(1)石灰水表面生成一层白膜;CO2+Ca(OH)2═CaCO3↓+H2O;
(2)水分;二氧化碳;CO2+2NaOH═Na2CO3+H2O。
20.解:(1)能用来鉴别稀硫酸与氢氧化钙溶液的物质是AB,是因为氢氧化铜和稀硫酸反应生成硫酸铜和水,过程中蓝色固体溶解,形成蓝色溶液,不能和氢氧化钙反应,二氧化碳能使澄清石灰水变浑浊,和稀硫酸混合无明显现象。
(2)要使反应①和②的现象不同,物质D可以是碳酸钠,是因为碳酸钠和稀硫酸反应生成二氧化碳气体,过程中产生气泡,和氢氧化钙反应生成碳酸钙沉淀。
(3)要除去多余的硫酸的原因:铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式:H2SO4+Fe═FeSO4+H2↑。
故填:AB;Na2CO3;H2SO4+Fe═FeSO4+H2↑。
21.解:(1)氢氧化钠能与某些非金属氧化物反应,暴露在空气中易变质,是因为二氧化碳和氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O,所以要密封保存;
实验室须密封保存的物质还有浓硫酸、氧化钙、浓盐酸等。
故填:2NaOH+CO2═Na2CO3+H2O;浓硫酸。
(2)能与氢氧化钠溶液反应的X中的一种物质可以是硫酸铜,这是因为硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠。
故填:硫酸铜。
一.选择题
1.我们已经学习和掌握了很多物质,并进行了分类.下列各组内物质表示同种物质的是( )
A.氢氧化钠、烧碱、火碱
B.氢氧化钙、消石灰、生石灰
C.盐酸、氯化氢、食盐
D.冰、干冰、可燃冰
2.下列叙述完全正确的是( )
A.可用肥皂水区别硬水与软水
B.用托盘天平称量8.10g氯化钠固体
C.在化学反应中只有燃烧才能放出热量
D.用氢氧化钠改良酸性土壤
3.物质的性质决定其用途,下列关于物质的用途不正确的是( )
A.干冰﹣人工降雨 B.铜丝﹣作导线
C.烧碱﹣治疗胃酸过多 D.熟石灰﹣改良酸性土壤
4.氢氧化钙的俗称是( )
A.烧碱 B.消石灰 C.纯碱 D.生石灰
5.冬春季节,园林工人会给许多树的树干刷一段石灰浆,下列有关说法正确的是( )
A.石灰浆属于溶液
B.石灰浆的主要成分是CaO
C.石灰浆可以防止树木上的害虫生卵
D.一段时间后树干上的白色物质是Ca(OH)2
6.农业生产中常用于改良酸性土壤的物质是( )
A.烧碱 B.熟石灰 C.氯化钾 D.硝酸铵
7.下列物质及其用途对应正确提( )
A.熟石灰﹣﹣改良碱性土壤
B.二氧化碳﹣﹣炼铁
C.钛合金﹣﹣航天航海器材
D.氢氧化钠溶液﹣﹣干燥二氧化硫
8.下列有关氢氧化钠的说法不正确的是( )
A.氢氧化钠有腐蚀性
B.固体氢氧化钠有挥发性
C.固体氢氧化钠能吸收水蒸气而潮解
D.氢氧化钠常用于造纸、炼油和橡胶工业
9.氢氧化钠是重要的化工原料,下列不是其俗称的是( )
A.纯碱 B.烧碱 C.苛性钠 D.火碱
10.氢氧化钠、氢氧化钙等是常见的碱,它们在水中都能解离出共同的( )
A.Ca2+ B.H+ C.Na+ D.OH﹣
11.氢氧化钙在农业上可用于改良酸性土壤。氢氧化钙的俗称是( )
A.小苏打 B.熟石灰 C.烧碱 D.纯碱
12.下列对实验现象的描述,不正确的是( )
A.向装有硫酸铜溶液的试管里滴加氢氧化钠溶液,产生蓝色絮状沉淀
B.硫在空气中燃烧产生淡蓝色的火焰,生成刺激性气味的二氧化硫气体
C.细铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体
D.镁条在空气中燃烧,发出耀眼白光,生成一种白色固体
13.对反应X+3NaOH═3Y+Fe(OH)3↓的分析,错误的是( )
A.Y中一定含有Na元素 B.X可以是单质
C.Y可能是NaCl D.X可能是FeCl3
14.向含有HCl和FeCl3的混合溶液中,逐滴加入NaOH溶液至过量。下列图象正确的是( )
A.
B.
C.
D.
15.某一溶液由盐酸、稀硫酸、碳酸钾、氯化铁中的两种混合而成。现向该混合溶液中滴入氢氧化钡溶液,产生的沉淀质量与加入氢氧化钡溶液体积如图所示,则下列判断正确的是( )
A.该溶液中含有硫酸和盐酸
B.该溶液中含有碳酸钾和硫酸
C.该溶液中含有盐酸和氯化铁
D.该溶液中含有稀硫酸和氯化铁
16.下列物质中能与澄清石灰水反应,但反应若不加指示剂则无明显现象的是( )
A.氯化铜溶液 B.碳酸钠溶液 C.氯化镁溶液 D.稀盐酸
17.物质的性质不仅决定了它的用途,还决定了它的保存方法。固体氢氧化钠具有以下性质,实验室中固体氢氧化钠必须密封保存的主要原因是( )
①有腐蚀性;
②易吸收水蒸汽而潮解;
③易溶于水,溶解时放出热量;
④能与空气中的二氧化碳反应。
A.①② B.①③ C.②④ D.③④
二.填空题
18.小明通过图示装置验证CO2能与NaOH发生化学反应。推注射器活塞向充满CO2的集气瓶中注入过量20%的NaOH溶液,振荡集气瓶后打开止水夹。
(1)打开止水夹后观察到的现象是氯化钙溶液流入左边集气瓶中,并且 。
(2)反应后将集气瓶中混合物过滤,所得溶液中除CaCl2、NaOH外,还存在的溶质有 。
19.回答下列问题:
(1)澄清石灰水若敞口久置,观察到现象是 。该反应的化学方程式为 。
(2)氢氧化钠露置在空气中不但能吸收 发生潮解,而且还能与空气中的 反应而变质,因此氢氧化钠必须密封保存。写出氢氧化钠露置空气中变质的化学方程式为: 。
20.如图为酸碱的化学性质知识网络,A、B、C、D是四种常见的不同类别的化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请你据图回答。
(1)A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质是 (填字母);
(2)要使反应①和②的现象不同,物质D可以是 (填化学式);
(3)稀硫酸在工业中还可以用于除锈,当铁锈除完后,还要用水把多余的硫酸冲洗掉,请问要除去多余的硫酸的原因是(请用化学方程式表示) 。
21.归纳总结是学习化学的一种方法。莉莉整理的氢氧化钠的化学性质如图。结合此图回答下列问题:
(1)氢氧化钠能与某些非金属氧化物反应,暴露在空气中易变质,反应的化学方程式为 ,所以要密封保存。实验室须密封保存的物质还有 (填一种)。
(2)写出能与氢氧化钠溶液反应的X中的一种物质 。
参考答案
一.选择题
1.解:A、氢氧化钠俗称火碱、烧碱、苛性钠,该选项组内物质表示的是同种物质,故选项正确。
B、氢氧化钙的俗称是熟石灰或消石灰,生石灰是氧化钙的俗称,该选项组内物质表示的不是同种物质,故选项错误。
C、盐酸是氯化氢气体的水溶液,食盐是氯化钠的俗称,该选项组内物质表示的不是同种物质,故选项错误。
D、冰是固态的水,干冰是固态的二氧化碳,可燃冰是甲烷的水合物,该选项组内物质表示的不是同种物质,故选项错误。
故选:A。
2.解:A.鉴别硬水与软水可用肥皂水,泡沫多浮渣少的是软水,泡沫少浮渣多的是硬水,故说法正确;
B.托盘天平只能精确到0.1g,所以不能称量出8.10g氯化钠固体,故说法错误;
C.在化学反应中不是只有燃烧才能放出热量,如氧化钙与水反应也会放出热量,故说法错误;
D.氢氧化钠具有强烈的腐蚀性,不能用于改良酸性土壤,故说法错误。
故选:A。
3.解:A、干冰升华吸热,使温度降低,可用于人工降雨,故选项说法正确。
B、铜具有优良的导电性,可用作导线,故选项说法正确。
C、烧碱具有强烈的腐蚀性,不能用于治疗胃酸过多,故选项说法错误。
D、熟石灰能与酸发生中和反应,可用于改良酸性土壤,故选项说法正确。
故选:C。
4.解:A、火碱是氢氧化钠的俗称,故选项错误。
B、氢氧化钙俗称熟石灰或消石灰,故选项正确。
C、纯碱是碳酸钠的俗称,故选项错误。
D、生石灰是氧化钙的俗称,故选项错误。
故选:B。
5.解:A.石灰浆是氢氧化钙的悬浊液,故错误;
B.石灰浆的主要成分是氢氧化钙,其化学式为Ca(OH)2,故错误;
C.石灰浆可以防止树木上的害虫生卵,故正确;
D.氢氧化钙能吸收空气中的二氧化碳生成碳酸钙白色沉淀,所以一段时间后树干上的白色物质是CaCO3,故错误。
故选:C。
6.解:A.烧碱是一种碱,显碱性,能与酸性物质反应,但是腐蚀性太强,价格较高,不能用于改良酸性土壤,故错误;
B.氢氧化钙具有碱性,农业生产中可用于改良酸性土壤,故正确;
C.氯化钾是一种盐,显中性,不能用于改良酸性土壤,故错误;
D.硝酸铵是一种盐,显酸性,不能用于改良酸性土壤,故错误。
故选:B。
7.解:
A、熟石灰呈碱性,用于改良酸性土壤,故错误;
B、二氧化碳没有还原性,不能用于炼铁,故错误;
C、钛合金具有密度小、耐高温、耐腐蚀性、强度高、机械性能好等优良性能,被广泛应用于航空、航天、航海、医疗器械等领域,故正确;
D、氢氧化钠溶液与二氧化硫反应,不能干燥二氧化硫,故错误;
故选:C。
8.解:A.氢氧化钠就有强烈的腐蚀性,故正确;
B.氢氧化钠固体没有挥发性,故错误;
C.氢氧化钠具有吸水性,氢氧化钠固体暴露在空气中吸收水分而溶解,故正确;
D.氢氧化钠常用于造纸、炼油和橡胶工业,故正确。
故选:B。
9.解:氢氧化钠俗称烧碱、火碱、苛性钠;纯碱是碳酸钠的俗称。
故选:A。
10.解:A、氢氧化钠在水中电离出钠离子和氢氧根离子,氢氧化钙在水中电离出钙离子和氢氧根离子,故错误;
B、酸在水中都能电离出离子的是氢离子,故错误;
C、氢氧化钠在水中电离出钠离子和氢氧根离子,氢氧化钙在水中电离出钙离子和氢氧根离子,故错误。
D、碱在水中都能电离出离子的是氢氧根离子,故正确;
故选:D。
11.解:氢氧化钙俗称熟石灰或消石灰,可用作建筑材料。
A、小苏打是碳酸氢钠的俗称,故A错误;
B、熟石灰是氢氧化钙的俗称,故B正确;
C、生石灰是氧化钙的俗称,故C错误;
D、纯碱是碳酸钠的俗称,故D错误。
故选:B。
12.解:A、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,氢氧化钠溶液加入硫酸铜溶液中产生蓝色絮状沉淀,故选项说法正确。
B、硫在空气中燃烧,发出淡蓝色火焰,生成刺激性气味的二氧化硫气体是实验结论而不是实验现象,故选项说法错误。
C、细铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故选项说法正确。
D、镁条在空气中燃烧,发出耀眼白光,生成一种白色固体,故选项说法正确。
故选:B。
13.解:A、由X+3NaOH═3Y+Fe(OH)3↓,由质量守恒定律,Y中一定含有Na元素,故选项说法正确。
B、X中含有铁元素,铁不能与氢氧化钠溶液反应,X不可能是单质,故选项说法错误。
C、Y可能是NaCl,则X是氯化铁,氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,故选项说法正确。
D、X可能是FeCl3,氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,故选项说法正确。
故选:B。
14.解:A、盐酸呈酸性,开始时溶液的pH小于7,氢氧化钠先与盐酸反应,溶液pH值变大,恰好中和时等于7,然后氢氧化钠与氯化铁反应生成氢氧化铁沉淀和氯化钠,pH不变,当氢氧化钠过量时,pH大于7,A错误;
B、向含有HCl和FeCl3的混合溶液中,逐滴加入NaOH溶液时,氢离子与氢氧根离子结合成水,铁离子与氢氧根离子结合成氢氧化铁沉淀,离子数目减小,导电性减弱,B错误;
C、向含有HCl和FeCl3的混合溶液中,逐滴加入NaOH溶液时,氢氧化钠溶液中有水,水的质量一直增加,C错误;
D、向含有HCl和FeCl3的混合溶液中,逐滴加入NaOH溶液至过量,氢氧化钠先与盐酸发生中和反应生成氯化钠和水,再与氯化铁反应生成氢氧化铁沉淀,随着反应的进行,氯化铁不断减少,直至反应停止,此时就不会有沉淀生成,D正确;
故选:D。
15.解:某一溶液由盐酸、稀硫酸、碳酸钾、氯化铁中的两种混合而成。现向该混合溶液中滴入氢氧化钡溶液,沉淀的质量先是零,再不断上升,最后形成一条水平直线,说明溶液中一定不含硫酸,因为硫酸与氢氧化钡溶液反应生成不溶于酸的硫酸钡沉淀,一开始就产生沉淀。观察选项C符合变化过程,稀盐酸先与氢氧化钡溶液反应生成
氯化钡溶液,稀盐酸消耗完,氯化铁与氢氧化钡溶液反应生成氢氧化铁沉淀和氯化钡,沉淀的质量先是零,再不断上升,最后形成一条水平直线。
故选:C。
16.解:A、铜离子和氢氧根离子会生成蓝色的氢氧化铁沉淀,有明显的现象,故A不符合题意;
B、碳酸根离子会和钙离子生成白色的碳酸钙沉淀,混合后溶液中出现浑浊,有明显的现象,故B不符合题意;
C、镁离子和氢氧根离子会生成白色氢氧化镁沉淀,有明显的现象,故C不符合题意;
D、稀盐酸和氢氧化钙发生中和反应生成了水,而没现象,需要借助指示剂,故D符合题意。
故选:D。
17.解:由于固体氢氧化钠在空气中易吸收水蒸气而潮解,且能与空气中的二氧化碳反应生成碳酸钠,所以固体氢氧化钠必须密封保存,以防止其变质,因此相关的性质主要是潮解及能与二氧化碳反应。
故选:C。
二.填空题
18.解:(1)推注射器活塞向充满CO2的集气瓶中注入过量20%的NaOH溶液,二氧化碳与氢氧化钠溶液反应生成碳酸钠和水,使瓶内压强减小;打开止水夹后观察到的现象是氯化钙溶液流入左边集气瓶中;碳酸钠与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,还会观察到溶液变浑浊。
(2)根据题意,反应后将集气瓶中混合物过滤,所得溶液中含有CaCl2、NaOH外,碳酸钠与氯化钙不能共存,则一定不含碳酸钠。碳酸钠与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,则还存在的溶质有氯化钠,其化学式为NaCl。
故答案为:
(1)溶液变浑浊;
(2)NaCl。
19.解:(1)澄清石灰水若敞口久置,能与空气中的二氧化碳反应生成碳酸钙沉淀和水,观察到现象是石灰水表面生成一层白膜,该反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O。
(2)氢氧化钠露置在空气中不但能吸收水分发生潮解,而且还能与空气中的二氧化碳反应而变质,因此氢氧化钠必须密封保存。二氧化碳与氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O。
故答案为:
(1)石灰水表面生成一层白膜;CO2+Ca(OH)2═CaCO3↓+H2O;
(2)水分;二氧化碳;CO2+2NaOH═Na2CO3+H2O。
20.解:(1)能用来鉴别稀硫酸与氢氧化钙溶液的物质是AB,是因为氢氧化铜和稀硫酸反应生成硫酸铜和水,过程中蓝色固体溶解,形成蓝色溶液,不能和氢氧化钙反应,二氧化碳能使澄清石灰水变浑浊,和稀硫酸混合无明显现象。
(2)要使反应①和②的现象不同,物质D可以是碳酸钠,是因为碳酸钠和稀硫酸反应生成二氧化碳气体,过程中产生气泡,和氢氧化钙反应生成碳酸钙沉淀。
(3)要除去多余的硫酸的原因:铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式:H2SO4+Fe═FeSO4+H2↑。
故填:AB;Na2CO3;H2SO4+Fe═FeSO4+H2↑。
21.解:(1)氢氧化钠能与某些非金属氧化物反应,暴露在空气中易变质,是因为二氧化碳和氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O,所以要密封保存;
实验室须密封保存的物质还有浓硫酸、氧化钙、浓盐酸等。
故填:2NaOH+CO2═Na2CO3+H2O;浓硫酸。
(2)能与氢氧化钠溶液反应的X中的一种物质可以是硫酸铜,这是因为硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠。
故填:硫酸铜。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
