2012【优化方案】精品课件:鲁科物理选修3-3第2章第2节
文档属性
| 名称 | 2012【优化方案】精品课件:鲁科物理选修3-3第2章第2节 |

|
|
| 格式 | rar | ||
| 文件大小 | 433.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 物理 | ||
| 更新时间 | 2011-12-20 00:00:00 | ||
图片预览










文档简介
(共36张PPT)
第2节 固体的微观结构
课前自主学案
核心要点突破
课标定位
课堂互动讲练
第2节
知能优化训练
课标定位
学习目标:1.了解对晶体结构的认识过程,知道晶体内部结构的特点.
2.理解晶体与非晶体存在差异的原因是其微观结构不同,并能够解释它们物理性质存在差异的原因.
3.了解金刚石与石墨存在差异的原因,并能够从其结构模型上进行分析.
重点难点:1.晶体的微观结构和晶体的结构类型.
2.固体特征的微观解释.
课前自主学案
一、晶体的结构
1.1912年,德国物理学家____,证实了晶体内部的物质微粒按一定规律整齐地排列.
2.组成晶体的物质微粒有规则地在空间排成____,呈现周而复始的____结构,说明晶体的微观结构具有______.
3.晶体内部各微粒之间存在着很强的__________,微粒被约束在一定的____位置上.
4.热运动时,组成晶体的物质微粒只能在各自的________附近做微小振动.
劳厄
阵列
有序
周期性
相互作用力
平衡
平衡位置
二、晶体的结合类型
按晶体微粒之间结合方式不同,可以将晶体分为________、________和________.离子晶体是由正、负离子通过______结合而成的晶体;原子晶体是相邻原子间通过______结合而成的晶体;金属晶体是微粒通过______结合而成的晶体.
离子晶体
原子晶体
金属晶体
离子键
共价键
金属键
三、固体特征的微观解释
1.晶体内部物质微粒的排列有一定规律,在宏观上具有规则的几何外形,而非晶体内部物质微粒的排列没有一定规律,在宏观上没有规则的几何外形.
2.在固体界面沿不同方向画出等长直线
(1)单晶体在不同直线上微粒的个数______,说明沿不同方向__________及________情况不同,在物理性质上表现为________.
不相等
微粒的排列
物质结构
各向异性
(2)非晶体在不同直线上微粒的个数________,说明沿不同方向________及________情况基本相同,在物理性质上表现为________.
3.同一种物质在不同条件下形成不同的晶体,由于________不同,物理性质有很大差异.
大致相等
微粒排列
物质结构
各向同性
微观结构
核心要点突破
一、晶体的微观结构及其特点
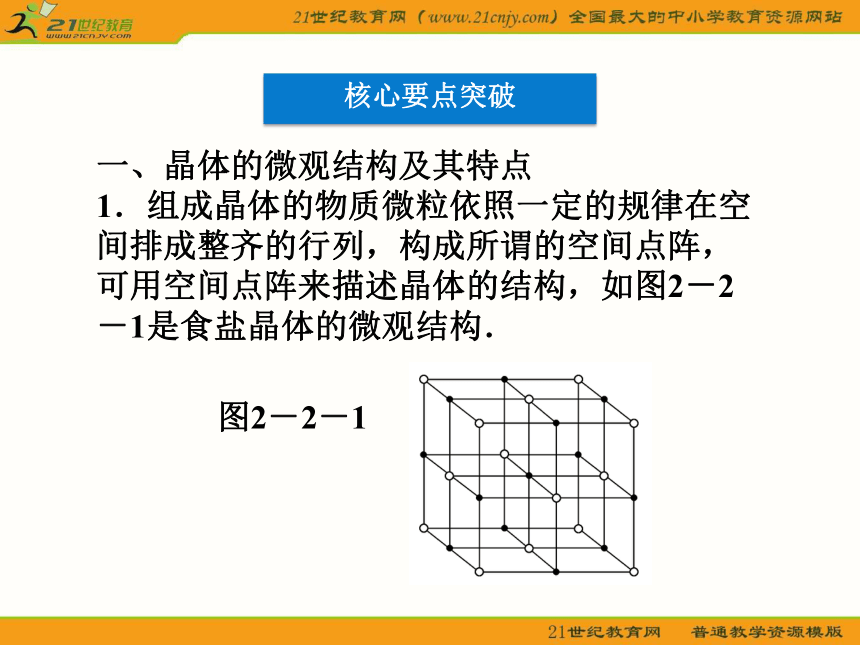
1.组成晶体的物质微粒依照一定的规律在空间排成整齐的行列,构成所谓的空间点阵,可用空间点阵来描述晶体的结构,如图2-2-1是食盐晶体的微观结构.
图2-2-1
2.单晶体的微观结构具有这样的特点
(1)组成单晶体的物质微粒(分子、原子或离子)依照一定的规律在空间中整齐地排列.
(2)单晶体中物质微粒的相互作用很强,微粒的热运动不足以克服它们间的相互作用而远离.
(3)微粒的热运动表现为在一定的平衡位置附近不停地做微小的振动.正是由于原子(或分子、离子)这种规则排列的空间周期性,所以有了单晶体的这种独特性质.
二、三类晶体结构与性质的比较
晶体类型 离子晶体 金属晶体 原子晶体
构成粒子 正、负离子 物质微粒 原子
粒子间作用 离子键 金属键 共价键
熔、沸点 较高 较高 很高
硬度 较大 较大 很大
导电性 熔化或溶于水时导电 导电 一般不导电
晶体类型 离子晶体 金属晶体 原子晶体
溶解性 多数溶于极性溶剂 不溶 不溶
实例 多数盐、强碱、多数金属氧化物 金属单质 金刚石、二氧化硅、晶体硅、碳化硅
三、固体特征的微观解释
1.对各向异性的微观解释
图2-2-2
如图2-2-2所示,这是在一个平面上晶体物质微粒的排列情况.从图上可以看出,在沿不同方向所画的等长直线AB、AC、AD上物质微粒的数目不同.直线AB上物质微粒较多,直线AD上较少,直线AC上更少.正因为在不同方向上物质微粒的排列情况不同,才引起晶体在不同方向上物理性质的不同.
2.对熔点的解释
给晶体加热到一定温度时,一部分微粒有足够的动能,克服微粒间的作用力,离开平衡位置,使规则的排列被破坏,晶体开始熔解,熔解时晶体吸收的热量全部用来破坏规则的排列,温度不发生变化.
3.对物质有几种晶体的解释
这是由于它们的物质微粒能够形成不同的晶体结构,例如碳原子按不同的结构排列可形成石墨和金刚石,二者在物理性质上有很大不同.白磷和红磷的化学成分相同,但白磷具有立方体结构,而红磷具有与石墨一样的层状结构.
4.多晶体的微观结构及性质
多晶体是由许多杂乱无章地排列着的小晶体(晶粒)组成的.平常见到的各种金属材料都是多晶体.把纯铁做成的样品放在显微镜下观察,可以看到它是由许许多多晶粒组成的.晶粒有大有小,最小的只有10-5 cm,最大的也不超过10-3 cm.每个晶粒都是一个小单晶体,具有各向异性的物理性质和规则的几何形状.因为晶粒在多晶体里杂乱无章地排列着,所以多晶体没有规则的几何形状,
也不显示各向异性.它在不同方向的物理性质是相同的,即各向同性.多晶体和非晶体的主要区别是多晶体有确定的熔点,而非晶体则没有.
课堂互动讲练
晶体结合类型的认识
下列关于晶体的结合类型说法正确的是( )
例1
A.不同晶体内部,物质微粒之间结合方式不相同
B.由正、负离子通过离子键结合而成的晶体叫做原子晶体
C.相邻原子之间通过共价键结合而成的晶体叫做离子晶体
D.物质微粒通过金属键结合而成的晶体叫做金属晶体
【精讲精析】 不同晶体内部,物质微粒之间结合方式不相同,选项A正确,由正、负离子通过离子键结合而成的晶体叫做离子晶体,选项B错误,相邻原子之间通过共价键结合而成的晶体叫做原子晶体,选项C错误,物质微粒通过金属键结合而成的晶体叫做金属晶体,选项D正确.
【答案】 AD
变式训练1 下列晶体中属于离子晶体的有________;属于原子晶体的有________;属于金属晶体的有________.
A.金刚石 B.氯化钠
C.锗 D.锡
E.银 F.镍
G.金
解析:根据晶体的结合类型可知氯化钠是离子晶体;锗、锡和金刚石是原子晶体;银、镍和金是金属晶体.
答案:B ACD EFG
下列关于晶体空间点阵的说法,正确的是( )
对固体微观结构的认识和理解
例2
A.构成晶体空间点阵的物质微粒,可以是分子,也可以是原子或离子
B.晶体的物质微粒之所以能构成空间点阵,是由于晶体中物质微粒之间相互作用很强,所以物质微粒都被牢牢地束缚在空间点阵的结点上不动
C.所谓空间点阵与空间点阵的结点,都是抽象的概念.结点是指组成晶体的物质微粒做永不停息的微小振动的平衡位置,物质微粒在结点附近的微小振动,就是热运动
D.相同的物质微粒,可以构成不同的空间点阵,也就是同一种物质能够生成不同的晶体,从而能够具有不同的物理性质
【精讲精析】 组成晶体的物质微粒可以是分子、原子或离子,这些物质微粒也就是分子动理论所说的分子.显然,组成晶体的物质微粒处在永不停息的无规则的热运动之中,物质微粒之间还存在相互作用,晶体的物质微粒之所以能构成空间点阵,是由于晶体中的物质微粒之间相互作用很强,物质微粒的热运动不足以克服这种相互作用而彼此远离,所以选项B的说法错误.
【答案】 ACD
变式训练2 关于晶体和非晶体的内部结构,正确的说法是( )
A.它们内部的物质微粒都有规则的空间分布
B.单晶体内部的物质微粒是有规则排列的,而非晶体内部物质微粒排列是不规则的
C.晶体内部的微粒是静止的,而非晶体内部的物质微粒是不停地运动着的
D.在物质内部的各个平面上,微粒数相等的是晶体,数量不等的是非晶体
解析:选B.单晶体内部微粒排列规则,而非晶体内部微粒排列不规则,晶体与非晶体内部的微粒都在不停地运动着.故A、C、D均不正确.
下列说法正确的是( )
A.晶体的各向异性是由于它的微粒按空间点阵排列
B.单晶体具有规则的几何外形是由于它的微粒按一定规律排列
C.非晶体有规则的几何形状和确定的熔点
D.石墨的硬度与金刚石差得太多,是由于它的微粒没有按空间点阵分布
固体特征的微观解释
例3
【思路点拨】 根据微粒的空间点阵结构分析.
【自主解答】 晶体内部微粒排列整齐,在不同方向上微粒数不同引起各向异性.也正是由于它的微粒按一定规律排列,使晶体具有规则的几何形状.石墨与金刚石的硬度相差甚远是由于它们内部微粒的排列结构不同,石墨的层状结构决定了它的质地柔软,而金刚石的网状结构决定了其中碳原子间的作用力很强,所以金刚石有很大的硬度.
【答案】 AB
【方法总结】 单晶体在沿不同的方向上,物质微粒的数目不同,即在不同方向上物质微粒的排列情况不同,从而引起单晶体在不同方向上的物理性质不同.有些物质在不同条件下生成不同的晶体,那是因为组成它们的微粒能够按照不同的规则在空间分布.例如:金刚石和石墨都是由碳元素构成的,它们有不同的点阵结构.
变式训练3 单晶体不同于非晶体,它具有规则的几何外形,在不同方向上物理性质不同,而且具有一定的熔点,下列哪些说法可以用来解释晶体的上述特性( )
A.组成晶体的物质微粒,在空间按一定的规律排成整齐的行列,构成特定的空间点阵
B.晶体在不同方向上物理性质不同,是由于不同方向上微粒数目不同,微粒间距离也不相同
C.晶体在不同方向上物理性质不同,是由于不同方向上的物质微粒的性质不同
D.晶体在熔化时吸收热量,全部用来瓦解晶体的空间点阵,转化为分子势能,因此,晶体在熔化过程中保持一定的温度不变.只有空间点阵完全被瓦解,晶体完全变为液体后,继续加热,温度才会升高
解析:选ABD.晶体微粒构成的空间点阵是晶体有规则几何外形的原因,晶体在物理性质上的各向异性是由于空间点阵中不同方向的微粒数目不同,微粒间距离也不相同.晶体熔点的存在是由于晶体在熔化时要吸收热量用来瓦解空间点阵,增加分子势能,熔化过程中分子的热运动的平均动能不变,即温度不变,只有当晶体全部转变为液体后温度才会继续升高,分子热运动的平均动能才会增加.
知能优化训练
本部分内容讲解结束
点此进入课件目录
按ESC键退出全屏播放
谢谢使用
第2节 固体的微观结构
课前自主学案
核心要点突破
课标定位
课堂互动讲练
第2节
知能优化训练
课标定位
学习目标:1.了解对晶体结构的认识过程,知道晶体内部结构的特点.
2.理解晶体与非晶体存在差异的原因是其微观结构不同,并能够解释它们物理性质存在差异的原因.
3.了解金刚石与石墨存在差异的原因,并能够从其结构模型上进行分析.
重点难点:1.晶体的微观结构和晶体的结构类型.
2.固体特征的微观解释.
课前自主学案
一、晶体的结构
1.1912年,德国物理学家____,证实了晶体内部的物质微粒按一定规律整齐地排列.
2.组成晶体的物质微粒有规则地在空间排成____,呈现周而复始的____结构,说明晶体的微观结构具有______.
3.晶体内部各微粒之间存在着很强的__________,微粒被约束在一定的____位置上.
4.热运动时,组成晶体的物质微粒只能在各自的________附近做微小振动.
劳厄
阵列
有序
周期性
相互作用力
平衡
平衡位置
二、晶体的结合类型
按晶体微粒之间结合方式不同,可以将晶体分为________、________和________.离子晶体是由正、负离子通过______结合而成的晶体;原子晶体是相邻原子间通过______结合而成的晶体;金属晶体是微粒通过______结合而成的晶体.
离子晶体
原子晶体
金属晶体
离子键
共价键
金属键
三、固体特征的微观解释
1.晶体内部物质微粒的排列有一定规律,在宏观上具有规则的几何外形,而非晶体内部物质微粒的排列没有一定规律,在宏观上没有规则的几何外形.
2.在固体界面沿不同方向画出等长直线
(1)单晶体在不同直线上微粒的个数______,说明沿不同方向__________及________情况不同,在物理性质上表现为________.
不相等
微粒的排列
物质结构
各向异性
(2)非晶体在不同直线上微粒的个数________,说明沿不同方向________及________情况基本相同,在物理性质上表现为________.
3.同一种物质在不同条件下形成不同的晶体,由于________不同,物理性质有很大差异.
大致相等
微粒排列
物质结构
各向同性
微观结构
核心要点突破
一、晶体的微观结构及其特点
1.组成晶体的物质微粒依照一定的规律在空间排成整齐的行列,构成所谓的空间点阵,可用空间点阵来描述晶体的结构,如图2-2-1是食盐晶体的微观结构.
图2-2-1
2.单晶体的微观结构具有这样的特点
(1)组成单晶体的物质微粒(分子、原子或离子)依照一定的规律在空间中整齐地排列.
(2)单晶体中物质微粒的相互作用很强,微粒的热运动不足以克服它们间的相互作用而远离.
(3)微粒的热运动表现为在一定的平衡位置附近不停地做微小的振动.正是由于原子(或分子、离子)这种规则排列的空间周期性,所以有了单晶体的这种独特性质.
二、三类晶体结构与性质的比较
晶体类型 离子晶体 金属晶体 原子晶体
构成粒子 正、负离子 物质微粒 原子
粒子间作用 离子键 金属键 共价键
熔、沸点 较高 较高 很高
硬度 较大 较大 很大
导电性 熔化或溶于水时导电 导电 一般不导电
晶体类型 离子晶体 金属晶体 原子晶体
溶解性 多数溶于极性溶剂 不溶 不溶
实例 多数盐、强碱、多数金属氧化物 金属单质 金刚石、二氧化硅、晶体硅、碳化硅
三、固体特征的微观解释
1.对各向异性的微观解释
图2-2-2
如图2-2-2所示,这是在一个平面上晶体物质微粒的排列情况.从图上可以看出,在沿不同方向所画的等长直线AB、AC、AD上物质微粒的数目不同.直线AB上物质微粒较多,直线AD上较少,直线AC上更少.正因为在不同方向上物质微粒的排列情况不同,才引起晶体在不同方向上物理性质的不同.
2.对熔点的解释
给晶体加热到一定温度时,一部分微粒有足够的动能,克服微粒间的作用力,离开平衡位置,使规则的排列被破坏,晶体开始熔解,熔解时晶体吸收的热量全部用来破坏规则的排列,温度不发生变化.
3.对物质有几种晶体的解释
这是由于它们的物质微粒能够形成不同的晶体结构,例如碳原子按不同的结构排列可形成石墨和金刚石,二者在物理性质上有很大不同.白磷和红磷的化学成分相同,但白磷具有立方体结构,而红磷具有与石墨一样的层状结构.
4.多晶体的微观结构及性质
多晶体是由许多杂乱无章地排列着的小晶体(晶粒)组成的.平常见到的各种金属材料都是多晶体.把纯铁做成的样品放在显微镜下观察,可以看到它是由许许多多晶粒组成的.晶粒有大有小,最小的只有10-5 cm,最大的也不超过10-3 cm.每个晶粒都是一个小单晶体,具有各向异性的物理性质和规则的几何形状.因为晶粒在多晶体里杂乱无章地排列着,所以多晶体没有规则的几何形状,
也不显示各向异性.它在不同方向的物理性质是相同的,即各向同性.多晶体和非晶体的主要区别是多晶体有确定的熔点,而非晶体则没有.
课堂互动讲练
晶体结合类型的认识
下列关于晶体的结合类型说法正确的是( )
例1
A.不同晶体内部,物质微粒之间结合方式不相同
B.由正、负离子通过离子键结合而成的晶体叫做原子晶体
C.相邻原子之间通过共价键结合而成的晶体叫做离子晶体
D.物质微粒通过金属键结合而成的晶体叫做金属晶体
【精讲精析】 不同晶体内部,物质微粒之间结合方式不相同,选项A正确,由正、负离子通过离子键结合而成的晶体叫做离子晶体,选项B错误,相邻原子之间通过共价键结合而成的晶体叫做原子晶体,选项C错误,物质微粒通过金属键结合而成的晶体叫做金属晶体,选项D正确.
【答案】 AD
变式训练1 下列晶体中属于离子晶体的有________;属于原子晶体的有________;属于金属晶体的有________.
A.金刚石 B.氯化钠
C.锗 D.锡
E.银 F.镍
G.金
解析:根据晶体的结合类型可知氯化钠是离子晶体;锗、锡和金刚石是原子晶体;银、镍和金是金属晶体.
答案:B ACD EFG
下列关于晶体空间点阵的说法,正确的是( )
对固体微观结构的认识和理解
例2
A.构成晶体空间点阵的物质微粒,可以是分子,也可以是原子或离子
B.晶体的物质微粒之所以能构成空间点阵,是由于晶体中物质微粒之间相互作用很强,所以物质微粒都被牢牢地束缚在空间点阵的结点上不动
C.所谓空间点阵与空间点阵的结点,都是抽象的概念.结点是指组成晶体的物质微粒做永不停息的微小振动的平衡位置,物质微粒在结点附近的微小振动,就是热运动
D.相同的物质微粒,可以构成不同的空间点阵,也就是同一种物质能够生成不同的晶体,从而能够具有不同的物理性质
【精讲精析】 组成晶体的物质微粒可以是分子、原子或离子,这些物质微粒也就是分子动理论所说的分子.显然,组成晶体的物质微粒处在永不停息的无规则的热运动之中,物质微粒之间还存在相互作用,晶体的物质微粒之所以能构成空间点阵,是由于晶体中的物质微粒之间相互作用很强,物质微粒的热运动不足以克服这种相互作用而彼此远离,所以选项B的说法错误.
【答案】 ACD
变式训练2 关于晶体和非晶体的内部结构,正确的说法是( )
A.它们内部的物质微粒都有规则的空间分布
B.单晶体内部的物质微粒是有规则排列的,而非晶体内部物质微粒排列是不规则的
C.晶体内部的微粒是静止的,而非晶体内部的物质微粒是不停地运动着的
D.在物质内部的各个平面上,微粒数相等的是晶体,数量不等的是非晶体
解析:选B.单晶体内部微粒排列规则,而非晶体内部微粒排列不规则,晶体与非晶体内部的微粒都在不停地运动着.故A、C、D均不正确.
下列说法正确的是( )
A.晶体的各向异性是由于它的微粒按空间点阵排列
B.单晶体具有规则的几何外形是由于它的微粒按一定规律排列
C.非晶体有规则的几何形状和确定的熔点
D.石墨的硬度与金刚石差得太多,是由于它的微粒没有按空间点阵分布
固体特征的微观解释
例3
【思路点拨】 根据微粒的空间点阵结构分析.
【自主解答】 晶体内部微粒排列整齐,在不同方向上微粒数不同引起各向异性.也正是由于它的微粒按一定规律排列,使晶体具有规则的几何形状.石墨与金刚石的硬度相差甚远是由于它们内部微粒的排列结构不同,石墨的层状结构决定了它的质地柔软,而金刚石的网状结构决定了其中碳原子间的作用力很强,所以金刚石有很大的硬度.
【答案】 AB
【方法总结】 单晶体在沿不同的方向上,物质微粒的数目不同,即在不同方向上物质微粒的排列情况不同,从而引起单晶体在不同方向上的物理性质不同.有些物质在不同条件下生成不同的晶体,那是因为组成它们的微粒能够按照不同的规则在空间分布.例如:金刚石和石墨都是由碳元素构成的,它们有不同的点阵结构.
变式训练3 单晶体不同于非晶体,它具有规则的几何外形,在不同方向上物理性质不同,而且具有一定的熔点,下列哪些说法可以用来解释晶体的上述特性( )
A.组成晶体的物质微粒,在空间按一定的规律排成整齐的行列,构成特定的空间点阵
B.晶体在不同方向上物理性质不同,是由于不同方向上微粒数目不同,微粒间距离也不相同
C.晶体在不同方向上物理性质不同,是由于不同方向上的物质微粒的性质不同
D.晶体在熔化时吸收热量,全部用来瓦解晶体的空间点阵,转化为分子势能,因此,晶体在熔化过程中保持一定的温度不变.只有空间点阵完全被瓦解,晶体完全变为液体后,继续加热,温度才会升高
解析:选ABD.晶体微粒构成的空间点阵是晶体有规则几何外形的原因,晶体在物理性质上的各向异性是由于空间点阵中不同方向的微粒数目不同,微粒间距离也不相同.晶体熔点的存在是由于晶体在熔化时要吸收热量用来瓦解空间点阵,增加分子势能,熔化过程中分子的热运动的平均动能不变,即温度不变,只有当晶体全部转变为液体后温度才会继续升高,分子热运动的平均动能才会增加.
知能优化训练
本部分内容讲解结束
点此进入课件目录
按ESC键退出全屏播放
谢谢使用
同课章节目录
- 第1章 分子动理论
- 导 入 走进微观世界
- 第1节 分子动理论的基本观点
- 第2节 气体分子运动与压强
- 第3节 温度与内能
- 第2章 固体
- 导 入 从古陶器到纳米技术
- 第1节 晶体和非晶体
- 第2节 固体的微观结构
- 第3节 材料科技与人类文明
- 第3章 液体
- 导 入 神奇的液体表面
- 第1节 液体的表面张力
- 第2节 毛细现象
- 第3节 液晶
- 第4章 气体
- 导 入 从天气预报谈起
- 第1节 气体实验定律
- 第2节 气体实验定律的微观解释
- 第3节 饱和汽
- 第4节 温度
- 专题探究 分子动理论及物质三态的实验与调研
- 第5章 热力学定律
- 导 入 水车和水泵
- 第1节 热力学第一定律
- 第2节 能量的转化与守恒
- 第3节 热力学第二定律
- 第4节 熵——无序程度的量度
- 第6章 热源与可持续发展
- 导 入 谢谢你,太阳
- 第1节 能源、环境与人类生存
- 第2节 能源的开发与环境保护
- 专题探究 能量与可持续发展的实验与调研
