利用化学方程式的简单计算
文档属性
| 名称 | 利用化学方程式的简单计算 |

|
|
| 格式 | rar | ||
| 文件大小 | 800.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2011-12-20 00:00:00 | ||
图片预览









文档简介
(共40张PPT)
2010年10月1日,搭载我国探月卫星嫦娥二号的长征三号丙运载火箭在西昌卫星发射中心三号塔架点火发射成功。
在发射过程中,第三级起推动作用时会发生什么反应?请写出化学方程式。
2H2+O2 2H2O +Q
发射嫦娥一号使用的火箭——长征三号甲第三级所用的推进剂是液氧、液氢。
化学方程式:
2H2 + O2 2H2O
点燃
物质的质量比:
2×2
32
2×18
4
32
36
:
:
上述化学方程式表示:
(1)质的含义:______________________________
(2)微观的含义:____________________________
(3)量的含义:______________________________
氢气在氧气中燃烧生成水
每两个氢分子与一个氧分子反应生成两个水分子
每4份质量的氢气与32份质量的氧气完全反应生成36份质量的水
根据氢气在氧气中燃烧的化学方程式,标出各物质的质量比:
2H2 + O2 2 H2O
2×1×2 :16×2 : 2 ×(2+16)
4 : 32 : 36
若: 4克 :( )克 : ( ) 克
若:( )克 : ( )克 : 18 克
32
36
16
2
若: ( )克 : 8 克 : ( )克
1
9
在化学反应中,反应物与生成物之间的质量比 。因此,利用此正比例关系,根据化学方程式由一种反应物(或生成物)的质量,可求另一种生成物(或反应物)的质量。
成正比关系
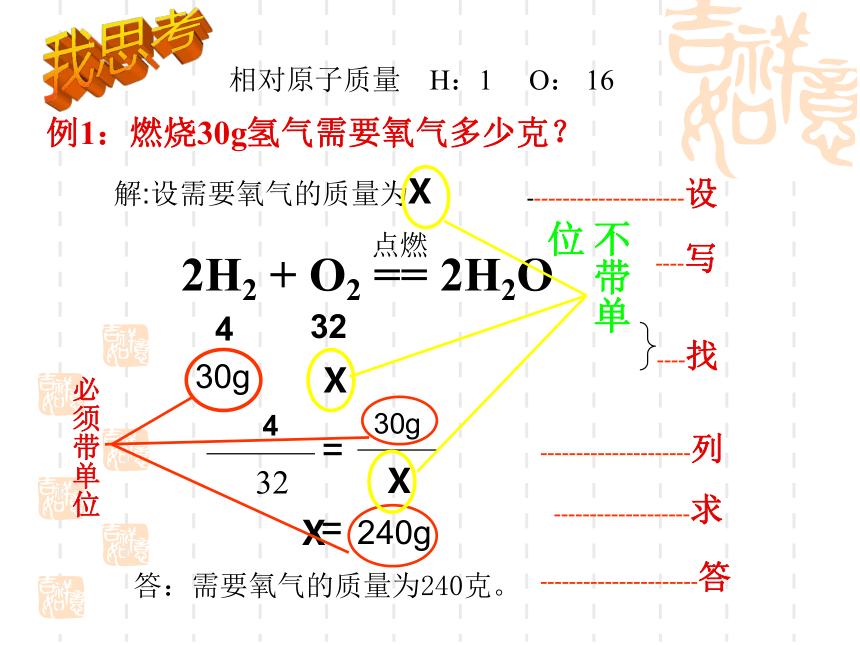
例1:燃烧30g氢气需要氧气多少克?
解:设需要氧气的质量为X
4
32
30g
X
X
30g
=
4
答:需要氧气的质量为240克。
----------------------设
----写
----找
---------------------列
-------------------求
----------------------答
必须带单位
2H2 + O2 == 2H2O
点燃
32
X
=
240g
不带单位
相对原子质量 H:1 O: 16
根据化学方程式计算的正确解题步骤
[解](1)设:设未知数(未知数不带单位)
(2)写:正确写出化学方程式
(3)找:找出已知量和待求量,算出质量比,把它们写在对应的位置上。
(4)列:列出比例式
(6)答:简明地写出答案
(5)求:求解
例2: 碳酸钙和盐酸反应生成二氧化碳:
CaCO3 + 2HCl CaCl2 + H2O + CO2
若需制备二氧化碳8.8g,至少需要碳酸钙多少克
解:设需要碳酸钙的质量为x
CaCO3 + 2HCl CaCl2 + H2O + CO2
44
100
8.8g
X
100
44
8.8g
X
=
X= 20g
答:至少需要碳酸钙20g
你会了吗
(1)将6g碳完全燃烧,则能生成多少克二氧化碳
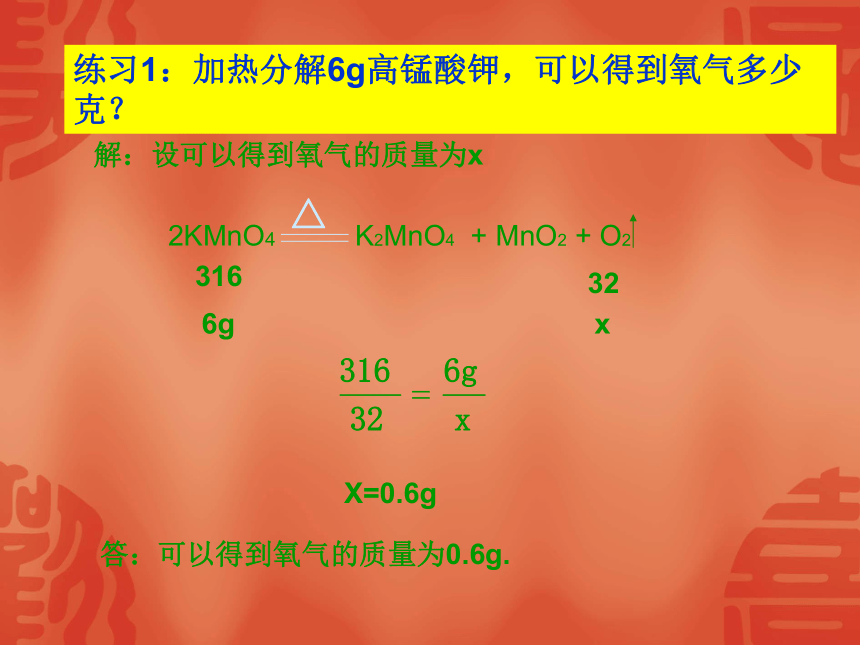
练习1:加热分解6g高锰酸钾,可以得到氧气多少克?
解:设可以得到氧气的质量为x
2KMnO4 K2MnO4 + MnO2 + O2
△
316
32
6g
x
X=0.6g
答:可以得到氧气的质量为0.6g.
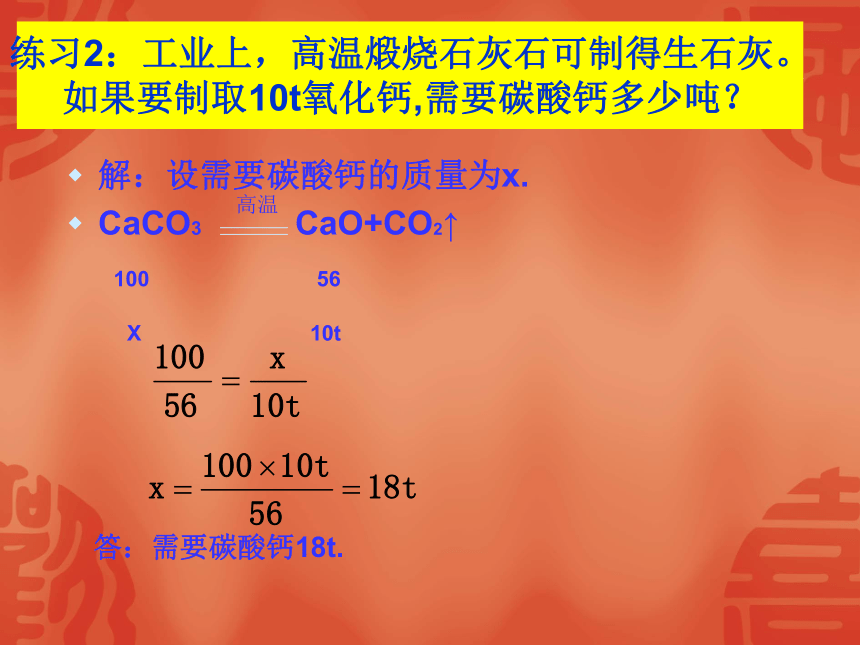
练习2:工业上,高温煅烧石灰石可制得生石灰。如果要制取10t氧化钙,需要碳酸钙多少吨?
解:设需要碳酸钙的质量为x.
CaCO3 CaO+CO2↑
高温
100
56
X
10t
答:需要碳酸钙18t.
想一想,做一做:
(1)某工厂需要100kg氧气做原料,若用电解水的方法来制取这些氧气,需消耗水的质量为多少
(2)在二氧化锰的催化下分解3.4g双氧水,最多可得到多少克氧气
解:设完全分解需要x Kg的高锰酸钾
KMnO4 ══ K2MnO4 + MnO2 + O2
158 32
x Kg 4.8
158 X
32 4.8
X=79Kg
答:需要79Kg的高锰酸钾。
47.4Kg
2008年北京奥运会,奥运圣火登上了世界最高点——珠穆朗玛峰。在登山过程中,人均需携带至少4.8Kg的氧气。若实验室用高锰酸钾为原料,制取相同质量的氧气,需多少千克的高锰酸钾?
2
↑
需要高锰酸钾的质量为X
X
316
Kg
=
需要高锰酸钾的质量为 47.4Kg
316
32
=
X
4.8Kg
△
练习1:(“中考题”)加热完全分解12.25克氯酸钾和3克二氧化锰的混合物,可以得到多少克氧气?(10分)
(相对原子质量 K:39 Cl: 35.5 O:16)
1分
2分
2分
2分
2分
1分
没带单位扣1分
设未知数不带单位
(列比例必须对应)
三个要领: 步骤要完整
格式要规范
得数要准确
三个关键:
准确书写化学式
化学方程式要配平
准确计算相对分子质量
化学方程式计算的注意事项:
把氯酸钾和二氧化锰的混合物15.5克加热至完全反应,冷 却后得剩余固体10.7克.试求:
(1)放出氧气多少克
(2)剩余固体是什么 各多少克
(3)参加反应的氯酸钾多少克
请你思考
本节课你学到了什么
第二课时
练习:
在实验室中用氢气还原氧化铜制取铜,若制取6.4克铜,需要氧化铜多少克?同时最少需用氢气多少克?
△
△
解:设需要氧化铜的质量为X,至少需要氢气为Y。
CuO+H2==Cu+H2O
80 2 64
X Y 6.4g
△
答:需要氧化铜的质量为8g,需要氢气的质量为0.2g。
例1:把氯酸钾和二氧化锰的混合物16克加热至不再有气体放出,冷却后称得剩余固体质量为11.2克。求反应所生成的气体的质量?混合物中二氧化锰的质量?
解:⑴氧气的质量为:16g-11.2g=4.8g
⑵设氯酸钾的质量为x
245 96
x 4.8g
x=12.25g
二氧化锰的质量为:16g-12.25g=3.75g
答:生成氧气的质量为4.8g,二氧化锰的质量为3.75g
例2:工业上常用石灰石制取生石灰,同时得到副产品二氧化碳气体,化学方程式如下:
CaCO3===CaO + CO2↑
现用100吨含杂质20%的石灰石,理论上可以得到含杂质12%的生石灰多少吨?
高温
例3:3g碳放在给定的氧气中充分燃烧.
第一次 第二次 第三次
O2的质量 6 13 8
生成CO2的质量 8.25 11 11
1、第____次恰好完全反应.
2、第_____次实验中O2有剩余,剩余____g.
3
2
5
例4:A+3B==2C+2D中,A与B的相对分子质量之比为9:11,已知1.8gA与一定量的B恰好完全反应生成5.1gD,则此反应中B和C的质量比为_______
2:1
例5:有一含杂质的的锌8 克与足量的稀硫酸反应共产生0.2克氢气,计算锌的纯度?
提示:
解:设参加反应的锌的质量为x
65
x
2
0.2g
答:锌的纯度为81%。
工业上电解氧化铝制取金属铝的化学方程式是:2Al2O3 4Al + 3O2 ↑,在解答“电解10t氧化铝最多可生产多少吨铝”的问题时,甲、乙两同学分别采用了两种不同的计算方法。
通电
解一: 设铝的质量为X
2Al2O3 4Al + 3O2
通电
204
108
10t
x
108
204
x
10t
=
x=5.3t
答:最多可生产5.3t铝
观察与思考:
解二:已知电解过程中,氧化铝中的铝元素全部转化为单质铝.氧化铝中铝元素的质量分数为:
2 ×27
2×27+3×16
× 100%
=
53.0%
10t氧化铝中含铝的质量:
10t × 53.0% = 5.3t
答:最多可生产5.3t铝
(两种计算方法依据的原理有什么不同?)
2010年10月1日,搭载我国探月卫星嫦娥二号的长征三号丙运载火箭在西昌卫星发射中心三号塔架点火发射成功。
在发射过程中,第三级起推动作用时会发生什么反应?请写出化学方程式。
2H2+O2 2H2O +Q
发射嫦娥一号使用的火箭——长征三号甲第三级所用的推进剂是液氧、液氢。
化学方程式:
2H2 + O2 2H2O
点燃
物质的质量比:
2×2
32
2×18
4
32
36
:
:
上述化学方程式表示:
(1)质的含义:______________________________
(2)微观的含义:____________________________
(3)量的含义:______________________________
氢气在氧气中燃烧生成水
每两个氢分子与一个氧分子反应生成两个水分子
每4份质量的氢气与32份质量的氧气完全反应生成36份质量的水
根据氢气在氧气中燃烧的化学方程式,标出各物质的质量比:
2H2 + O2 2 H2O
2×1×2 :16×2 : 2 ×(2+16)
4 : 32 : 36
若: 4克 :( )克 : ( ) 克
若:( )克 : ( )克 : 18 克
32
36
16
2
若: ( )克 : 8 克 : ( )克
1
9
在化学反应中,反应物与生成物之间的质量比 。因此,利用此正比例关系,根据化学方程式由一种反应物(或生成物)的质量,可求另一种生成物(或反应物)的质量。
成正比关系
例1:燃烧30g氢气需要氧气多少克?
解:设需要氧气的质量为X
4
32
30g
X
X
30g
=
4
答:需要氧气的质量为240克。
----------------------设
----写
----找
---------------------列
-------------------求
----------------------答
必须带单位
2H2 + O2 == 2H2O
点燃
32
X
=
240g
不带单位
相对原子质量 H:1 O: 16
根据化学方程式计算的正确解题步骤
[解](1)设:设未知数(未知数不带单位)
(2)写:正确写出化学方程式
(3)找:找出已知量和待求量,算出质量比,把它们写在对应的位置上。
(4)列:列出比例式
(6)答:简明地写出答案
(5)求:求解
例2: 碳酸钙和盐酸反应生成二氧化碳:
CaCO3 + 2HCl CaCl2 + H2O + CO2
若需制备二氧化碳8.8g,至少需要碳酸钙多少克
解:设需要碳酸钙的质量为x
CaCO3 + 2HCl CaCl2 + H2O + CO2
44
100
8.8g
X
100
44
8.8g
X
=
X= 20g
答:至少需要碳酸钙20g
你会了吗
(1)将6g碳完全燃烧,则能生成多少克二氧化碳
练习1:加热分解6g高锰酸钾,可以得到氧气多少克?
解:设可以得到氧气的质量为x
2KMnO4 K2MnO4 + MnO2 + O2
△
316
32
6g
x
X=0.6g
答:可以得到氧气的质量为0.6g.
练习2:工业上,高温煅烧石灰石可制得生石灰。如果要制取10t氧化钙,需要碳酸钙多少吨?
解:设需要碳酸钙的质量为x.
CaCO3 CaO+CO2↑
高温
100
56
X
10t
答:需要碳酸钙18t.
想一想,做一做:
(1)某工厂需要100kg氧气做原料,若用电解水的方法来制取这些氧气,需消耗水的质量为多少
(2)在二氧化锰的催化下分解3.4g双氧水,最多可得到多少克氧气
解:设完全分解需要x Kg的高锰酸钾
KMnO4 ══ K2MnO4 + MnO2 + O2
158 32
x Kg 4.8
158 X
32 4.8
X=79Kg
答:需要79Kg的高锰酸钾。
47.4Kg
2008年北京奥运会,奥运圣火登上了世界最高点——珠穆朗玛峰。在登山过程中,人均需携带至少4.8Kg的氧气。若实验室用高锰酸钾为原料,制取相同质量的氧气,需多少千克的高锰酸钾?
2
↑
需要高锰酸钾的质量为X
X
316
Kg
=
需要高锰酸钾的质量为 47.4Kg
316
32
=
X
4.8Kg
△
练习1:(“中考题”)加热完全分解12.25克氯酸钾和3克二氧化锰的混合物,可以得到多少克氧气?(10分)
(相对原子质量 K:39 Cl: 35.5 O:16)
1分
2分
2分
2分
2分
1分
没带单位扣1分
设未知数不带单位
(列比例必须对应)
三个要领: 步骤要完整
格式要规范
得数要准确
三个关键:
准确书写化学式
化学方程式要配平
准确计算相对分子质量
化学方程式计算的注意事项:
把氯酸钾和二氧化锰的混合物15.5克加热至完全反应,冷 却后得剩余固体10.7克.试求:
(1)放出氧气多少克
(2)剩余固体是什么 各多少克
(3)参加反应的氯酸钾多少克
请你思考
本节课你学到了什么
第二课时
练习:
在实验室中用氢气还原氧化铜制取铜,若制取6.4克铜,需要氧化铜多少克?同时最少需用氢气多少克?
△
△
解:设需要氧化铜的质量为X,至少需要氢气为Y。
CuO+H2==Cu+H2O
80 2 64
X Y 6.4g
△
答:需要氧化铜的质量为8g,需要氢气的质量为0.2g。
例1:把氯酸钾和二氧化锰的混合物16克加热至不再有气体放出,冷却后称得剩余固体质量为11.2克。求反应所生成的气体的质量?混合物中二氧化锰的质量?
解:⑴氧气的质量为:16g-11.2g=4.8g
⑵设氯酸钾的质量为x
245 96
x 4.8g
x=12.25g
二氧化锰的质量为:16g-12.25g=3.75g
答:生成氧气的质量为4.8g,二氧化锰的质量为3.75g
例2:工业上常用石灰石制取生石灰,同时得到副产品二氧化碳气体,化学方程式如下:
CaCO3===CaO + CO2↑
现用100吨含杂质20%的石灰石,理论上可以得到含杂质12%的生石灰多少吨?
高温
例3:3g碳放在给定的氧气中充分燃烧.
第一次 第二次 第三次
O2的质量 6 13 8
生成CO2的质量 8.25 11 11
1、第____次恰好完全反应.
2、第_____次实验中O2有剩余,剩余____g.
3
2
5
例4:A+3B==2C+2D中,A与B的相对分子质量之比为9:11,已知1.8gA与一定量的B恰好完全反应生成5.1gD,则此反应中B和C的质量比为_______
2:1
例5:有一含杂质的的锌8 克与足量的稀硫酸反应共产生0.2克氢气,计算锌的纯度?
提示:
解:设参加反应的锌的质量为x
65
x
2
0.2g
答:锌的纯度为81%。
工业上电解氧化铝制取金属铝的化学方程式是:2Al2O3 4Al + 3O2 ↑,在解答“电解10t氧化铝最多可生产多少吨铝”的问题时,甲、乙两同学分别采用了两种不同的计算方法。
通电
解一: 设铝的质量为X
2Al2O3 4Al + 3O2
通电
204
108
10t
x
108
204
x
10t
=
x=5.3t
答:最多可生产5.3t铝
观察与思考:
解二:已知电解过程中,氧化铝中的铝元素全部转化为单质铝.氧化铝中铝元素的质量分数为:
2 ×27
2×27+3×16
× 100%
=
53.0%
10t氧化铝中含铝的质量:
10t × 53.0% = 5.3t
答:最多可生产5.3t铝
(两种计算方法依据的原理有什么不同?)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
