铁的冶炼
图片预览




文档简介
(共20张PPT)
铁的冶炼
青州市普通初级中学 鲁宁宁
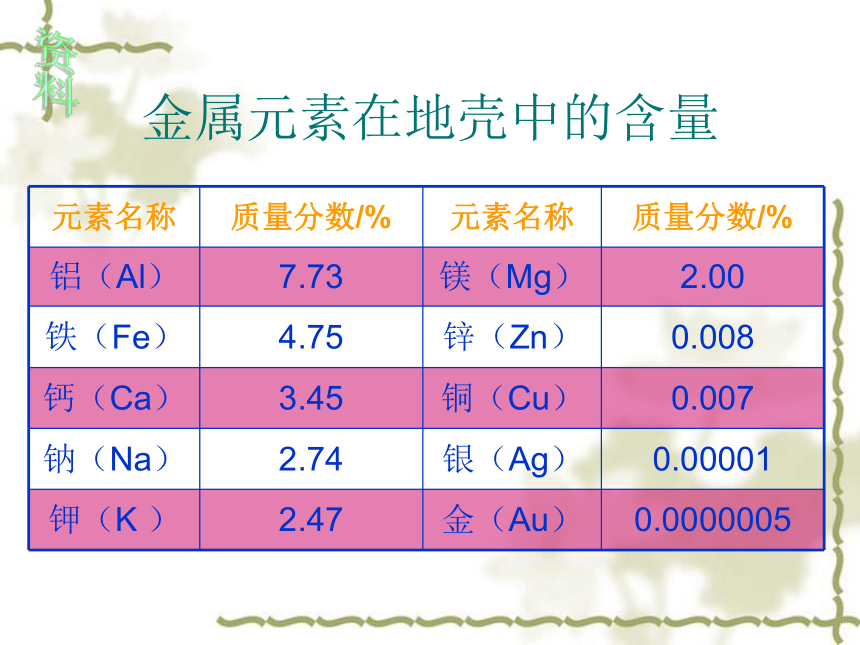
金属元素在地壳中的含量
元素名称 质量分数/% 元素名称 质量分数/%
铝(Al) 7.73 镁(Mg) 2.00
铁(Fe) 4.75 锌(Zn) 0.008
钙(Ca) 3.45 铜(Cu) 0.007
钠(Na) 2.74 银(Ag) 0.00001
钾(K ) 2.47 金(Au) 0.0000005
金属元素在自然界中的存在形式(1)
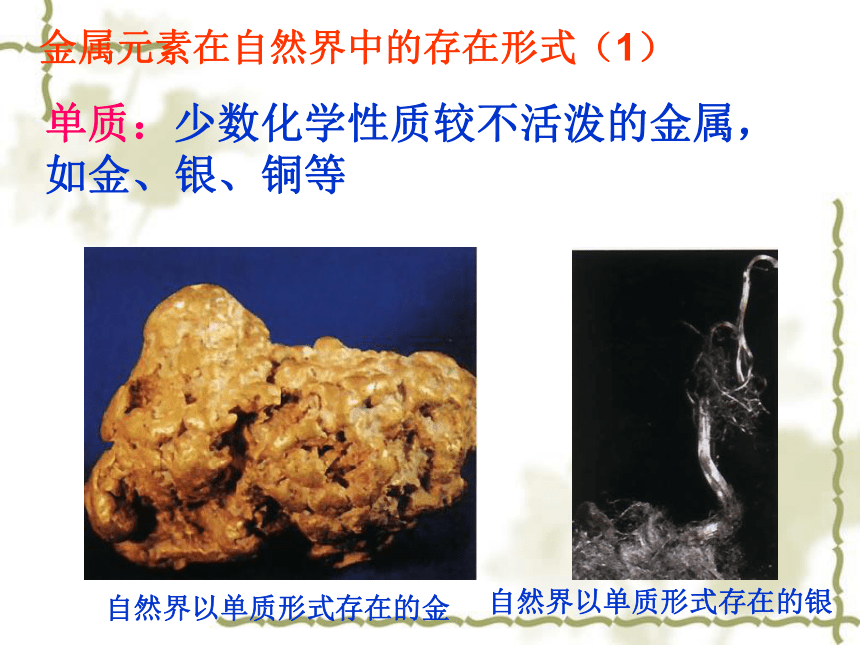
单质:少数化学性质较不活泼的金属,如金、银、铜等
自然界以单质形式存在的金
自然界以单质形式存在的银
金属元素在自然界中的存在形式(2)
化合物:化学性质较活泼的金属,如铁、锌、钠和钙等
孔雀石(Cu2(OH)2CO3 )
闪锌矿
孔雀石
赤铁矿
黄铁矿FeS2
菱铁矿FeCO3
Fe2O3
矿石:工业上把能用来提炼金属的矿物。
磁铁矿 Fe3O4
铁矿石
孔雀石 Cu2(OH)2CO3
赤铜矿 Cu2O
黄铜矿 CuFeS2
辉铜矿 Cu2S
铜
矿
石
钢铁的用途
CO
澄清石灰水
气囊
Fe2O3
讨论
CO
变浑浊
磁铁
澄清石灰水
讨论
1、此实验中观察到的现象是什么?化学反应方程式是?
3、这个实验应该注意哪些问题?
2、CO的化学性质与前面学的哪种气体类似?
讨论
3CO+ Fe2O3 3CO2 + 2 Fe
高温
实验
现象:红色的氧化铁粉末逐渐变成黑色 粉末,
生成的气体能使澄清的石灰水变浑浊
H2的化学性质:1、可燃性。2、还原性(使某些金属氧化物还原为单质,如H2+CuO Cu+H2O)
1、实验步骤应是:先通一会儿CO再加热,实验结束后先撤酒精灯、冷却后撤CO。
2、尾气要用气囊收集或用
酒精灯点燃。
原因
1、实验步骤应是:先通一会儿CO再加热,实验结束后先撤酒精灯,冷却后撤CO。
CO有剧毒要注意尾气处理。
注意事项及其原因
(1)CO是可燃性气体,加热前应保持管内气体纯度防止爆炸。(2)防止Fe又生成Fe2O3以至实验失败。
2、尾气要用气囊收集或用酒精灯点燃。
1、一氧化碳还原氧化铁中的还原剂是( )
2、请同学们自学课本17页小组合作完成下表
生铁的冶炼
主要设备 原料 反应原理
一氧化碳
高炉
铁矿石、焦炭、石灰石
在高温条件下,利用焦炭和氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
铁矿石
焦炭
热空气
炉渣出口
生铁出口
石灰石
有关杂质问题的计算
例 1000t含氧化铁80%的赤铁矿石,理论上可炼出含铁96%的生铁的质量是多少?
解:氧化铁的质量: 1000t× 80% =800t
设:理论上可炼出铁的质量为X
Fe2O3 + 3CO 2Fe + 3CO2
高温
160 2×56
800t X
160
X
2×56
800t
X = 560t
折合为含铁96%的生铁的质量为560t÷96%=583t
答:1000t可炼出生铁为583t。
练习:
1、某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,
该厂理论上可以日产Fe98%的生铁多少t
2、冶炼2000t含杂质3%的生铁,需要含Fe3O4的赤铁矿
石多少t
铁的冶炼
青州市普通初级中学 鲁宁宁
金属元素在地壳中的含量
元素名称 质量分数/% 元素名称 质量分数/%
铝(Al) 7.73 镁(Mg) 2.00
铁(Fe) 4.75 锌(Zn) 0.008
钙(Ca) 3.45 铜(Cu) 0.007
钠(Na) 2.74 银(Ag) 0.00001
钾(K ) 2.47 金(Au) 0.0000005
金属元素在自然界中的存在形式(1)
单质:少数化学性质较不活泼的金属,如金、银、铜等
自然界以单质形式存在的金
自然界以单质形式存在的银
金属元素在自然界中的存在形式(2)
化合物:化学性质较活泼的金属,如铁、锌、钠和钙等
孔雀石(Cu2(OH)2CO3 )
闪锌矿
孔雀石
赤铁矿
黄铁矿FeS2
菱铁矿FeCO3
Fe2O3
矿石:工业上把能用来提炼金属的矿物。
磁铁矿 Fe3O4
铁矿石
孔雀石 Cu2(OH)2CO3
赤铜矿 Cu2O
黄铜矿 CuFeS2
辉铜矿 Cu2S
铜
矿
石
钢铁的用途
CO
澄清石灰水
气囊
Fe2O3
讨论
CO
变浑浊
磁铁
澄清石灰水
讨论
1、此实验中观察到的现象是什么?化学反应方程式是?
3、这个实验应该注意哪些问题?
2、CO的化学性质与前面学的哪种气体类似?
讨论
3CO+ Fe2O3 3CO2 + 2 Fe
高温
实验
现象:红色的氧化铁粉末逐渐变成黑色 粉末,
生成的气体能使澄清的石灰水变浑浊
H2的化学性质:1、可燃性。2、还原性(使某些金属氧化物还原为单质,如H2+CuO Cu+H2O)
1、实验步骤应是:先通一会儿CO再加热,实验结束后先撤酒精灯、冷却后撤CO。
2、尾气要用气囊收集或用
酒精灯点燃。
原因
1、实验步骤应是:先通一会儿CO再加热,实验结束后先撤酒精灯,冷却后撤CO。
CO有剧毒要注意尾气处理。
注意事项及其原因
(1)CO是可燃性气体,加热前应保持管内气体纯度防止爆炸。(2)防止Fe又生成Fe2O3以至实验失败。
2、尾气要用气囊收集或用酒精灯点燃。
1、一氧化碳还原氧化铁中的还原剂是( )
2、请同学们自学课本17页小组合作完成下表
生铁的冶炼
主要设备 原料 反应原理
一氧化碳
高炉
铁矿石、焦炭、石灰石
在高温条件下,利用焦炭和氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
铁矿石
焦炭
热空气
炉渣出口
生铁出口
石灰石
有关杂质问题的计算
例 1000t含氧化铁80%的赤铁矿石,理论上可炼出含铁96%的生铁的质量是多少?
解:氧化铁的质量: 1000t× 80% =800t
设:理论上可炼出铁的质量为X
Fe2O3 + 3CO 2Fe + 3CO2
高温
160 2×56
800t X
160
X
2×56
800t
X = 560t
折合为含铁96%的生铁的质量为560t÷96%=583t
答:1000t可炼出生铁为583t。
练习:
1、某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,
该厂理论上可以日产Fe98%的生铁多少t
2、冶炼2000t含杂质3%的生铁,需要含Fe3O4的赤铁矿
石多少t
同课章节目录
