人教版高中化学必修Ⅱ3.3生活中两种常见的有机物-(共34张ppt)
文档属性
| 名称 | 人教版高中化学必修Ⅱ3.3生活中两种常见的有机物-(共34张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 837.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-21 00:00:00 | ||
图片预览








文档简介
(共34张PPT)
第三节:生活中两种常见的有机物
一、乙醇(俗称_________)
酒精
乙醇的物理性质
无色
有特殊香味的液体,
密度比水的小,
沸点78.5℃,易挥发,
能够溶解多种有机物和无机物,能与水以任意比互溶
思考:乙醇分子结构的实验测定
CH3-O-
CH3
CH3CH2OH
乙醇的分子式是C2H6O,根据分子式及各原子的价键关系写出乙醇的两种可能的结构__________________、____________________________,乙醇分子究竟是哪一种结构?怎样通过实验方法进行测定呢?
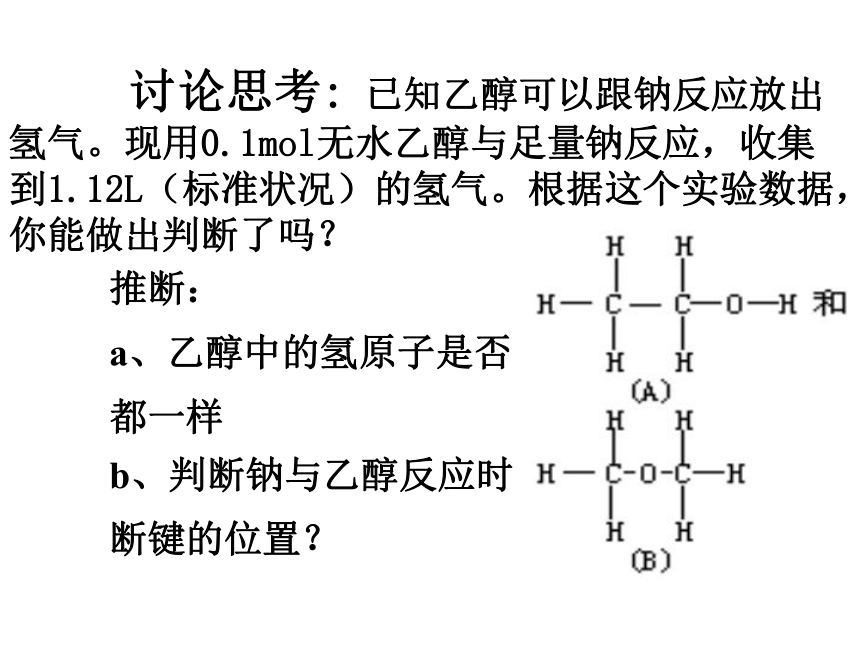
讨论思考:
已知乙醇可以跟钠反应放出氢气。现用0.1mol无水乙醇与足量钠反应,收集到1.12L(标准状况)的氢气。根据这个实验数据,你能做出判断了吗?
b、判断钠与乙醇反应时
断键的位置?
推断:
a、乙醇中的氢原子是否
都一样
C—C—O—H
H
H
H
H
H
结构式:
CH3CH2OH
或C2H5OH
羟基:
写作-OH
分子式:
二、乙醇的结构
C2H6O
结构简式:
三、几个概念
③羟基:
有机化合物分子中含有_____的基团,称为羟基
①烃的衍生物:从结构上看,烃分子中的氢原子被其他_________________所取代而生成的一系列化合物成为烃的衍生物。
②官能团:使烃的衍生物具有不同于烃的特殊性质的__________,称为官能团。
-OH
原子或原子团
基团
四、乙醇的化学性质
1、乙醇与金属钠的反应
物质
金属钠的变化
气体燃烧现象
检验产物
水
乙醇
钠沉在液面下,反应缓慢
产生淡蓝色火焰
烧杯壁上出现液滴,石灰水不浑浊
产生淡蓝色火焰
烧杯壁上出现液滴,石灰水不浑浊
钠浮在水面上熔成闪亮的小球,钠迅速移动
C—C—O—H
H
H
H
H
H
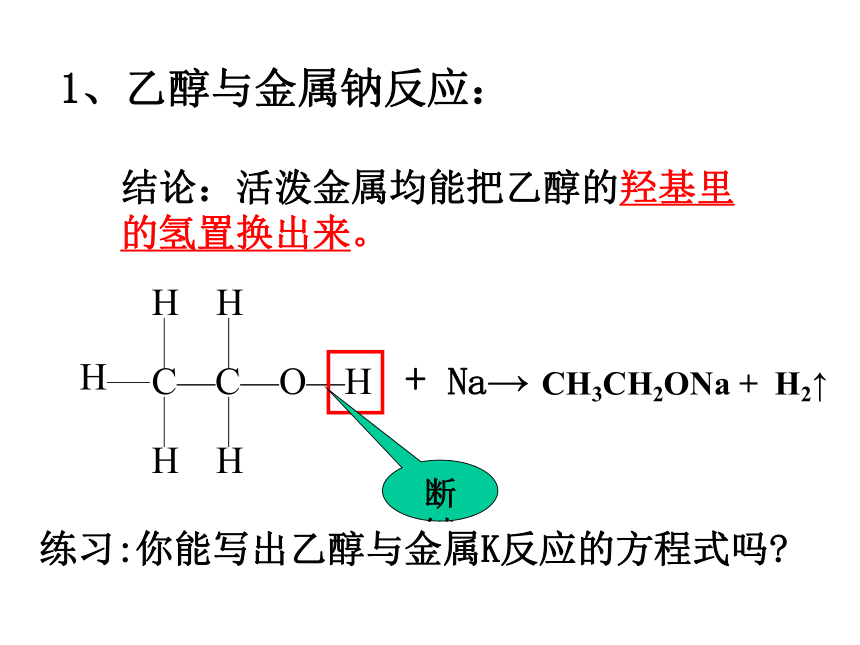
1、乙醇与金属钠反应:
2H-O-H
+
2Na
=
2NaOH
+
H2↑
结论:活泼金属均能把乙醇的羟基里的氢置换出来。
+
Na→
CH3CH2ONa
+
H2↑
断键
练习:你能写出乙醇与金属K反应的方程式吗?
脱氢
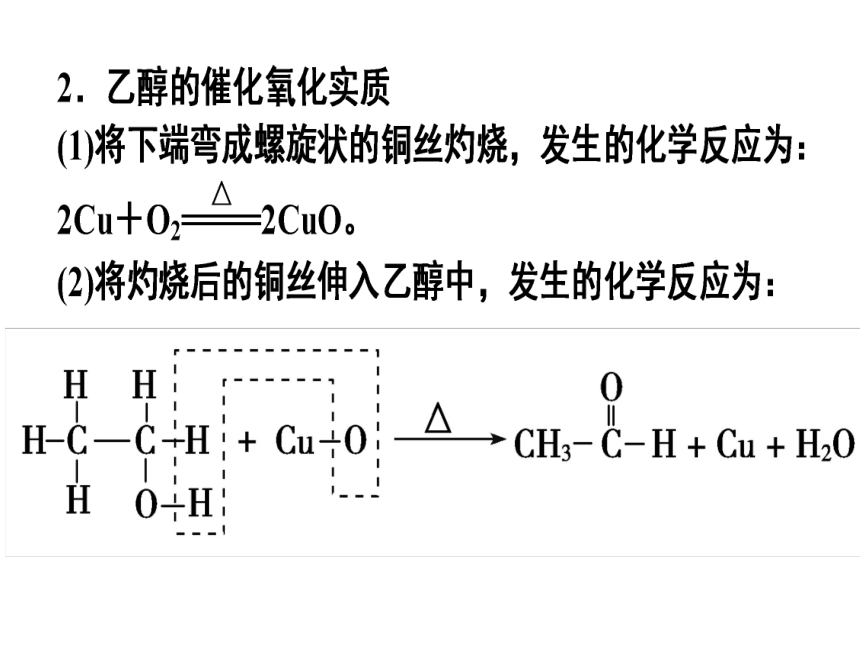
2、氧化反应
a:乙醇在空气中燃烧燃烧?:
C2H5OH+3O2
→
2CO2+2H2O
点燃
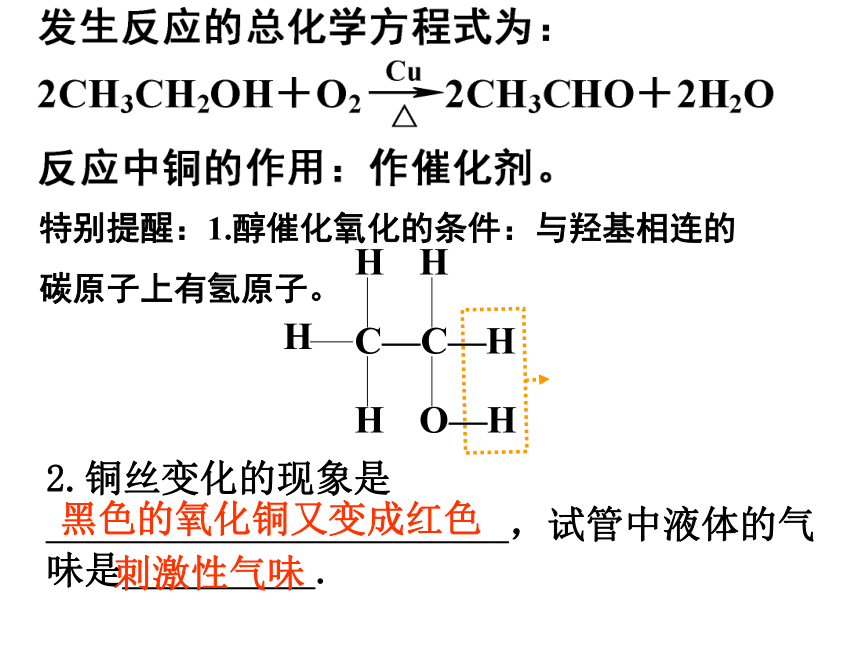
特别提醒:1.醇催化氧化的条件:与羟基相连的碳原子上有氢原子。
2.铜丝变化的现象是________________________,试管中液体的气味是__________.
黑色的氧化铜又变成红色
刺激性气味
C—C—H
H
H
H
H
O—H
C.与强氧化剂反应
乙醇还可以与______________溶液或________溶液反应,被直接氧化成__________________。
酸性高锰酸钾
酸性重铬酸钾
乙酸
3、消去反应(分子内脱水)
浓H2SO4
1700C
H
C
C
H
CH2=CH2
+H2O
H
H
H
OH
消去(脱水)
浓硫酸的作用:催化剂、脱水剂
应用:实验室乙烯的制备
[讨论] 在下图所示的乙醇分子结构中:
H H② ①
⑤
?
H―C―C―O―H
??????????????????????????????
③
?
④H H
什么情况下,①键断裂??????
什么情况下,②、④键断裂?
什么情况下,①、③键断裂?
什么情况下,⑤键才断裂?
羟基与氢氧根离子的比较
注意:
羟基
氢氧根离子
电子式
电荷数
存在形式
相同点
不显电性
带一个单位负电荷
组成元素相同
能独立存在于离子晶体或溶液中
不能独立存在
..
O
..
.
..
..
H
..
.
..
..
H
O
一、乙酸(俗称_________)
醋酸
1、?
乙酸的物理性质
有强烈刺激性气味无色液体,
沸点117.9℃,
熔点16.6℃;
易溶于水、乙醇等有机溶剂。
无水乙酸又叫冰醋酸
2.乙酸的结构与分子模型
甲基
羧基
分子式:
结构式
结构简式
或
C2H4O2
乙酸分子比例模型
推测:
羧基的性质
想一想?
羟基
上的反应
结构分析
发生在
羧基
受C=O的影响:
断碳氧单键
氢氧健更易断
上的反应
发生在
受-O-H的影响:
碳氧双键不易断
乙酸的化学性质
(一)
酸性:
CH3COOH
CH3COO-+H+
(1)如何证明乙酸具有酸的通性?
活泼的金属、酸碱指示剂、碱、碱性氧化物、某些盐
小结:乙酸可以与________________________
________________________等反应而显出酸性。
试设计实验证明乙酸的酸性与碳酸酸性的强弱?并写出化学方程式。
写出醋酸除水垢的化学方程式:
2CH3COO
H+Na2CO3=
2CH3COONa
H2O+CO2↑
2CH3COO
H+CaCO3=
(CH3COO)2Ca
H2O+CO2↑
(2)乙酸的酯化反应
实验步骤:药品及添加
的先后顺序:____________________________
实验现象:____________________________
________________________________________
结论:______________________________
____________________________
乙醇、浓硫酸、乙酸
碳酸钠饱和溶液的上方有无色透明的油状液体产生,并可闻到香味
在有浓硫酸存在、加热的条件下,乙醇与乙酸发生反应
CH3COO
H+HOC2H5
浓硫酸
△
CH3COOC2H5+H2O
O
CH3C—
O—H
+
H—O—C2H5
O
CH3C—O—C2H5
+
H2
O
浓H2SO4
18
18
同位素示踪法:
如何测出乙酸与乙醇反应,哪种物质提供-H,哪种物质提供-OH?
结论:有机酸与醇反应脱水,酸
脱羟基(-OH),醇脱氢(-H)后生成酯
思考:
①浓硫酸的作用是什么?
②饱和碳酸钠溶液的作用是什么?
③饱和碳酸钠溶液上方的导管要为什么恰好在液面上?有无改进的方法?
催化剂、吸水剂
溶解未反应的乙醇、中和乙酸、减小酯在其中的溶解
防倒吸
4.碎瓷片作用:防止暴沸
乙酸乙酯的生成实验改进
(3)酯化反应概念:___________________________________,酯化反应是_______________反应,反应物不能________变成生成物;为了提高反应速率,一般要加入__________做催化剂,并加热。
有机酸和醇反应生成酯和水反应
可逆
完全
浓硫酸
三、酯
1.概念
酯是羧酸中的_____被—OR′取代后的产物,可简写
成_________,官能团为_________或
__________。
2.性质
(1)物理性质
酯在水中的溶解性:一般________;密度:比水___,具有_____气味。
(2)化学性质:能发生_____反应,酸性条件下水解生成醇和酸。
—OH
RCOOR′
—COO—
不溶于水
小
芳香
水解
O
CH3—C—O—H
酸性
酯化
小结:
1.关于乙酸的下列说法中不正确的是
(
)
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸
D
练
习
2、
酯化反应属于(
).
A.中和反应
B.不可逆反应
C.离子反应
D.取代反应
D
C
3、
若乙酸分子中的氧都是18O,乙醇分
子中的氧都是16O,二者在浓H2SO4作用
下发生反应,一段时间后,分子中含有
18O的物质有(
)
A
1种
B
2种
C
3
种
D
4种
生成物中水的相对分子质量为
。
20
第三节:生活中两种常见的有机物
一、乙醇(俗称_________)
酒精
乙醇的物理性质
无色
有特殊香味的液体,
密度比水的小,
沸点78.5℃,易挥发,
能够溶解多种有机物和无机物,能与水以任意比互溶
思考:乙醇分子结构的实验测定
CH3-O-
CH3
CH3CH2OH
乙醇的分子式是C2H6O,根据分子式及各原子的价键关系写出乙醇的两种可能的结构__________________、____________________________,乙醇分子究竟是哪一种结构?怎样通过实验方法进行测定呢?
讨论思考:
已知乙醇可以跟钠反应放出氢气。现用0.1mol无水乙醇与足量钠反应,收集到1.12L(标准状况)的氢气。根据这个实验数据,你能做出判断了吗?
b、判断钠与乙醇反应时
断键的位置?
推断:
a、乙醇中的氢原子是否
都一样
C—C—O—H
H
H
H
H
H
结构式:
CH3CH2OH
或C2H5OH
羟基:
写作-OH
分子式:
二、乙醇的结构
C2H6O
结构简式:
三、几个概念
③羟基:
有机化合物分子中含有_____的基团,称为羟基
①烃的衍生物:从结构上看,烃分子中的氢原子被其他_________________所取代而生成的一系列化合物成为烃的衍生物。
②官能团:使烃的衍生物具有不同于烃的特殊性质的__________,称为官能团。
-OH
原子或原子团
基团
四、乙醇的化学性质
1、乙醇与金属钠的反应
物质
金属钠的变化
气体燃烧现象
检验产物
水
乙醇
钠沉在液面下,反应缓慢
产生淡蓝色火焰
烧杯壁上出现液滴,石灰水不浑浊
产生淡蓝色火焰
烧杯壁上出现液滴,石灰水不浑浊
钠浮在水面上熔成闪亮的小球,钠迅速移动
C—C—O—H
H
H
H
H
H
1、乙醇与金属钠反应:
2H-O-H
+
2Na
=
2NaOH
+
H2↑
结论:活泼金属均能把乙醇的羟基里的氢置换出来。
+
Na→
CH3CH2ONa
+
H2↑
断键
练习:你能写出乙醇与金属K反应的方程式吗?
脱氢
2、氧化反应
a:乙醇在空气中燃烧燃烧?:
C2H5OH+3O2
→
2CO2+2H2O
点燃
特别提醒:1.醇催化氧化的条件:与羟基相连的碳原子上有氢原子。
2.铜丝变化的现象是________________________,试管中液体的气味是__________.
黑色的氧化铜又变成红色
刺激性气味
C—C—H
H
H
H
H
O—H
C.与强氧化剂反应
乙醇还可以与______________溶液或________溶液反应,被直接氧化成__________________。
酸性高锰酸钾
酸性重铬酸钾
乙酸
3、消去反应(分子内脱水)
浓H2SO4
1700C
H
C
C
H
CH2=CH2
+H2O
H
H
H
OH
消去(脱水)
浓硫酸的作用:催化剂、脱水剂
应用:实验室乙烯的制备
[讨论] 在下图所示的乙醇分子结构中:
H H② ①
⑤
?
H―C―C―O―H
??????????????????????????????
③
?
④H H
什么情况下,①键断裂??????
什么情况下,②、④键断裂?
什么情况下,①、③键断裂?
什么情况下,⑤键才断裂?
羟基与氢氧根离子的比较
注意:
羟基
氢氧根离子
电子式
电荷数
存在形式
相同点
不显电性
带一个单位负电荷
组成元素相同
能独立存在于离子晶体或溶液中
不能独立存在
..
O
..
.
..
..
H
..
.
..
..
H
O
一、乙酸(俗称_________)
醋酸
1、?
乙酸的物理性质
有强烈刺激性气味无色液体,
沸点117.9℃,
熔点16.6℃;
易溶于水、乙醇等有机溶剂。
无水乙酸又叫冰醋酸
2.乙酸的结构与分子模型
甲基
羧基
分子式:
结构式
结构简式
或
C2H4O2
乙酸分子比例模型
推测:
羧基的性质
想一想?
羟基
上的反应
结构分析
发生在
羧基
受C=O的影响:
断碳氧单键
氢氧健更易断
上的反应
发生在
受-O-H的影响:
碳氧双键不易断
乙酸的化学性质
(一)
酸性:
CH3COOH
CH3COO-+H+
(1)如何证明乙酸具有酸的通性?
活泼的金属、酸碱指示剂、碱、碱性氧化物、某些盐
小结:乙酸可以与________________________
________________________等反应而显出酸性。
试设计实验证明乙酸的酸性与碳酸酸性的强弱?并写出化学方程式。
写出醋酸除水垢的化学方程式:
2CH3COO
H+Na2CO3=
2CH3COONa
H2O+CO2↑
2CH3COO
H+CaCO3=
(CH3COO)2Ca
H2O+CO2↑
(2)乙酸的酯化反应
实验步骤:药品及添加
的先后顺序:____________________________
实验现象:____________________________
________________________________________
结论:______________________________
____________________________
乙醇、浓硫酸、乙酸
碳酸钠饱和溶液的上方有无色透明的油状液体产生,并可闻到香味
在有浓硫酸存在、加热的条件下,乙醇与乙酸发生反应
CH3COO
H+HOC2H5
浓硫酸
△
CH3COOC2H5+H2O
O
CH3C—
O—H
+
H—O—C2H5
O
CH3C—O—C2H5
+
H2
O
浓H2SO4
18
18
同位素示踪法:
如何测出乙酸与乙醇反应,哪种物质提供-H,哪种物质提供-OH?
结论:有机酸与醇反应脱水,酸
脱羟基(-OH),醇脱氢(-H)后生成酯
思考:
①浓硫酸的作用是什么?
②饱和碳酸钠溶液的作用是什么?
③饱和碳酸钠溶液上方的导管要为什么恰好在液面上?有无改进的方法?
催化剂、吸水剂
溶解未反应的乙醇、中和乙酸、减小酯在其中的溶解
防倒吸
4.碎瓷片作用:防止暴沸
乙酸乙酯的生成实验改进
(3)酯化反应概念:___________________________________,酯化反应是_______________反应,反应物不能________变成生成物;为了提高反应速率,一般要加入__________做催化剂,并加热。
有机酸和醇反应生成酯和水反应
可逆
完全
浓硫酸
三、酯
1.概念
酯是羧酸中的_____被—OR′取代后的产物,可简写
成_________,官能团为_________或
__________。
2.性质
(1)物理性质
酯在水中的溶解性:一般________;密度:比水___,具有_____气味。
(2)化学性质:能发生_____反应,酸性条件下水解生成醇和酸。
—OH
RCOOR′
—COO—
不溶于水
小
芳香
水解
O
CH3—C—O—H
酸性
酯化
小结:
1.关于乙酸的下列说法中不正确的是
(
)
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸
D
练
习
2、
酯化反应属于(
).
A.中和反应
B.不可逆反应
C.离子反应
D.取代反应
D
C
3、
若乙酸分子中的氧都是18O,乙醇分
子中的氧都是16O,二者在浓H2SO4作用
下发生反应,一段时间后,分子中含有
18O的物质有(
)
A
1种
B
2种
C
3
种
D
4种
生成物中水的相对分子质量为
。
20
