2020-2021学年高二化学鲁科版(2019)选择性必修3第一章第二节 有机化合物的结构与性质课件(共106张ppt)
文档属性
| 名称 | 2020-2021学年高二化学鲁科版(2019)选择性必修3第一章第二节 有机化合物的结构与性质课件(共106张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-23 00:00:00 | ||
图片预览










文档简介
(共106张PPT)
第2节 有机化合物的结构与性质
一、碳原子的成键特点
1.碳原子的成键特点
碳原子最外层有___个电子,通常以___________的形式与其他原子成键,达到最
外层___个电子的稳定结构。
2.结合方式的多样性
(1)碳原子之间可以形成_____,也可以形成_____,还可以形成_____。
(2)多个碳原子可以相互结合形成_____结构,也可以形成_____结构。
(3)碳原子除了彼此间成键外,还可以与____________等其他元素的原子成键。
四
共用电子对
八
单键
双键
三键
H、O、N、Cl
环状
开链
二、碳原子的成键方式
1.两类碳原子
(1)饱和碳原子:与__个原子形成共价键(单键)的碳原子。
(2)不饱和碳原子:成键原子数目小于4的碳原子。
4
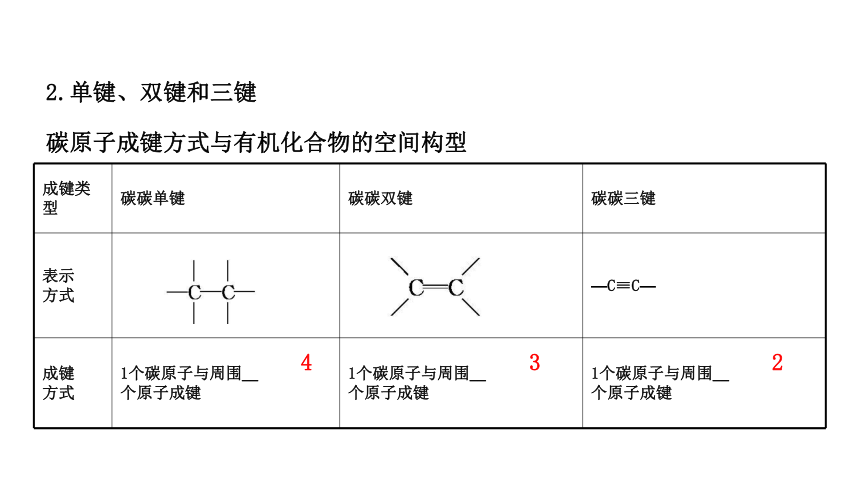
成键类型
碳碳单键
碳碳双键
碳碳三键
表示
方式
—C≡C—
成键
方式
1个碳原子与周围__
个原子成键
1个碳原子与周围__
个原子成键
1个碳原子与周围__
个原子成键
2.单键、双键和三键
碳原子成键方式与有机化合物的空间构型
4
3
2
成键类型
碳碳单键
碳碳双键
碳碳三键
碳原
子的
饱和性
_____
_______
_______
空间
构型
_______形
_____形
_____形
碳原子与周围4个
原子形成_______结
构
形成双键的碳原子
以及与之相连的原
子处于同一_____上
形成三键的碳原子
以及与之相连的原
子处于同一_____上
饱和
不饱和
不饱和
四面体
平面
直线
四面体
平面
直线
3.极性键和非极性键
(1)极性键:_____元素的两个原子之间形成的共价键,共用电子对将偏向吸引电子
能力_____的一方。如
、
、
型共价键。
(2)非极性键:_____元素的两个原子间形成的共价键,共用电子对_______于任何
一方,因此参与成键的两个原子都不显电性。如
、
、
型共价键。
三、有机化合物的同分异构现象
1.同分异构现象:有机化合物_________相同而_____不同的现象。
2.同分异构体:分子组成_____而结构_____的有机化合物。
不同
较强
相同
不偏向
分子组成
结构
相同
不同
3.常见类型
(1)碳骨架异构。
由于_______不同,产生的异构现象。
如CH3CH2CH2CH3与
碳骨架
(2)官能团异构。
①位置异构
由于官能团在碳链中_____不同而产生的同分异构现象,如CH3CH2CH==CH2与
________________。
②类型异构
分子式相同,但具有_____________而产生的同分异构现象,如CH3CH2OH与
___________。
位置
CH3—CH==CH—CH3
不同的官能团
CH3—O—CH3
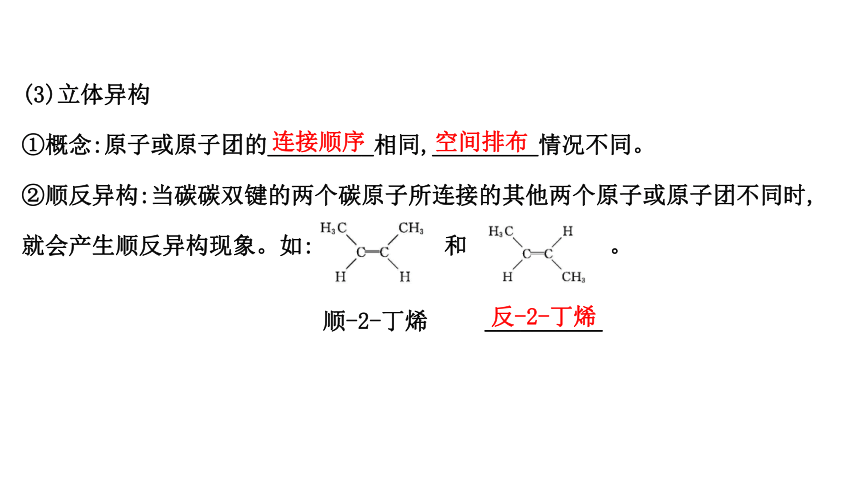
(3)立体异构
①概念:原子或原子团的_________相同,_________情况不同。
②顺反异构:当碳碳双键的两个碳原子所连接的其他两个原子或原子团不同时,
就会产生顺反异构现象。如:
和
。
连接顺序
空间排布
顺-2-丁烯
__________
反-2-丁烯
【?判一判】
(1)相对分子质量相同的几种化合物互为同分异构体。
( )
提示:×。相对分子质量相同分子式不一定相同。
(2)
和
,
和
均互为同分异构体。
( )
提示:×。前者为同一种物质。
【?情境·思考】
异丁烯是重要的化工原料,主要用于制备丁基橡胶、聚异丁烯、甲基丙烯腈、抗氧剂、叔丁酚、叔丁基醚等。目前生产异丁烯的方法有轻油C4馏分分离、叔丁醇脱水、醚化裂解等。你知道丁烯的几种同分异构体吗?
提示:3。三种碳链及双键的排列方式为
、
、
。
四、有机化合物结构和性质之间的关系
1.官能团与有机化合物性质之间的关系
(1)关系
一种官能团决定_____有机化合物的_____特性。
(2)原因
①一些官能团含有_____较强的键,容易发生相关的反应。
②一些官能团含有_______碳原子,容易发生相关的反应。
一类
化学
极性
不饱和
2.不同基团间的相互影响与有机化合物性质的关系
(1)官能团与_________之间也存在相互影响。
(2)羧酸和醇、醇和酚之所以化学性质不同,主要是因为_____连接的原子团或基
团不同;醛和酮化学性质不同,主要是因为_____所连的原子团或基团不同。
(3)醛和酮的化学性质不同,因为醛羰基上连有_______,酮羰基上不连_______。
相邻基团
羟基
羰基
氢原子
氢原子
(1)苯不能使酸性高锰酸钾溶液褪色,但是将甲苯通入酸性高锰酸钾溶液中,酸性
高锰酸钾溶液的紫红色褪去,原因是什么?
提示:甲苯中甲基由于苯环的影响变得更活泼能被酸性高锰酸钾溶液氧化。
(2)将乙烷和乙烯分别通入Br2(CCl4)溶液中,各有什么现象?试从结构角度分析原
因。
提示:现象分别是:Br2(CCl4)溶液不褪色,Br2(CCl4)溶液褪色。其原因是:乙烯分
子中含有不饱和键
。活泼性强,其中一个共价键易断裂,发生加成反应,而
乙烷属于饱和烃,不发生加成反应。
【情境·思考】
维生素C又叫L-抗坏血酸,缺少维生素C容易使人得坏血病。其结构简式如下。维生素C泡腾片是人们补充维C的方法之一,也可通过多吃水果进行补充。
通过学过的知识可知维C中含有哪些官能团?能发生哪些反应类型?
提示:含有酯基、醇羟基和碳碳双键。能发生酯化、水解、加成等反应。
知识点一 有机物的空间结构及共线、共面的判断技巧
【重点释疑】
1.基本结构四类型
(1)甲烷。
①甲烷分子为正四面体结构。
②甲基上的四个原子不共面。
(2)乙烯。
①乙烯分子为平面形结构。
②乙烯分子中双键碳原子和与之相连的4个氢原子在同一平面上。
③烯烃分子中双键碳原子和与双键碳原子直接相连的4个原子在同一平面上。
(3)乙炔。
①乙炔分子为直线形结构。
②乙炔分子中三键碳原子和与之相连的2个氢原子在同一直线上。
③炔烃中三键碳原子和与三键碳原子直接相连的2个原子在同一直线上。
(4)苯。
①苯分子为平面形结构。
②苯分子中6个碳原子与6个氢原子在同一平面上。
③芳香烃中苯环上的6个碳原子和与其直接相连的6个原子一定在同一平面上。
2.组合结构
组合结构就是将前面的四种类型的基团按一定方式连接成某种有机物。组合结
构分子中原子的位置关系。如
,作如下分析(图示)
其中可能共平面的原子最多有20个(M+N),最少有14个(N),肯定共直线的原子
最多有6个(L)。
【易错提醒】有机化合物共线共面问题的几个注意点
(1)由于单键可以旋转,所以与苯环或者乙烯上连接的甲基上的氢原子有可能与苯环或者乙烯结构共平面,也有可能不共平面,但共面时最多只有一个。
(2)饱和碳原子的四条键中相邻的两条键的键角并不一定是109°28′。只有当与碳原子相连的四个原子相同时,键角才是109°28′,形成的是以碳原子为中心的正四面体,若另外四个原子不完全相同,则键角不是109°28′,围成的图形也不再是正四面体。
【思考·讨论】
(1)下列分子中的14个碳原子不可能处在同一平面内的是哪些?
①
②
③
④
提示:②④。②中—C(CH3)3的中心碳原子位于一个四面体的中心,故—C(CH3)3的4个碳原子不可能在同一平面上。此外,④中同时连接两个苯环的那个碳原子是饱和碳原子,该C原子与其相连的3个C原子一定不共面。
(2)苯分子是平面结构,与氢气完全加成后生成的环己烷,还是平面结构吗?
提示:环己烷不是平面结构。苯与氢气加成生成的环己烷中,碳原子都是饱和碳原子,因此不再是平面结构。
【案例示范】
【典例】(2019·全国卷Ⅲ)下列化合物的分子中,所有原子可能共平面的是
( )
A.甲苯 B.乙烷 C.丙炔 D.1,3-丁二烯
【解题指南】解答本题需注意以下两点:
(1)碳碳单键可以旋转;
(2)饱和碳原子的四个共价键之间的夹角。
【解析】选D。有机物中如果有碳原子形成4个单键时,四个单键指向四面体的四个顶点,该有机物不可能所有原子共平面。甲苯、乙烷、丙炔中均含有甲基,不可能所有原子共平面,A、B、C错误。1,3-丁二烯中两个双键确定的两个平面以单键连接,由于单键可以旋转,所有原子可能共平面,D正确。
【母题追问】A中甲苯最多有多少个原子共面?
提示:苯环结构上有12个原子共面,加上甲基上的一个氢原子共13个原子共面。
【规律方法】用拆分法判断共线、共面问题
【迁移·应用】
1.甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是
( )
A.分子式为C25H20
B.该化合物为芳香烃
C.该化合物分子中所有原子不可能处于同一平面
D.分子中所有原子一定处于同一平面
【解析】选D。本题实际上是考查甲烷的正四面体结构。烃分子中氢原子被其他原子取代后,其空间位置不变,由于甲烷分子中的四个氢原子位于正四面体的四个顶点上,当四个氢原子全部被苯基取代后,苯基就排在正四面体的四个顶点上,故该化合物分子中所有原子不可能处于同一平面。
2.(2020·蚌埠高二检测)下列叙述正确的是
( )
A.丙烷分子中3个碳原子一定在同一条直线上
B.甲苯分子中7个碳原子都在同一平面上
C.乙烷分子中碳原子和全部氢原子可能在同一平面上
D.2-丁烯分子中4个碳原子可能在同一条直线上
【解析】选B。
分子中:1,3号碳原子和2号碳上的两个氢原子,可
看成是2号碳形成的四面体结构,三个碳原子只共面但一定不共线,A不正确。甲
苯分子中—CH3里的碳原子占据了苯分子中一个H原子的位置,所以甲苯分子中
7个碳原子都在同一平面内,B正确。烷烃分子中的C、H原子形成的是类似于甲
烷的四面体结构,乙烷分子中碳原子和全部氢原子不可能在同一平面上,C不正
确。2-丁烯
可看成1,4碳原子取代乙烯分子中的两个
氢原子所形成的结构,4个碳原子在同一个平面内,但是不可能在同一条直线上,
D不正确。
3.某烃结构简式为
,有关其结构的说法,正确的是
( )
A.所有原子可能在同一平面内
B.所有原子可能在同一条直线上
C.所有碳原子可能在同一平面内
D.所有氢原子可能在同一平面内
【解析】选C。该烃含有苯环、—C≡C—、
,所有碳原子可能都在同一平面内,但最多有19个原子共面,即甲基上有2个氢原子不可能在该平面内,有5个碳原子和1个氢原子共线。
【补偿训练】
下列关于CH3—CH
CH—C≡C—CF3分子结构的叙述中正确的是
( )
A.6个碳原子有可能都在一条直线上
B.有5个碳原子可能在一条直线上
C.6个碳原子一定都在同一平面上
D.6个碳原子不可能都在同一平面上
【解析】选C。根据乙烯分子中的6个原子共平面,键角120°;乙炔分子中的4个原子共直线,键角180°,可推知题给有机物的碳链骨架结构如下:
由上面的碳链骨架结构很容易看出:题给有机物分子中的6个碳原子不可能都在一条直线上,而是一定都在同一平面上,最多4个碳原子在一条直线上。
知识点二 同分异构体的书写及判断
【重点释疑】
1.同分异构体的书写
(1)烷烃同分异构体的书写——减碳法
实例:下面以己烷(C6H14)为例说明(为了简便易看,在所写结构式中省去了H原子)。
a.将分子中全部碳原子连成直链作为母链。
C—C—C—C—C—C
b.从母链的一端取下1个C原子,依次连接在母链中心对称线一侧的各个C原子上,即得到多个带有甲基、主链比母链少1个C原子的异构体骨架。
c.从母链上一端取下两个C原子,使这两个C原子相连(整连)或分开(散连),依次连接在母链所剩下的各个C原子上,得多个带1个乙基或两个甲基、主链比母链少两个C原子的异构体骨架。
故己烷(C6H14)共有5种同分异构体。
(2)烯烃同分异构体的书写(限单烯烃范围内)
C5H10同分异构体的书写
a.先写碳骨架异构:
、
、
b.再写官能团位置异构:根据碳4价的原则,在碳骨架异构中找出可能加入双键
的位置(箭头所指位置)。
c.最后写官能团类型异构:
分子式为C5H10的环烷烃:
(3)烃的含氧衍生物同分异构体的书写
书写方法:一般按碳骨架异构→官能团位置异构→官能团类型异构的顺序来书
写。下面以C5H12O为例说明。
a.碳骨架异构:5个碳原子的碳链有3种连接方式:
C—C—C—C—C
b.官能团位置异构:对于醇类,在碳链各碳原子上连接羟基,用“↓”表示连接的
不同位置。
c.官能团类型异构:通式为CnH2n+2O的有机物在中学阶段只能是醇或醚,对于醚
类,位置异构是因氧元素的位置不同而导致的。
分析知分子式为C5H12O的有机物共有8种醇和6种醚,总共14种同分异构体。
2.同分异构体数目的判断方法
(1)基元法
记住常见烃基的异构体种数,可快速判断含官能团有机化合物同分异构体的数目。
—C3H7有两种,—C4H9有4种,—C5H11有8种,如C4H9Cl、C4H9OH、C4H9—CHO等各有
4种同分异构体。
(2)换元法
如:若C3H8的二氯代物有四种同分异构体,则其六氯代物的同分异构体也为四种
(H和Cl相互替代)。
(3)等效氢法
等效氢法是判断同分异构体数目的重要方法,其规律有:
①分子中同一个碳原子上的氢原子等效;
②与同一个碳原子相连的甲基上的氢原子等效。如新戊烷(
)分子中
的12个氢原子是等效的;
③同一分子中处于轴对称位置或镜面对称位置上的氢原子是等效的。如
分子中,在苯环所在的平面内有两条互相垂直的对称轴,故
有两类等效氢;
分子中的18个氢原子是等效的。
等效氢原子的种类数等于一元取代物的种类数。
(4)定一(或二)移一法
对于二元取代物的同分异构体的判定,可固定一个取代基位置,再移动另一取代
基,以确定同分异构体数目。
如:分析C3H6Cl2的同分异构体,可先固定其中一个—Cl的位置,再移动另外一
个—Cl的位置,从而得到其同分异构体为
、
、
、
。
如C3H6ClF的同分异构体(先把氯原子固定在一个碳原子上,用
标
记)。
【思考·讨论】
(1)分子式相同结构不同的有机物互为同分异构体,分子式相同,相对分子质量一定相同,相对分子质量相同的有机物一定是同分异构体吗?
提示:不一定。因为相对分子质量相同分子式不一定相同。例如:乙醇和甲酸相对分子质量都为46。
(2)C4H8属于烯烃的同分异构体有几种?试写出其结构简式。
提示:C4H8属于烯烃的结构有3种,其结构简式分别为
(3)萘(
)的二氯代物有10种,八氯代物有几种?
提示:利用换元法可知,八氯萘可以看成是十氯萘上的两个Cl原子被两个H原子取
代的产物,也有10种。
【案例示范】
【典例】(2020·济南高二检测)某烷烃相对分子质量为86,如果分子中含有
3个—CH3、2个—CH2—和1个
,则该结构的烃的一氯取代物(不考虑立体异
构)最多可能有
( )
A.9种
B.6种
C.5种
D.4种
【解析】选A。根据烷烃的通式CnH2n+2,14n+2=86,解得n=6,该分子是己烷,含有上述基团的分子有CH3CH2CH2CH(CH3)2和CH3CH2CH(CH3)CH2CH3,CH3CH2CH2CH(CH3)2分子是不对称分子,一氯代物有5种,CH3CH2CH(CH3)CH2CH3分子是对称分子,一氯代物有4种,共9种,选A。
【规律方法】同分异构体的书写规律
【迁移·应用】
1.(2018·全国卷Ⅰ)环之间共用一个碳原子的化合物称为螺环化合物,螺[2.2]
戊烷(
)是最简单的一种。下列关于该化合物的说法错误的是
( )
A.与环戊烯互为同分异构体
B.二氯代物超过两种
C.所有碳原子均处同一平面
D.生成1
mol
C5H12至少需要2
mol
H2
【解析】选C。环戊烯与螺[2.2]戊烷(
)的分子式均为C5H8,二者互为同分
异构体,故A正确;二氯取代中可以取代同一个碳原子上的氢原子,也可以取代同
侧碳原子上或者两侧的碳原子上的氢原子……,因此其二氯代物超过两种,B正
确;螺[2.2]戊烷(
)中中心原子含有四个单键,故所有碳原子一定不处于
同一平面,C不正确;螺[2.2]戊烷(
)的分子式为C5H8,若生成1
mol
C5H12则
至少需要2
mol
H2,D正确。
2.主链上有6个碳原子,有甲基、乙基两个支链的烷烃有
(
)
A.2种
B.3种
C.4种
D.5种
【解析】选C。主链6个C,则乙基只能在第3个C上,甲基可以在中间所有的C上,该分子不对称,甲基分别在中间四个碳原子上,共有4种。
【补偿训练】
下列各组指定物质的同分异构体数目相等的是
( )
A.乙烷的二氯代物和丙烷的一氯代物
B.丙烷的一氯代物和戊烷
C.苯的二氯代物和苯的一硝基代物
D.C3H5Br3和C5H11Br
【解析】选A。乙烷的二氯代物有2种同分异构体,丙烷的一氯代物也有2种同分异构体,A项正确;丙烷的一氯代物有2种同分异构体,戊烷有3种同分异构体,B项错误;苯的二氯代物有3种同分异构体,苯的一硝基代物只有1种结构,C项错误;C3H5Br3有5种同分异构体,而C5H11Br有8种同分异构体,D项错误。
【素养提升】
有机环状化合物在新型材料、新型药物等方面应用十分广泛,除传统的环烷烃、芳香烃之外,近年来科学家用合成方法制备了多种新的环状有机物,例如环辛四烯、正四面体烷、金刚烷、棱晶烷、立方烷等,其分子具有如下图所示立体结构。
(1)上述八种环状有机物中,哪些物质之间互为同分异构体?
提示:苯与棱晶烷的分子式均为C6H6,环辛四烯与立方烷的分子式均为C8H8,但是它们的结构都不相同,故互为同分异构体。
(2)上述物质中,一氯代物种类最多的物质是哪一种?二氯代物最多的呢?
提示:一氯代物最多的是金刚烷,有2种,其他七种物质的一氯代物均为1种;二氯代物种类最多的是金刚烷,有6种。
1.下列关于有机化合物的表示方法中不正确的是
( )
A.乙烯:CH2CH2
B.异戊烷:
C.乙酸乙酯:CH3COOCH2CH3
D.甲烷:
【解析】选A。A、C两项表示物质的结构简式,其中乙烯结构简式中的碳碳双键不可省略,应写成CH2==CH2;B项表示物质的键线式;D项表示物质的结构式。
2.(2020·济宁高二检测)下列物质的分子是平面结构的是
( )
A.CH4 B.CH2==CH2
C.HC≡C—CH3
D.
【解析】选B。有机化合物分子中,碳原子最外层有四对共用电子。若形成四个相同单键,如CH4,则键角为109°28′,为正四面体形;若形成双键,键角为120°,如CH2==CH2,属平面结构;若形成三键,键角为180°,如HC≡CH,属直线形。C选项中甲基上的氢原子与其他原子不共面。
3.
是由苯环和甲基结合而成的,苯不能够使酸性KMnO4溶液褪色,而甲苯
能够使酸性KMnO4溶液褪色是因为
( )
A.烷烃能使酸性KMnO4溶液褪色
B.苯环能使酸性KMnO4溶液褪色
C.苯环使甲基的活性增强而导致的
D.甲基使苯环的活性增强而导致的
【解析】选C。有机化合物分子中邻近基团间往往存在着相互影响,这种影响会使有机化合物表现出一些特性。甲苯能够使酸性KMnO4溶液褪色是苯环使甲基的活性增强而导致的。
4.轴烯是一类独特的星形环烃。三元轴烯(
)与苯
( )
A.均为芳香烃
B.互为同素异形体
C.互为同系物
D.互为同分异构体
【解析】选D。三元轴烯与苯分子式都是C6H6,二者分子式相同,结构不同,互为同
分异构体,D项正确。
5.分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)
( )
A.3种
B.4种
C.5种
D.6种
【解析】选B。分子式为C4H10O是醇或醚。若物质可以与金属Na发生反应放出氢气,则该物质是醇,C4H10O可以看成是C4H10的分子中的一个H原子被羟基—OH取代产生的,—C4H9有4种不同的结构,因此符合该性质的醇的种类也应该是4种。
6.已知碳碳单键可以绕键轴自由旋转,某烃的结构简式如图。下列有关说法正确的是
( )
A.分子中至少有9个碳原子处于同一平面上
B.分子中至少有10个碳原子处于同一平面上
C.分子中至少有11个碳原子处于同一平面上
D.分子中所有的原子可能共平面
【解析】选C。将题给分子表示为
,容易看出,两个苯环所在的
平面可能重合,而苯环上所连的其他原子均可视为取代了苯分子中的氢原子,因
而与苯环共平面,所以该烃中所有的碳原子都可能共平面,但不是所有原子共平
面。当连接两苯环的碳碳单键旋转时,两个苯环可能不共面,但由于带“
”的6
个碳原子共线,所以至少有11个碳原子处于同一平面上,C正确。
7.CO2的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸的反应:
3NH3+3CO2
+3H2O
(1)其分子式是什么?如果把氮原子换成碳原子分子式又是什么?
提示:由三聚氰酸的结构简式可知其分子式为C3H3N3O3;换后多了三个氢原子,所以是C6H6O3。
(2)分子中有哪些极性共价键?
提示:分子中存在O—H、C—O、N—C、N
C键,都属于极性键,所以分子中不存在非极性键。
(3)假设六元环是和苯环一样的平面结构,此分子中所有的原子是否一定共面?
提示:不一定。因为羟基和另外一个原子相连时是V形结构,所以所有原子不一定共面。
二 有机化合物的结构与性质
【基础达标】(40分钟 70分)
一、选择题(本题包括10小题,每小题5分,共50分)
1.下列有机物分子中的所有原子一定处于同一平面上的是
( )
【解析】选A。甲基是四面体结构,所以B、D中所有原子一定不共面,由于单键可以旋转,所以C不一定共面。
2.(2020·三亚高二检测)下列有机物的同分异构体数目判断错误的是
( )
选
项
有机物
同分异构
体数目
A
分子式为C5H12
3
B
分子式为C5H10,能使溴的四氯化碳溶液褪色
5
C
分子式为C4H10O,能与Na反应生成氢气
4
D
分子式为C4H8O2,能与NaHCO3反应
3
【解析】选D。戊烷C5H12有3种同分异构体,分别为正戊烷、异戊烷与新戊烷,A正确;能使溴的四氯化碳溶液褪色,说明C5H10为戊烯,分别为1-戊烯、2-戊烯、2-甲基-1-丁烯、2-甲基-2-丁烯、3-甲基-1-丁烯,故共有5种同分异构体,B正确;能与Na反应生成氢气说明为醇类,C4H10O可写成C4H9OH,丁基有4种结构,故共有4种醇,C正确;能与NaHCO3反应说明为羧酸,C4H8O2可写成C3H7COOH,丙基有2种,故有2种丁酸,D错误。
3.碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图。下列有关该物质的说法正确的是
( )
A.分子式为C3H2O3
B.分子中含6个σ键
C.分子中只有极性键
D.8.6
g该物质完全燃烧得到6.72
L
CO2
【解析】选A。由图示可知,该物质的分子式为C3H2O3,A项正确;分子中的碳碳双键和碳氧双键中各有一个σ键,碳氧单键全部是σ键(4个),碳氢键也是σ键(2个),分子中共有8个σ键,B项错误;分子中的碳氧键和碳氢键都是极性键,而碳碳键是非极性键,C项错误;8.6
g该物质的物质的量为0.1
mol,完全燃烧后得到0.3
mol
CO2,在标准状况下的体积是6.72
L,D项未指明是否在标准状况下,D项错误。
4.某烃有两种或两种以上的同分异构体,其同分异构体中的某一种烃的一氯代物只有一种,则这种烃可能是
( )
①分子中具有7个碳原子的芳香烃
②分子中具有4个碳原子的烷烃
③分子中具有5个碳原子的烷烃
④分子中具有8个碳原子的烷烃
A.①②
B.②③
C.③④
D.②④
【解析】选C。分子中含有1~10个碳原子的烷烃中,一氯代物只有一种的有CH4、C(CH3)4和CH3CH3、(CH3)3CC(CH3)3,其中CH4、CH3CH3没有同分异构体,不合题意,另外两种的分子式分别为C5H12和C8H18,③、④符合题意,C项正确。
5.(2020·保定高二检测)烯烃、炔烃、芳香烃和乙醛都能发生加成反应,这是因为它们都含有
( )
A.单键
B.不饱和碳原子
C.非极性键
D.碳原子
【解析】选B。只有具有不饱和碳原子的有机化合物才能发生加成反应。
6.分子式为C7H16,且有一个支链的有机物有(不考虑立体异构)
( )
A.1种
B.2种
C.3种
D.4种
【解析】选C。分子式为C7H16,且有一个支链,如为甲基,则主链有6个C原子,由结构对称可知为
CH3CH(CH3)CH2CH2CH2CH3、
CH3CH2CH
(CH3)CH2CH2CH3;
如支链为乙基,则主链为5个C原子,为
CH3CH2CH(CH2CH3)CH2CH3,共3种。
7.(双选)霉酚酸是一种生物活性化合物。下列有关霉酚酸的说法正确的是
( )
A.分子式为C17H20O6
B.处于同一平面的原子至多9个
C.只有2种官能团
D.一定条件下,
1
mol霉酚酸最多可与4
mol
H2反应
【解析】选A、D。由结构简式可知该有机物的分子式为C17H20O6,A正确;分子中有苯环,共面原子数至少为12个,B错误;有羟基、醚键、羧基、酯基和碳碳双键五种官能团,C错误;分子中有一个苯环和一个碳碳双键,1
mol霉酚酸最多可与
4
mol
H2反应,D正确。
8.下列各组物质不属于同分异构体的是
( )
A.2,2-二甲基丙醇(
)和2-甲基丁醇(
)
B.
和
C.2-甲基丁烷(
)和戊烷
D.甲基丙烯酸(
)和甲酸丙酯
【解析】选D。甲基丙烯酸的分子式为C4H6O2,甲酸丙酯(HCOOC3H7)的分子式为C4H8O2,故二者不属于同分异构体。
9.以物质a为原料,制备物质(金刚烷)的合成路线如图所示:
关于以上有机物说法中错误的是
( )
A.物质b的分子式为C10H12
B.b可以由2
mol
a反应得到,发生的是加成反应
C.物质c与物质d互为同分异构体
D.物质d的二氯代物有4种
【解析】选D。A.根据键线式的特点,物质b的分子式为C10H12,A正确;B.b中含有
10个碳原子,可以由2
mol
a发生加成反应得到,反应类型为加成反应,B正确;C.
物质c与物质d的分子式为C10H16,分子式相同,结构不同互为同分异构体,C正确;
D.给d中碳原子编号
,其中有2种H(其中1、3、5、7等效,2、4、6、
8、9、10等效),一氯代物有2种,二氯代物先固定一个Cl在1号碳,另一个Cl可在
2、3、4号碳,共3种,再固定1个Cl在2号碳,另一个Cl可在2、4、6号碳,
合计6种,D错误。
10.(2020·潍坊高二检测)有4种碳骨架如下的烃。下列说法正确的是
( )
①a和d是同分异构体
②b和c是同系物
③a和d都能发生加聚反应
④只有b和c能发生取代反应
A.①②
B.①④
C.②③
D.①②③
【解析】选A。由图可知a为2-甲基丙烯[(CH3)2C﹦CH2],分子式为C4H8;
b为新戊烷[(CH3)4C],分子式为C5H12;c为2-甲基丙烷[(CH3)3CH],分子式为C4H10;d为环丁烷,分子式为C4H8,故可知①②正确;d不能发生加聚反应,故③错;a、d也能发生取代反应,故④错;选A。
二、非选择题(本题包括2小题,共20分)
11.(10分)某有机化合物的结构如下,分析其结构并回答下列问题:
(1)写出其分子式:__________________。?
(2)其中含有________个不饱和碳原子,分子中有________种双键。?
(3)分子中的极性键有?______________(写两种即可)。?
(4)分子中的饱和碳原子有________个;一定与苯环处于同一平面的碳原子有________个。?
(5)分子中—C≡C—H的结构中碳氢键和碳碳三键之间的键角约为__________。
【解析】与4个原子或原子团相连的碳原子是饱和碳原子,反之是不饱和碳原子。苯环结构中,环上的6个碳原子和与它们直接相连的6个原子共12个原子一定共面,因此直接与苯环相连的碳原子一定与苯环共平面,这样的碳原子有3个,由于碳碳三键是直线形,使得这两个碳原子均与苯环共平面,故一共有4个碳原子与苯环位于同一平面。
答案:(1)C16H16O5 (2)12 2 (3)C﹦O键、C—H键、O—H键、C—O键(写出两种即可)
(4)4 4 (5)180°
12.(10分)(1)有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是________。?
A.1
mol甲分子内含有10
mol共价键
B.由乙分子构成的物质不能发生氧化反应
C.丙分子中只含有非极性键
D.分子丁显然是不可能合成的
(2)“立方烷”是一种新合成的烃,其分子为正方体结构,其碳骨架结构如图所示。
①“立方烷”的分子式为__________。?
②碳碳键键角是________(填度数)。?
(3)化学式为C6H12的某烯烃的所有碳原子都在同一个平面上,则该烯烃的结构简式为________,键线式为________,分子式为C10H18的链烃分子中所有碳原子也可能在同一平面上,它的结构简式为________(只写一种)。?
【解析】(1)1
mol甲分子中含有6
mol碳碳键,4
mol碳氢键,A正确;乙分子可以发生燃烧反应,即氧化反应,B错误;丙分子中既有极性键又有非极性键,C错误;丁分子中碳不符合四价键原则,不可能合成,D正确。
(2)①立方体为一对称结构,有8个顶点,每个顶点为1个碳原子,这个碳原子和相邻的3个顶点上的碳原子以共价键结合,碳原子有4个价电子,所以每个碳原子还能再和1个氢原子相结合,故立方烷的分子式为C8H8。②在立方烷中每个面上都是正方形结构,每2个碳碳共价键构成一个直角,所以键角(碳碳共价键的夹角)是90°。
(3)C6H12中有6个碳原子,根据C2H4分子的6个原子共平面的原理,C6H12中6个碳处于C2H4中6个原子位置,则能使6个碳原子共平面。C10H18与C10H22比较分子中少4个H,可能会有一个三键或两个双键,但含有一个三键不可能使10个碳原子处于同一平面上,因此应含有两个双键。
答案:(1)BC (2)①C8H8 ②90°
【能力提升】(20分钟 30分)
一、选择题(本题包括2小题,每小题8分,共16分)
13.(2020·威海高二检测)医学上在对抗癌物质的研究中发现
具
有抗癌作用,而
没有抗癌作用,对此下列有关叙述正确的是
( )
A.两者互为同分异构体,都是以Pt原子为中心的四面体结构
B.两者互为同分异构体,都是以Pt原子为中心的平面结构
C.两者为同一物质,都是以Pt原子为中心的四面体结构
D.两者为同一物质,都是以Pt原子为中心的平面结构
【解析】选B。由信息可知两种化合物性质不同,则其结构不同,两者互为同分异构体,且为平面结构。若为四面体结构,则是一种物质,不互为同分异构体。
14.(双选)2015年10月,中国药学家屠呦呦获得了诺贝尔生理学或医学奖,获奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”。如图是青蒿素的结构简式,下列有关青蒿素的说法中不正确的是
( )
A.青蒿素的分子式为C15H22O5
B.青蒿素有—O—O—键,具有较强的氧化性
C.青蒿素易溶于水、乙醇、苯
D.青蒿素不易发生水解
【解析】选C、D。A项,根据青蒿素的结构简式判断其分子式为C15H22O5,正确;B项,青蒿素分子中含有—O—O—键,具有较强的氧化性,正确;C项,该有机物含有较多疏水基,难溶于水,错误;D项,青蒿素分子中含有—COO—,可在碱性条件下发生水解,错误。
二、非选择题(本题包括1小题,共14分)
15.丙烯酰胺是一种重要的有机合成中间体。它的球棍模型如下图所示:(图中“棍”代表单键、双键或三键,不同颜色的球表示不同原子:C、H、O、N)
(1)丙烯酰胺的分子式为____________,结构简式为______________。?
(2)有关丙烯酰胺的说法正确的是________。?
A.丙烯酰胺分子内所有原子不可能都在同一平面内
B.丙烯酰胺属于烃的含氧衍生物
C.丙烯酰胺能够使酸性高锰酸钾溶液褪色
D.丙烯酰胺能够使溴的四氯化碳溶液褪色
(3)工业上生产丙烯酰胺的方法之一是(反应均在一定条件下进行):
反应Ⅰ和反应Ⅱ都是原子利用率100%的反应,反应Ⅰ所需另一反应物的分子式为________,反应Ⅱ的方程式为________。?
(4)聚丙烯酰胺(PAM)是一种合成有机高分子絮凝剂,写出由丙烯酰胺合成聚丙烯酰胺的化学方程式______________。?
【解析】该题给出的信息是丙烯酰胺的球棍模型,通过模型中球的颜色及大小可以确定这些“球”所代表的原子,通过原子类别可以确定“棍”为单键、双键还是三键。通过丙烯酰胺分子的球棍模型可知,其含有4种原子,在有机化合物中最小的原子是氢原子,故5个白球就是氢原子,通过“丙”字可知三个“绿球”是碳原子,而直接以单原子连接在碳原子上的多为氢原子和氧原子,故“红球”为氧原子,那么“蓝球”就是氮原子。
(1)由上面的分析可知丙烯酰胺的分子式为C3H5ON,结构简式为
。
(2)有双键能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色。分子中有氨基呈
三角锥形,所有分子不可能共面。分子中有氮元素,不是烃的含氧衍生物。
(3)对于原子利用率100%的反应,其中一种反应物的推断可以采用“减法”,即
用生成物减去一种反应物。由此可知反应Ⅰ所需另一反应物的分子式为HCN;反
应Ⅱ所需另一反应物的分子式为H2O。
(4)丙烯酰胺中的碳碳双键可以发生聚合反应(加聚反应)而生成聚丙烯酰胺。
答案:
第2节 有机化合物的结构与性质
一、碳原子的成键特点
1.碳原子的成键特点
碳原子最外层有___个电子,通常以___________的形式与其他原子成键,达到最
外层___个电子的稳定结构。
2.结合方式的多样性
(1)碳原子之间可以形成_____,也可以形成_____,还可以形成_____。
(2)多个碳原子可以相互结合形成_____结构,也可以形成_____结构。
(3)碳原子除了彼此间成键外,还可以与____________等其他元素的原子成键。
四
共用电子对
八
单键
双键
三键
H、O、N、Cl
环状
开链
二、碳原子的成键方式
1.两类碳原子
(1)饱和碳原子:与__个原子形成共价键(单键)的碳原子。
(2)不饱和碳原子:成键原子数目小于4的碳原子。
4
成键类型
碳碳单键
碳碳双键
碳碳三键
表示
方式
—C≡C—
成键
方式
1个碳原子与周围__
个原子成键
1个碳原子与周围__
个原子成键
1个碳原子与周围__
个原子成键
2.单键、双键和三键
碳原子成键方式与有机化合物的空间构型
4
3
2
成键类型
碳碳单键
碳碳双键
碳碳三键
碳原
子的
饱和性
_____
_______
_______
空间
构型
_______形
_____形
_____形
碳原子与周围4个
原子形成_______结
构
形成双键的碳原子
以及与之相连的原
子处于同一_____上
形成三键的碳原子
以及与之相连的原
子处于同一_____上
饱和
不饱和
不饱和
四面体
平面
直线
四面体
平面
直线
3.极性键和非极性键
(1)极性键:_____元素的两个原子之间形成的共价键,共用电子对将偏向吸引电子
能力_____的一方。如
、
、
型共价键。
(2)非极性键:_____元素的两个原子间形成的共价键,共用电子对_______于任何
一方,因此参与成键的两个原子都不显电性。如
、
、
型共价键。
三、有机化合物的同分异构现象
1.同分异构现象:有机化合物_________相同而_____不同的现象。
2.同分异构体:分子组成_____而结构_____的有机化合物。
不同
较强
相同
不偏向
分子组成
结构
相同
不同
3.常见类型
(1)碳骨架异构。
由于_______不同,产生的异构现象。
如CH3CH2CH2CH3与
碳骨架
(2)官能团异构。
①位置异构
由于官能团在碳链中_____不同而产生的同分异构现象,如CH3CH2CH==CH2与
________________。
②类型异构
分子式相同,但具有_____________而产生的同分异构现象,如CH3CH2OH与
___________。
位置
CH3—CH==CH—CH3
不同的官能团
CH3—O—CH3
(3)立体异构
①概念:原子或原子团的_________相同,_________情况不同。
②顺反异构:当碳碳双键的两个碳原子所连接的其他两个原子或原子团不同时,
就会产生顺反异构现象。如:
和
。
连接顺序
空间排布
顺-2-丁烯
__________
反-2-丁烯
【?判一判】
(1)相对分子质量相同的几种化合物互为同分异构体。
( )
提示:×。相对分子质量相同分子式不一定相同。
(2)
和
,
和
均互为同分异构体。
( )
提示:×。前者为同一种物质。
【?情境·思考】
异丁烯是重要的化工原料,主要用于制备丁基橡胶、聚异丁烯、甲基丙烯腈、抗氧剂、叔丁酚、叔丁基醚等。目前生产异丁烯的方法有轻油C4馏分分离、叔丁醇脱水、醚化裂解等。你知道丁烯的几种同分异构体吗?
提示:3。三种碳链及双键的排列方式为
、
、
。
四、有机化合物结构和性质之间的关系
1.官能团与有机化合物性质之间的关系
(1)关系
一种官能团决定_____有机化合物的_____特性。
(2)原因
①一些官能团含有_____较强的键,容易发生相关的反应。
②一些官能团含有_______碳原子,容易发生相关的反应。
一类
化学
极性
不饱和
2.不同基团间的相互影响与有机化合物性质的关系
(1)官能团与_________之间也存在相互影响。
(2)羧酸和醇、醇和酚之所以化学性质不同,主要是因为_____连接的原子团或基
团不同;醛和酮化学性质不同,主要是因为_____所连的原子团或基团不同。
(3)醛和酮的化学性质不同,因为醛羰基上连有_______,酮羰基上不连_______。
相邻基团
羟基
羰基
氢原子
氢原子
(1)苯不能使酸性高锰酸钾溶液褪色,但是将甲苯通入酸性高锰酸钾溶液中,酸性
高锰酸钾溶液的紫红色褪去,原因是什么?
提示:甲苯中甲基由于苯环的影响变得更活泼能被酸性高锰酸钾溶液氧化。
(2)将乙烷和乙烯分别通入Br2(CCl4)溶液中,各有什么现象?试从结构角度分析原
因。
提示:现象分别是:Br2(CCl4)溶液不褪色,Br2(CCl4)溶液褪色。其原因是:乙烯分
子中含有不饱和键
。活泼性强,其中一个共价键易断裂,发生加成反应,而
乙烷属于饱和烃,不发生加成反应。
【情境·思考】
维生素C又叫L-抗坏血酸,缺少维生素C容易使人得坏血病。其结构简式如下。维生素C泡腾片是人们补充维C的方法之一,也可通过多吃水果进行补充。
通过学过的知识可知维C中含有哪些官能团?能发生哪些反应类型?
提示:含有酯基、醇羟基和碳碳双键。能发生酯化、水解、加成等反应。
知识点一 有机物的空间结构及共线、共面的判断技巧
【重点释疑】
1.基本结构四类型
(1)甲烷。
①甲烷分子为正四面体结构。
②甲基上的四个原子不共面。
(2)乙烯。
①乙烯分子为平面形结构。
②乙烯分子中双键碳原子和与之相连的4个氢原子在同一平面上。
③烯烃分子中双键碳原子和与双键碳原子直接相连的4个原子在同一平面上。
(3)乙炔。
①乙炔分子为直线形结构。
②乙炔分子中三键碳原子和与之相连的2个氢原子在同一直线上。
③炔烃中三键碳原子和与三键碳原子直接相连的2个原子在同一直线上。
(4)苯。
①苯分子为平面形结构。
②苯分子中6个碳原子与6个氢原子在同一平面上。
③芳香烃中苯环上的6个碳原子和与其直接相连的6个原子一定在同一平面上。
2.组合结构
组合结构就是将前面的四种类型的基团按一定方式连接成某种有机物。组合结
构分子中原子的位置关系。如
,作如下分析(图示)
其中可能共平面的原子最多有20个(M+N),最少有14个(N),肯定共直线的原子
最多有6个(L)。
【易错提醒】有机化合物共线共面问题的几个注意点
(1)由于单键可以旋转,所以与苯环或者乙烯上连接的甲基上的氢原子有可能与苯环或者乙烯结构共平面,也有可能不共平面,但共面时最多只有一个。
(2)饱和碳原子的四条键中相邻的两条键的键角并不一定是109°28′。只有当与碳原子相连的四个原子相同时,键角才是109°28′,形成的是以碳原子为中心的正四面体,若另外四个原子不完全相同,则键角不是109°28′,围成的图形也不再是正四面体。
【思考·讨论】
(1)下列分子中的14个碳原子不可能处在同一平面内的是哪些?
①
②
③
④
提示:②④。②中—C(CH3)3的中心碳原子位于一个四面体的中心,故—C(CH3)3的4个碳原子不可能在同一平面上。此外,④中同时连接两个苯环的那个碳原子是饱和碳原子,该C原子与其相连的3个C原子一定不共面。
(2)苯分子是平面结构,与氢气完全加成后生成的环己烷,还是平面结构吗?
提示:环己烷不是平面结构。苯与氢气加成生成的环己烷中,碳原子都是饱和碳原子,因此不再是平面结构。
【案例示范】
【典例】(2019·全国卷Ⅲ)下列化合物的分子中,所有原子可能共平面的是
( )
A.甲苯 B.乙烷 C.丙炔 D.1,3-丁二烯
【解题指南】解答本题需注意以下两点:
(1)碳碳单键可以旋转;
(2)饱和碳原子的四个共价键之间的夹角。
【解析】选D。有机物中如果有碳原子形成4个单键时,四个单键指向四面体的四个顶点,该有机物不可能所有原子共平面。甲苯、乙烷、丙炔中均含有甲基,不可能所有原子共平面,A、B、C错误。1,3-丁二烯中两个双键确定的两个平面以单键连接,由于单键可以旋转,所有原子可能共平面,D正确。
【母题追问】A中甲苯最多有多少个原子共面?
提示:苯环结构上有12个原子共面,加上甲基上的一个氢原子共13个原子共面。
【规律方法】用拆分法判断共线、共面问题
【迁移·应用】
1.甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是
( )
A.分子式为C25H20
B.该化合物为芳香烃
C.该化合物分子中所有原子不可能处于同一平面
D.分子中所有原子一定处于同一平面
【解析】选D。本题实际上是考查甲烷的正四面体结构。烃分子中氢原子被其他原子取代后,其空间位置不变,由于甲烷分子中的四个氢原子位于正四面体的四个顶点上,当四个氢原子全部被苯基取代后,苯基就排在正四面体的四个顶点上,故该化合物分子中所有原子不可能处于同一平面。
2.(2020·蚌埠高二检测)下列叙述正确的是
( )
A.丙烷分子中3个碳原子一定在同一条直线上
B.甲苯分子中7个碳原子都在同一平面上
C.乙烷分子中碳原子和全部氢原子可能在同一平面上
D.2-丁烯分子中4个碳原子可能在同一条直线上
【解析】选B。
分子中:1,3号碳原子和2号碳上的两个氢原子,可
看成是2号碳形成的四面体结构,三个碳原子只共面但一定不共线,A不正确。甲
苯分子中—CH3里的碳原子占据了苯分子中一个H原子的位置,所以甲苯分子中
7个碳原子都在同一平面内,B正确。烷烃分子中的C、H原子形成的是类似于甲
烷的四面体结构,乙烷分子中碳原子和全部氢原子不可能在同一平面上,C不正
确。2-丁烯
可看成1,4碳原子取代乙烯分子中的两个
氢原子所形成的结构,4个碳原子在同一个平面内,但是不可能在同一条直线上,
D不正确。
3.某烃结构简式为
,有关其结构的说法,正确的是
( )
A.所有原子可能在同一平面内
B.所有原子可能在同一条直线上
C.所有碳原子可能在同一平面内
D.所有氢原子可能在同一平面内
【解析】选C。该烃含有苯环、—C≡C—、
,所有碳原子可能都在同一平面内,但最多有19个原子共面,即甲基上有2个氢原子不可能在该平面内,有5个碳原子和1个氢原子共线。
【补偿训练】
下列关于CH3—CH
CH—C≡C—CF3分子结构的叙述中正确的是
( )
A.6个碳原子有可能都在一条直线上
B.有5个碳原子可能在一条直线上
C.6个碳原子一定都在同一平面上
D.6个碳原子不可能都在同一平面上
【解析】选C。根据乙烯分子中的6个原子共平面,键角120°;乙炔分子中的4个原子共直线,键角180°,可推知题给有机物的碳链骨架结构如下:
由上面的碳链骨架结构很容易看出:题给有机物分子中的6个碳原子不可能都在一条直线上,而是一定都在同一平面上,最多4个碳原子在一条直线上。
知识点二 同分异构体的书写及判断
【重点释疑】
1.同分异构体的书写
(1)烷烃同分异构体的书写——减碳法
实例:下面以己烷(C6H14)为例说明(为了简便易看,在所写结构式中省去了H原子)。
a.将分子中全部碳原子连成直链作为母链。
C—C—C—C—C—C
b.从母链的一端取下1个C原子,依次连接在母链中心对称线一侧的各个C原子上,即得到多个带有甲基、主链比母链少1个C原子的异构体骨架。
c.从母链上一端取下两个C原子,使这两个C原子相连(整连)或分开(散连),依次连接在母链所剩下的各个C原子上,得多个带1个乙基或两个甲基、主链比母链少两个C原子的异构体骨架。
故己烷(C6H14)共有5种同分异构体。
(2)烯烃同分异构体的书写(限单烯烃范围内)
C5H10同分异构体的书写
a.先写碳骨架异构:
、
、
b.再写官能团位置异构:根据碳4价的原则,在碳骨架异构中找出可能加入双键
的位置(箭头所指位置)。
c.最后写官能团类型异构:
分子式为C5H10的环烷烃:
(3)烃的含氧衍生物同分异构体的书写
书写方法:一般按碳骨架异构→官能团位置异构→官能团类型异构的顺序来书
写。下面以C5H12O为例说明。
a.碳骨架异构:5个碳原子的碳链有3种连接方式:
C—C—C—C—C
b.官能团位置异构:对于醇类,在碳链各碳原子上连接羟基,用“↓”表示连接的
不同位置。
c.官能团类型异构:通式为CnH2n+2O的有机物在中学阶段只能是醇或醚,对于醚
类,位置异构是因氧元素的位置不同而导致的。
分析知分子式为C5H12O的有机物共有8种醇和6种醚,总共14种同分异构体。
2.同分异构体数目的判断方法
(1)基元法
记住常见烃基的异构体种数,可快速判断含官能团有机化合物同分异构体的数目。
—C3H7有两种,—C4H9有4种,—C5H11有8种,如C4H9Cl、C4H9OH、C4H9—CHO等各有
4种同分异构体。
(2)换元法
如:若C3H8的二氯代物有四种同分异构体,则其六氯代物的同分异构体也为四种
(H和Cl相互替代)。
(3)等效氢法
等效氢法是判断同分异构体数目的重要方法,其规律有:
①分子中同一个碳原子上的氢原子等效;
②与同一个碳原子相连的甲基上的氢原子等效。如新戊烷(
)分子中
的12个氢原子是等效的;
③同一分子中处于轴对称位置或镜面对称位置上的氢原子是等效的。如
分子中,在苯环所在的平面内有两条互相垂直的对称轴,故
有两类等效氢;
分子中的18个氢原子是等效的。
等效氢原子的种类数等于一元取代物的种类数。
(4)定一(或二)移一法
对于二元取代物的同分异构体的判定,可固定一个取代基位置,再移动另一取代
基,以确定同分异构体数目。
如:分析C3H6Cl2的同分异构体,可先固定其中一个—Cl的位置,再移动另外一
个—Cl的位置,从而得到其同分异构体为
、
、
、
。
如C3H6ClF的同分异构体(先把氯原子固定在一个碳原子上,用
标
记)。
【思考·讨论】
(1)分子式相同结构不同的有机物互为同分异构体,分子式相同,相对分子质量一定相同,相对分子质量相同的有机物一定是同分异构体吗?
提示:不一定。因为相对分子质量相同分子式不一定相同。例如:乙醇和甲酸相对分子质量都为46。
(2)C4H8属于烯烃的同分异构体有几种?试写出其结构简式。
提示:C4H8属于烯烃的结构有3种,其结构简式分别为
(3)萘(
)的二氯代物有10种,八氯代物有几种?
提示:利用换元法可知,八氯萘可以看成是十氯萘上的两个Cl原子被两个H原子取
代的产物,也有10种。
【案例示范】
【典例】(2020·济南高二检测)某烷烃相对分子质量为86,如果分子中含有
3个—CH3、2个—CH2—和1个
,则该结构的烃的一氯取代物(不考虑立体异
构)最多可能有
( )
A.9种
B.6种
C.5种
D.4种
【解析】选A。根据烷烃的通式CnH2n+2,14n+2=86,解得n=6,该分子是己烷,含有上述基团的分子有CH3CH2CH2CH(CH3)2和CH3CH2CH(CH3)CH2CH3,CH3CH2CH2CH(CH3)2分子是不对称分子,一氯代物有5种,CH3CH2CH(CH3)CH2CH3分子是对称分子,一氯代物有4种,共9种,选A。
【规律方法】同分异构体的书写规律
【迁移·应用】
1.(2018·全国卷Ⅰ)环之间共用一个碳原子的化合物称为螺环化合物,螺[2.2]
戊烷(
)是最简单的一种。下列关于该化合物的说法错误的是
( )
A.与环戊烯互为同分异构体
B.二氯代物超过两种
C.所有碳原子均处同一平面
D.生成1
mol
C5H12至少需要2
mol
H2
【解析】选C。环戊烯与螺[2.2]戊烷(
)的分子式均为C5H8,二者互为同分
异构体,故A正确;二氯取代中可以取代同一个碳原子上的氢原子,也可以取代同
侧碳原子上或者两侧的碳原子上的氢原子……,因此其二氯代物超过两种,B正
确;螺[2.2]戊烷(
)中中心原子含有四个单键,故所有碳原子一定不处于
同一平面,C不正确;螺[2.2]戊烷(
)的分子式为C5H8,若生成1
mol
C5H12则
至少需要2
mol
H2,D正确。
2.主链上有6个碳原子,有甲基、乙基两个支链的烷烃有
(
)
A.2种
B.3种
C.4种
D.5种
【解析】选C。主链6个C,则乙基只能在第3个C上,甲基可以在中间所有的C上,该分子不对称,甲基分别在中间四个碳原子上,共有4种。
【补偿训练】
下列各组指定物质的同分异构体数目相等的是
( )
A.乙烷的二氯代物和丙烷的一氯代物
B.丙烷的一氯代物和戊烷
C.苯的二氯代物和苯的一硝基代物
D.C3H5Br3和C5H11Br
【解析】选A。乙烷的二氯代物有2种同分异构体,丙烷的一氯代物也有2种同分异构体,A项正确;丙烷的一氯代物有2种同分异构体,戊烷有3种同分异构体,B项错误;苯的二氯代物有3种同分异构体,苯的一硝基代物只有1种结构,C项错误;C3H5Br3有5种同分异构体,而C5H11Br有8种同分异构体,D项错误。
【素养提升】
有机环状化合物在新型材料、新型药物等方面应用十分广泛,除传统的环烷烃、芳香烃之外,近年来科学家用合成方法制备了多种新的环状有机物,例如环辛四烯、正四面体烷、金刚烷、棱晶烷、立方烷等,其分子具有如下图所示立体结构。
(1)上述八种环状有机物中,哪些物质之间互为同分异构体?
提示:苯与棱晶烷的分子式均为C6H6,环辛四烯与立方烷的分子式均为C8H8,但是它们的结构都不相同,故互为同分异构体。
(2)上述物质中,一氯代物种类最多的物质是哪一种?二氯代物最多的呢?
提示:一氯代物最多的是金刚烷,有2种,其他七种物质的一氯代物均为1种;二氯代物种类最多的是金刚烷,有6种。
1.下列关于有机化合物的表示方法中不正确的是
( )
A.乙烯:CH2CH2
B.异戊烷:
C.乙酸乙酯:CH3COOCH2CH3
D.甲烷:
【解析】选A。A、C两项表示物质的结构简式,其中乙烯结构简式中的碳碳双键不可省略,应写成CH2==CH2;B项表示物质的键线式;D项表示物质的结构式。
2.(2020·济宁高二检测)下列物质的分子是平面结构的是
( )
A.CH4 B.CH2==CH2
C.HC≡C—CH3
D.
【解析】选B。有机化合物分子中,碳原子最外层有四对共用电子。若形成四个相同单键,如CH4,则键角为109°28′,为正四面体形;若形成双键,键角为120°,如CH2==CH2,属平面结构;若形成三键,键角为180°,如HC≡CH,属直线形。C选项中甲基上的氢原子与其他原子不共面。
3.
是由苯环和甲基结合而成的,苯不能够使酸性KMnO4溶液褪色,而甲苯
能够使酸性KMnO4溶液褪色是因为
( )
A.烷烃能使酸性KMnO4溶液褪色
B.苯环能使酸性KMnO4溶液褪色
C.苯环使甲基的活性增强而导致的
D.甲基使苯环的活性增强而导致的
【解析】选C。有机化合物分子中邻近基团间往往存在着相互影响,这种影响会使有机化合物表现出一些特性。甲苯能够使酸性KMnO4溶液褪色是苯环使甲基的活性增强而导致的。
4.轴烯是一类独特的星形环烃。三元轴烯(
)与苯
( )
A.均为芳香烃
B.互为同素异形体
C.互为同系物
D.互为同分异构体
【解析】选D。三元轴烯与苯分子式都是C6H6,二者分子式相同,结构不同,互为同
分异构体,D项正确。
5.分子式为C4H10O并能与金属钠反应放出氢气的有机物有(不含立体异构)
( )
A.3种
B.4种
C.5种
D.6种
【解析】选B。分子式为C4H10O是醇或醚。若物质可以与金属Na发生反应放出氢气,则该物质是醇,C4H10O可以看成是C4H10的分子中的一个H原子被羟基—OH取代产生的,—C4H9有4种不同的结构,因此符合该性质的醇的种类也应该是4种。
6.已知碳碳单键可以绕键轴自由旋转,某烃的结构简式如图。下列有关说法正确的是
( )
A.分子中至少有9个碳原子处于同一平面上
B.分子中至少有10个碳原子处于同一平面上
C.分子中至少有11个碳原子处于同一平面上
D.分子中所有的原子可能共平面
【解析】选C。将题给分子表示为
,容易看出,两个苯环所在的
平面可能重合,而苯环上所连的其他原子均可视为取代了苯分子中的氢原子,因
而与苯环共平面,所以该烃中所有的碳原子都可能共平面,但不是所有原子共平
面。当连接两苯环的碳碳单键旋转时,两个苯环可能不共面,但由于带“
”的6
个碳原子共线,所以至少有11个碳原子处于同一平面上,C正确。
7.CO2的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸的反应:
3NH3+3CO2
+3H2O
(1)其分子式是什么?如果把氮原子换成碳原子分子式又是什么?
提示:由三聚氰酸的结构简式可知其分子式为C3H3N3O3;换后多了三个氢原子,所以是C6H6O3。
(2)分子中有哪些极性共价键?
提示:分子中存在O—H、C—O、N—C、N
C键,都属于极性键,所以分子中不存在非极性键。
(3)假设六元环是和苯环一样的平面结构,此分子中所有的原子是否一定共面?
提示:不一定。因为羟基和另外一个原子相连时是V形结构,所以所有原子不一定共面。
二 有机化合物的结构与性质
【基础达标】(40分钟 70分)
一、选择题(本题包括10小题,每小题5分,共50分)
1.下列有机物分子中的所有原子一定处于同一平面上的是
( )
【解析】选A。甲基是四面体结构,所以B、D中所有原子一定不共面,由于单键可以旋转,所以C不一定共面。
2.(2020·三亚高二检测)下列有机物的同分异构体数目判断错误的是
( )
选
项
有机物
同分异构
体数目
A
分子式为C5H12
3
B
分子式为C5H10,能使溴的四氯化碳溶液褪色
5
C
分子式为C4H10O,能与Na反应生成氢气
4
D
分子式为C4H8O2,能与NaHCO3反应
3
【解析】选D。戊烷C5H12有3种同分异构体,分别为正戊烷、异戊烷与新戊烷,A正确;能使溴的四氯化碳溶液褪色,说明C5H10为戊烯,分别为1-戊烯、2-戊烯、2-甲基-1-丁烯、2-甲基-2-丁烯、3-甲基-1-丁烯,故共有5种同分异构体,B正确;能与Na反应生成氢气说明为醇类,C4H10O可写成C4H9OH,丁基有4种结构,故共有4种醇,C正确;能与NaHCO3反应说明为羧酸,C4H8O2可写成C3H7COOH,丙基有2种,故有2种丁酸,D错误。
3.碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图。下列有关该物质的说法正确的是
( )
A.分子式为C3H2O3
B.分子中含6个σ键
C.分子中只有极性键
D.8.6
g该物质完全燃烧得到6.72
L
CO2
【解析】选A。由图示可知,该物质的分子式为C3H2O3,A项正确;分子中的碳碳双键和碳氧双键中各有一个σ键,碳氧单键全部是σ键(4个),碳氢键也是σ键(2个),分子中共有8个σ键,B项错误;分子中的碳氧键和碳氢键都是极性键,而碳碳键是非极性键,C项错误;8.6
g该物质的物质的量为0.1
mol,完全燃烧后得到0.3
mol
CO2,在标准状况下的体积是6.72
L,D项未指明是否在标准状况下,D项错误。
4.某烃有两种或两种以上的同分异构体,其同分异构体中的某一种烃的一氯代物只有一种,则这种烃可能是
( )
①分子中具有7个碳原子的芳香烃
②分子中具有4个碳原子的烷烃
③分子中具有5个碳原子的烷烃
④分子中具有8个碳原子的烷烃
A.①②
B.②③
C.③④
D.②④
【解析】选C。分子中含有1~10个碳原子的烷烃中,一氯代物只有一种的有CH4、C(CH3)4和CH3CH3、(CH3)3CC(CH3)3,其中CH4、CH3CH3没有同分异构体,不合题意,另外两种的分子式分别为C5H12和C8H18,③、④符合题意,C项正确。
5.(2020·保定高二检测)烯烃、炔烃、芳香烃和乙醛都能发生加成反应,这是因为它们都含有
( )
A.单键
B.不饱和碳原子
C.非极性键
D.碳原子
【解析】选B。只有具有不饱和碳原子的有机化合物才能发生加成反应。
6.分子式为C7H16,且有一个支链的有机物有(不考虑立体异构)
( )
A.1种
B.2种
C.3种
D.4种
【解析】选C。分子式为C7H16,且有一个支链,如为甲基,则主链有6个C原子,由结构对称可知为
CH3CH(CH3)CH2CH2CH2CH3、
CH3CH2CH
(CH3)CH2CH2CH3;
如支链为乙基,则主链为5个C原子,为
CH3CH2CH(CH2CH3)CH2CH3,共3种。
7.(双选)霉酚酸是一种生物活性化合物。下列有关霉酚酸的说法正确的是
( )
A.分子式为C17H20O6
B.处于同一平面的原子至多9个
C.只有2种官能团
D.一定条件下,
1
mol霉酚酸最多可与4
mol
H2反应
【解析】选A、D。由结构简式可知该有机物的分子式为C17H20O6,A正确;分子中有苯环,共面原子数至少为12个,B错误;有羟基、醚键、羧基、酯基和碳碳双键五种官能团,C错误;分子中有一个苯环和一个碳碳双键,1
mol霉酚酸最多可与
4
mol
H2反应,D正确。
8.下列各组物质不属于同分异构体的是
( )
A.2,2-二甲基丙醇(
)和2-甲基丁醇(
)
B.
和
C.2-甲基丁烷(
)和戊烷
D.甲基丙烯酸(
)和甲酸丙酯
【解析】选D。甲基丙烯酸的分子式为C4H6O2,甲酸丙酯(HCOOC3H7)的分子式为C4H8O2,故二者不属于同分异构体。
9.以物质a为原料,制备物质(金刚烷)的合成路线如图所示:
关于以上有机物说法中错误的是
( )
A.物质b的分子式为C10H12
B.b可以由2
mol
a反应得到,发生的是加成反应
C.物质c与物质d互为同分异构体
D.物质d的二氯代物有4种
【解析】选D。A.根据键线式的特点,物质b的分子式为C10H12,A正确;B.b中含有
10个碳原子,可以由2
mol
a发生加成反应得到,反应类型为加成反应,B正确;C.
物质c与物质d的分子式为C10H16,分子式相同,结构不同互为同分异构体,C正确;
D.给d中碳原子编号
,其中有2种H(其中1、3、5、7等效,2、4、6、
8、9、10等效),一氯代物有2种,二氯代物先固定一个Cl在1号碳,另一个Cl可在
2、3、4号碳,共3种,再固定1个Cl在2号碳,另一个Cl可在2、4、6号碳,
合计6种,D错误。
10.(2020·潍坊高二检测)有4种碳骨架如下的烃。下列说法正确的是
( )
①a和d是同分异构体
②b和c是同系物
③a和d都能发生加聚反应
④只有b和c能发生取代反应
A.①②
B.①④
C.②③
D.①②③
【解析】选A。由图可知a为2-甲基丙烯[(CH3)2C﹦CH2],分子式为C4H8;
b为新戊烷[(CH3)4C],分子式为C5H12;c为2-甲基丙烷[(CH3)3CH],分子式为C4H10;d为环丁烷,分子式为C4H8,故可知①②正确;d不能发生加聚反应,故③错;a、d也能发生取代反应,故④错;选A。
二、非选择题(本题包括2小题,共20分)
11.(10分)某有机化合物的结构如下,分析其结构并回答下列问题:
(1)写出其分子式:__________________。?
(2)其中含有________个不饱和碳原子,分子中有________种双键。?
(3)分子中的极性键有?______________(写两种即可)。?
(4)分子中的饱和碳原子有________个;一定与苯环处于同一平面的碳原子有________个。?
(5)分子中—C≡C—H的结构中碳氢键和碳碳三键之间的键角约为__________。
【解析】与4个原子或原子团相连的碳原子是饱和碳原子,反之是不饱和碳原子。苯环结构中,环上的6个碳原子和与它们直接相连的6个原子共12个原子一定共面,因此直接与苯环相连的碳原子一定与苯环共平面,这样的碳原子有3个,由于碳碳三键是直线形,使得这两个碳原子均与苯环共平面,故一共有4个碳原子与苯环位于同一平面。
答案:(1)C16H16O5 (2)12 2 (3)C﹦O键、C—H键、O—H键、C—O键(写出两种即可)
(4)4 4 (5)180°
12.(10分)(1)有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是________。?
A.1
mol甲分子内含有10
mol共价键
B.由乙分子构成的物质不能发生氧化反应
C.丙分子中只含有非极性键
D.分子丁显然是不可能合成的
(2)“立方烷”是一种新合成的烃,其分子为正方体结构,其碳骨架结构如图所示。
①“立方烷”的分子式为__________。?
②碳碳键键角是________(填度数)。?
(3)化学式为C6H12的某烯烃的所有碳原子都在同一个平面上,则该烯烃的结构简式为________,键线式为________,分子式为C10H18的链烃分子中所有碳原子也可能在同一平面上,它的结构简式为________(只写一种)。?
【解析】(1)1
mol甲分子中含有6
mol碳碳键,4
mol碳氢键,A正确;乙分子可以发生燃烧反应,即氧化反应,B错误;丙分子中既有极性键又有非极性键,C错误;丁分子中碳不符合四价键原则,不可能合成,D正确。
(2)①立方体为一对称结构,有8个顶点,每个顶点为1个碳原子,这个碳原子和相邻的3个顶点上的碳原子以共价键结合,碳原子有4个价电子,所以每个碳原子还能再和1个氢原子相结合,故立方烷的分子式为C8H8。②在立方烷中每个面上都是正方形结构,每2个碳碳共价键构成一个直角,所以键角(碳碳共价键的夹角)是90°。
(3)C6H12中有6个碳原子,根据C2H4分子的6个原子共平面的原理,C6H12中6个碳处于C2H4中6个原子位置,则能使6个碳原子共平面。C10H18与C10H22比较分子中少4个H,可能会有一个三键或两个双键,但含有一个三键不可能使10个碳原子处于同一平面上,因此应含有两个双键。
答案:(1)BC (2)①C8H8 ②90°
【能力提升】(20分钟 30分)
一、选择题(本题包括2小题,每小题8分,共16分)
13.(2020·威海高二检测)医学上在对抗癌物质的研究中发现
具
有抗癌作用,而
没有抗癌作用,对此下列有关叙述正确的是
( )
A.两者互为同分异构体,都是以Pt原子为中心的四面体结构
B.两者互为同分异构体,都是以Pt原子为中心的平面结构
C.两者为同一物质,都是以Pt原子为中心的四面体结构
D.两者为同一物质,都是以Pt原子为中心的平面结构
【解析】选B。由信息可知两种化合物性质不同,则其结构不同,两者互为同分异构体,且为平面结构。若为四面体结构,则是一种物质,不互为同分异构体。
14.(双选)2015年10月,中国药学家屠呦呦获得了诺贝尔生理学或医学奖,获奖理由是“因为发现青蒿素——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”。如图是青蒿素的结构简式,下列有关青蒿素的说法中不正确的是
( )
A.青蒿素的分子式为C15H22O5
B.青蒿素有—O—O—键,具有较强的氧化性
C.青蒿素易溶于水、乙醇、苯
D.青蒿素不易发生水解
【解析】选C、D。A项,根据青蒿素的结构简式判断其分子式为C15H22O5,正确;B项,青蒿素分子中含有—O—O—键,具有较强的氧化性,正确;C项,该有机物含有较多疏水基,难溶于水,错误;D项,青蒿素分子中含有—COO—,可在碱性条件下发生水解,错误。
二、非选择题(本题包括1小题,共14分)
15.丙烯酰胺是一种重要的有机合成中间体。它的球棍模型如下图所示:(图中“棍”代表单键、双键或三键,不同颜色的球表示不同原子:C、H、O、N)
(1)丙烯酰胺的分子式为____________,结构简式为______________。?
(2)有关丙烯酰胺的说法正确的是________。?
A.丙烯酰胺分子内所有原子不可能都在同一平面内
B.丙烯酰胺属于烃的含氧衍生物
C.丙烯酰胺能够使酸性高锰酸钾溶液褪色
D.丙烯酰胺能够使溴的四氯化碳溶液褪色
(3)工业上生产丙烯酰胺的方法之一是(反应均在一定条件下进行):
反应Ⅰ和反应Ⅱ都是原子利用率100%的反应,反应Ⅰ所需另一反应物的分子式为________,反应Ⅱ的方程式为________。?
(4)聚丙烯酰胺(PAM)是一种合成有机高分子絮凝剂,写出由丙烯酰胺合成聚丙烯酰胺的化学方程式______________。?
【解析】该题给出的信息是丙烯酰胺的球棍模型,通过模型中球的颜色及大小可以确定这些“球”所代表的原子,通过原子类别可以确定“棍”为单键、双键还是三键。通过丙烯酰胺分子的球棍模型可知,其含有4种原子,在有机化合物中最小的原子是氢原子,故5个白球就是氢原子,通过“丙”字可知三个“绿球”是碳原子,而直接以单原子连接在碳原子上的多为氢原子和氧原子,故“红球”为氧原子,那么“蓝球”就是氮原子。
(1)由上面的分析可知丙烯酰胺的分子式为C3H5ON,结构简式为
。
(2)有双键能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色。分子中有氨基呈
三角锥形,所有分子不可能共面。分子中有氮元素,不是烃的含氧衍生物。
(3)对于原子利用率100%的反应,其中一种反应物的推断可以采用“减法”,即
用生成物减去一种反应物。由此可知反应Ⅰ所需另一反应物的分子式为HCN;反
应Ⅱ所需另一反应物的分子式为H2O。
(4)丙烯酰胺中的碳碳双键可以发生聚合反应(加聚反应)而生成聚丙烯酰胺。
答案:
