2020-2021学年高二化学鲁科版(2019)选择性必修3第一章第三节烃— 烷烃及其性质课件(共96张ppt)
文档属性
| 名称 | 2020-2021学年高二化学鲁科版(2019)选择性必修3第一章第三节烃— 烷烃及其性质课件(共96张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-23 00:00:00 | ||
图片预览






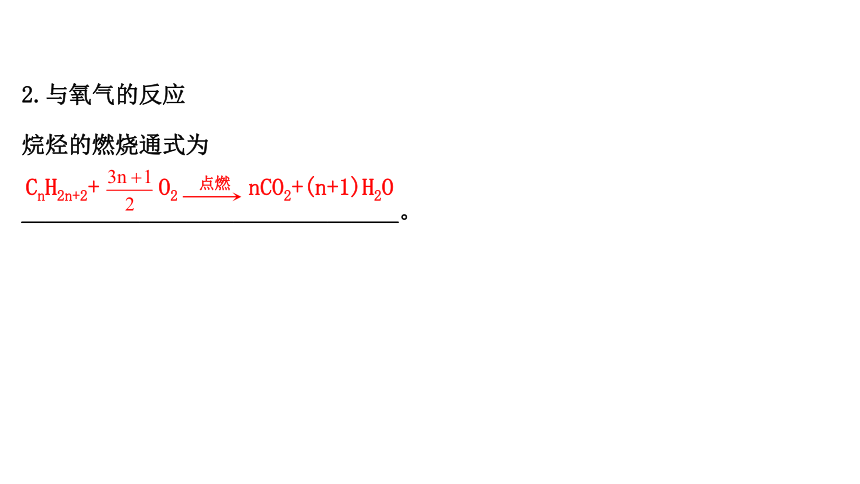




文档简介
(共96张PPT)
第3节 烃
第1课时 烷烃及其性质
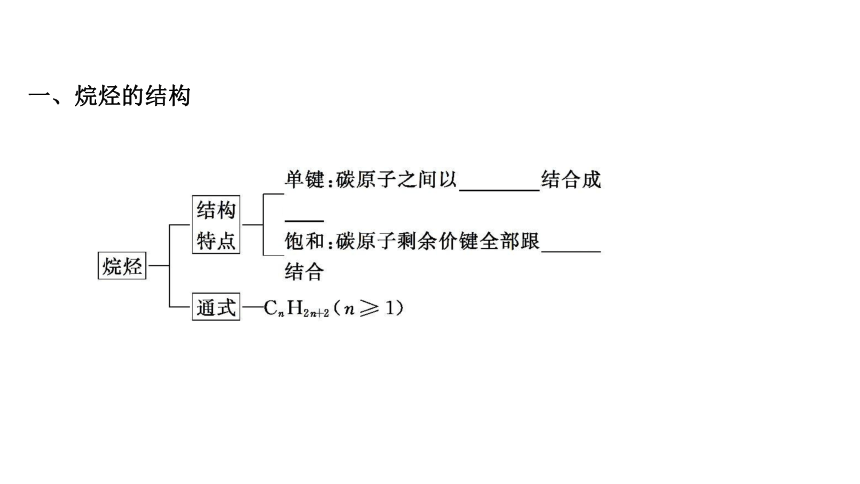
一、烷烃的结构
二、烷烃的物理性质
1.递变规律(随碳原子数n递增)
2.相似性
烷烃均_____水,相对密度均_____水的密度。
【?判一判】
(1)分子中全是碳碳单键的烃一定是烷烃。
( )
提示:×。环烷烃中碳原子也全是碳碳单键。
(2)C2H6、C3H8、C4H10的熔沸点依次升高。
( )
提示:√。烷烃随着碳原子数的增多熔沸点升高。
难溶
小于
三、烷烃的化学性质
烷烃的化学性质与甲烷类似,通常较稳定,与_____________________不反应,
但一定条件下可燃烧,与氯气等发生取代反应。
1.与卤素单质的反应
在光照条件下,烷烃与Cl2、Br2等卤素单质的气体发生取代反应。
(1)乙烷在光照下与氯气发生取代反应生成一氯代物的化学方程式为
____________________________。
强酸、强碱及强氧化剂
光
CH3CH3+Cl2
CH3CH2Cl+HCl
(2)分子中碳链较长的烷烃与氯气反应时,不同_______断裂可以得到不同的取代
产物,如丙烷与氯气在光照条件下发生取代反应的产物是
(1-氯丙烷)、
(2-氯丙烷)。丁烷如果和氯气发生取代反应生成一氯代物,会有多少种?
提示:四种。CH2(Cl)CH2CH2CH3
,CH3CH(Cl)CH2CH3
,C(Cl)(CH3)3,CH(CH3)2CH2Cl。
碳氢键
2.与氧气的反应
烷烃的燃烧通式为
________________________________。
点燃
CnH2n+2+
O2
nCO2+(n+1)H2O
【?情境·思考】天然气的主要成分是甲烷,是一种十分重要的“清洁能源”,与液化石油气(主要成分是丙烷、丁烷)一样都是常用的家用燃气。随着现代社会对环境保护要求的提高,液化石油气正逐渐被天然气所取代。居民家庭中在将液化石油气更换为天然气时,通常需要更换燃气灶具或调整进气量,为什么?
提示:等物质的量的天然气与液化石油气完全燃烧耗氧量不同,即在燃气进气量一致的情况下,充分燃烧需要的空气量不同,因此需要更换燃气灶具或调整进气量。
知识点一 烷烃的取代反应
反应条件
光照
反应物
烷烃和气态卤素单质(烷烃与卤素单质的水溶液不反应)
化学键变化
断键:C—H键和X—X键
成键:C—X键和H—X键
取代特点
分子中的氢原子被卤素原子逐步取代,往往是各步反应同时发生
产物
特点
种类
多种卤代烷烃的混合物,HX的物质的量最多
产物
的量
①根据碳元素守恒,烷烃的物质的量等于所有卤代烷烃的物质的量之和
②根据取代反应的特点,有机物中卤素的物质的量等于HX的物质的量等于反应了的X2的物质的量,即反应了的n(X2)=n(一卤代物)+2n(二卤代物)+3n(三卤代物)+……=n(HX)
关键能力·素养形成
【方法规律】关于取代反应和置换反应的判断的简单方法
(1)看参与反应的物质类别:若物质类别是无机物,一定是置换反应,若物质类别均是有机物,则一定不是置换反应。
(2)看产物中是否有单质生成:若产物中有单质生成,一定不是取代反应。
【思考·讨论】
(1)烷烃的取代产物卤代烃是一类重要的有机化工原料,请问通过烷烃和卤素单质1∶1混合在光照的条件下能不能得到纯净的一卤代物?
提示:不能。不管比例如何,烷烃和卤素单质的反应都不能停留在第一步,所以得到的卤代烃是混合物。
(2)己烷能不能和溴水在光照下发生取代反应?如果把己烷和溴水混合在一起振荡后有什么现象?
提示:不能。卤素单质的水溶液不能和烷烃发生取代反应。如果把己烷和溴水混合,己烷能把溴单质从水中萃取出来,所以现象是液体分层,上层溶液为橙红色,下层无色。
【案例示范】
【典例】把1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在盛有Na2SiO3溶液的水槽里,放在光亮处。
(1)试管中观察到的现象:
①_________________;?
②_________________;?
③_________________。?
(2)水槽中观察到的现象:_____________________________。
(3)写出有关反应的化学方程式
①CH4和Cl2反应(第一步)
________________。
②Na2SiO3溶液中发生的反应________________。??
(4)待反应完成后,测得四种取代物物质的量相等,则反应中消耗Cl2的体积为____________。?
【解析】CH4和Cl2在光照条件下生成CH3Cl、CH2Cl2、CHCl3、CCl4、HCl,随着反应的进行,Cl2不断消耗,黄绿色逐渐变浅。又由于生成的CH2Cl2、CHCl3、CCl4常温下均为无色油状液体,使试管壁上有油滴出现。因生成的HCl易溶于水,反应后试管内气体压强减小,液面在试管内上升。HCl溶于水后与Na2SiO3反应生成白色絮状沉淀。因为CH4与Cl2发生取代反应生成的4种取代产物中的碳原子均来自CH4,由碳原子守恒可知,1
mol
CH4共生成1
mol
取代产物,且每一种取代产物物质的量均为0.25
mol。由于CH3Cl、CH2Cl2、CHCl3、CCl4分子中的氯原子均来自Cl2,
由CH4和Cl2反应的方程式知有机物中含有氯原子的物质的量:0.25
mol+0.25
mol
×2+0.25
mol×3+0.25
mol×4=2.5
mol。Cl2中进入HCl和进入有机物的氯原子的物质的量相同,故n(Cl2)=2.5
mol。
答案:(1)①气体颜色逐渐变浅
②试管中液面上升
③试管壁上有油状液滴
(2)有白色絮状沉淀生成
(3)①CH4+Cl2
CH3Cl+HCl
②Na2SiO3+2HCl
H2SiO3↓+2NaCl (4)2.5
【母题追问】若将Na2SiO3溶液改为紫色石蕊试液或浓氨水,则现象是
__________________________________________________________________。?
提示:若水槽中改盛紫色石蕊试液,HCl溶解后溶液显酸性,试液显红色。若水槽中改盛浓氨水,挥发出的氨气与试管中生成的HCl气体相遇会产生白烟。
【易错提醒】烷烃与卤素单质发生取代反应两个注意事项
(1)烷烃只能与卤素单质在光照条件下发生取代反应,不能与其水溶液发生取代反应。取代反应得到的不只是一氯代物,烷烃分子中的所有氢原子都可被氯原子取代。
(2)烷烃和氯气发生取代反应,有1
mol
H原子被取代,生成1
mol
HCl,消耗1
mol
Cl2,因此参加反应的Cl2的物质的量与生成的HCl的物质的量相等;生成物中HCl最多。
【迁移·应用】
1.将试管中的甲烷和氯气光照一段时间后,拔开橡胶塞,实验过程中不可能观察到的现象是
( )
A.试管中气体的黄绿色变浅
B.试管中有火星出现
C.试管内壁有油状液滴出现
D.试管口有白雾
【解析】选B。甲烷和氯气光照一段时间后试管内气体颜色逐渐变浅,内壁有油状液滴出现,拔开橡胶塞试管口有少量白雾出现。
2.(2018·全国卷Ⅱ)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是
( )
【解析】选D。甲烷与氯气发生取代反应生成CH3Cl、CH2Cl2、CHCl3、CCl4和HCl,因此观察到试管内颜色变浅,生成的CH2Cl2、CHCl3、CCl4为油状液体,且氯气易溶于有机物,故观察到试管内壁有浅黄色的油状液滴,只有CH3Cl和HCl为气体,因此反应后气体的体积减小,且HCl易溶于水,因此导致试管内压强减小,饱和食盐水会进入试管内形成一段水柱,因此答案为D。
【补偿训练】
如图,一端封闭的U形管,封闭着的一端有一段CH4和Cl2的混合气体,在水平部分有一段气柱,其他两段为液柱,已知液体与气体不反应,使CH4和Cl2在稍暗的光线下缓慢反应,则中间气柱的长度如何变化(假设中间气柱未移出U形管的水平部分)
( )
A.变大 B.变小
C.不变
D.难以确定
【解析】选A。在光照条件下,CH4与Cl2反应可生成多种产物,其中有3种产物(CH2Cl2、CHCl3、CCl4)常温下为液体,而使封闭一端气体的物质的量减小,故压强减小,左侧液面上升,右侧液面下降,两侧液柱差竖直长度减小,使水平处气柱压强减小,因温度不变故气柱体积增大。
【素养提升】
氯乙烷具有冷冻麻醉作用,从而使局部产生快速镇痛效果,氯乙烷喷雾剂主要用于运动中各种急性闭合性损伤,如肌肉拉伤、挫伤、关节扭挫伤以及骨折、脱臼整复。该喷雾剂的主要成分为氯乙烷,其结构简式为CH3—CH2Cl。
(1)氯乙烷还属于烷烃吗?
提示:不属于烷烃,氯乙烷中除含有碳、氢元素外,还含有氯元素,属于烃的衍生物。
(2)根据所学知识,探究以下制取氯乙烷的可行性。
①乙烷和氯气发生取代反应。
提示:乙烷和氯气发生取代反应得到一氯乙烷到六氯乙烷及HCl的混合物。方案不可行。
②乙烯和氯化氢发生加成反应。
提示:乙烯和氯化氢发生加成反应得到纯净的一氯乙烷,方案可行。
知识点二 烃燃烧的规律和应用
【重点释疑】
1.烃的燃烧规律
(1)烃的燃烧通式:CxHy+
O2
xCO2+
H2O。
(2)烃燃烧的三个规律
①等质量的烃完全燃烧
②等物质的量的烃完全燃烧
a.烃分子中
的数值越大,则耗氧量越大。
b.烃分子中x的数值越大,完全燃烧生成的CO2越多。
c.烃分子中y的数值越大,完全燃烧生成的H2O的物质的量越多。
③最简式相同的烃燃烧
a.最简式相同的烃,C、H的质量分数相同。
b.等质量的最简式相同的烃完全燃烧时,耗氧量相同、产生的CO2、H2O的质量、
物质的量均相同。
2.燃烧规律的应用
(1)若反应前后温度保持在100
℃以上,则烃完全燃烧前后的体积变化为
CxHy+
O2
xCO2+
H2O ΔV
1
x+
x
-1
故反应前后气体体积的变化ΔV仅与氢原子数y有关。
(2)若反应前后温度低于100
℃,此时气体体积一定是减少的,减少的气体体积
为ΔV=1+
,也与氢原子数有关。
【易错提醒】利用烃类燃烧的通式进行计算时的注意点
(1)水的状态是液态还是气态,从条件上看温度是在100
℃以下还是以上。
(2)气态烃完全燃烧前后,体积变化值也只与烃中的氢原子个数有关,根据体积
差值可以求出氢原子的个数或氢原子的平均个数。
(3)要注意检验氧气是否足量。
【思考·讨论】
(1)等物质的量的甲烷、乙烷、丙烷完全燃烧消耗氧气的物质的量之比为多少?
提示:4∶7∶10。由烃类燃烧的通式CxHy+
O2
xCO2+
H2O可知,等物质
的量的烃完全燃烧时耗氧量的大小取决于
的数值大小,从而可得其比值为
4∶7∶10。
(2)1
mol的烷烃同系物分别充分燃烧时,其耗氧量有何特点?
提示:1
mol有机物每增加一个“CH2”,耗O2量增加1.5
mol。烷烃同系物在分
子组成上若相差x个CH2原子团,耗氧量则相差1.5x
mol。
【典例】(2020·青岛高二检测)现有CH4、C2H4、C2H6、C3H6、C3H8五种有机物。
(1)等质量的以上物质中,在相同状况下体积最大的是__________;?
(2)等质量的以上物质完全燃烧时,消耗O2的量最多的是__________;?
(3)同状况、等体积、等物质的量的以上物质完全燃烧时,消耗O2的量最多的是__________;?
(4)等质量的以上物质完全燃烧时,生成的CO2最多的是__________,生成水最多的是__________。?
【解题指南】解答本题应注意以下两点:
(1)等物质的量的烃完全燃烧时烃分子中
的数值越大,则耗氧量越大。
(2)等质量的烃完全燃烧时烃分子中y/x越大,则耗氧量越大。
【解析】V=Vm·
,等质量时,气体体积与气体的摩尔质量成反比,所以等质量
的五种气体,在相同状况下,CH4的体积最大。对于等质量的烃CxHy,完全燃烧时
耗氧量的多少取决于
的大小,
越大,耗氧量越多,生成的H2O物质的量越
大,CO2的物质的量越小。同状况、等体积、等物质的量的烃CxHy完全燃烧,
耗氧量取决于
的相对大小。
答案:(1)CH4 (2)CH4 (3)C3H8 (4)C2H4、C3H6 CH4
【母题追问】(1)在120
℃,1.01×105
Pa时,以上气态烃和足量的O2完全燃烧,相同条件下测得反应前后气体体积没有发生变化的是哪些?
提示:CH4、C2H4。水为气体且氢原子数为4时反应前后体积不变。
(2)如果1
mol两种混合气体完全燃烧生成1.5
mol的二氧化碳和2
mol的水,混合气体可能是以上五种中的哪两种?
提示:碳原子数平均是1.5,所以一定有CH4,氢原子平均是4个,所以另外一种烃也是4个,即C2H4。
【规律方法】判断混合烃的组成规律
在同温同压下,1体积气态烃完全燃烧生成x体积CO2和y体积水蒸气,当为混合烃时,若x<2,则必含CH4,若y<2,则必含C2H2。
【迁移·应用】
1.A、B两种烃的混合物,当混合物的质量一定时,无论A、B以何种比例混合,完全燃烧产生的CO2的量均相等。在①同分异构体,②同系物,③具有相同的最简式,④含碳的质量分数相同,选项中符合上述条件的组合是
( )
A.①②④ B.①③④ C.②③④ D.①②③
【解析】选B。混合物的质量一定,无论以何种比例混合,燃烧产生的CO2量均相等,说明A、B中的碳质量分数相等,也可以是最简式相同。同分异构体分子式相同,最简式也相同。
2.某烃A的相对分子质量为84。回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是____________(填字母)。?
A.C7H12O2 B.C6H14
C.C6H14O
D.C7H14O3
(2)若烃A为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。A的结构简式为________________。?
(3)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为__________________。?
【解析】相对分子质量为84的烃,其分子式为C6H12,为烯烃或环烷烃。
(1)1
mol
C7H12O2充分燃烧消耗氧气9
mol,1
mol
C6H14充分燃烧消耗氧气
9.5
mol,1
mol
C6H14O充分燃烧消耗氧气9
mol,1
mol
C7H14O3充分燃烧消耗氧
气9
mol,应选B。
(2)链烃A与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种,说明该
烃分子高度对称,结构简式为
(CH3)2C====C(CH3)2。
(3)不能使溴水褪色,说明为饱和烃,一氯代物只有一种,则只能为环己烷。
答案:(1)B (2)(CH3)2C====C(CH3)2 (3)
【补偿训练】
一种气态烷烃和一种气态烯烃,它们分子里的碳原子数相等。将1.0体积这种混合气体在氧气中完全燃烧,生成2.0
体积的CO2和2.4
体积的水蒸气(气体
体积均在相同状况下测定),则混合气体中烷烃和烯烃的体积比为
( )
A.3∶1 B.1∶3
C.2∶3 D.3∶2
【解析】选C。根据阿伏加德罗定律,相同状况下,气体的体积之比等于物质的量之比,可知1
mol混合烃充分燃烧后生成2
mol
CO2和2.4
mol
H2O,则混合烃的平均分子组成为C2H4.8。又知烷烃和烯烃分子里的碳原子数相同,可以判定它们分别是C2H6和C2H4。无论C2H6与C2H4以怎样的体积比混合,它们的平均碳原子个数都是2。因此符合题意的烷烃和烯烃的体积比,将由它们分子里所含的氢原子个数决定。可用十字交叉法求解:
【课堂回眸】
1.如图所示均能表示甲烷的分子结构,下列说法错误的是
( )
A.Ⅰ将各原子看成了质点,为立体结构示意图
B.Ⅱ为电子式,表示甲烷分子中有8个电子
C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键
D.Ⅳ为空间填充模型,能表示出甲烷的空间构型及各原子的相对大小
【解析】选B。Ⅱ表示电子式,但略去了碳原子的内层电子,甲烷分子中应含有10个电子。
2.下列关于烷烃性质的叙述中,不正确的是
( )
A.烷烃随相对分子质量的增大,熔点、沸点逐渐升高,常温下的状态由气态递变到液态,相对分子质量大的则为固态
B.烷烃的密度随相对分子质量的增大逐渐增大
C.烷烃跟卤素单质在光照条件下能发生取代反应
D.烷烃能使溴水、酸性KMnO4溶液都褪色
【解析】选D。烷烃是饱和烃,化学性质稳定,具有代表性的反应是取代反应,C对;与烷烃发生取代反应的必须是卤素单质,溴水不能与烷烃反应,酸性KMnO4溶液也不能将烷烃氧化,D错。
3.物质的量相同的下列烃,完全燃烧,耗氧量最多的是
( )
A.C2H6 B.C4H6
C.C5H10
D.C7H8
【解析】选D。依据1
mol
CxHy耗氧
mol来确定:1
mol
C2H6耗氧2
mol+
mol=3.5
mol;1
mol
C4H6耗氧4
mol
+
mol=5.5
mol;1
mol
C5H10
耗氧
5
mol+
mol=7.5
mol;1
mol
C7H8耗氧7
mol+
mol=9
mol。
4.标准状况下将35
mL气态烷烃完全燃烧,恢复到原来状况下,得到二氧化碳气体140
mL,则该烃的分子式为
( )
A.C5H12
B.C4H10
C.C2H6
D.C3H8
【解析】选B。根据同温、同压下气体的体积比等于分子数比,烷烃分子数与二氧化碳气体分子数比为35
mL/140
mL=1/4,该烃1个分子中含有4个碳原子,即该烷烃为丁烷。
5.已知液化气的主要成分是丙烷,下列有关丙烷的叙述不正确的是
( )
A.是直链烃,但分子中碳原子不在一条直线上
B.在光照条件下能够与氯气发生取代反应
C.丙烷的球棍模型图为
D.1
mol丙烷完全燃烧消耗5
mol
O2
【解析】选C。C3H8是直链烃,其中的碳原子为饱和碳原子,和与之相邻的四个原子形成四面体结构,故3个碳原子不在一条直线上,A项正确;C3H8在光照时与Cl2发生取代反应,B项正确;丙烷的球棍模型图中漏掉了两个氢原子,C项错误;1
mol丙烷完全燃烧需消耗5
mol
O2,D项正确。
【补偿训练】
某运动会火炬所用燃料为65%的丁烷(C4H10)和35%的丙烷。下列说法不正确的是
( )
A.火炬燃烧主要是将化学能转变为热能和光能
B.正丁烷的沸点比丙烷高
C.丁烷和丙烷都不溶于水
D.丁烷和丙烷的燃烧产物对环境无影响
【解析】选D。燃烧主要是将化学能转化成光能和热能,A正确;烷烃的熔沸点随着碳原子数的增加逐渐变大,B正确;烷烃均不溶于水,C正确;丁烷和丙烷的燃烧产物中的二氧化碳可以引起温室效应,D错误。
6.丁烷的分子结构可简写成键线式结构
,有机物A的键线式结构为
,则:
(1)有机物A的分子式为______________。?
(2)用系统命名法命名有机物A,其名称为__________。?
(3)有机物A完全燃烧的化学方程式为____________。?
(4)有机物A与Cl2发生反应生成的一氯代物有________种,写出A与Cl2反应生成任
意一种一氯代物的反应方程式________________。?
【解析】(1)根据丁烷的键线式可知,A的结构为
CH3—C(CH3)2—CH(CH3)—CH2—CH3,所以分子式为C8H18。(2)根据A的结构简式为
CH3—C(CH3)2—CH(CH3)—CH2—CH3可知,该有机物的系统命名为2,2,3-三甲基戊
烷。(3)A燃烧的反应方程式为2C8H18+25O2
16CO2+18H2O。(4)A的氢原子的种类
一共有5种,所以一氯代物一共有5种,结构简式分别为
CH2Cl—C(CH3)2—CH(CH3)—CH2—CH3,
C(CH3)3—CCl(CH3)—CH2—CH3,
C(CH3)3—CH(CH2Cl)—CH2—CH3,
C(CH3)3—CH(CH3)—CHCl—CH3,
C(CH3)3—CH(CH3)—CH2—CH2Cl。
答案:(1)C8H18 (2)2,2,3-三甲基戊烷
(3)2C8H18+25O2
16CO2+18H2O
(4)5
C(CH3)3CH(CH3)CH2CH3+Cl2
C(CH3)3CH(CH3)CH2CH2Cl+HCl(合理即可)
三 烷烃及其性质
【基础达标】(40分钟 70分)
一、选择题(本题包括10小题,每小题5分,共50分)
1.下列说法正确的是
( )
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B.分子组成符合CnH2n+2的烃一定是烷烃
C.正戊烷分子中所有的碳原子均在同一条直线上
D.碳、氢原子个数比为1∶3的烷烃有两种
【解析】选B。A项中环烷烃也符合要求,但它不是链烃,属于环烃;C项中由碳原子的成键方式和键角特征知,碳原子呈折线方式排列,因此正戊烷中的碳原子不在同一直线上;D项中n(C)∶n(H)=1∶3时必为C2H6,一定是乙烷。
2.(2020·泰安高二检测)从石油分馏得到的固体石蜡(主要成分为烷烃),用氯气漂白后,燃烧时会产生含氯元素的气体,这是由于石蜡在漂白时与氯气发生过
( )
A.加成反应
B.取代反应
C.聚合反应
D.催化裂化反应
【解析】选B。烷烃和氯气发生取代反应。
3.若要使0.5
mol
CH4完全与氯气发生取代反应,并生成相同物质的量的4种取代物。则需要氯气的物质的量为
( )
A.2.5
mol
B.2
mol
C.1.25
mol
D.0.5
mol
【解析】选C。0.5
mol
CH4完全与Cl2反应生成CH3Cl、CH2Cl2、CHCl3、CCl4的量均为0.125
mol,被取代的氢原子的物质的量为(1+2+3+4)×0.125
mol=1.25
mol,发生取代反应时,每有1
mol氢原子被取代,消耗1
mol
Cl2,故该反应需要氯气的物质的量为1.25
mol。
4.下列烷烃分子中的1个氢原子被溴原子取代后,不可能产生同分异构体的是
( )
A.CH3CH2CH2CH3
B.
C.CH3CH2CH3
D.
【解析】选B。利用对称轴法和等效氢原子法均可得到答案:
A项
,有两类氢原子,其一溴代物有两种;B项中四个甲基连在同
一个碳原子上,所有氢原子相同,其一溴代物只有一种;C项
,有两
种氢原子,其一溴代物有两种;D项中分子
不对称,有四类氢原子,
其一溴代物有四种。
5.(双选)一定条件下,两种气态烃的混合物共1
mol,在空气中完全燃烧生成
1.5
mol
CO2和2
mol水蒸气。关于该混合物的说法正确的是
( )
A.一定有甲烷
B.一定有乙烷
C.一定含有甲烷,可能含有乙烯
D.可能是甲烷和丙烷的混合物
【解析】选A、C。设混合烃的平均分子式为CxHy,则有
列式解得x=1.5,y=4。即混合烃的平均分子式为C1.5H4,则其中一定含有CH4,且另一种必须是含有4个H的烃。
【补偿训练】
把a
mol
H2和b
mol
C2H4混合,在一定条件下使它们一部分发生反应生成
w
mol
C2H6,将反应混合气体完全燃烧,消耗氧气的物质的量为
( )
A.a+3b
mol
B.
+3b
mol
C.
+3b+
w
mol
D.
+3b-
w
mol
【解析】选B。根据守恒关系,消耗的O2与生成的C2H6多少无关。
直接求a
mol
H2和b
mol
C2H4耗氧量。
6.关于CH4和
的叙述正确的是
( )
A.均能用组成通式CnH2n+2来表示
B.与所有烷烃互为同素异形体
C.因为它们结构相似,所以它们的化学性质相似,物理性质相同
D.通常情况下它们都是气态烷烃,均与Cl2发生取代反应
【解析】选A。二者均为烷烃,互为同系物,化学性质相似,但物理性质不同,后者为液态。
7.(2020·苏州高二检测)丙烷(C3H8)常作为一种环保燃料。下列有关说法中,正确的是
( )
A.丙烷既能发生取代反应,又能发生加成反应
B.丙烷完全燃烧,其产物对空气没有污染
C.丙烷燃料电池中,丙烷在正极发生反应
D.丙烷的一氯代物有三种同分异构体
【解析】选B。烷烃能发生取代反应,但不能发生加成反应,A错误;丙烷完全燃烧生成CO2和H2O,不会对空气造成污染,B正确;丙烷燃料电池中,丙烷发生氧化反应,应在负极上发生反应,C错误;丙烷中存在对称碳原子,只有两种氢原子,故其一氯代物只有两种,D错误。
8.C4H10的二氯取代物异构体数目为
( )
A.7种 B.8种 C.9种 D.10种
【解析】选C。C4H10的结构简式有2种,CH3CH2CH2CH3和CH3CH(CH3)2,
2个氯原子在CH3CH2CH2CH3上的取代物有(1,1)、(1,2)、(1,3)、(1,4)、(2,2)、(2,3),2个氯原子在CH3CH(CH3)2上的取代物有(1,1)、(1,2)、(1,3),共9种,C项正确。
【补偿训练】
下列表格中烷烃的一氯代物只有一种,仔细分析其结构和组成的变化规律,判断第4位烷烃的分子式是
( )
A.C36H72
B.C36H74
C.C53H106
D.C53H108
【解析】选D。每个碳上连相同的甲基,其氢原子只有一种,一氯代物只有一种,由递变规律可知,第4位烷烃是将第3位烷烃上的氢原子被甲基取代所得,分子式为C53H108。
9.(双选)下列关于甲烷的叙述中不正确的是
( )
A.甲烷分子的空间构型是正四面体,所以CH2Cl2有两种不同构型
B.甲烷可以与氯气发生取代反应,因此,甲烷能使氯水褪色
C.甲烷能够燃烧,在一定条件下会发生爆炸,因此,是矿井安全的重要威胁之一
D.甲烷不能使KMnO4溶液褪色
【解析】选A、B。甲烷分子的空间构型是正四面体,二氯甲烷(CH2Cl2)只有一种结构,A错误;甲烷可以与纯卤素单质(氯气)发生取代反应,不是氯水,B错误;矿井中存在甲烷气体,甲烷易燃易爆,因此甲烷是矿井安全的重要威胁之一,C正确;甲烷常温下性质稳定,与KMnO4溶液、酸或碱等均不反应,D正确。
10.(2020·南京高二检测)常温下,1
mol某烷烃在光照条件下与氯气发生取代反应,若在适当的条件下,完全取代需要消耗6
mol
Cl2,则下列判断正确的是
( )
A.该烷烃的分子式为C5H12
B.可以用AgNO3溶液检验反应生成的无机产物
C.该烷烃的四氯代物有1种
D.反应容器中,一氯代物所占的物质的量分数最大
【解析】选B。1
mol某烷烃在光照条件下与氯气发生取代反应,若在适当的条件下,完全取代需要消耗6
mol
Cl2,说明分子中含有6个H原子,该烷烃的分子式为C2H6,故A错误;氯化氢能使AgNO3溶液产生白色沉淀,故B正确;该烷烃的四氯代物有1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷,共2种,故C错误;反应容器中,氯化氢所占的物质的量分数最大,故D错误。
【易错提醒】烷烃和卤素单质的取代反应产物,卤化氢的产量最大。
二、非选择题(本题包括2小题,共20分)
11.(10分)已知烷烃A的密度是相同条件下H2密度的36倍。
(1)该烷烃A的分子式为__________________。?
(2)写出A可能存在的结构简式:_____________。?
(3)若A的某种同分异构体B的一氯代物只有一种。
①用系统命名法命名,B的名称为___________________;?
②B与Cl2发生反应生成一氯代物的化学方程式为___________________;?
③B燃烧的化学方程式为___________________。?
【解析】根据A的密度是相同条件下H2密度的36倍,推知其相对分子质量为72,
设分子式为CnH2n+2,求得n=5,则分子式为C5H12。
答案:(1)C5H12
(2)CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、
CH3C(CH3)2CH3 (3)①2,2-二甲基丙烷
②CH3—C(CH3)2—CH3+Cl2
CH3—C(CH3)2—CH2Cl+HCl
③C5H12+8O2
5CO2+6H2O
12.(10分)环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂):
回答下列问题:
(1)环烷烃与________是同分异构体。?
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是________(填名称),判断依据为__?__。?
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为?________(不需注明反应条件)。?
(4)写出鉴别环丙烷与丙烯的一种方法,试剂_______;?现象与结论______。
【解析】(1)环烷烃与单烯烃有相同的组成通式CnH2n,故当含碳原子数相同时互为同分异构体。
(2)可根据反应条件判断反应的难易。
(3)开环后链两端分别连接组成加成试剂的两个原子或基团。
(4)由题给信息可知,酸性KMnO4溶液只能氧化烯,而不能氧化环烷烃,故可用酸性KMnO4溶液作试剂鉴别环丙烷和丙烯。
答案:(1)含相同碳原子的单烯烃
(2)环丙烷 在都使用催化剂的条件下,加成反应的温度最低
(3)
(4)酸性KMnO4溶液 紫色褪去的是丙烯,不褪色的是环丙烷(其他合理答案也可)
【能力提升】(20分钟 30分)
一、选择题(本题包括2小题,每小题8分,共16分)
13.(2020·济宁高二检测)正己烷是优良的有机溶剂,其球棍模型为
,
X是它的一种同分异构体,且X分子的主链上含有4个碳原子。下列有关说法中正
确的是
( )
A.X分子中可能含有三个甲基
B.X的一氯代物一定有三种
C.X的沸点比正己烷低
D.标准状况下,11.2
L
X含2.5NA个C—C键
【解析】选C。由题意可知X的结构简式可能为
或
。
二者分子中均含4个甲基,A错;后者一氯代物有两种,B错;标准状况下二者均为
液态,D错。
14.(双选)篮烷的结构如图所示,下列说法正确的是
( )
A.篮烷的分子式为C12H14
B.篮烷分子中存在3个六元环
C.篮烷分子中存在3个五元环
D.篮烷的一氯代物共有5种同分异构体
【解析】选A、B。A项,先数清C的个数,C原子为12个,然后搞清每个C上连有几
个H原子(只有两个C原子上连有两个H原子,有10个“
”),显然篮烷的分
子式为C12H14,所以A项正确;篮烷分子中存在3个六元环、2个五元环、3个四元环,
所以B项正确,C项错误;篮烷的一氯代物有4种(如图),所以D项错误。
二、非选择题(本题包括1小题,共14分)
15.某烷烃汽化后的体积为2
mL,在一密闭容器中与
16
mL氧气恰好完全反应生成二氧化碳和水蒸气(反应前后均为相同状态)
(1)求该烷烃的分子式。
(2)写出该烷烃的所有同分异构体的结构简式。
(3)若该烷烃的一氯代物只有一种,写出该烷烃的结构简式。
【解析】设该烷烃分子式为CnH2n+2,
则由
可得n=5,故该烷烃的分子式为C5H12,为戊烷,其同分异构体有正戊烷、异戊烷和
新戊烷三种;若该烷烃的一氯代物只有一种,则分子中12个氢原子等效,
只有
符合。
答案:(1)C5H12
第3节 烃
第1课时 烷烃及其性质
一、烷烃的结构
二、烷烃的物理性质
1.递变规律(随碳原子数n递增)
2.相似性
烷烃均_____水,相对密度均_____水的密度。
【?判一判】
(1)分子中全是碳碳单键的烃一定是烷烃。
( )
提示:×。环烷烃中碳原子也全是碳碳单键。
(2)C2H6、C3H8、C4H10的熔沸点依次升高。
( )
提示:√。烷烃随着碳原子数的增多熔沸点升高。
难溶
小于
三、烷烃的化学性质
烷烃的化学性质与甲烷类似,通常较稳定,与_____________________不反应,
但一定条件下可燃烧,与氯气等发生取代反应。
1.与卤素单质的反应
在光照条件下,烷烃与Cl2、Br2等卤素单质的气体发生取代反应。
(1)乙烷在光照下与氯气发生取代反应生成一氯代物的化学方程式为
____________________________。
强酸、强碱及强氧化剂
光
CH3CH3+Cl2
CH3CH2Cl+HCl
(2)分子中碳链较长的烷烃与氯气反应时,不同_______断裂可以得到不同的取代
产物,如丙烷与氯气在光照条件下发生取代反应的产物是
(1-氯丙烷)、
(2-氯丙烷)。丁烷如果和氯气发生取代反应生成一氯代物,会有多少种?
提示:四种。CH2(Cl)CH2CH2CH3
,CH3CH(Cl)CH2CH3
,C(Cl)(CH3)3,CH(CH3)2CH2Cl。
碳氢键
2.与氧气的反应
烷烃的燃烧通式为
________________________________。
点燃
CnH2n+2+
O2
nCO2+(n+1)H2O
【?情境·思考】天然气的主要成分是甲烷,是一种十分重要的“清洁能源”,与液化石油气(主要成分是丙烷、丁烷)一样都是常用的家用燃气。随着现代社会对环境保护要求的提高,液化石油气正逐渐被天然气所取代。居民家庭中在将液化石油气更换为天然气时,通常需要更换燃气灶具或调整进气量,为什么?
提示:等物质的量的天然气与液化石油气完全燃烧耗氧量不同,即在燃气进气量一致的情况下,充分燃烧需要的空气量不同,因此需要更换燃气灶具或调整进气量。
知识点一 烷烃的取代反应
反应条件
光照
反应物
烷烃和气态卤素单质(烷烃与卤素单质的水溶液不反应)
化学键变化
断键:C—H键和X—X键
成键:C—X键和H—X键
取代特点
分子中的氢原子被卤素原子逐步取代,往往是各步反应同时发生
产物
特点
种类
多种卤代烷烃的混合物,HX的物质的量最多
产物
的量
①根据碳元素守恒,烷烃的物质的量等于所有卤代烷烃的物质的量之和
②根据取代反应的特点,有机物中卤素的物质的量等于HX的物质的量等于反应了的X2的物质的量,即反应了的n(X2)=n(一卤代物)+2n(二卤代物)+3n(三卤代物)+……=n(HX)
关键能力·素养形成
【方法规律】关于取代反应和置换反应的判断的简单方法
(1)看参与反应的物质类别:若物质类别是无机物,一定是置换反应,若物质类别均是有机物,则一定不是置换反应。
(2)看产物中是否有单质生成:若产物中有单质生成,一定不是取代反应。
【思考·讨论】
(1)烷烃的取代产物卤代烃是一类重要的有机化工原料,请问通过烷烃和卤素单质1∶1混合在光照的条件下能不能得到纯净的一卤代物?
提示:不能。不管比例如何,烷烃和卤素单质的反应都不能停留在第一步,所以得到的卤代烃是混合物。
(2)己烷能不能和溴水在光照下发生取代反应?如果把己烷和溴水混合在一起振荡后有什么现象?
提示:不能。卤素单质的水溶液不能和烷烃发生取代反应。如果把己烷和溴水混合,己烷能把溴单质从水中萃取出来,所以现象是液体分层,上层溶液为橙红色,下层无色。
【案例示范】
【典例】把1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在盛有Na2SiO3溶液的水槽里,放在光亮处。
(1)试管中观察到的现象:
①_________________;?
②_________________;?
③_________________。?
(2)水槽中观察到的现象:_____________________________。
(3)写出有关反应的化学方程式
①CH4和Cl2反应(第一步)
________________。
②Na2SiO3溶液中发生的反应________________。??
(4)待反应完成后,测得四种取代物物质的量相等,则反应中消耗Cl2的体积为____________。?
【解析】CH4和Cl2在光照条件下生成CH3Cl、CH2Cl2、CHCl3、CCl4、HCl,随着反应的进行,Cl2不断消耗,黄绿色逐渐变浅。又由于生成的CH2Cl2、CHCl3、CCl4常温下均为无色油状液体,使试管壁上有油滴出现。因生成的HCl易溶于水,反应后试管内气体压强减小,液面在试管内上升。HCl溶于水后与Na2SiO3反应生成白色絮状沉淀。因为CH4与Cl2发生取代反应生成的4种取代产物中的碳原子均来自CH4,由碳原子守恒可知,1
mol
CH4共生成1
mol
取代产物,且每一种取代产物物质的量均为0.25
mol。由于CH3Cl、CH2Cl2、CHCl3、CCl4分子中的氯原子均来自Cl2,
由CH4和Cl2反应的方程式知有机物中含有氯原子的物质的量:0.25
mol+0.25
mol
×2+0.25
mol×3+0.25
mol×4=2.5
mol。Cl2中进入HCl和进入有机物的氯原子的物质的量相同,故n(Cl2)=2.5
mol。
答案:(1)①气体颜色逐渐变浅
②试管中液面上升
③试管壁上有油状液滴
(2)有白色絮状沉淀生成
(3)①CH4+Cl2
CH3Cl+HCl
②Na2SiO3+2HCl
H2SiO3↓+2NaCl (4)2.5
【母题追问】若将Na2SiO3溶液改为紫色石蕊试液或浓氨水,则现象是
__________________________________________________________________。?
提示:若水槽中改盛紫色石蕊试液,HCl溶解后溶液显酸性,试液显红色。若水槽中改盛浓氨水,挥发出的氨气与试管中生成的HCl气体相遇会产生白烟。
【易错提醒】烷烃与卤素单质发生取代反应两个注意事项
(1)烷烃只能与卤素单质在光照条件下发生取代反应,不能与其水溶液发生取代反应。取代反应得到的不只是一氯代物,烷烃分子中的所有氢原子都可被氯原子取代。
(2)烷烃和氯气发生取代反应,有1
mol
H原子被取代,生成1
mol
HCl,消耗1
mol
Cl2,因此参加反应的Cl2的物质的量与生成的HCl的物质的量相等;生成物中HCl最多。
【迁移·应用】
1.将试管中的甲烷和氯气光照一段时间后,拔开橡胶塞,实验过程中不可能观察到的现象是
( )
A.试管中气体的黄绿色变浅
B.试管中有火星出现
C.试管内壁有油状液滴出现
D.试管口有白雾
【解析】选B。甲烷和氯气光照一段时间后试管内气体颜色逐渐变浅,内壁有油状液滴出现,拔开橡胶塞试管口有少量白雾出现。
2.(2018·全国卷Ⅱ)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是
( )
【解析】选D。甲烷与氯气发生取代反应生成CH3Cl、CH2Cl2、CHCl3、CCl4和HCl,因此观察到试管内颜色变浅,生成的CH2Cl2、CHCl3、CCl4为油状液体,且氯气易溶于有机物,故观察到试管内壁有浅黄色的油状液滴,只有CH3Cl和HCl为气体,因此反应后气体的体积减小,且HCl易溶于水,因此导致试管内压强减小,饱和食盐水会进入试管内形成一段水柱,因此答案为D。
【补偿训练】
如图,一端封闭的U形管,封闭着的一端有一段CH4和Cl2的混合气体,在水平部分有一段气柱,其他两段为液柱,已知液体与气体不反应,使CH4和Cl2在稍暗的光线下缓慢反应,则中间气柱的长度如何变化(假设中间气柱未移出U形管的水平部分)
( )
A.变大 B.变小
C.不变
D.难以确定
【解析】选A。在光照条件下,CH4与Cl2反应可生成多种产物,其中有3种产物(CH2Cl2、CHCl3、CCl4)常温下为液体,而使封闭一端气体的物质的量减小,故压强减小,左侧液面上升,右侧液面下降,两侧液柱差竖直长度减小,使水平处气柱压强减小,因温度不变故气柱体积增大。
【素养提升】
氯乙烷具有冷冻麻醉作用,从而使局部产生快速镇痛效果,氯乙烷喷雾剂主要用于运动中各种急性闭合性损伤,如肌肉拉伤、挫伤、关节扭挫伤以及骨折、脱臼整复。该喷雾剂的主要成分为氯乙烷,其结构简式为CH3—CH2Cl。
(1)氯乙烷还属于烷烃吗?
提示:不属于烷烃,氯乙烷中除含有碳、氢元素外,还含有氯元素,属于烃的衍生物。
(2)根据所学知识,探究以下制取氯乙烷的可行性。
①乙烷和氯气发生取代反应。
提示:乙烷和氯气发生取代反应得到一氯乙烷到六氯乙烷及HCl的混合物。方案不可行。
②乙烯和氯化氢发生加成反应。
提示:乙烯和氯化氢发生加成反应得到纯净的一氯乙烷,方案可行。
知识点二 烃燃烧的规律和应用
【重点释疑】
1.烃的燃烧规律
(1)烃的燃烧通式:CxHy+
O2
xCO2+
H2O。
(2)烃燃烧的三个规律
①等质量的烃完全燃烧
②等物质的量的烃完全燃烧
a.烃分子中
的数值越大,则耗氧量越大。
b.烃分子中x的数值越大,完全燃烧生成的CO2越多。
c.烃分子中y的数值越大,完全燃烧生成的H2O的物质的量越多。
③最简式相同的烃燃烧
a.最简式相同的烃,C、H的质量分数相同。
b.等质量的最简式相同的烃完全燃烧时,耗氧量相同、产生的CO2、H2O的质量、
物质的量均相同。
2.燃烧规律的应用
(1)若反应前后温度保持在100
℃以上,则烃完全燃烧前后的体积变化为
CxHy+
O2
xCO2+
H2O ΔV
1
x+
x
-1
故反应前后气体体积的变化ΔV仅与氢原子数y有关。
(2)若反应前后温度低于100
℃,此时气体体积一定是减少的,减少的气体体积
为ΔV=1+
,也与氢原子数有关。
【易错提醒】利用烃类燃烧的通式进行计算时的注意点
(1)水的状态是液态还是气态,从条件上看温度是在100
℃以下还是以上。
(2)气态烃完全燃烧前后,体积变化值也只与烃中的氢原子个数有关,根据体积
差值可以求出氢原子的个数或氢原子的平均个数。
(3)要注意检验氧气是否足量。
【思考·讨论】
(1)等物质的量的甲烷、乙烷、丙烷完全燃烧消耗氧气的物质的量之比为多少?
提示:4∶7∶10。由烃类燃烧的通式CxHy+
O2
xCO2+
H2O可知,等物质
的量的烃完全燃烧时耗氧量的大小取决于
的数值大小,从而可得其比值为
4∶7∶10。
(2)1
mol的烷烃同系物分别充分燃烧时,其耗氧量有何特点?
提示:1
mol有机物每增加一个“CH2”,耗O2量增加1.5
mol。烷烃同系物在分
子组成上若相差x个CH2原子团,耗氧量则相差1.5x
mol。
【典例】(2020·青岛高二检测)现有CH4、C2H4、C2H6、C3H6、C3H8五种有机物。
(1)等质量的以上物质中,在相同状况下体积最大的是__________;?
(2)等质量的以上物质完全燃烧时,消耗O2的量最多的是__________;?
(3)同状况、等体积、等物质的量的以上物质完全燃烧时,消耗O2的量最多的是__________;?
(4)等质量的以上物质完全燃烧时,生成的CO2最多的是__________,生成水最多的是__________。?
【解题指南】解答本题应注意以下两点:
(1)等物质的量的烃完全燃烧时烃分子中
的数值越大,则耗氧量越大。
(2)等质量的烃完全燃烧时烃分子中y/x越大,则耗氧量越大。
【解析】V=Vm·
,等质量时,气体体积与气体的摩尔质量成反比,所以等质量
的五种气体,在相同状况下,CH4的体积最大。对于等质量的烃CxHy,完全燃烧时
耗氧量的多少取决于
的大小,
越大,耗氧量越多,生成的H2O物质的量越
大,CO2的物质的量越小。同状况、等体积、等物质的量的烃CxHy完全燃烧,
耗氧量取决于
的相对大小。
答案:(1)CH4 (2)CH4 (3)C3H8 (4)C2H4、C3H6 CH4
【母题追问】(1)在120
℃,1.01×105
Pa时,以上气态烃和足量的O2完全燃烧,相同条件下测得反应前后气体体积没有发生变化的是哪些?
提示:CH4、C2H4。水为气体且氢原子数为4时反应前后体积不变。
(2)如果1
mol两种混合气体完全燃烧生成1.5
mol的二氧化碳和2
mol的水,混合气体可能是以上五种中的哪两种?
提示:碳原子数平均是1.5,所以一定有CH4,氢原子平均是4个,所以另外一种烃也是4个,即C2H4。
【规律方法】判断混合烃的组成规律
在同温同压下,1体积气态烃完全燃烧生成x体积CO2和y体积水蒸气,当为混合烃时,若x<2,则必含CH4,若y<2,则必含C2H2。
【迁移·应用】
1.A、B两种烃的混合物,当混合物的质量一定时,无论A、B以何种比例混合,完全燃烧产生的CO2的量均相等。在①同分异构体,②同系物,③具有相同的最简式,④含碳的质量分数相同,选项中符合上述条件的组合是
( )
A.①②④ B.①③④ C.②③④ D.①②③
【解析】选B。混合物的质量一定,无论以何种比例混合,燃烧产生的CO2量均相等,说明A、B中的碳质量分数相等,也可以是最简式相同。同分异构体分子式相同,最简式也相同。
2.某烃A的相对分子质量为84。回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是____________(填字母)。?
A.C7H12O2 B.C6H14
C.C6H14O
D.C7H14O3
(2)若烃A为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。A的结构简式为________________。?
(3)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为__________________。?
【解析】相对分子质量为84的烃,其分子式为C6H12,为烯烃或环烷烃。
(1)1
mol
C7H12O2充分燃烧消耗氧气9
mol,1
mol
C6H14充分燃烧消耗氧气
9.5
mol,1
mol
C6H14O充分燃烧消耗氧气9
mol,1
mol
C7H14O3充分燃烧消耗氧
气9
mol,应选B。
(2)链烃A与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种,说明该
烃分子高度对称,结构简式为
(CH3)2C====C(CH3)2。
(3)不能使溴水褪色,说明为饱和烃,一氯代物只有一种,则只能为环己烷。
答案:(1)B (2)(CH3)2C====C(CH3)2 (3)
【补偿训练】
一种气态烷烃和一种气态烯烃,它们分子里的碳原子数相等。将1.0体积这种混合气体在氧气中完全燃烧,生成2.0
体积的CO2和2.4
体积的水蒸气(气体
体积均在相同状况下测定),则混合气体中烷烃和烯烃的体积比为
( )
A.3∶1 B.1∶3
C.2∶3 D.3∶2
【解析】选C。根据阿伏加德罗定律,相同状况下,气体的体积之比等于物质的量之比,可知1
mol混合烃充分燃烧后生成2
mol
CO2和2.4
mol
H2O,则混合烃的平均分子组成为C2H4.8。又知烷烃和烯烃分子里的碳原子数相同,可以判定它们分别是C2H6和C2H4。无论C2H6与C2H4以怎样的体积比混合,它们的平均碳原子个数都是2。因此符合题意的烷烃和烯烃的体积比,将由它们分子里所含的氢原子个数决定。可用十字交叉法求解:
【课堂回眸】
1.如图所示均能表示甲烷的分子结构,下列说法错误的是
( )
A.Ⅰ将各原子看成了质点,为立体结构示意图
B.Ⅱ为电子式,表示甲烷分子中有8个电子
C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键
D.Ⅳ为空间填充模型,能表示出甲烷的空间构型及各原子的相对大小
【解析】选B。Ⅱ表示电子式,但略去了碳原子的内层电子,甲烷分子中应含有10个电子。
2.下列关于烷烃性质的叙述中,不正确的是
( )
A.烷烃随相对分子质量的增大,熔点、沸点逐渐升高,常温下的状态由气态递变到液态,相对分子质量大的则为固态
B.烷烃的密度随相对分子质量的增大逐渐增大
C.烷烃跟卤素单质在光照条件下能发生取代反应
D.烷烃能使溴水、酸性KMnO4溶液都褪色
【解析】选D。烷烃是饱和烃,化学性质稳定,具有代表性的反应是取代反应,C对;与烷烃发生取代反应的必须是卤素单质,溴水不能与烷烃反应,酸性KMnO4溶液也不能将烷烃氧化,D错。
3.物质的量相同的下列烃,完全燃烧,耗氧量最多的是
( )
A.C2H6 B.C4H6
C.C5H10
D.C7H8
【解析】选D。依据1
mol
CxHy耗氧
mol来确定:1
mol
C2H6耗氧2
mol+
mol=3.5
mol;1
mol
C4H6耗氧4
mol
+
mol=5.5
mol;1
mol
C5H10
耗氧
5
mol+
mol=7.5
mol;1
mol
C7H8耗氧7
mol+
mol=9
mol。
4.标准状况下将35
mL气态烷烃完全燃烧,恢复到原来状况下,得到二氧化碳气体140
mL,则该烃的分子式为
( )
A.C5H12
B.C4H10
C.C2H6
D.C3H8
【解析】选B。根据同温、同压下气体的体积比等于分子数比,烷烃分子数与二氧化碳气体分子数比为35
mL/140
mL=1/4,该烃1个分子中含有4个碳原子,即该烷烃为丁烷。
5.已知液化气的主要成分是丙烷,下列有关丙烷的叙述不正确的是
( )
A.是直链烃,但分子中碳原子不在一条直线上
B.在光照条件下能够与氯气发生取代反应
C.丙烷的球棍模型图为
D.1
mol丙烷完全燃烧消耗5
mol
O2
【解析】选C。C3H8是直链烃,其中的碳原子为饱和碳原子,和与之相邻的四个原子形成四面体结构,故3个碳原子不在一条直线上,A项正确;C3H8在光照时与Cl2发生取代反应,B项正确;丙烷的球棍模型图中漏掉了两个氢原子,C项错误;1
mol丙烷完全燃烧需消耗5
mol
O2,D项正确。
【补偿训练】
某运动会火炬所用燃料为65%的丁烷(C4H10)和35%的丙烷。下列说法不正确的是
( )
A.火炬燃烧主要是将化学能转变为热能和光能
B.正丁烷的沸点比丙烷高
C.丁烷和丙烷都不溶于水
D.丁烷和丙烷的燃烧产物对环境无影响
【解析】选D。燃烧主要是将化学能转化成光能和热能,A正确;烷烃的熔沸点随着碳原子数的增加逐渐变大,B正确;烷烃均不溶于水,C正确;丁烷和丙烷的燃烧产物中的二氧化碳可以引起温室效应,D错误。
6.丁烷的分子结构可简写成键线式结构
,有机物A的键线式结构为
,则:
(1)有机物A的分子式为______________。?
(2)用系统命名法命名有机物A,其名称为__________。?
(3)有机物A完全燃烧的化学方程式为____________。?
(4)有机物A与Cl2发生反应生成的一氯代物有________种,写出A与Cl2反应生成任
意一种一氯代物的反应方程式________________。?
【解析】(1)根据丁烷的键线式可知,A的结构为
CH3—C(CH3)2—CH(CH3)—CH2—CH3,所以分子式为C8H18。(2)根据A的结构简式为
CH3—C(CH3)2—CH(CH3)—CH2—CH3可知,该有机物的系统命名为2,2,3-三甲基戊
烷。(3)A燃烧的反应方程式为2C8H18+25O2
16CO2+18H2O。(4)A的氢原子的种类
一共有5种,所以一氯代物一共有5种,结构简式分别为
CH2Cl—C(CH3)2—CH(CH3)—CH2—CH3,
C(CH3)3—CCl(CH3)—CH2—CH3,
C(CH3)3—CH(CH2Cl)—CH2—CH3,
C(CH3)3—CH(CH3)—CHCl—CH3,
C(CH3)3—CH(CH3)—CH2—CH2Cl。
答案:(1)C8H18 (2)2,2,3-三甲基戊烷
(3)2C8H18+25O2
16CO2+18H2O
(4)5
C(CH3)3CH(CH3)CH2CH3+Cl2
C(CH3)3CH(CH3)CH2CH2Cl+HCl(合理即可)
三 烷烃及其性质
【基础达标】(40分钟 70分)
一、选择题(本题包括10小题,每小题5分,共50分)
1.下列说法正确的是
( )
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B.分子组成符合CnH2n+2的烃一定是烷烃
C.正戊烷分子中所有的碳原子均在同一条直线上
D.碳、氢原子个数比为1∶3的烷烃有两种
【解析】选B。A项中环烷烃也符合要求,但它不是链烃,属于环烃;C项中由碳原子的成键方式和键角特征知,碳原子呈折线方式排列,因此正戊烷中的碳原子不在同一直线上;D项中n(C)∶n(H)=1∶3时必为C2H6,一定是乙烷。
2.(2020·泰安高二检测)从石油分馏得到的固体石蜡(主要成分为烷烃),用氯气漂白后,燃烧时会产生含氯元素的气体,这是由于石蜡在漂白时与氯气发生过
( )
A.加成反应
B.取代反应
C.聚合反应
D.催化裂化反应
【解析】选B。烷烃和氯气发生取代反应。
3.若要使0.5
mol
CH4完全与氯气发生取代反应,并生成相同物质的量的4种取代物。则需要氯气的物质的量为
( )
A.2.5
mol
B.2
mol
C.1.25
mol
D.0.5
mol
【解析】选C。0.5
mol
CH4完全与Cl2反应生成CH3Cl、CH2Cl2、CHCl3、CCl4的量均为0.125
mol,被取代的氢原子的物质的量为(1+2+3+4)×0.125
mol=1.25
mol,发生取代反应时,每有1
mol氢原子被取代,消耗1
mol
Cl2,故该反应需要氯气的物质的量为1.25
mol。
4.下列烷烃分子中的1个氢原子被溴原子取代后,不可能产生同分异构体的是
( )
A.CH3CH2CH2CH3
B.
C.CH3CH2CH3
D.
【解析】选B。利用对称轴法和等效氢原子法均可得到答案:
A项
,有两类氢原子,其一溴代物有两种;B项中四个甲基连在同
一个碳原子上,所有氢原子相同,其一溴代物只有一种;C项
,有两
种氢原子,其一溴代物有两种;D项中分子
不对称,有四类氢原子,
其一溴代物有四种。
5.(双选)一定条件下,两种气态烃的混合物共1
mol,在空气中完全燃烧生成
1.5
mol
CO2和2
mol水蒸气。关于该混合物的说法正确的是
( )
A.一定有甲烷
B.一定有乙烷
C.一定含有甲烷,可能含有乙烯
D.可能是甲烷和丙烷的混合物
【解析】选A、C。设混合烃的平均分子式为CxHy,则有
列式解得x=1.5,y=4。即混合烃的平均分子式为C1.5H4,则其中一定含有CH4,且另一种必须是含有4个H的烃。
【补偿训练】
把a
mol
H2和b
mol
C2H4混合,在一定条件下使它们一部分发生反应生成
w
mol
C2H6,将反应混合气体完全燃烧,消耗氧气的物质的量为
( )
A.a+3b
mol
B.
+3b
mol
C.
+3b+
w
mol
D.
+3b-
w
mol
【解析】选B。根据守恒关系,消耗的O2与生成的C2H6多少无关。
直接求a
mol
H2和b
mol
C2H4耗氧量。
6.关于CH4和
的叙述正确的是
( )
A.均能用组成通式CnH2n+2来表示
B.与所有烷烃互为同素异形体
C.因为它们结构相似,所以它们的化学性质相似,物理性质相同
D.通常情况下它们都是气态烷烃,均与Cl2发生取代反应
【解析】选A。二者均为烷烃,互为同系物,化学性质相似,但物理性质不同,后者为液态。
7.(2020·苏州高二检测)丙烷(C3H8)常作为一种环保燃料。下列有关说法中,正确的是
( )
A.丙烷既能发生取代反应,又能发生加成反应
B.丙烷完全燃烧,其产物对空气没有污染
C.丙烷燃料电池中,丙烷在正极发生反应
D.丙烷的一氯代物有三种同分异构体
【解析】选B。烷烃能发生取代反应,但不能发生加成反应,A错误;丙烷完全燃烧生成CO2和H2O,不会对空气造成污染,B正确;丙烷燃料电池中,丙烷发生氧化反应,应在负极上发生反应,C错误;丙烷中存在对称碳原子,只有两种氢原子,故其一氯代物只有两种,D错误。
8.C4H10的二氯取代物异构体数目为
( )
A.7种 B.8种 C.9种 D.10种
【解析】选C。C4H10的结构简式有2种,CH3CH2CH2CH3和CH3CH(CH3)2,
2个氯原子在CH3CH2CH2CH3上的取代物有(1,1)、(1,2)、(1,3)、(1,4)、(2,2)、(2,3),2个氯原子在CH3CH(CH3)2上的取代物有(1,1)、(1,2)、(1,3),共9种,C项正确。
【补偿训练】
下列表格中烷烃的一氯代物只有一种,仔细分析其结构和组成的变化规律,判断第4位烷烃的分子式是
( )
A.C36H72
B.C36H74
C.C53H106
D.C53H108
【解析】选D。每个碳上连相同的甲基,其氢原子只有一种,一氯代物只有一种,由递变规律可知,第4位烷烃是将第3位烷烃上的氢原子被甲基取代所得,分子式为C53H108。
9.(双选)下列关于甲烷的叙述中不正确的是
( )
A.甲烷分子的空间构型是正四面体,所以CH2Cl2有两种不同构型
B.甲烷可以与氯气发生取代反应,因此,甲烷能使氯水褪色
C.甲烷能够燃烧,在一定条件下会发生爆炸,因此,是矿井安全的重要威胁之一
D.甲烷不能使KMnO4溶液褪色
【解析】选A、B。甲烷分子的空间构型是正四面体,二氯甲烷(CH2Cl2)只有一种结构,A错误;甲烷可以与纯卤素单质(氯气)发生取代反应,不是氯水,B错误;矿井中存在甲烷气体,甲烷易燃易爆,因此甲烷是矿井安全的重要威胁之一,C正确;甲烷常温下性质稳定,与KMnO4溶液、酸或碱等均不反应,D正确。
10.(2020·南京高二检测)常温下,1
mol某烷烃在光照条件下与氯气发生取代反应,若在适当的条件下,完全取代需要消耗6
mol
Cl2,则下列判断正确的是
( )
A.该烷烃的分子式为C5H12
B.可以用AgNO3溶液检验反应生成的无机产物
C.该烷烃的四氯代物有1种
D.反应容器中,一氯代物所占的物质的量分数最大
【解析】选B。1
mol某烷烃在光照条件下与氯气发生取代反应,若在适当的条件下,完全取代需要消耗6
mol
Cl2,说明分子中含有6个H原子,该烷烃的分子式为C2H6,故A错误;氯化氢能使AgNO3溶液产生白色沉淀,故B正确;该烷烃的四氯代物有1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷,共2种,故C错误;反应容器中,氯化氢所占的物质的量分数最大,故D错误。
【易错提醒】烷烃和卤素单质的取代反应产物,卤化氢的产量最大。
二、非选择题(本题包括2小题,共20分)
11.(10分)已知烷烃A的密度是相同条件下H2密度的36倍。
(1)该烷烃A的分子式为__________________。?
(2)写出A可能存在的结构简式:_____________。?
(3)若A的某种同分异构体B的一氯代物只有一种。
①用系统命名法命名,B的名称为___________________;?
②B与Cl2发生反应生成一氯代物的化学方程式为___________________;?
③B燃烧的化学方程式为___________________。?
【解析】根据A的密度是相同条件下H2密度的36倍,推知其相对分子质量为72,
设分子式为CnH2n+2,求得n=5,则分子式为C5H12。
答案:(1)C5H12
(2)CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、
CH3C(CH3)2CH3 (3)①2,2-二甲基丙烷
②CH3—C(CH3)2—CH3+Cl2
CH3—C(CH3)2—CH2Cl+HCl
③C5H12+8O2
5CO2+6H2O
12.(10分)环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂):
回答下列问题:
(1)环烷烃与________是同分异构体。?
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是________(填名称),判断依据为__?__。?
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件下反应,其化学方程式为?________(不需注明反应条件)。?
(4)写出鉴别环丙烷与丙烯的一种方法,试剂_______;?现象与结论______。
【解析】(1)环烷烃与单烯烃有相同的组成通式CnH2n,故当含碳原子数相同时互为同分异构体。
(2)可根据反应条件判断反应的难易。
(3)开环后链两端分别连接组成加成试剂的两个原子或基团。
(4)由题给信息可知,酸性KMnO4溶液只能氧化烯,而不能氧化环烷烃,故可用酸性KMnO4溶液作试剂鉴别环丙烷和丙烯。
答案:(1)含相同碳原子的单烯烃
(2)环丙烷 在都使用催化剂的条件下,加成反应的温度最低
(3)
(4)酸性KMnO4溶液 紫色褪去的是丙烯,不褪色的是环丙烷(其他合理答案也可)
【能力提升】(20分钟 30分)
一、选择题(本题包括2小题,每小题8分,共16分)
13.(2020·济宁高二检测)正己烷是优良的有机溶剂,其球棍模型为
,
X是它的一种同分异构体,且X分子的主链上含有4个碳原子。下列有关说法中正
确的是
( )
A.X分子中可能含有三个甲基
B.X的一氯代物一定有三种
C.X的沸点比正己烷低
D.标准状况下,11.2
L
X含2.5NA个C—C键
【解析】选C。由题意可知X的结构简式可能为
或
。
二者分子中均含4个甲基,A错;后者一氯代物有两种,B错;标准状况下二者均为
液态,D错。
14.(双选)篮烷的结构如图所示,下列说法正确的是
( )
A.篮烷的分子式为C12H14
B.篮烷分子中存在3个六元环
C.篮烷分子中存在3个五元环
D.篮烷的一氯代物共有5种同分异构体
【解析】选A、B。A项,先数清C的个数,C原子为12个,然后搞清每个C上连有几
个H原子(只有两个C原子上连有两个H原子,有10个“
”),显然篮烷的分
子式为C12H14,所以A项正确;篮烷分子中存在3个六元环、2个五元环、3个四元环,
所以B项正确,C项错误;篮烷的一氯代物有4种(如图),所以D项错误。
二、非选择题(本题包括1小题,共14分)
15.某烷烃汽化后的体积为2
mL,在一密闭容器中与
16
mL氧气恰好完全反应生成二氧化碳和水蒸气(反应前后均为相同状态)
(1)求该烷烃的分子式。
(2)写出该烷烃的所有同分异构体的结构简式。
(3)若该烷烃的一氯代物只有一种,写出该烷烃的结构简式。
【解析】设该烷烃分子式为CnH2n+2,
则由
可得n=5,故该烷烃的分子式为C5H12,为戊烷,其同分异构体有正戊烷、异戊烷和
新戊烷三种;若该烷烃的一氯代物只有一种,则分子中12个氢原子等效,
只有
符合。
答案:(1)C5H12
