(人教版)2020-2021学年九年级下册化学单元测试卷 第九单元 溶液基础卷(Word版含解析答案)
文档属性
| 名称 | (人教版)2020-2021学年九年级下册化学单元测试卷 第九单元 溶液基础卷(Word版含解析答案) |  | |
| 格式 | zip | ||
| 文件大小 | 273.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-02-24 08:23:38 | ||
图片预览


文档简介
第九单元
溶液基础卷
1.生活中的下列事件,利用了溶解原理的是(
)
A.将硬水变为软水
B.用洗洁精洗去餐具上的油污
C.用汽油洗去衣服上的油污
D.海水晒盐
2.下列说法正确的是(
)
A.植物油与水混合一定形成溶液
B.将100
g
10%的氯化钠溶液倒掉一半,剩余溶液的质量分数变为5%
C.饱和溶液一定是浓溶液
D.生活中利用洗涤剂清洗油污属于乳化现象
3.通常状况下,下列溶液的溶质为液体的是(??
)
A.蔗糖溶液?????B.酒精溶液?????C.氯化钠溶液?????D.澄清石灰水
4.下列有关溶液的说法正确的是
(
)
A.溶液均是无色的、透明的
B.可溶性物质溶于水时一定会放出热量
C.石灰水的溶质是石灰
D.溶液的均一性是指同一溶液各部分的性质、组成相同
5.下列过程吸收热量的是(
)
A.氢氧化钠固体溶于水
B.硝酸铵固体溶于水
C.把水加入生石灰中
D.氢氧化钠溶液与稀硫酸反应
6.下列洗涤或除污过程应用乳化原理的是(
)
A.用钢丝球刷除炒菜锅上的污垢
B.用酒精除去衣服上的碘
C.用汽油除去衣服上的油污
D.用洗洁精洗去餐具上的油脂
7.使某不饱和溶液变为饱和溶液,下列方法中最可靠的是(
)
A.升高温度
B.加入溶质
C.降低温度
D.倒掉一部分溶液
8.向一瓶接近饱和的氯化铵溶液中,逐渐加人氯化铵晶体,下列图像符合溶液中溶质质量变化规律的是(
)
A.B.
C.D.
9.生活中的下列现象,能说明气体的溶解度随压强变化而变化的是(
)
A.夏季,鱼塘中的鱼常常会浮在水面呼吸
B.喝了汽水以后,常常会打嗝
C.打开汽水瓶盖,有大量气泡冒出
D.烧开水时,沸腾前水中有气泡产生
10.若要增加汽水中的二氧化碳,下列操作可行的是(
)
A.增加水量
B.持续通二氧化碳
C.升温
D.加压
11.现有一杯20的某溶质的溶液.欲改变其溶质质量分数,一定可行的方法是(
)
A.加入一定量的溶质
B.增大压强
C.升温到60
D.加入一定量的水
12.用溶质质量分数为98%的浓硫酸10
mL(密度为1.84
g.
mL-1)配制溶质质量分数为10%的硫酸溶
液,需要量取水的体积是(
)
A.180
mL
B.
170
mL
C.162
mL
D.
88
mL
13.某同学模拟闽籍化学家侯德榜的“侯氏制碱法”制纯碱,需用50.0g水配制20℃的NaCl饱和溶液(20℃时NaCl的溶解度为36.0g),应称取NaCl的质量为(??
)
A.18.0g??????B.16.0g??????C.13.2g??????D.11.5g
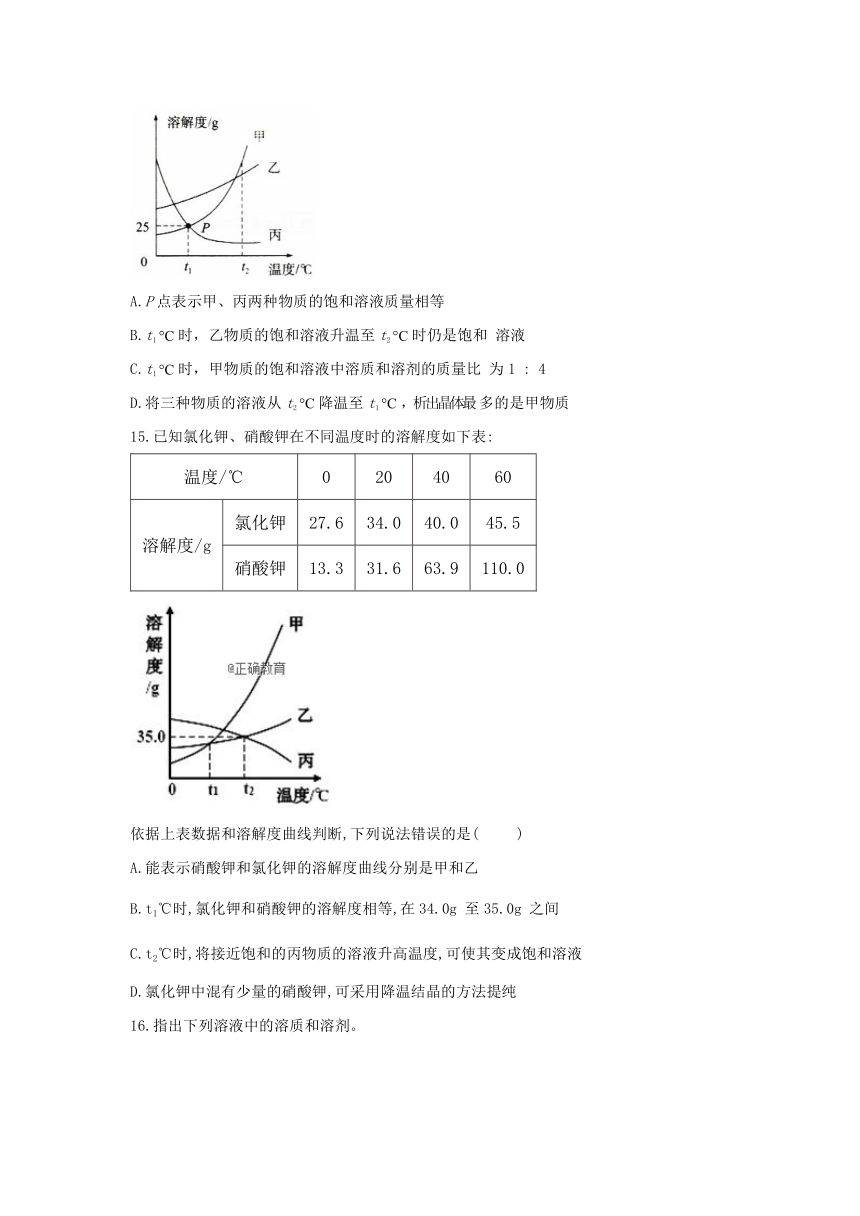
14.如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是(
)
A.P点表示甲、丙两种物质的饱和溶液质量相等
B.t1时,乙物质的饱和溶液升温至t2时仍是饱和
溶液
C.t1时,甲物质的饱和溶液中溶质和溶剂的质量比
为1
:
4
D.将三种物质的溶液从t2降温至t1,析出晶体最
多的是甲物质
15.已知氯化钾、硝酸钾在不同温度时的溶解度如下表:
温度/℃
0
20
40
60
溶解度/g
氯化钾
27.6
34.0
40.0
45.5
硝酸钾
13.3
31.6
63.9
110.0
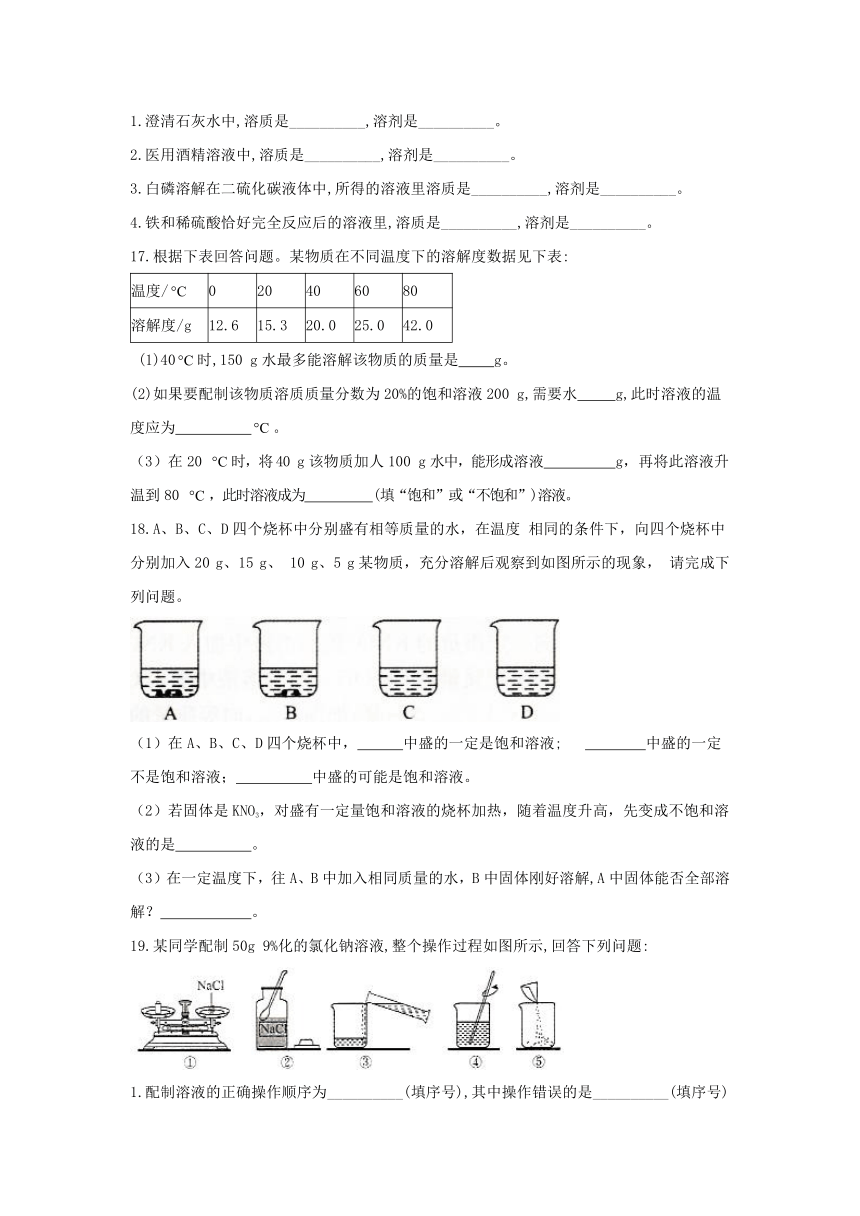
依据上表数据和溶解度曲线判断,下列说法错误的是(??
)
A.能表示硝酸钾和氯化钾的溶解度曲线分别是甲和乙
B.t1℃时,氯化钾和硝酸钾的溶解度相等,在34.0g
至35.0g
之间
C.t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液
D.氯化钾中混有少量的硝酸钾,可采用降温结晶的方法提纯
16.指出下列溶液中的溶质和溶剂。
1.澄清石灰水中,溶质是__________,溶剂是__________。
2.医用酒精溶液中,溶质是__________,溶剂是__________。
3.白磷溶解在二硫化碳液体中,所得的溶液里溶质是__________,溶剂是__________。
4.铁和稀硫酸恰好完全反应后的溶液里,溶质是__________,溶剂是__________。
17.根据下表回答问题。某物质在不同温度下的溶解度数据见下表:
温度/
0
20
40
60
80
溶解度/g
12.6
15.3
20.0
25.0
42.0
(1)40时,150
g水最多能溶解该物质的质量是
g。
(2)如果要配制该物质溶质质量分数为20%的饱和溶液200
g,需要水
g,此时溶液的温度应为
。
(3)在20
时,将40
g该物质加人100
g水中,能形成溶液
g,再将此溶液升温到80
,此时溶液成为
(填“饱和”或“不饱和”)溶液。
18.A、B、C、D四个烧杯中分别盛有相等质量的水,在温度
相同的条件下,向四个烧杯中分别加入20
g、15
g、
10
g、5
g某物质,充分溶解后观察到如图所示的现象,
请完成下列问题。
(1)在A、B、C、D四个烧杯中,
中盛的一定是饱和溶液;
中盛的一定不是饱和溶液;
中盛的可能是饱和溶液。
(2)若固体是KNO3,对盛有一定量饱和溶液的烧杯加热,随着温度升高,先变成不饱和溶液的是
。
(3)在一定温度下,往A、B中加入相同质量的水,B中固体刚好溶解,A中固体能否全部溶解?
。
19.某同学配制50g
9%化的氯化钠溶液,整个操作过程如图所示,回答下列问题:
1.配制溶液的正确操作顺序为__________(填序号),其中操作错误的是__________(填序号)
2.图②中盛放氯化钠固体的仪器名称是__________,需称取氧化钠__________g。
3.量水时选用的量筒的量程最合适的是__________(填字母),读数时视线要与量筒内__________保持水平。
A.10
mL????
B.25
mL?????
C.50
mL?????
D.100
mL
20.向盛有28
g氯
化钡和氯化钠固体混合物的烧杯中加入273.
3
g水,
固体完全溶解。再逐滴加入一定质量分数的硫酸钠溶液,反应过程中生成沉淀的质量与所加硫酸钠溶液的质量关系如图所示。(化学方程式为Na2SO4
+
BaCl2=2NaCl+BaSO4↓
)
请计算:
(1)固体混合物中氯化钡的质量。
(2)恰好完全反应时,所得溶液中溶质的质量分数
答案以及解析
1.答案:C
解析:生活中将硬水变为软水是加热煮沸过程.故A选项不符合题意;用洗洁精洗去餐具上的油污是因为洗洁精具有乳化作用,故B选项不符合题意;用汽油清洗油污是利用了汽油能溶解油污来达到目的的.利用的是溶解原理,故C选项符合题意;海水晒盐是蒸发结晶,故D选项不符合题意。
2.答案:D
3.答案:B
解析:A、蔗糖溶液是蔗糖的水溶液,蔗糖是溶质,水的溶剂,溶质为固体,故选项错误;
B、酒精溶液是酒精的水溶液,酒精是溶质,水的溶剂,溶质为液体,故选项正确;
C、氯化钠溶液是氯化钠的水溶液,氯化钠是溶质,水的溶剂,溶质为固体,故选项错误;
D、澄清的石灰水是氢氧化钙的水溶液,氢氧化钙是溶质,水的溶剂,溶质为固体,故选项错误。
4.答案:D
解析:溶液的特征:均一、稳定的混合物,溶液可以有颜色.如硫酸铜溶液是蓝色的.故A错误;物质溶于水,有的放热.有的吸热,如氢氧化钠溶于水放热.硝酸铵溶于水吸热,故B错误;石灰水的溶质是氢氧化钙,故C错误;溶液的均一性是指同一溶液各部分的性质、组成相同,故D正确。
5.答案:B
解析:氢氧化钠固体溶于水时会放出热量.A不符合题意;硝酸铵固体溶于水会吸热,B符合题意;水与生石灰反应会放出热量.C不符合题意;镁与稀硫酸反应会放出热量,D不符合题意。
6.答案:D
7.答案:B
解析:要使不饱和溶液变为饱和溶液,加入溶质或蒸发溶剂适合于所有溶液,但升温或降温则需看该物质的溶解度受温度影响的情况.若溶解度随温度升高而增大,则需降温,反之则需升温;倒掉一部分溶液不能改变溶液的状态。
8.答案:C
解析:不饱和氯化铵溶液中含有一定量的溶质氯化铵,所以加入氯化铵之前,不饱和的氯化铵溶液中溶质的质量不为0,故A错误;向一定量不饱和氯化铵溶液中逐渐加入氯化铵固体时,氯化铵能够继续溶解,溶质质量增加,直到达到饱和状态时氯化铵的质量为一定值,故B错误、C正确;在一定温度下,在一定量的溶剂里.氯化按不能无限溶解,故D错误。
9.答案:C
解析:夏季,鱼塘中的鱼常常会浮在水面呼吸,是因为夏季气温升高.氧气的溶解度减小,溶解在水中的氧气减少,故A不符合题意;
喝了汽水以后常常会打嗝,是由于胃内的温度高,二氧化碳的溶解度变小,故B不符合题意;
打开汽水瓶盖,压强变小,汽水中的二氧化碳的溶解度减小,故大量的气体冲出,说明了气体的溶解度随压强的减小而减小,故C符合题意;
烧开水时,沸腾前水中有气泡产生,是因为随着温度的升高,原本水中溶有的气体的溶解度减小,因此有气泡产生,故D不符合题意。
10.答案:D
解析:气体的溶解度随温度的升高而减小,随着压强的增大而增大,若要增加汽水中的二氧化碳.可采用加压或降温的方法,故选D。
11.答案:D
解析:加入一定量的溶质,若溶液饱和,则不再溶解.故溶质质量分数不一定改变.故A不可行;压强影响的是气体物质的溶解度,所以增大压强溶质质量分数不一定改变,故B不可行;升高温度.溶质和溶剂的质量不一定改变,所以溶质质量分数不一定改变,故C不可行;加入一定量的水.溶剂增加,故溶质质量分数一定变小,故D可行。
12.答案:C
解析:设配制成的稀硫酸的质量为x,根据溶液稀释前后溶质的质量不变.则1.84
g?mL-1×10mL×98%=10%x,解得x=180.32
g.水的质量=稀溶液的质量-浓溶液的质量,需要水的质量为180.32
g-1.84
g?mL-1×10
mL=161.92g≈162g(合162mL)
13.答案:A
解析:20℃时NaCl的溶解度为36.0g,即100g水中最多溶解36.0g氯化钠固体。那么50g水中最近18.0g氯化钠固体。故选A。
14.答案:C
解析:P点表示t1时甲、丙两种物质的溶解度相等,饱和溶
液的质量不一定相等,故A错误;乙物质的溶解度随温度的
升高而增大,所以t1时,乙物质的饱和溶液升温至t2时
会变成不饱和溶液,故B错误;
t1时,甲物质的溶解度是
25
g,所以甲物质的饱和溶液中溶质和溶剂的质量比=25
g
:
100
g=l
:
4,故C正确;三种物质的溶液质量不能确定,所以
从t2降温至t1,析出晶体的多少不能确定,故D错误。
15.答案:D
解析:A、通过分析溶解度表中的数据可知,硝酸钾的溶解度受温度变化影响较大,氯化钾的溶解度受温度变化影响较小,所以能表示硝酸钾和氯化钾的溶解度曲线分别是甲和乙,正确;B、通过分析溶解度表中的数据可知,t1℃时,氯化钾和硝酸钾的溶解度相等,在34.0g至35.0g之间,正确;C、丙物质的溶解度随温度的升高而减小,所以t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液,正确;D、氯化钾的溶解度受温度变化影响较小,所以氯化钾中混有少量的硝酸钾,可采用蒸发结晶的方法提纯,错误。故选D。
16.答案:1.氢氧化钙;
水;
2.酒精;
水;
3.白磷;
二硫化碳;
4.硫酸亚铁;
水
解析:石灰水是氢氧化钙溶于水后得到的溶液,溶质是
氢氧化钙.溶剂是水:医用酒精溶液是酒精与水的混合物.
溶剂是水.溶质是酒精;白磷溶解在二硫化碳液体中.溶质
是白磷.溶剂是二硫化碳:铁和稀硫酸恰好完全反应生成硫
酸亚铁和氢气,則所得溶液中溶质为硫酸亚铁.溶剂为水。
17.答案:(1)30
(2)160
;60
(3)115.3;不饱和
解析:(1)40
时.该物质的溶解度为20.
0
g.即40
时.100
g水中最多溶解20
g溶质.則150
g水最多能溶解该物质的质量为。(2)200
g饱和溶液中溶质的质量为200
g×20%
=
40g.配制该物盾的溶质质量分数为20%的饱和溶液200
g,需要
水的质量为200
g-40
g=
160
g;
设200
g
20%的饱和溶液在某溫度下的溶解度为s,
,s=25
g,
根据图表可知.在60时该物质的溶解度为25
g。
(3)20时.将40
g该物廣加入100
g水中,因为此溫度下
溶解度为15.
3
g,能形成溶液的质量=
100
g+15.
3
g
=
115.
3
g.将该溶液升溫到80,此溫度下,其溶解度为
42
g.则得到的是不饱和溶液。
18.答案:(1)A、B
D
C
(2)B
(3)不能(或否)
解析:(1)依据饱和溶液的概念可知,A、B中有固体出现.一定是饱和溶液,C中的溶质质量比D多,可能是恰好溶解达到饱和.而D—定不饱和。(2)因KNO3的溶解度随温度的升高而增大,A和B—定是饱和溶液.B中的硝酸钾比A中的少.则升溫B先变为不饱和。(3)在一定温度下,往A、B中加入相同质量的水,因A中溶质比B中的多,B中固体刚好溶解时.A中肯定还有固体剩余。
19.答案:1.②①⑤③④;①;2.广口瓶;4.5;3.C;凹液面的最低处
解析:(1)配制50
g
9%的氯化钠溶液时,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,配制溶液的正确操作顺序为②①⑤③④;在称量药品时应“左物右码”,图中所示操作砝码与药品位置放反了,所以搡作错误的是①。
(2)图②中盛放氯化钠固体的仪器名称是广口瓶;溶质质量=溶液质量×溶质的质量分数,配制50
g
9%的氮化钠溶液,需称取氯化钠的质量=50
g×9%=4.5
g。
(3)溶剂质量=溶液质量-溶质质量,所需溶剂的质量为50
g-4.5
g=45.5
g(合45.5
mL),应用规格为50
mL的量筒量取水的体积;读数时视线要与量筒内凹液面的最低处保持水平。
20.答案:(1)解:设固体混合物中氯化钡的质量为x,生成氯化钠的质量为y。
Na2SO4+BaCl2
=2NaCl+BaSO4↓
208
117
233
x
y
23.3g
,
解得x=20.8g,y=11.7g.
(2)恰好完全反应时,所得溶液中溶质的质量分数
解析:根据反应的化学方程式计算解答。
溶液基础卷
1.生活中的下列事件,利用了溶解原理的是(
)
A.将硬水变为软水
B.用洗洁精洗去餐具上的油污
C.用汽油洗去衣服上的油污
D.海水晒盐
2.下列说法正确的是(
)
A.植物油与水混合一定形成溶液
B.将100
g
10%的氯化钠溶液倒掉一半,剩余溶液的质量分数变为5%
C.饱和溶液一定是浓溶液
D.生活中利用洗涤剂清洗油污属于乳化现象
3.通常状况下,下列溶液的溶质为液体的是(??
)
A.蔗糖溶液?????B.酒精溶液?????C.氯化钠溶液?????D.澄清石灰水
4.下列有关溶液的说法正确的是
(
)
A.溶液均是无色的、透明的
B.可溶性物质溶于水时一定会放出热量
C.石灰水的溶质是石灰
D.溶液的均一性是指同一溶液各部分的性质、组成相同
5.下列过程吸收热量的是(
)
A.氢氧化钠固体溶于水
B.硝酸铵固体溶于水
C.把水加入生石灰中
D.氢氧化钠溶液与稀硫酸反应
6.下列洗涤或除污过程应用乳化原理的是(
)
A.用钢丝球刷除炒菜锅上的污垢
B.用酒精除去衣服上的碘
C.用汽油除去衣服上的油污
D.用洗洁精洗去餐具上的油脂
7.使某不饱和溶液变为饱和溶液,下列方法中最可靠的是(
)
A.升高温度
B.加入溶质
C.降低温度
D.倒掉一部分溶液
8.向一瓶接近饱和的氯化铵溶液中,逐渐加人氯化铵晶体,下列图像符合溶液中溶质质量变化规律的是(
)
A.B.
C.D.
9.生活中的下列现象,能说明气体的溶解度随压强变化而变化的是(
)
A.夏季,鱼塘中的鱼常常会浮在水面呼吸
B.喝了汽水以后,常常会打嗝
C.打开汽水瓶盖,有大量气泡冒出
D.烧开水时,沸腾前水中有气泡产生
10.若要增加汽水中的二氧化碳,下列操作可行的是(
)
A.增加水量
B.持续通二氧化碳
C.升温
D.加压
11.现有一杯20的某溶质的溶液.欲改变其溶质质量分数,一定可行的方法是(
)
A.加入一定量的溶质
B.增大压强
C.升温到60
D.加入一定量的水
12.用溶质质量分数为98%的浓硫酸10
mL(密度为1.84
g.
mL-1)配制溶质质量分数为10%的硫酸溶
液,需要量取水的体积是(
)
A.180
mL
B.
170
mL
C.162
mL
D.
88
mL
13.某同学模拟闽籍化学家侯德榜的“侯氏制碱法”制纯碱,需用50.0g水配制20℃的NaCl饱和溶液(20℃时NaCl的溶解度为36.0g),应称取NaCl的质量为(??
)
A.18.0g??????B.16.0g??????C.13.2g??????D.11.5g
14.如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是(
)
A.P点表示甲、丙两种物质的饱和溶液质量相等
B.t1时,乙物质的饱和溶液升温至t2时仍是饱和
溶液
C.t1时,甲物质的饱和溶液中溶质和溶剂的质量比
为1
:
4
D.将三种物质的溶液从t2降温至t1,析出晶体最
多的是甲物质
15.已知氯化钾、硝酸钾在不同温度时的溶解度如下表:
温度/℃
0
20
40
60
溶解度/g
氯化钾
27.6
34.0
40.0
45.5
硝酸钾
13.3
31.6
63.9
110.0
依据上表数据和溶解度曲线判断,下列说法错误的是(??
)
A.能表示硝酸钾和氯化钾的溶解度曲线分别是甲和乙
B.t1℃时,氯化钾和硝酸钾的溶解度相等,在34.0g
至35.0g
之间
C.t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液
D.氯化钾中混有少量的硝酸钾,可采用降温结晶的方法提纯
16.指出下列溶液中的溶质和溶剂。
1.澄清石灰水中,溶质是__________,溶剂是__________。
2.医用酒精溶液中,溶质是__________,溶剂是__________。
3.白磷溶解在二硫化碳液体中,所得的溶液里溶质是__________,溶剂是__________。
4.铁和稀硫酸恰好完全反应后的溶液里,溶质是__________,溶剂是__________。
17.根据下表回答问题。某物质在不同温度下的溶解度数据见下表:
温度/
0
20
40
60
80
溶解度/g
12.6
15.3
20.0
25.0
42.0
(1)40时,150
g水最多能溶解该物质的质量是
g。
(2)如果要配制该物质溶质质量分数为20%的饱和溶液200
g,需要水
g,此时溶液的温度应为
。
(3)在20
时,将40
g该物质加人100
g水中,能形成溶液
g,再将此溶液升温到80
,此时溶液成为
(填“饱和”或“不饱和”)溶液。
18.A、B、C、D四个烧杯中分别盛有相等质量的水,在温度
相同的条件下,向四个烧杯中分别加入20
g、15
g、
10
g、5
g某物质,充分溶解后观察到如图所示的现象,
请完成下列问题。
(1)在A、B、C、D四个烧杯中,
中盛的一定是饱和溶液;
中盛的一定不是饱和溶液;
中盛的可能是饱和溶液。
(2)若固体是KNO3,对盛有一定量饱和溶液的烧杯加热,随着温度升高,先变成不饱和溶液的是
。
(3)在一定温度下,往A、B中加入相同质量的水,B中固体刚好溶解,A中固体能否全部溶解?
。
19.某同学配制50g
9%化的氯化钠溶液,整个操作过程如图所示,回答下列问题:
1.配制溶液的正确操作顺序为__________(填序号),其中操作错误的是__________(填序号)
2.图②中盛放氯化钠固体的仪器名称是__________,需称取氧化钠__________g。
3.量水时选用的量筒的量程最合适的是__________(填字母),读数时视线要与量筒内__________保持水平。
A.10
mL????
B.25
mL?????
C.50
mL?????
D.100
mL
20.向盛有28
g氯
化钡和氯化钠固体混合物的烧杯中加入273.
3
g水,
固体完全溶解。再逐滴加入一定质量分数的硫酸钠溶液,反应过程中生成沉淀的质量与所加硫酸钠溶液的质量关系如图所示。(化学方程式为Na2SO4
+
BaCl2=2NaCl+BaSO4↓
)
请计算:
(1)固体混合物中氯化钡的质量。
(2)恰好完全反应时,所得溶液中溶质的质量分数
答案以及解析
1.答案:C
解析:生活中将硬水变为软水是加热煮沸过程.故A选项不符合题意;用洗洁精洗去餐具上的油污是因为洗洁精具有乳化作用,故B选项不符合题意;用汽油清洗油污是利用了汽油能溶解油污来达到目的的.利用的是溶解原理,故C选项符合题意;海水晒盐是蒸发结晶,故D选项不符合题意。
2.答案:D
3.答案:B
解析:A、蔗糖溶液是蔗糖的水溶液,蔗糖是溶质,水的溶剂,溶质为固体,故选项错误;
B、酒精溶液是酒精的水溶液,酒精是溶质,水的溶剂,溶质为液体,故选项正确;
C、氯化钠溶液是氯化钠的水溶液,氯化钠是溶质,水的溶剂,溶质为固体,故选项错误;
D、澄清的石灰水是氢氧化钙的水溶液,氢氧化钙是溶质,水的溶剂,溶质为固体,故选项错误。
4.答案:D
解析:溶液的特征:均一、稳定的混合物,溶液可以有颜色.如硫酸铜溶液是蓝色的.故A错误;物质溶于水,有的放热.有的吸热,如氢氧化钠溶于水放热.硝酸铵溶于水吸热,故B错误;石灰水的溶质是氢氧化钙,故C错误;溶液的均一性是指同一溶液各部分的性质、组成相同,故D正确。
5.答案:B
解析:氢氧化钠固体溶于水时会放出热量.A不符合题意;硝酸铵固体溶于水会吸热,B符合题意;水与生石灰反应会放出热量.C不符合题意;镁与稀硫酸反应会放出热量,D不符合题意。
6.答案:D
7.答案:B
解析:要使不饱和溶液变为饱和溶液,加入溶质或蒸发溶剂适合于所有溶液,但升温或降温则需看该物质的溶解度受温度影响的情况.若溶解度随温度升高而增大,则需降温,反之则需升温;倒掉一部分溶液不能改变溶液的状态。
8.答案:C
解析:不饱和氯化铵溶液中含有一定量的溶质氯化铵,所以加入氯化铵之前,不饱和的氯化铵溶液中溶质的质量不为0,故A错误;向一定量不饱和氯化铵溶液中逐渐加入氯化铵固体时,氯化铵能够继续溶解,溶质质量增加,直到达到饱和状态时氯化铵的质量为一定值,故B错误、C正确;在一定温度下,在一定量的溶剂里.氯化按不能无限溶解,故D错误。
9.答案:C
解析:夏季,鱼塘中的鱼常常会浮在水面呼吸,是因为夏季气温升高.氧气的溶解度减小,溶解在水中的氧气减少,故A不符合题意;
喝了汽水以后常常会打嗝,是由于胃内的温度高,二氧化碳的溶解度变小,故B不符合题意;
打开汽水瓶盖,压强变小,汽水中的二氧化碳的溶解度减小,故大量的气体冲出,说明了气体的溶解度随压强的减小而减小,故C符合题意;
烧开水时,沸腾前水中有气泡产生,是因为随着温度的升高,原本水中溶有的气体的溶解度减小,因此有气泡产生,故D不符合题意。
10.答案:D
解析:气体的溶解度随温度的升高而减小,随着压强的增大而增大,若要增加汽水中的二氧化碳.可采用加压或降温的方法,故选D。
11.答案:D
解析:加入一定量的溶质,若溶液饱和,则不再溶解.故溶质质量分数不一定改变.故A不可行;压强影响的是气体物质的溶解度,所以增大压强溶质质量分数不一定改变,故B不可行;升高温度.溶质和溶剂的质量不一定改变,所以溶质质量分数不一定改变,故C不可行;加入一定量的水.溶剂增加,故溶质质量分数一定变小,故D可行。
12.答案:C
解析:设配制成的稀硫酸的质量为x,根据溶液稀释前后溶质的质量不变.则1.84
g?mL-1×10mL×98%=10%x,解得x=180.32
g.水的质量=稀溶液的质量-浓溶液的质量,需要水的质量为180.32
g-1.84
g?mL-1×10
mL=161.92g≈162g(合162mL)
13.答案:A
解析:20℃时NaCl的溶解度为36.0g,即100g水中最多溶解36.0g氯化钠固体。那么50g水中最近18.0g氯化钠固体。故选A。
14.答案:C
解析:P点表示t1时甲、丙两种物质的溶解度相等,饱和溶
液的质量不一定相等,故A错误;乙物质的溶解度随温度的
升高而增大,所以t1时,乙物质的饱和溶液升温至t2时
会变成不饱和溶液,故B错误;
t1时,甲物质的溶解度是
25
g,所以甲物质的饱和溶液中溶质和溶剂的质量比=25
g
:
100
g=l
:
4,故C正确;三种物质的溶液质量不能确定,所以
从t2降温至t1,析出晶体的多少不能确定,故D错误。
15.答案:D
解析:A、通过分析溶解度表中的数据可知,硝酸钾的溶解度受温度变化影响较大,氯化钾的溶解度受温度变化影响较小,所以能表示硝酸钾和氯化钾的溶解度曲线分别是甲和乙,正确;B、通过分析溶解度表中的数据可知,t1℃时,氯化钾和硝酸钾的溶解度相等,在34.0g至35.0g之间,正确;C、丙物质的溶解度随温度的升高而减小,所以t2℃时,将接近饱和的丙物质的溶液升高温度,可使其变成饱和溶液,正确;D、氯化钾的溶解度受温度变化影响较小,所以氯化钾中混有少量的硝酸钾,可采用蒸发结晶的方法提纯,错误。故选D。
16.答案:1.氢氧化钙;
水;
2.酒精;
水;
3.白磷;
二硫化碳;
4.硫酸亚铁;
水
解析:石灰水是氢氧化钙溶于水后得到的溶液,溶质是
氢氧化钙.溶剂是水:医用酒精溶液是酒精与水的混合物.
溶剂是水.溶质是酒精;白磷溶解在二硫化碳液体中.溶质
是白磷.溶剂是二硫化碳:铁和稀硫酸恰好完全反应生成硫
酸亚铁和氢气,則所得溶液中溶质为硫酸亚铁.溶剂为水。
17.答案:(1)30
(2)160
;60
(3)115.3;不饱和
解析:(1)40
时.该物质的溶解度为20.
0
g.即40
时.100
g水中最多溶解20
g溶质.則150
g水最多能溶解该物质的质量为。(2)200
g饱和溶液中溶质的质量为200
g×20%
=
40g.配制该物盾的溶质质量分数为20%的饱和溶液200
g,需要
水的质量为200
g-40
g=
160
g;
设200
g
20%的饱和溶液在某溫度下的溶解度为s,
,s=25
g,
根据图表可知.在60时该物质的溶解度为25
g。
(3)20时.将40
g该物廣加入100
g水中,因为此溫度下
溶解度为15.
3
g,能形成溶液的质量=
100
g+15.
3
g
=
115.
3
g.将该溶液升溫到80,此溫度下,其溶解度为
42
g.则得到的是不饱和溶液。
18.答案:(1)A、B
D
C
(2)B
(3)不能(或否)
解析:(1)依据饱和溶液的概念可知,A、B中有固体出现.一定是饱和溶液,C中的溶质质量比D多,可能是恰好溶解达到饱和.而D—定不饱和。(2)因KNO3的溶解度随温度的升高而增大,A和B—定是饱和溶液.B中的硝酸钾比A中的少.则升溫B先变为不饱和。(3)在一定温度下,往A、B中加入相同质量的水,因A中溶质比B中的多,B中固体刚好溶解时.A中肯定还有固体剩余。
19.答案:1.②①⑤③④;①;2.广口瓶;4.5;3.C;凹液面的最低处
解析:(1)配制50
g
9%的氯化钠溶液时,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,配制溶液的正确操作顺序为②①⑤③④;在称量药品时应“左物右码”,图中所示操作砝码与药品位置放反了,所以搡作错误的是①。
(2)图②中盛放氯化钠固体的仪器名称是广口瓶;溶质质量=溶液质量×溶质的质量分数,配制50
g
9%的氮化钠溶液,需称取氯化钠的质量=50
g×9%=4.5
g。
(3)溶剂质量=溶液质量-溶质质量,所需溶剂的质量为50
g-4.5
g=45.5
g(合45.5
mL),应用规格为50
mL的量筒量取水的体积;读数时视线要与量筒内凹液面的最低处保持水平。
20.答案:(1)解:设固体混合物中氯化钡的质量为x,生成氯化钠的质量为y。
Na2SO4+BaCl2
=2NaCl+BaSO4↓
208
117
233
x
y
23.3g
,
解得x=20.8g,y=11.7g.
(2)恰好完全反应时,所得溶液中溶质的质量分数
解析:根据反应的化学方程式计算解答。
同课章节目录
